Хлорид рутения(III)
 | |
 | |
| Идентификаторы | |
|---|---|
| |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.030.139 |
ПабХим CID | |
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| RuCl 3 · x H 2 O | |
| Молярная масса | 207.43 g/mol |
| Температура плавления | >500°C (разлагается) |
| Растворим, безводный нерастворим | |
| +1998.0·10 −6 см 3 /моль | |
| Структура | |
| тригональный (RuCl 3 ), hP8 | |
| П3с1, № 158 | |
| октаэдрический | |
| Опасности | |
| точка возгорания | негорючий |
| Родственные соединения | |
Другие анионы | Бромид рутения(III) |
Другие катионы | Хлорид родия(III) Хлорид железа(III) |
Родственные соединения | Четырехокись рутения |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Хлорид рутения(III) – химическое соединение формулы RuCl 3 . «Хлорид рутения (III)» чаще относится к гидрату RuCl 3 · x H 2 O. Как безводные, так и гидратированные виды представляют собой темно-коричневые или черные твердые вещества. Гидрат с различной пропорцией кристаллизационной воды , часто приближающейся к тригидрату, является широко используемым исходным материалом в рутения химии .
Приготовление и свойства
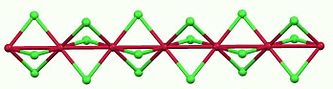
[ редактировать ]Безводный хлорид рутения (III) обычно получают нагреванием порошкообразного металлического рутения с хлором . В первоначальном синтезе хлорирование проводилось в присутствии монооксида углерода , продукт переносился потоком газа и кристаллизовался при охлаждении. [1] [2] две полиморфные модификации RuCl 3 Известны . Черная α-форма имеет CrCl 3 структуру типа с длинными контактами Ru-Ru размером 346 мкм . Этот полиморф имеет сотовые слои Ru. 3+ которые окружены октаэдрической клеткой Cl − анионы. Катионы рутения являются магнитными и находятся в низкоспиновом основном состоянии J~1/2 с суммарным угловым моментом L=1. [3] [4] Слои α-RuCl 3 накладываются друг на друга под действием слабых сил Ван-дер-Ваальса . Их можно расколоть, чтобы сформировать монослои, используя скотч. [5]
Темно-коричневая метастабильная β-форма кристаллизуется в гексагональной ячейке; эта форма состоит из бесконечных цепочек октаэдров с общими гранями с контактами Ru-Ru 283 пм, аналогичных структуре трихлорида циркония . β-форма необратимо превращается в α-форму при 450–600 °С. β-форма диамагнитна, тогда как α-RuCl 3 парамагнитна при комнатной температуре. [6]
Пары RuCl 3 разлагаются на элементы при высоких температурах; при изменение энтальпии 750 °С (1020 К), Δ diss H 1020 оценивается как +240 кДж/моль.
Физика твердого тела
[ редактировать ]α-RuCl 3 был предложен в качестве кандидата Китаевского квантово -спинового жидкого состояния. [7] когда рассеяние нейтронов выявило необычный магнитный спектр, [8] [9] [10] и тепловой транспорт выявил киральные майорановские фермионы под воздействием магнитного поля. [11]
Координационная химия гидратированного трихлорида рутения
[ редактировать ]O , наиболее доступное соединение рутения, RuCl 3 · x H 2 является предшественником многих сотен химических соединений. Примечательным свойством комплексов рутения, хлоридов и других соединений, является наличие более чем одной степени окисления, некоторые из которых кинетически инертны. Все переходные металлы второго и третьего ряда образуют исключительно низкоспиновые комплексы, тогда как рутений отличается стабильностью соседних степеней окисления, особенно Ru(II), Ru(III) (как и в исходном RuCl 3 · x H 2 O) и Ру(IV).
Иллюстративные комплексы на основе «трихлорида рутения».
[ редактировать ]- RuCl 2 (PPh 3 ) 3 , растворимый в бензоле компонент шоколадного цвета, который, в свою очередь, также является универсальным исходным материалом. Возникает примерно так: [12]
- 2 RuCl 3 · x H 2 O + 7 PPh 3 → 2 RuCl 2 (PPh 3 ) 3 + OPPH 3 + 5 H 2 O + 2 HCl
- Хлорид дирутения тетраацетат , полимер смешанной валентности, получают восстановлением трихлорида рутения в уксусной кислоте.
- [RuCl 2 ( C 6 H 6 )] 2 возникает из 1,3-циклогексадиена или 1,4-циклогексадиена следующим образом: [13] [14]
- 2 RuCl 3 · x H 2 O + 2 C 6 H 8 → [RuCl 2 (C 6 H 6 )] 2 + 6 H 2 O + 2 HCl + H 2
- Ru(bipy) 3 Cl 2 , интенсивно люминесцентная соль с долгоживущим возбужденным состоянием, возникающая следующим образом: [15]
- 2 RuCl 3 · x H 2 O + 6 bipy + CH 3 CH 2 OH → 2 [Ru(bipy) 3 ]Cl 2 + 6 H 2 O + CH 3 CHO + 2 HCl
Эта реакция протекает через промежуточный цис-Ru(bipy) 2 Cl 2 . [15]
- 2 RuCl 3 · x H 2 O + 2 C 5 Me 5 H → [RuCl 2 (C 5 Me 5 )] 2 + 6 H 2 O + 2 HCl
[RuCl 2 (C 5 Me 5 )] 2 может быть дополнительно восстановлен до [RuCl(C 5 Me 5 )] 4 .
- Ru( C 5 H 7 O 2 ) 3 возникает следующим образом: [17]
- RuCl 3 · x H 2 O + 3 C 5 H 8 O 2 → Ru(C 5 H 7 O 2 ) 3 + 3 H 2 O + 3 HCl
- RuO 4 , получают окислением.
Некоторые из этих соединений использовались в исследованиях, связанных с двумя Нобелевскими премиями . Рёдзи Ноёри был удостоен Нобелевской премии по химии в 2001 году за разработку практических катализаторов асимметричного гидрирования на основе рутения. Роберт Х. Граббс был удостоен Нобелевской премии по химии в 2005 году за разработку практических катализаторов метатезиса алкенов на основе производных алкилидена рутения .
Производные угарного газа
[ редактировать ]RuCl 3 (H 2 O) x реагирует с окисью углерода в мягких условиях. [18] Напротив, хлориды железа не реагируют с CO. CO восстанавливает красно-коричневый трихлорид до желтоватых частиц Ru (II). В частности, воздействие на этанольный раствор RuCl 3 (H 2 O) x 1 атм CO дает, в зависимости от конкретных условий, [Ru 2 Cl 4 (CO) 4 ], [Ru 2 Cl 4 (CO) 4 ] 2− , и [RuCl 3 (CO) 3 ] − . Добавление к таким растворам лигандов (L) дает соединения Ru-Cl-CO-L (L = PR 3 ). Восстановление этих карбонилированных растворов Zn дает оранжевый треугольный кластер. Ру 3 (СО) 12 .
- 3 RuCl 3 · x H 2 O + 4,5 Zn + 12 CO (высокое давление) → Ru 3 (CO) 12 + 3 x H 2 O + 4,5 ZnCl 2
Источники
[ редактировать ]- Беккер, Рамона; Хартвиг, Хельга; Кеппе, Герберт; Ванечек, Ганс; Велич, Пол; Варнке, Рудольф; Клетка, Анна (1978). Варнке, Рудольф (ред.). Гмелин Справочник по неорганической химии . дои : 10.1007/978-3-662-06224-1 . ISBN 978-3-662-06226-5 .
Ссылки
[ редактировать ]- ^ Реми, Х.; Кюн, М. (1924). «Вклад в химию платиновых металлов. V. Термическое разложение трихлорида рутения и диоксида рутения». З. Анорг. Генерал Хим . 137 (1): 365–388. дои : 10.1002/zaac.19241370127 .
- ^ Бублиц, Д.Э.; МакИвен, МЫ; Кляйнберг, Дж. (1961). «Рутеноцен». Органические синтезы . 41 : 96. дои : 10.15227/orgsyn.041.0096 .
- ^ Флетчер, Дж. М.; Гарднер, МЫ; Хупер, EW; Хайд, КР; Мур, Ф.Х.; Вудхед, Дж. Л. (сентябрь 1963 г.). «Безводные хлориды рутения». Природа . 199 (4898): 1089–1090. Бибкод : 1963Natur.199.1089F . дои : 10.1038/1991089a0 . ISSN 0028-0836 . S2CID 4179795 .
- ^ Отвес, КВт; Клэнси, JP; Сандилендс, ЖЖ; Шанкар, В. Виджай; Ху, Ю.Ф.; Берч, Канзас; Ки, Хэ Ён; Ким, Янг-Джун (29 июля 2014 г.). «α-RuCl 3 : спин-орбитальный изолятор Мотта на сотовой решетке». Физический обзор B . 90 (4): 041112. arXiv : 1403.0883 . Бибкод : 2014PhRvB..90d1112P . дои : 10.1103/physrevb.90.041112 . ISSN 1098-0121 . S2CID 29688091 .
- ^ Чжоу, Бойи; Ван, Ипин; Остерхудт, Гэвин Б.; Лампен-Келли, Паула; Мандрус, Дэвид; Он, Руи; Берч, Кеннет С.; Хенриксен, Эрик А. (2019). «Возможные структурные преобразования и усиленные магнитные флуктуации в расслоенном αRuCl 3 ». Журнал физики и химии твердого тела . 128 : 291–295. arXiv : 1709.00431 . Бибкод : 2019JPCS..128..291Z . дои : 10.1016/j.jpcs.2018.01.026 . ISSN 0022-3697 . S2CID 103743571 .
- ^ Флетчер, Дж. М.; Гарднер, МЫ; Фокс, AC; Топпинг, Г. (1967). «Рентгеновские, инфракрасные и магнитные исследования α- и β-трихлорида рутения». Журнал Химического общества A: Неорганическое, физическое, теоретическое : 1038–1045. дои : 10.1039/J19670001038 .
- ^ Банерджи, А.; Бриджес, Калифорния; Ян, Ж.-К.; Аксель, А.А.; Ли, Л.; Стоун, МБ; Гранрот, GE; Ламсден, доктор медицины; Ю, Ю. (4 апреля 2016 г.). «Приблизительное поведение Китаевской квантово-спиновой жидкости в сотовом магните». Природные материалы . 15 (7): 733–740. arXiv : 1504.08037 . Бибкод : 2016NatMa..15..733B . дои : 10.1038/nmat4604 . ISSN 1476-1122 . ПМИД 27043779 . S2CID 3406627 .
- ^ Банерджи, Арнаб; Ян, Цзяцян; Нолле, Йоханнес; Бриджес, Крейг А.; Стоун, Мэтью Б.; Ламсден, Марк Д.; Мандрус, Дэвид Г.; Теннант, Дэвид А.; Месснер, Родерих (9 июня 2017 г.). «Рассеяние нейтронов в ближайшей квантово-спиновой жидкости α-RuCl 3». Наука . 356 (6342): 1055–1059. arXiv : 1609.00103 . Бибкод : 2017Sci...356.1055B . дои : 10.1126/science.aah6015 . ISSN 0036-8075 . ПМИД 28596361 . S2CID 206652434 .
- ^ До, Сын Хван; Пак Сан Ён; Ёситаке, Джунки; Насу, Джоджи; Мотоме, Юкитоши; Квон, Ён Сын; Адроха, DT; Вонешен, диджей; Ким, Кё (18 сентября 2017 г.). «Майорановские фермионы в квантовой спиновой системе Китаева α-RuCl3» . Физика природы . 13 (11): 1079–1084. Бибкод : 2017NatPh..13.1079D . дои : 10.1038/nphys4264 . ISSN 1745-2473 . S2CID 126423385 .
- ^ Банерджи, Арнаб; Лампен-Келли, Паула; Нолле, Йоханнес; Бальц, Кристиан; Аксель, Адам Энтони; Уинн, Барри; Лю, Яохуа; Пажеровский, Дэниел; Ян, Цзяцян; Бриджес, Крейг А.; Савич, Андрей Т.; Чакумакос, Брайан С.; Ламсден, Марк Д.; Теннант, Дэвид Алан; Месснер, Родерих; Мандрус, Дэвид Г.; Наглер, Стивен Э. (20 февраля 2018 г.). «Возбуждения в индуцированном полем квантово-спиновом жидком состоянии α-RuCl 3». npj Квантовые материалы . 3 (1): 8. arXiv : 1706.07003 . Бибкод : 2018npjQM...3....8B . дои : 10.1038/s41535-018-0079-2 . ISSN 2397-4648 . S2CID 55484993 .
- ^ Касахара, Ю.; Ониши, Т.; Мизуками, Ю.; Танака, О.; Ма, Сысяо; Сугии, К.; Курита, Н.; Танака, Х.; Насу, Дж. (июль 2018 г.). «Майорановское квантование и полуцелый тепловой квантовый эффект Холла в спиновой жидкости Китаева». Природа . 559 (7713): 227–231. arXiv : 1805.05022 . Бибкод : 2018Natur.559..227K . дои : 10.1038/s41586-018-0274-0 . ISSN 0028-0836 . ПМИД 29995863 . S2CID 49664700 .
- ^ PS Холлман, Т. А. Стивенсон, Г. Уилкинсон «Тетракис (трифенилфосфин) дихлор-рутений (II) и трис (трифенилфосфин)-дихлоррутений (II)» Неорганический синтез, 1970, том 12, . два : 10.1002/9780470132432.ch40
- ^ Беннетт, Мартин А.; Смит, Энтони К. (1 января 1974 г.). «Ареновые комплексы рутения (II), образующиеся при дегидрировании циклогексадиенов трихлоридом рутения (III)» . Журнал Химического общества, Dalton Transactions (2): 233–241. дои : 10.1039/dt9740000233 . ISSN 1364-5447 .
- ^ Беннетт, Массачусетс; Хуанг, Теннесси; Мэтисон, Т.В. и Смит, А.К. (1982). (η 6 -Гексаметилбензол)рутениевые комплексы . Неорганические синтезы . Том. 21. С. 74–8. дои : 10.1002/9780470132524.ch16 . ISBN 9780470132524 .
- ^ Перейти обратно: а б Брумхед, Дж.А.; Янг, К.Г. (1990). Трис(2,2'-бипиридин)рутений(II)дихлорид гексагидрат . Неорганические синтезы. Том. 28. С. 338–340. дои : 10.1002/9780470132593.ch86 . ISBN 9780470132593 .
- ^ Кёлле, Урих; Косаковский, Януш (1992). Ди-мк-Хлор-Бис[(η5-пентаметилциклопентадиенил)хлоррутений(III)], [Cp*RuCl 2 ] 2 и Ди-мк-метоксо-бис(η5-пентаметилциклопентадиенил)дирутений(II), [Cp*RuOMe] 2 . Неорганические синтезы. Том 29. С. 225–228. дои : 10.1002/9780470132609.ch52 . ISBN 9780470132609 .
- ^ Гупта, А. (2000). «Улучшение синтеза и реакционной способности трис (ацетилацетонато) рутения (III)». Индийский химический журнал, раздел A. 39А (4): 457. ISSN 0376-4710 .
- ^ Хилл, А.Ф. (2000). « Простые» карбонилы рутения: новые пути базовой реакции Хибера». Энджью. хим. Межд. Эд. 39 (1): 130–134. doi : 10.1002/(SICI)1521-3773(20000103)39:1<130::AID-ANIE130>3.0.CO;2-6 . ПМИД 10649352 .
Дальнейшее чтение
[ редактировать ]- Карлсен, PHJ; Мартин, Виктор С.; и др. (1981). «Значительно улучшенная процедура окисления органических соединений, катализируемого тетраоксидом рутения». Дж. Орг. хим. 46 (19): 3936. doi : 10.1021/jo00332a045 .
- Коттон, ЮАР (1997). Химия драгоценных металлов . дои : 10.1007/978-94-009-1463-6 . ISBN 0-7514-0413-6 .
- Икария, Такао; Мурата, Кунихико; Ноёри, Рёдзи (2006). «Бифункциональные молекулярные катализаторы на основе переходных металлов для асимметричного синтеза». Орг. Биомол. Хим . 4 (3): 393–406. дои : 10.1039/B513564H . ПМИД 16446796 . S2CID 29116338 .