Хлорид европия(III)
 | |
 | |
| Имена | |
|---|---|
| ИЮПАК имена Хлорид европия(III) трихлорид европия | |
| Идентификаторы | |
| |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.030.025 |
| Номер ЕС |
|
ПабХим CID | |
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| ЭуСl 3 | |
| Молярная масса | 258.323 g/mol 366,41 г/моль (гексагидрат) |
| Температура плавления | 632 ° C (1170 ° F; 905 К) разлагается. |
| Растворимость в других растворителях | Растворимый |
| Структура | |
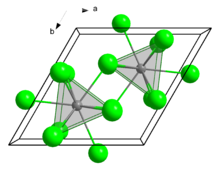
| шестиугольный ( UCl 3 тип ), hP8 | |
| Р6 3 /м, №176 | |
| Треугольная треугольная призматика (девятикоординатный) | |
| Родственные соединения | |
Другие анионы | Оксид европия(III) |
Другие катионы | Хлорид самария(III) Хлорид гадолиния(III) |
Родственные соединения | европия дихлорид |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Хлорид европия(III) представляет собой неорганическое соединение формулы EuCl 3 . соединение Безводное представляет собой твердое вещество желтого цвета. Будучи гигроскопичным, он быстро поглощает воду с образованием белого кристаллического гексагидрата EuCl 3 ·6H 2 O, бесцветного. Соединение используется в исследованиях.
Подготовка
[ редактировать ]Обработка Eu 2 O 3 водным раствором HCl дает гидрат хлорида европия (EuCl 3 ·6H 2 O). Эту соль невозможно сделать безводной при нагревании. Вместо этого получается оксихлорид .Безводный EuCl 3 часто получают «методом хлорида аммония », начиная с Eu 2 O 3 [1] [2] или гидрат хлорида европия (EuCl 3 ·6H 2 O) при осторожном нагревании до 230°С. [3] Этими методами получают (NH 4 ) 2 [EuCl 5 ]:
- 10 NH 4 Cl + Eu 2 O 3 → 2 (NH 4 ) 2 [EuCl 5 ] + 6 NH 3 + 3 H 2 O
- EuCl 3 ·6H 2 O + 2 NH 4 Cl → (NH 4 ) 2 [EuCl 5 ] + 6 H 2 O
Пентахлорид термически разлагается по следующему уравнению:
- (NH 4 ) 2 [EuCl 5 ] → 2 NH 4 Cl + EuCl 3
Реакция термолиза протекает с участием (NH 4 )[Eu 2 Cl 7 ].
Реакции
[ редактировать ]Хлорид европия(III) является предшественником других соединений европия. Его можно превратить в бис(триметилсилил)амид соответствующего металла посредством метатезиса соли с бис(триметилсилил)амидом лития . [4] Реакцию проводят в ТГФ и требуют выдержки при кипении с обратным холодильником.
- EuCl 3 + 3 LiN(SiMe 3 ) 2 → Eu(N(SiMe 3 ) 2 ) 3 + 3 LiCl
Eu(N(SiMe 3 ) 2 ) 3 является исходным материалом для более сложных координационных комплексов .
Восстановление газообразным водородом при нагревании дает EuCl 2 . Последний использован для получения металлоорганических соединений европия(II), таких как комплексы бис(пентаметилциклопентадиенил)европия(II). [5] [6] Хлорид европия(III) можно использовать в качестве отправной точки для получения других европия солей .
Структура
[ редактировать ]В твердом состоянии он кристаллизуется в UCl3 мотиве . Центры ЕС являются девятикоординатными. [7]
Библиография
[ редактировать ]- Уэст, RC, изд. (1972). Справочник по химии и физике (53-е изд.). Кливленд, Огайо: Chemical Rubber Co.
Ссылки
[ редактировать ]- ^ Мейер, Г. (1989). Путь хлорида аммония к безводным хлоридам редкоземельных элементов - пример YCl 3 . Неорганические синтезы. Том. 25. С. 146–150. дои : 10.1002/9780470132562.ch35 . ISBN 978-0-470-13256-2 .
- ^ Эдельманн, FT; Поремба, П. (1997). Херрманн, Вашингтон (ред.). Синтетические методы металлоорганической и неорганической химии . Том. VI. Штутгарт: Георг Тиме Верлаг. ISBN 3-13-103021-6 .
- ^ Тейлор, доктор медицины; Картер, CP (1962). «Получение безводных галогенидов лантаноидов, особенно йодидов». Журнал неорганической и ядерной химии . 24 (4): 387–391. дои : 10.1016/0022-1902(62)80034-7 .
- ^ Брэдли, Дональд С.; Готра, Джогиндер С.; Харт, Ф. Алан (1973). «Низкие координационные числа в соединениях лантаноидов и актинидов. Часть I. Получение и характеристика трис{бис(триметилсилил)-амидо}лантанидов» . Журнал Химического общества, Dalton Transactions (10): 1021–1023. дои : 10.1039/DT9730001021 .
- ^ Тилли, Т. Дон; Андерсен, Ричард А.; Спенсер, Брок; Рубен, Хелена; Залкин, Аллан; Темплтон, Дэвид Х. (1980). «Химия двухвалентных лантаноидов. Производные бис(пентаметилциклопентадиенил)европия(II) и -иттербия(II): кристаллическая структура бис(пентаметилциклопентадиенил)(тетрагидрофуран иттербий(II)-гемитолуола при 176 К» . Неорганическая химия . 19 (10): 2999 .дои 10.1021 / : ic50212a031 .
- ^ Эванс, Уильям Дж.; Хьюз, Лаура А.; Хануса, Тимоти П. (1986). «Синтез и рентгенокристаллическая структура бис(пентаметилциклопентадиенильных) комплексов самария и европия: (C 5 Me 5 ) 2 Sm и (C 5 Me 5 ) 2 Eu». Металлоорганические соединения . 5 (7): 1285. doi : 10.1021/om00138a001 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
