Фотохимия

Фотохимия - это ветвь химии, связанная с химическими эффектами света. Как правило, этот термин используется для описания химической реакции, вызванной поглощением ультрафиолета ( длина волны от 100 до 400 нм ), видимой (400–750 нм) или инфракрасного излучения (750–2500 нм). [ 1 ]
В природе фотохимия имеет огромное значение, поскольку она является основой фотосинтеза, зрения и образования витамина D с солнечным светом. [ 2 ] Это также отвечает за появление мутаций ДНК, ведущих к раку кожи. [ 3 ]
Фотохимические реакции происходят иначе, чем реакции, управляемые температурой. Фотохимические пути получают доступ к высокоэнергетическим промежуточным соединениям, которые не могут генерироваться термически, тем самым преодолевая большие барьеры активации в течение короткого периода времени и позволяя реакциям, иначе недоступные тепловыми процессами. Фотохимия также может быть разрушительной, как показано фотодеградацией пластмасс .
Концепция
[ редактировать ]Закон Гротосс - законодательство и закон Старк -Эйнштейн
[ редактировать ]Фотоэкссификация - это первый шаг в фотохимическом процессе, где реагент повышается до состояния более высокой энергии, возбужденного состояния . Первый закон фотохимии, известный как Закон Гротросс - сделки (для химиков Теодор Гротосс и Джон В. Дрейпер ), утверждает, что свет должен поглощать химическим веществом для того, чтобы фотохимическая реакция имела место. Согласно второму закону фотохимии, известного как Закон Старк -Эйнштейна (для физиков Йоханнеса Старка и Альберта Эйнштейна ), для каждого фотона света, поглощенного химической системой, не более одной молекулы активируется для фотохимической реакции, как определено, не более одной молекулы активируется для фотохимической реакции, как определено не более одной молекулы. квантовым урожайностью . [ 4 ] [ 5 ]
Флуоресценция и фосфорценция
[ редактировать ]Когда молекула или атом в основном состоянии (S 0 ) поглощает свет, один электрон возбуждается до более высокого уровня орбитальной. Этот электрон поддерживает свое вращение в соответствии с правилом выбора спина; Другие переходы нарушат закон сохранения углового импульса . Возбуждение в более высокое синглетное состояние может быть от HOMO до LUMO или до более высокой орбиты, так что состояния синглетного возбуждения S 1 , S 2 , S 3 возможны ... при разных энергиях.
Правило Каши предусматривает, что более высокие синглетные состояния быстро расслабится путем безлуационного распада или внутреннего преобразования (IC) в S 1 . Таким образом, S 1 обычно, но не всегда, единственным соответствующим синглетным возбужденным состоянием. Это возбужденное состояние S 1 может дополнительно расслабиться до S 0 от IC, но также путем разрешенного радиационного перехода от S 1 к S 0 , который излучает фотон; Этот процесс называется флуоресценцией .
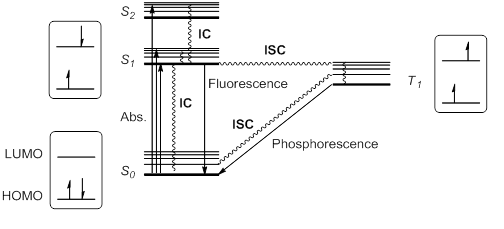
В качестве альтернативы, возбужденное состояние S 1 может пройти инверсию вращения и генерировать триплетное возбужденное состояние T 1, имеющее два непарных электрона с одинаковым вращением. Это нарушение правила выбора вращения возможна с помощью межсистемного пересечения (ISC) колебательных и электронных уровней S 1 и T 1 . В соответствии с правилом максимальной множественности Hund , это состояние T 1 было бы несколько более стабильным, чем S 1 .
Это триплетное состояние может расслабиться до основного состояния S 0 с помощью радиационного ISC или радиационного пути, называемого фосфоресценцией . Этот процесс подразумевает изменение электронного спина, которое запрещено правилами отбора спинового отбора, что делает фосфоресценцию (от T 1 до S 0 ) намного медленнее, чем флуоресценция (от S 1 до S 0 ). Таким образом, триплетные государства обычно имеют более длительную жизнь, чем синглетные государства. Эти переходы обычно суммируются на энергетической диаграмме состояния или диаграмме Jablonski , парадигме молекулярной фотохимии.
Эти возбужденные виды, либо S 1 , либо T 1 , имеют половину-пустую низкоэнергетическую орбиту и, следовательно, более окисляют, чем основное состояние. Но в то же время у них есть электрон в высокоэнергетической орбитале и, следовательно, более уменьшает . В целом, возбужденные виды склонны участвовать в процессах переноса электронов. [ 6 ]
Экспериментальная установка
[ редактировать ]
Фотохимические реакции требуют источника света, который излучает длины волн, соответствующий электронной переходу в реагенте. В ранних экспериментах (и в повседневной жизни) солнечный свет был источником света, хотя он полихроматический. [ 7 ] Ртутные лампы чаще встречаются в лаборатории. Лампы ртути низкого давления в основном испускаются при 254 нм. Для полихроматических источников диапазоны длины волны могут быть выбраны с использованием фильтров. Альтернативно, лазерные лучи обычно являются монохроматическими (хотя две или более длины волн могут быть получены с использованием нелинейной оптики ), а светодиоды имеют относительно узкую полосу , которую можно эффективно использовать, а также лампы рионета, чтобы получить приблизительно монохроматические балки.

Излучаемый свет должен достигать целевой функциональной группы, не будучи блокированным реактором, средней или другими присутствующими функциональными группами . Для многих приложений Quartz используется для реакторов, а также для содержания лампы. Pyrex поглощает длины волн короче 275 нм. Растворитель . является важным экспериментальным параметром Растворители являются потенциальными реагентами, и по этой причине хлорированные растворители избегают, поскольку связь C -CL может привести к хлорированию субстрата. Сильно поглощающие растворители не позволяют фотонам достигать субстрата. Растворители углеводородов поглощают только на коротких длин волн и, таким образом, предпочтительны для фотохимических экспериментов, требующих высокоэнергетических фотонов. Растворители, содержащие ненасыщение , поглощают на более длинных длин волн и могут с пользой отфильтровать короткие длины волны. Например, циклогексан и ацетон «отрезаны» (сильно поглощают) на длинах волн короче 215 и 330 нм соответственно.
Как правило, длина волны, используемая для индукции фотохимического процесса, выбирается на основе спектра поглощения реактивных видов, чаще всего максимум поглощения. За последние годы [ когда? ] Тем не менее, было продемонстрировано, что в большинстве реакций, образующих связь, спектр поглощения не позволяет выбирать оптимальную длину волны для достижения наивысшего выхода реакции на основе абсорбтивности. Это фундаментальное несоответствие между абсорбтивностью и реакционной способностью было выяснено с помощью так называемых фотохимических графиков . [ 8 ] [ 9 ]
Фотохимия в сочетании с химией потока
[ редактировать ]Фотохимия с непрерывным потоком предлагает несколько преимуществ по сравнению с пакетной фотохимией. Фотохимические реакции обусловлены количеством фотонов, способных активировать молекулы, вызывающие желаемую реакцию. Большое соотношение поверхности к объему к объему микрореактора максимизирует освещение и в то же время обеспечивает эффективное охлаждение, что уменьшает тепловые боковые продукты. [ 10 ]
Принципы
[ редактировать ]В случае фотохимических реакций свет обеспечивает энергию активации . Упрощенно, свет является одним из механизмов для обеспечения энергии активации, необходимой для многих реакций. Если используется лазерный свет, можно выборочно возбудить молекулу, чтобы получить желаемое электронное и колебательное состояние. [ 11 ] В равной степени излучение из конкретного состояния может быть избирательно контролироваться, предоставляя меру населения этого штата. Если химическая система находится при низком давлении, это позволяет ученым наблюдать распределение энергии продуктов химической реакции до того, как различия в энергии будут смазаны и усреднены с помощью повторных столкновений.
Поглощение фотона молекулой реагента может также позволить реакции возникать не только путем перемещения молекулы к необходимой энергии активации, но и путем изменения симметрии электронной конфигурации молекулы, обеспечивая непреодолимый путь реакции, как описано, как описано, как описано, как описано, как описано, как описано, как описано правилами отбора Вудворда - Хоффмана . [2+2] реакция циклоадрирования является одним из примеров перициклической реакции , которая может быть проанализирована с использованием этих правил или с соответствующей пограничной теорией молекулярной орбитали .
Некоторые фотохимические реакции на несколько порядков быстрее, чем тепловые реакции; Реакции ровно, пока 10 −9 секунды и связанные с ними процессы ровно, пока 10 −15 Секунды часто наблюдаются.
Фотон может быть поглощен непосредственно реагентом или фотосенсибилизатором , который поглощает фотон и передает энергию реагенту. Противоположный процесс, когда фотоэкссбранение деактивируется химическим реагентом, называется гашением .
Большинство фотохимических преобразований происходят через серию простых шагов, известных как первичные фотохимические процессы. Одним из распространенных примеров этих процессов является перенос протона возбужденного состояния.
Фотохимические реакции
[ редактировать ]Примеры фотохимических реакций
[ редактировать ]- Фотосинтез : Растения используют солнечную энергию для преобразования углекислого газа и воды в глюкозу и кислород .
- Образование человека витамина D при воздействии солнечного света.
- Биолюминесценция : например , в светлячках , фермент в животе катализирует реакцию, которая вызывает свет. [ 12 ]
- Полимеризации начались фотоинициаторами , которые разлагаются при поглощении света, чтобы получить свободные радикалы для радикальной полимеризации .
- Фотодеградация многих веществ, например, поливинилхлорид и FP . Спектеточные бутылки часто изготавливаются из затемненного стекла для защиты лекарств от фотодеградации.
- Фотохимические перестройки , например , фотоизомеризация , перенос атома водорода и фотохимические электроциклические реакции . [ 13 ] [ 14 ]
- Фотодинамическая терапия : свет используется для уничтожения опухолей путем действия синглетного кислорода, генерируемого фотосенсибилизированными реакциями триплетного кислорода . Типичные фотосенсибилизаторы включают тетрафенилпорфирин и метиленовый синий . Полученный синглетный кислород является агрессивным окислителем, способным преобразовать связи C -H в группы C -OH.
- Диазо процесс печати
- Фоторезистская технология , используемая при производстве микроэлектронных компонентов.
- Видение инициируется фотохимической реакцией родопсина . [ 15 ]
- Фотохимическое производство Toray ε-caprolactame. [ 16 ]
- Фотохимическое производство артемизинина , антималарийского препарата. [ 17 ] [ 18 ]
- Фотоалкилирование , используемое для индуцированного светом добавлением алкильных групп к молекулам.
- ДНК: фотодимеризация, приводящая к циклобутановому пиримидиновому диме. [ 19 ]
Органическая фотохимия
[ редактировать ]Примерами фотохимических органических реакций являются электроциклические реакции , радикальные реакции , фотоизомеризация и норландские реакции . [ 20 ] [ 21 ]
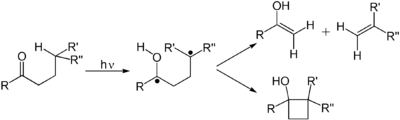
Алкены подвергаются многим важным реакциям, которые проходят через фотон-индуцированный π к π* переход. Первому электронному возбужденному состоянию алкена отсутствует π-связь , так что вращение вокруг связи C-C быстрое, а молекула вовлекается в реакции, не наблюдаемые термически. Эти реакции включают в себя изомеризацию цис-транс и циклическую обработку в другое (основное состояние) алкен, чтобы получить циклобутана производные . Изомеризация цис-транс-транс (поли) алкена участвует в сетчатке , компоненте механизма зрения . Димеризация алкенов имеет отношение к фотодаму ДНК , где димеры тимина наблюдаются при освещающей ДНК с помощью ультрафиолетового излучения. Такие димеры мешают транскрипции . , индуцированной фотохимически, Полезные эффекты солнечного света связаны с реакцией эргостерола давая витамин D. В реакции Demayo алкен реагирует с 1,3-дикетоном, реагирует через свой enol , чтобы получить 1,5-дикетон. Еще одна распространенная фотохимическая реакция Говарда Циммермана Перестановление .
В промышленном применении около 100 000 тонн бензилхлорида ежегодно готовит газофазной фотохимической реакцией толуола с хлором . [ 22 ] Свет поглощается молекулами хлора, при этом низкая энергия этого перехода указывает желтоватым цветом газа. Фотон индуцирует гомолиз связи Cl-Cl, а полученный хлорный радикал преобразует толуол в бензил-радикал:
- Cl 2 + Hν → 2 Cl ·
- C 6 H 5 CH 3 + Cl · → C 6 H 5 Ch 2 · + HCl
- C 6 H 5 Ch 2 · + Cl · → C 6 H 5 CH 2 Cl
Меркаптаны могут быть получены путем фотохимического добавления сероводорода (H 2 с) в альфа -олефины .
Неорганическая и органическая фотохимия
[ редактировать ]Координационные комплексы и органометаллические соединения также фотореактивны. Эти реакции могут повлечь за собой изомеризацию цис-транс. Чаще всего фотореакции приводят к диссоциации лигандов, поскольку фотон возбуждает электрон на металле с орбиталом, которая противоречит лигандам. Таким образом, металлические карбонилы , которые сопротивляются тепловой замене, подвергаются декарбонилированию при облучении ультрафиолетовым светом. Ультрафиолетовое излучение раствора молибдена THF гексакарбонила дает комплекс THF, который синтетически полезен:
- Mo (co) 6 + thf → (co) 5 (thf) + co
В связанной реакции фотолиз железа пентакарбонила дает диронно -неакарбонил (см. Рисунок):
- 2 Fe (co) 5 → Fe 2 (co) 9 + co
Выбор фотореактивных координационных комплексов может подвергаться процессам снижения окисления посредством переноса одного электрона. Эта перенос электрона может происходить во внутренней или внешней координационной сфере металла. [ 23 ]
Типы фотохимических реакций
[ редактировать ]Вот несколько различных типов фотохимических реакций -
- Фото-диссоциация: ab + h ν → a* + b*
- Фото индуцированные перестройки, изомеризация : a + h ν → b
- Фотография: A + B + H ν → AB + C
- Фото-сиденью: A + BC + H ν → AB + C
- Фото- окислительно-восстановительная реакция : a + b + h ν → a- + b +
Исторический
[ редактировать ]Хотя отбеливание уже давно практиковалось, первая фотохимическая реакция была описана Trommsdorff в 1834 году. [ 24 ] Он заметил, что кристаллы соединения α-сантонина , когда он подвергался воздействию солнечного света, стал желтым и лопнул. В исследовании 2007 года реакция была описана как последовательность трех этапов, происходящих в монокристалле. [ 25 ]
Первый шаг - это реакция перегруппировки на промежуточное соединение циклопентадиенона ( 2 ), вторая - димеризация в реакции диэлс -альдер ( 3 ), а третий - внутримолекулярное [2+2] циклоатделение ( 4 ). Эффект разрыва объясняется большим изменением объема кристалла при димеризации.
Специализированные журналы
[ редактировать ]- Журнал фотохимии и фотобиологии [1]
- Хемфотохим [2]
- Фотохимия и фотобиология [3]
- Фотохимические и фотобиологические науки [4]
- Фотохимия [5]
Учившиеся общества
[ редактировать ]- Межамериканское фотохимическое общество
- Европейская фотохимия Ассоциация
- Азиатская и океаническая фотохимия Ассоциация
Международные конференции
[ редактировать ]- Симпозиум IUPAC по фотохимии (биеннале)
- Международная конференция по фотохимитрии (биеннале)
Организации этих конференций проводятся Международным фондом фотохимии . [ 26 ]
Смотрите также
[ редактировать ]- Фотонная молекула
- Фотоэлектрохимическая ячейка
- Фотохимические логические ворота
- Фотосинтез
- Светозависимые реакции
- Список фотохимиков
- Одиночные фотонные источники
- Фотогеохимия
- Фотоэлектрический эффект
- Фотолиз
- План
Ссылки
[ редактировать ]- ^ Iupac , сборник химической терминологии , 2 -е изд. («Золотая книга») (1997). Онлайн -исправленная версия: (2006–) « Фотохимия ». два : 10.1351/goldbook.p04588
- ^ Glusac, Ksenija (2016). «Что свет когда -либо делал для химии?». Природная химия . 8 (8): 734–735. BIBCODE : 2016Natch ... 8..734G . doi : 10.1038/nchem.2582 . PMID 27442273 .
- ^ Дж. Кадет и Т. Дуки Фотохим. & Photobiol. Наука 2018 (17) стр. 1816-1841 Doi: 10.1039/c7pp00395a
- ^ Calvert, JG; Питтс, JN Photochemistry . Wiley & Sons: Нью-Йорк, США, 1966. Каталог Конгресса Номер: 65-24288
- ^ Фотохимия , веб -сайт Уильяма Реуша (Университет штата Мичиган), доступ к 26 июня 2016 года
- ^ Уэйн, CE; Уэйн, RP Photochemistry , 1 -е изд.; Издательство Оксфордского университета: Оксфорд, Великобритания, перепечатано 2005. ISBN 0-19-855886-4 .
- ^ Циаминик, Джакомо; Серебро, П. (май 1901 г.). «Эффекты химического освещения» . Отчеты немецкого химического общества . 34 (2): 2040–2046. Doi : 10.1002/cber.190103402118 . ISSN 0365-9496 .
- ^ Иршадин, Ишрат Мохамед; Уолден, Сара Л.; Вегенер, Мартин; Truong, Vinh x.; Фриш, Хендрик; Блинко, Джеймс П.; Барнер-Коволлик, Кристофер (2021-12-22). «За графиками действий в действии: глубокое понимание фотохимической реакционной способности» . Журнал Американского химического общества . 143 (50): 21113–21126. doi : 10.1021/jacs.1c09419 . ISSN 0002-7863 . PMID 34859671 . S2CID 244880552 .
- ^ Уолден, Сара Л.; Кэрролл, Джошуа А.; Unterreiner, Andreas-Neil; Барнер-Коволлик, Кристофер (2023-11-08). «Фотохимические графики действия показывают фундаментальное несоответствие между поглощаемостью и фотохимической реактивностью» . Продвинутая наука . 11 (3): E2306014. doi : 10.1002/Advs.202306014 . ISSN 2198-3844 . PMC 10797470 . PMID 37937391 .
- ^ Oelgemöller, Michael; Shvydkiv, Oksana (2011). «Последние достижения в области фотохимии микрофлоу» . Молекулы . 16 (9): 7522–7550. doi : 10.3390/molecules16097522 . PMC 6264405 . PMID 21894087 .
- ^ Мензель, Ян. Нобл, Бенджамин Б.; Лауэр, Андреа; Coote, Michelle L.; Блинко, Джеймс П.; Барнер-Коволлик, Кристофер (2017). «Зависимость длины волны от световых циклистов». Журнал Американского химического общества . 139 (44): 15812–15820. doi : 10.1021/jacs.7b08047 . HDL : 1885/209117 . ISSN 0002-7863 . PMID 29024596 .
- ^ Saunders, DS (2002-11-11). Часы насекомых, третье издание . Elsevier Science. п. 179. ISBN 0444504079 .
- ^ Lefebvre, Corentin; Хоффманн, Норберт (2021-01-01), Тёрёк, Бела; Schäfer, Christian (Eds.), «Восьмая глава - фотохимические перестройки в органическом синтезе и концепцию фотона как реагента без прослеживания» , Нетрадиционные методы активации в зеленых и устойчивых приложениях , достижения в зеленой и устойчивой химии, Elsevier, с. 283 –328, doi : 10.1016/b978-0-12-819009-8.00008-6 , ISBN 978-0-12-819009-8 , S2CID 234209169 , получен 2022-01-24
- ^ Lefebvre, Corentin; Фортье, Лукас; Хоффманн, Норберт (2020). «Фотохимические перестройки в гетероциклической химии» . Европейский журнал органической химии . 2020 (10): 1393–1404. doi : 10.1002/ejoc.201901190 . ISSN 1099-0690 . S2CID 204117942 .
- ^ Дугав, Кристоф (2006-10-06). Изомеризация CIS-транс в биохимии . Джон Уайли и сыновья. С. 56 . ISBN 9783527313044 .
- ^ Протти, Стефано; Фагнони, Маурицио (2009). «Солнечная сторона химии: зеленый синтез солнечным светом» . Фотохимические и фотобиологические науки . 8 (11): 1499–516. doi : 10.1039/b909128a . PMID 19862408 . S2CID 9323784 .
- ^ Пеплоу, Марк (17 апреля 2013 г.). «Sanofi запускает производство лекарств от малярии» . Мир химии .
- ^ Паддон, CJ; Westfall, PJ; Pitera, DJ; Бенджамин, К.; Фишер, К.; Макфи, Д.; Leavell, MD; Тай, А.; Main, A.; ENG, D.; Поличук, DR (2013). «Высокоуровневое полусинтетическое производство мощного противомалярийного артемизинина» . Природа . 496 (7446): 528–532. Bibcode : 2013natur.496..528p . doi : 10.1038/nature12051 . ISSN 0028-0836 . PMID 23575629 .
- ^ Циклобутан- типа пиримидиновых димеров в полинуклеотидах, RB Setlow, Science 1966 Vol. 153, с. 379, doi: 10.1126/science.153.3734.379
- ^ Клан, Петр; Wirz, Jakob (2009-03-23). Фотохимия органических соединений: от концепций до практики . Джон Уайли и сыновья. ISBN 978-1405190886 .
- ^ Турро, Николас Дж.; Рамамурти, В.; Scaiano, Juan C. (2010). Современная молекулярная фотохимия органических молекул . Университетские научные книги. ISBN 978-1891389252 .
- ^ Россберг, Манфред; Лендл, Вильгельм; Pfleiderer, Gerhard; Тёгель, Адольф; Дрехер, Эберхард-Людвиг; Лангер, Эрнст; Рассаэртс, Хайнц; Клейншмидт, Питер; Страк, Хайнц; Кук, Ричард; Бек, уве; Lipper, Карл-аугуст; Торкельсон, Теодор Р.; Лозер, Экхард; Beutel, Klaus K.; Человек, Тревор (2006). «Хлорированные углеводороды». Энциклопедия промышленной химии Уллмана . Doi : 10.1002/14356007.a06_233.pub2 . ISBN 3527306730 .
- ^ Бальзани, Винченцо; Carassiti, Vittorio (1970). Фотохимия координационных соединений . Нью -Йорк, Нью -Йорк: Academic Press, Inc. с. 37–39. ISBN 9780120772506 .
- ^ Дроммсдорф, Германн (1834). «О Сантонине» . Анналы фармации . 11 (2): 190–207. Doi : 10.1002/jlac.18340110207 .
- ^ Натараджан, Арункумар; Цай, CK; Хан, Саид I.; Маккаррен, Патрик; Houk, Kn; Гарсия-Гарибей, Мигель А. (2007). «Фоторагентность α-сантонина представляет собой реакцию с одним кристаллом до сингл-каристал: давно сохраняющийся секрет в твердотельной органической химии». Журнал Американского химического общества . 129 (32): 9846–9847. doi : 10.1021/ja073189o . PMID 17645337 .
- ^ IUPAC Symposia по фотохимии. Краткая история, С. Браславский, Chemistry International, март -апрель 2014 года.
Дальнейшее чтение
[ редактировать ]- Боуэн, EJ , химические аспекты света . Оксфорд: Clarendon Press , 1942. 2 -е издание , 1946.
- Фотохимия
