Регуляция экспрессии генов
Регуляция экспрессии генов , или регуляция генов , [1] включает широкий спектр механизмов, которые используются клетками для увеличения или уменьшения продукции специфических генных продуктов ( белка или РНК ). Сложные программы экспрессии генов широко наблюдаются в биологии, например, для запуска путей развития, реагирования на стимулы окружающей среды или адаптации к новым источникам пищи. Практически любой этап экспрессии генов можно модулировать: от инициации транскрипции до процессинга РНК и посттрансляционной модификации белка. Часто один ген-регулятор контролирует другой и так далее в сети генного регулирования .
Регуляция генов важна для вирусов , прокариот и эукариот , поскольку она повышает универсальность и адаптируемость организма , позволяя клетке экспрессировать белок, когда это необходимо. Хотя еще в 1951 году Барбара МакКлинток показала взаимодействие между двумя генетическими локусами, Активатором ( Ac ) и Диссоциатором ( Ds ), в формировании цвета семян кукурузы, первым открытием системы регуляции генов широко считается идентификация в 1961 году. - lac оперона , открытого Франсуа Жакобом и Жаком Моно , в котором некоторые ферменты, участвующие в метаболизме лактозы, экспрессируются E. coli только в присутствии лактозы и отсутствия глюкозы.
В многоклеточных организмах регуляция генов стимулирует клеточную дифференцировку и морфогенез у эмбриона, что приводит к созданию разных типов клеток, которые обладают разными профилями экспрессии генов из одной и той же последовательности генома . Хотя это не объясняет, как возникла регуляция генов, биологи-эволюционисты включают это в качестве частичного объяснения того, как эволюция работает на молекулярном уровне , и это занимает центральное место в науке эволюционной биологии развития («эво-дево»).
Регулируемые этапы экспрессии генов
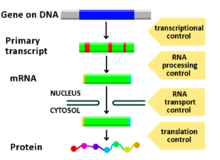
[ редактировать ]Любой этап экспрессии гена можно модулировать: от передачи сигнала до транскрипции и посттрансляционной модификации белка. Ниже приводится список стадий, на которых регулируется экспрессия генов, где наиболее широко используемым моментом является инициация транскрипции, первая стадия транскрипции: [ нужна ссылка ]
- Преобразование сигнала
- Хроматин , ремоделирование хроматина , хроматиновые домены
- Транскрипция
- Посттранскрипционная модификация
- Транспорт РНК
- Перевод
- деградация мРНК
Модификация ДНК
[ редактировать ]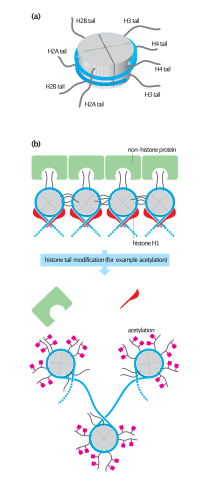
У эукариот расположение крупных участков ДНК может зависеть от структуры ее хроматина , которая может изменяться в результате модификаций гистонов , направляемых метилированием ДНК , нкРНК или ДНК-связывающего белка . Следовательно, эти модификации могут повышать или понижать экспрессию гена. Некоторые из этих модификаций, регулирующих экспрессию генов, передаются по наследству и называются эпигенетической регуляцией . [ нужна ссылка ]
Структурный
[ редактировать ]Транскрипция ДНК определяется ее структурой. В целом плотность его упаковки указывает на частоту транскрипции. Октамерные белковые комплексы, называемые гистонами, вместе с сегментом ДНК, намотанным вокруг восьми белков-гистонов (вместе называемых нуклеосомой), ответственны за величину суперспирализации ДНК, и эти комплексы могут быть временно модифицированы такими процессами, как фосфорилирование , или более навсегда. модифицируются такими процессами, как метилирование . Считается, что такие модификации ответственны за более или менее постоянные изменения уровней экспрессии генов. [2]
Химическая
[ редактировать ]Метилирование ДНК является распространенным методом подавления генов. ДНК обычно метилируется ферментами метилтрансферазой на цитозиновых нуклеотидах в динуклеотидной последовательности CpG (также называемой « островками CpG », когда она плотно сгруппирована). Анализ характера метилирования в данной области ДНК (которая может быть промотором) может быть достигнут с помощью метода, называемого бисульфитным картированием. Метилированные остатки цитозина в результате обработки не изменяются, тогда как неметилированные заменяются на урацил. Различия анализируются с помощью секвенирования ДНК или методов, разработанных для количественного определения SNP, таких как Pyrosequencing ( Biotage ) или MassArray ( Sequenom ), измеряющих относительные количества C/T в динуклеотиде CG. Считается, что аномальные паттерны метилирования участвуют в онкогенезе. [3]
Ацетилирование гистонов также является важным процессом транскрипции. Ферменты гистон-ацетилтрансферазы (HAT), такие как CREB-связывающий белок, также отделяют ДНК от гистонового комплекса, позволяя продолжить транскрипцию. Часто метилирование ДНК и деацетилирование гистонов работают вместе, вызывая молчание генов . Сочетание этих двух факторов, по-видимому, является сигналом для более плотной упаковки ДНК, что снижает экспрессию генов. [ нужна ссылка ]
Регуляция транскрипции
[ редактировать ]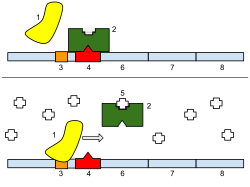
Таким образом, регуляция транскрипции контролирует, когда происходит транскрипция и сколько РНК создается. Транскрипция гена РНК-полимеразой может регулироваться несколькими механизмами. Факторы специфичности изменяют специфичность РНК-полимеразы для данного промотора или набора промоторов, делая более или менее вероятным ее связывание с ними (т.е. сигма-факторы, используемые в прокариотической транскрипции ). Репрессоры связываются с оператором , кодирующим последовательности на цепи ДНК, которые расположены близко к промоторной области или перекрывают ее, препятствуя продвижению РНК-полимеразы по цепи, тем самым препятствуя экспрессии гена. Изображение справа демонстрирует регуляцию репрессора в лаковом опероне. Общие факторы транскрипции помещают РНК-полимеразу в начало кодирующей белок последовательности, а затем высвобождают полимеразу для транскрипции мРНК. Активаторы усиливают взаимодействие между РНК-полимеразой и конкретным промотором , способствуя экспрессии гена. Активаторы делают это, увеличивая притяжение РНК-полимеразы к промотору, посредством взаимодействия с субъединицами РНК-полимеразы или косвенно, изменяя структуру ДНК. Энхансеры — это участки на спирали ДНК, которые связываются активаторами, чтобы замкнуть ДНК в петлю, доставляя определенный промотор к инициационному комплексу. Энхансеры гораздо чаще встречаются у эукариот, чем у прокариот, и на сегодняшний день существует лишь несколько примеров. [4] Сайленсеры — это участки последовательностей ДНК, которые при связывании с определенными факторами транскрипции могут подавлять экспрессию гена.
Регуляция РНК
[ редактировать ]РНК может быть важным регулятором активности генов, например, посредством микроРНК (миРНК), антисмысловой РНК или длинной некодирующей РНК (днРНК). LncRNA отличаются от мРНК в том смысле, что они имеют определенное субклеточное расположение и функции. Впервые было обнаружено, что они расположены в ядре и хроматине , а их локализация и функции в настоящее время весьма разнообразны. Некоторые из них все еще находятся в хроматине, где взаимодействуют с белками. Хотя эта днРНК в конечном итоге влияет на экспрессию генов при нейрональных заболеваниях, таких как болезни Паркинсона , Хантингтона и Альцгеймера , другие, такие как PNCTR (богатые пиримидином некодирующие транскрипторы), играют роль в раке легких . Учитывая их роль в заболеваниях, днРНК являются потенциальными биомаркерами и могут быть полезными мишенями для лекарств или генной терапии , хотя пока не существует одобренных препаратов, воздействующих на днРНК. Число днРНК в геноме человека остается плохо изученным, но по некоторым оценкам оно варьируется от 16 000 до 100 000 генов lnc. [5]
Эпигенетическая регуляция генов
[ редактировать ]
Эпигенетика относится к модификации генов, не меняющей последовательность ДНК или РНК. Эпигенетические модификации также являются ключевым фактором, влияющим на экспрессию генов . Они встречаются в геномной ДНК и гистонах , а их химические модификации более эффективно регулируют экспрессию генов. В клетках млекопитающих существует несколько модификаций ДНК (обычно метилирование ) и более 100 модификаций РНК». Эти модификации приводят к изменению связывания белка с ДНК и изменению стабильности РНК и эффективности трансляции . [6]
Особые случаи в биологии человека и заболеваниях
[ редактировать ]Регуляция транскрипции при раке
[ редактировать ]У позвоночных большинство промоторов генов содержат островок CpG с многочисленными сайтами CpG . [7] Когда многие сайты CpG промотора гена метилированы, ген замолкает. [8] Колоректальный рак обычно имеет от 3 до 6 мутаций водителя и от 33 до 66 мутаций автостопщика или пассажира. [9] Однако подавление транскрипции может иметь большее значение, чем мутация, в возникновении рака. Например, при колоректальном раке около 600–800 генов транскрипционно подавляются в результате метилирования CpG-островков (см. Регуляция транскрипции при раке ). Репрессия транскрипции при раке может также происходить за счет других эпигенетических механизмов, таких как изменение экспрессии микроРНК . [10] При раке молочной железы репрессия транскрипции BRCA1 может происходить чаще из-за сверхэкспрессии микроРНК-182, чем из-за гиперметилирования промотора BRCA1 (см. Низкая экспрессия BRCA1 при раке молочной железы и яичников ).
Регуляция транскрипции при зависимости
[ редактировать ]Одной из основных особенностей зависимости является ее устойчивость. Стойкие поведенческие изменения, по-видимому, обусловлены долговременными изменениями, возникающими в результате эпигенетических изменений, влияющих на экспрессию генов в определенных областях мозга. [11] Злоупотребление наркотиками вызывает три типа эпигенетических изменений в мозге. Это (1) , ацетилирование и метилирование гистонов (2) метилирование ДНК в CpG и (3) эпигенетическое подавление или усиление микроРНК сайтах . [11] [12] ( см. в разделе «Эпигенетика кокаиновой зависимости Некоторые подробности ».)
Хроническое потребление никотина у мышей изменяет эпигенетический контроль клеток головного мозга за экспрессией генов посредством ацетилирования гистонов . Это увеличивает экспрессию в мозге белка FosB, важного при зависимости. [13] Сигаретная зависимость также изучалась примерно у 16 000 человек, включая никогда не куривших, нынешних курильщиков и тех, кто бросил курить на срок до 30 лет. [14] В клетках крови более 18 000 сайтов CpG (из примерно 450 000 проанализированных сайтов CpG в геноме) часто изменяли метилирование у нынешних курильщиков. Эти сайты CpG встречаются более чем в 7000 генах, или примерно в трети известных генов человека. Большинство дифференциально метилированных сайтов CpG вернулись к уровню никогда не куривших в течение пяти лет после прекращения курения. Однако 2568 CpG среди 942 генов оставались дифференциально метилированными у бывших и никогда не куривших. Такие оставшиеся эпигенетические изменения можно рассматривать как «молекулярные шрамы». [12] это может повлиять на экспрессию генов.
На моделях грызунов наркотики, вызывающие злоупотребление, включая кокаин, [15] метамфетамин, [16] [17] алкоголь [18] и продукты табачного дыма, [19] все они вызывают повреждение ДНК в мозге. Во время репарации повреждений ДНК некоторые отдельные события репарации могут изменить метилирование ДНК и/или ацетилирование или метилирование гистонов в местах повреждения и, таким образом, могут способствовать образованию эпигенетического рубца на хроматине. [20]
Такие эпигенетические шрамы, вероятно, способствуют стойким эпигенетическим изменениям, возникающим при зависимости.
Регуляция транскрипции в обучении и памяти
[ редактировать ]
У млекопитающих метилирование цитозина (см. рисунок) в ДНК является основным регуляторным медиатором. Метилированные цитозины в основном встречаются в динуклеотидных последовательностях, где за цитозином следует гуанин, сайт CpG . Общее количество CpG-сайтов в геноме человека составляет около 28 миллионов. [21] и обычно около 70% всех сайтов CpG содержат метилированный цитозин. [22]
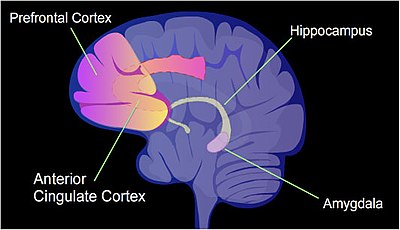
У крысы болезненный опыт обучения, контекстуальная обусловленность страхом , может привести к появлению на всю жизнь страшных воспоминаний после одного тренировочного мероприятия. [23] Метилирование цитозина изменено в промоторных областях примерно 9,17% всех генов в ДНК нейронов гиппокампа крысы, подвергшейся кратковременному воздействию страха . [24] Гиппокамп — это место, где изначально хранятся новые воспоминания.
Метилирование CpG в промоторной области гена подавляет транскрипцию. [25] в то время как метилирование CpG в теле гена увеличивает экспрессию. [26] Ферменты ТЕТ играют центральную роль в деметилировании метилированных цитозинов. Деметилирование CpG в промоторе гена под действием фермента TET увеличивает транскрипцию гена. [27]
контекстуальное кондиционирование страха Когда к крысе применяется крысы возникает более 5000 дифференциально метилированных областей (DMR) (по 500 нуклеотидов каждый) , в нейронном геноме гиппокампа как через один час, так и через 24 часа после кондиционирования в гиппокампе. [24] Это вызывает активацию около 500 генов (часто из-за деметилирования сайтов CpG в области промотора) и подавление активности около 1000 генов (часто из-за вновь образованного 5-метилцитозина в сайтах CpG в области промотора). Паттерн индуцированных и репрессированных генов в нейронах, по-видимому, обеспечивает молекулярную основу для формирования первых временных воспоминаний об этом тренировочном событии в гиппокампе мозга крысы. [24]
Посттранскрипционная регуляция
[ редактировать ]После транскрипции ДНК и образования мРНК должна существовать какая-то регуляция того, насколько мРНК транслируется в белки. Клетки делают это путем модуляции кэпирования, сплайсинга, добавления поли(А)-хвоста, скорости ядерного экспорта, специфичной для последовательности, и, в некоторых контекстах, секвестрации транскрипта РНК. Эти процессы происходят у эукариот, но не у прокариот. Эта модуляция является результатом действия белка или транскрипта, который, в свою очередь, регулируется и может иметь сродство к определенным последовательностям.
Три основных нетранслируемых региона и микроРНК
[ редактировать ]Три основных нетранслируемых участка (3'-UTR) информационных РНК (мРНК) часто содержат регуляторные последовательности, которые посттранскрипционно влияют на экспрессию генов. [28] Такие 3'-UTR часто содержат как сайты связывания микроРНК (миРНК), так и регуляторные белки. Связываясь со специфическими сайтами внутри 3'-UTR, микроРНК могут снижать экспрессию генов различных мРНК, либо ингибируя трансляцию, либо непосредственно вызывая деградацию транскрипта. 3'-UTR также может иметь участки сайленсера, которые связывают белки-репрессоры, ингибирующие экспрессию мРНК.
3'-UTR часто содержит элементы ответа микроРНК (MRE) . MRE — это последовательности, с которыми связываются микроРНК. Это преобладающие мотивы в 3'-UTR. Среди всех регуляторных мотивов в 3'-UTR (например, включая сайленсеры), MRE составляют около половины мотивов.
По состоянию на 2014 год miRBase веб-сайт [29] архив последовательностей и аннотаций микроРНК содержит 28 645 записей о 233 биологических видах. Из них 1881 микроРНК находились в аннотированных локусах микроРНК человека. Было предсказано, что микроРНК содержат в среднем около четырехсот целевых мРНК (влияющих на экспрессию нескольких сотен генов). [30] Фрейдман и др. [30] подсчитали, что> 45 000 целевых сайтов микроРНК в 3'-UTR мРНК человека консервативны выше фоновых уровней, и> 60% генов, кодирующих белки человека, находились под селективным давлением для поддержания спаривания с микроРНК.
Прямые эксперименты показывают, что одна микроРНК может снизить стабильность сотен уникальных мРНК. [31] Другие эксперименты показывают, что одна микроРНК может подавлять продукцию сотен белков, но эта репрессия часто бывает относительно легкой (менее чем в 2 раза). [32] [33]
Эффекты нарушения регуляции экспрессии генов микроРНК, по-видимому, важны при раке. [34] Например, в исследовании 2015 года при раке желудочно-кишечного тракта девять микроРНК были идентифицированы как эпигенетически измененные и эффективные в подавлении ферментов репарации ДНК. [35]
Эффекты нарушения регуляции экспрессии генов микроРНК также кажутся важными при нервно-психических расстройствах, таких как шизофрения , биполярное расстройство , большое депрессивное расстройство , болезнь Паркинсона , болезнь Альцгеймера и расстройства аутистического спектра . [36] [37] [38]
Регулирование перевода
[ редактировать ]Трансляция мРНК также может контролироваться рядом механизмов, преимущественно на уровне инициации. Рекрутирование малой рибосомальной субъединицы действительно может модулироваться вторичной структурой мРНК, связыванием антисмысловой РНК или связыванием белка. Как у прокариот, так и у эукариот существует большое количество РНК-связывающих белков, которые часто направляются к своей целевой последовательности посредством вторичной структуры транскрипта, которая может меняться в зависимости от определенных условий, например температуры или присутствия лиганда (аптамера). . Некоторые транскрипты действуют как рибозимы и саморегулируют свою экспрессию.
Примеры регуляции генов
[ редактировать ]- Индукция фермента представляет собой процесс, при котором молекула (например, лекарство) индуцирует (т.е. инициирует или усиливает) экспрессию фермента.
- Индукция белков теплового шока у плодовой мушки Drosophila melanogaster .
- Оперон Lac — интересный пример того, как можно регулировать экспрессию генов.
- Вирусы, несмотря на то, что имеют всего несколько генов, обладают механизмами регулирования экспрессии своих генов, обычно на ранней и поздней фазе, с использованием коллинеарных систем, регулируемых антитерминаторами ( фаг лямбда ) или модуляторами сплайсинга ( ВИЧ ).
- Gal4 является активатором транскрипции, который контролирует экспрессию GAL1, GAL7 и GAL10 (все из которых кодируют метаболизм галактозы у дрожжей). Система GAL4/UAS использовалась у множества организмов разных типов для изучения экспрессии генов. [39]
Биология развития
[ редактировать ]Большое количество изученных регуляторных систем взято из биологии развития . Примеры включают в себя:
- Коллинеарность кластера генов Hox с их вложенным передне-задним паттерном.
- Генерация паттерна руки (цифры - межпальцы): градиент звукового ежа (секретируемый индуцирующий фактор) от зоны поляризующей активности в конечности, который создает градиент активного Gli3, который активирует Гремлина, который ингибирует BMP, также секретируемые в конечности, приводит к формированию знакопеременного характера активности в результате этой реакционно-диффузионной системы .
- Сомитогенез — образование сегментов (сомитов) из единой ткани (пресомитной мезодермы ). Они формируются последовательно от переднего к заднему. Это достигается у амниот, возможно, посредством двух противоположных градиентов: ретиноевой кислоты в переднем (волновом фронте) и Wnt и Fgf в заднем, соединенных с осциллирующим паттерном (часы сегментации), состоящим из FGF + Notch и Wnt в противофазе. [40]
- Определение пола в соме дрозофилы требует определения соотношения аутосомных генов и генов, кодируемых половой хромосомой , что приводит к выработке бесполого фактора сплайсинга у самок, что приводит к образованию женской изоформы двойного пола. [41]
Схема
[ редактировать ]Повышающая и понижающая регуляция
[ редактировать ]Повышающая регуляция — это процесс, происходящий внутри клетки и запускаемый сигналом (исходящим внутри или снаружи клетки), который приводит к усилению экспрессии одного или нескольких генов и, как следствие, белков, кодируемых этими генами. И наоборот, понижающая регуляция — это процесс, приводящий к снижению экспрессии генов и соответствующих белков.
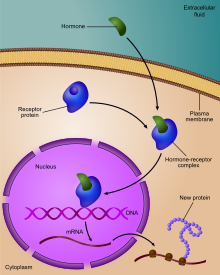
- Повышающая регуляция происходит, например, когда в клетке не хватает какого-либо рецептора. В этом случае больше рецепторного белка синтезируется и транспортируется к мембране клетки и, таким образом, чувствительность клетки возвращается к норме, восстанавливая гомеостаз .
- Снижение регуляции происходит, например, когда клетка подвергается чрезмерной стимуляции нейротрансмиттером , гормоном или лекарством в течение длительного периода времени, и экспрессия рецепторного белка снижается, чтобы защитить клетку (см. также тахифилаксию ).
Индуцибельные и репрессируемые системы
[ редактировать ]
Регуляцию генов можно резюмировать реакцией соответствующей системы:
- Индуцибельные системы. Индуцибельная система выключена, если не присутствует какая-либо молекула (называемая индуктором), которая обеспечивает экспрессию генов. Говорят, что молекула «вызывает экспрессию». То, каким образом это происходит, зависит от механизмов контроля, а также от различий между прокариотическими и эукариотическими клетками.
- Репрессируемые системы. Репрессируемая система активна, за исключением присутствия какой-либо молекулы (называемой корепрессором), которая подавляет экспрессию генов. Говорят, что молекула «подавляет экспрессию». То, каким образом это происходит, зависит от механизмов контроля, а также от различий между прокариотическими и эукариотическими клетками.
Система GAL4/UAS является примером как индуцируемой, так и репрессируемой системы. Gal4 связывается с вышележащей активационной последовательностью (UAS), чтобы активировать транскрипцию кассеты GAL1/GAL7/GAL10. С другой стороны, ответ MIG1 на присутствие глюкозы может ингибировать GAL4 и, следовательно, останавливать экспрессию кассеты GAL1/GAL7/GAL10. [42]
Теоретические схемы
[ редактировать ]- Репрессор/индуктор: активация сенсора приводит к изменению экспрессии гена.
- отрицательная обратная связь: генный продукт прямо или косвенно подавляет собственную продукцию, что может привести к
- сохранение уровней транскриптов постоянными/пропорциональными фактору
- подавление неконтролируемых реакций в сочетании с петлей положительной обратной связи
- создание осциллятора, воспользовавшись задержкой транскрипции и трансляции, учитывая, что период полураспада мРНК и белка короче
- положительная обратная связь: генный продукт прямо или косвенно регулирует собственную продукцию, что может привести к
- усиление сигнала
- бистабильные переключатели, когда два гена ингибируют друг друга и оба имеют положительную обратную связь.
- генерация шаблона
Методы исследования
[ редактировать ]
В целом, в большинстве экспериментов по изучению дифференциальной экспрессии использовались целоклеточные экстракты РНК, называемые равновесными уровнями, чтобы определить, какие гены изменились и насколько. Однако они не информативны о том, где произошла регуляция, и могут маскировать конфликтующие регуляторные процессы ( см. Посттранскрипционная регуляция ), но они по-прежнему наиболее часто анализируются ( количественная ПЦР и микроматрица ДНК ).
При изучении экспрессии генов существует несколько методов рассмотрения различных этапов. У эукариот к ним относятся:
- Локальное хроматиновое окружение региона можно определить с помощью анализа ChIP-чипа путем выявления РНК-полимеразы II , гистона 3 модификаций , белка группы Trithorax , белка группы Polycomb или любого другого ДНК-связывающего элемента, к которому доступно хорошее антитело. .
- Эпистатические взаимодействия можно исследовать с помощью синтетического генетического массива. анализа
- Из-за посттранскрипционной регуляции скорость транскрипции и общий уровень РНК значительно различаются. Для измерения скорости транскрипции можно провести ядерный анализ и разрабатываются новые высокопроизводительные методы, использующие тиоловую маркировку вместо радиоактивности . [43]
- Из ядра выходит только 5% РНК, полимеризованной в ядре. [44] и деградируют не только интроны, абортивные продукты и бессмысленные транскрипты. Таким образом, различия в ядерном и цитоплазматическом уровнях можно увидеть, разделив две фракции путем мягкого лизиса. [45]
- Альтернативный сплайсинг можно анализировать с помощью массива сплайсинга или массива мозаики ( см. Микрочип ДНК ).
- Вся РНК in vivo образует комплексы РНП . Количество транскриптов, связанных с конкретным белком, также можно проанализировать с помощью RIP-Chip . Например, DCP2 укажет на секвестрированный белок; рибосом связывание полисом ) и индикация транскриптов, активных в транскрипции (хотя в некоторых лабораториях все еще популярен более устаревший метод, называемый фракционированием
- Уровни белка можно анализировать с помощью масс-спектрометрии , которую можно сравнивать только с количественными данными ПЦР , поскольку данные микрочипов являются относительными, а не абсолютными.
- Скорость деградации РНК и белка измеряют с помощью ингибиторов транскрипции ( актиномицин D или α-аманитин ) или ингибиторов трансляции ( циклогексимид ) соответственно.
См. также
[ редактировать ]- Искусственные факторы транскрипции (небольшие молекулы, имитирующие белок фактора транскрипции)
- Сотовая модель
- Консервативная некодирующая последовательность ДНК
- Энхансер (генетика)
- Генная структура
- Пространственно-временная экспрессия генов
- Системы регуляторных генов глюкозилтрансфераз (Rgg/SHP)
Примечания и ссылки
[ редактировать ]- ^ «Можно ли включать и выключать гены в клетках?» . Домашний справочник по генетике .
- ^ Белл Дж.Т., Пай А.А., Пикрелл Дж.К., Гаффни Д.Дж., Пике-Режи Р., Дегнер Дж.Ф. и др. (2011). «Схемы метилирования ДНК связаны с генетическими изменениями и вариациями экспрессии генов в клеточных линиях HapMap» . Геномная биология . 12 (1): Р10. дои : 10.1186/gb-2011-12-1-r10 . ПМК 3091299 . ПМИД 21251332 .
- ^ Вертино П.М., Спилларе Э.А., Харрис К.С., Бэйлин С.Б. (апрель 1993 г.). «Измененные закономерности хромосомного метилирования сопровождают индуцированную онкогенами трансформацию эпителиальных клеток бронхов человека» (PDF) . Исследования рака . 53 (7): 1684–9. ПМИД 8453642 .
- ^ Остин С., Диксон Р. (июнь 1992 г.). «Прокариотический энхансер-связывающий белок NTRC обладает АТФазной активностью, которая зависит от фосфорилирования и ДНК» . Журнал ЭМБО . 11 (6): 2219–28. дои : 10.1002/j.1460-2075.1992.tb05281.x . ПМК 556689 . ПМИД 1534752 .
- ^ Стателло Л., Го С.Дж., Чен Л.Л., Уарте М. (февраль 2021 г.). «Регуляция гена длинными некодирующими РНК и его биологические функции» . Обзоры природы. Молекулярно-клеточная биология . 22 (2): 96–118. дои : 10.1038/s41580-020-00315-9 . ISSN 1471-0072 . ПМЦ 7754182 . ПМИД 33353982 .
- ^ Кан Р.Л., Чен Дж., Саллам Т. (июль 2021 г.). «Перекресток между эпитранскриптомными и эпигенетическими механизмами регуляции генов» . Тенденции в генетике . 38 (2): 182–193. дои : 10.1016/j.tig.2021.06.014 . ПМК 9093201 . ПМИД 34294427 . S2CID 236200223 .
- ^ Саксонов С., Берг П., Брютлаг Д.Л. (январь 2006 г.). «Полногеномный анализ динуклеотидов CpG в геноме человека позволяет выделить два различных класса промоторов» . Труды Национальной академии наук Соединенных Штатов Америки . 103 (5): 1412–7. Бибкод : 2006PNAS..103.1412S . дои : 10.1073/pnas.0510310103 . ПМЦ 1345710 . ПМИД 16432200 .
- ^ Птица А (январь 2002 г.). «Схемы метилирования ДНК и эпигенетическая память» . Гены и развитие . 16 (1): 6–21. дои : 10.1101/gad.947102 . ПМИД 11782440 .
- ^ Фогельштейн Б., Пападопулос Н., Велкулеску В.Е., Чжоу С., Диас Л.А., Кинцлер К.В. (март 2013 г.). «Пейзажи генома рака» . Наука . 339 (6127): 1546–58. Бибкод : 2013Sci...339.1546V . дои : 10.1126/science.1235122 . ПМК 3749880 . ПМИД 23539594 .
- ^ Тесситоре А., Чиччарелли Г., Дель Веккьо Ф., Гаджиано А., Верцелла Д., Фискьетти М. и др. (2014). «МикроРНК в сети повреждения/восстановления ДНК и раке» . Международный журнал геномики . 2014 : 820248. doi : 10.1155/2014/820248 . ПМЦ 3926391 . ПМИД 24616890 .
- ^ Перейти обратно: а б Nestler EJ (январь 2014 г.). «Эпигенетические механизмы наркомании» . Нейрофармакология . 76 Часть Б: 259–68. doi : 10.1016/j.neuropharm.2013.04.004 . ПМЦ 3766384 . ПМИД 23643695 .
- ^ Перейти обратно: а б Робисон А.Дж., Нестлер Э.Дж. (октябрь 2011 г.). «Транскрипционные и эпигенетические механизмы зависимости» . Обзоры природы. Нейронаука . 12 (11): 623–37. дои : 10.1038/nrn3111 . ПМЦ 3272277 . ПМИД 21989194 .
- ^ Левин А., Хуанг Ю., Дрисальди Б., Гриффин Е.А., Поллак Д.Д., Сюй С. и др. (ноябрь 2011 г.). «Молекулярный механизм шлюзового препарата: эпигенетические изменения, инициированные экспрессией гена никотина кокаином» . Наука трансляционной медицины . 3 (107): 107ра109. doi : 10.1126/scitranslmed.3003062 . ПМК 4042673 . ПМИД 22049069 .
- ^ Джоханес Р., Джаст А.С., Мариони Р.Э., Пиллинг Л.К., Рейнольдс Л.М., Мандавия П.Р. и др. (октябрь 2016 г.). «Эпигенетические признаки курения сигарет» . Кровообращение: сердечно-сосудистая генетика . 9 (5): 436–447. doi : 10.1161/CIRCGENETICS.116.001506 . ПМК 5267325 . ПМИД 27651444 .
- ^ де Соуза М.Ф., Гонсалес Т.А., Стейнмец А., Моура Дж., Саффи Дж., Гомес Р., Баррос Х.М. (апрель 2014 г.). «Кокаин вызывает повреждение ДНК в различных областях мозга самок крыс при различных гормональных условиях». Клиническая и экспериментальная фармакология и физиология . 41 (4): 265–9. дои : 10.1111/1440-1681.12218 . ПМИД 24552452 . S2CID 20849951 .
- ^ Джонсон З., Вентерс Дж., Гуаррачи Ф.А., Зеваил-Фут М. (июнь 2015 г.). «Метамфетамин вызывает повреждение ДНК в определенных областях мозга самок крыс». Клиническая и экспериментальная фармакология и физиология . 42 (6): 570–5. дои : 10.1111/1440-1681.12404 . ПМИД 25867833 . S2CID 24182756 .
- ^ Токунага И., Исигами А., Кубо С., Готода Т., Китамура О. (август 2008 г.). «Пероксидативное повреждение ДНК и апоптоз в мозге крыс, обработанных метамфетамином» . Журнал медицинских расследований . 55 (3–4): 241–5. дои : 10.2152/jmi.55.241 . ПМИД 18797138 .
- ^ Рултен С.Л., Ходдер Э., Рипли Т.Л., Стивенс Д.Н., Мейн Л.В. (июль 2008 г.). «Алкоголь вызывает повреждение ДНК и белок D2 анемии Фанкони, вовлекающий FANCD2 в пути реакции на повреждение ДНК в мозге» . Алкоголизм: клинические и экспериментальные исследования . 32 (7): 1186–96. дои : 10.1111/j.1530-0277.2008.00673.x . ПМИД 18482162 .
- ^ Адхами Н., Чен Ю., Мартинс-Грин М. (октябрь 2017 г.). «Биомаркеры заболевания могут быть обнаружены у мышей уже через 4 недели после начала воздействия табачного дыма от третьих рук, эквивалентного тем, которые обнаруживаются в домах курильщиков» . Клиническая наука . 131 (19): 2409–2426. дои : 10.1042/CS20171053 . ПМИД 28912356 .
- ^ Дабин Дж., Фортуни А., Polo SE (июнь 2016 г.). «Поддержание эпигенома в ответ на повреждение ДНК» . Молекулярная клетка . 62 (5): 712–27. doi : 10.1016/j.molcel.2016.04.006 . ПМК 5476208 . ПМИД 27259203 .
- ^ Левквист С., Додд И.Б., Снеппен К., Хаертер Дж.О. (июнь 2016 г.). «Метилирование ДНК в эпигеномах человека зависит от локальной топологии сайтов CpG» . Исследования нуклеиновых кислот . 44 (11): 5123–32. дои : 10.1093/нар/gkw124 . ПМЦ 4914085 . ПМИД 26932361 .
- ^ Джаббари К., Бернарди Дж. (май 2004 г.). «Метилирование цитозина и частоты CpG, TpG (CpA) и TpA». Джин . 333 : 143–9. дои : 10.1016/j.gene.2004.02.043 . ПМИД 15177689 .
- ^ Ким Джей-Джей, Юнг М.В. (2006). «Нейральные цепи и механизмы, участвующие в формировании павловского страха: критический обзор» . Неврологические и биоповеденческие обзоры . 30 (2): 188–202. doi : 10.1016/j.neubiorev.2005.06.005 . ПМЦ 4342048 . ПМИД 16120461 .
- ^ Перейти обратно: а б с Дьюк К.Г., Кеннеди Эй.Дж., Гэвин К.Ф., Дэй Дж.Дж., Суэтт Дж.Д. (июль 2017 г.). «Эпигеномная реорганизация в гиппокампе, зависящая от опыта» . Обучение и память . 24 (7): 278–288. дои : 10.1101/lm.045112.117 . ПМК 5473107 . ПМИД 28620075 .
- ^ Вебер М., Хеллманн И., Стадлер М.Б., Рамос Л., Паабо С., Ребхан М., Шубелер Д. (апрель 2007 г.). «Распространение, потенциал молчания и эволюционное влияние метилирования ДНК промотора в геноме человека». Нат. Жене . 39 (4): 457–66. дои : 10.1038/ng1990 . ПМИД 17334365 . S2CID 22446734 .
- ^ Ян X, Хан Х, Де Карвалью Д.Д., Лэй Ф.Д., Джонс П.А., Лян Г. (октябрь 2014 г.). «Метилирование тел генов может изменить экспрессию генов и является терапевтической мишенью при раке» . Раковая клетка . 26 (4): 577–90. дои : 10.1016/j.ccr.2014.07.028 . ПМК 4224113 . ПМИД 25263941 .
- ^ Маедер М.Л., Ангстман Дж.Ф., Ричардсон М.Е., Линдер С.Дж., Касио В.М., Цай С.К., Хо К.Х., Сандер Дж.Д., Рейон Д., Бернштейн Б.Е., Костелло Дж.Ф., Уилкинсон М.Ф., Йонг Дж.К. (декабрь 2013 г.). «Направленное деметилирование ДНК и активация эндогенных генов с использованием программируемых слитых белков TALE-TET1» . Нат. Биотехнология . 31 (12): 1137–42. дои : 10.1038/nbt.2726 . ПМЦ 3858462 . ПМИД 24108092 .
- ^ Огородников А, Каргаполова Ю, Данквардт С (июнь 2016 г.). «Процессинг и расширение транскриптома на 3'-конце мРНК в норме и при заболеваниях: поиск правильного конца» . Архив Пфлюгерса . 468 (6): 993–1012. дои : 10.1007/s00424-016-1828-3 . ПМЦ 4893057 . ПМИД 27220521 .
- ^ miRBase.org
- ^ Перейти обратно: а б Фридман Р.К., Фарх К.К., Бердж CB, Бартель Д.П. (январь 2009 г.). «Большинство мРНК млекопитающих являются консервативными мишенями микроРНК» . Геномные исследования . 19 (1): 92–105. дои : 10.1101/гр.082701.108 . ПМЦ 2612969 . ПМИД 18955434 .
- ^ Лим Л.П., Лау Н.К., Гарретт-Энгеле П., Гримсон А., Шелтер Дж.М., Касл Дж. и др. (февраль 2005 г.). «Анализ на микрочипах показывает, что некоторые микроРНК подавляют большое количество целевых мРНК». Природа . 433 (7027): 769–73. Бибкод : 2005Natur.433..769L . дои : 10.1038/nature03315 . ПМИД 15685193 . S2CID 4430576 .
- ^ Зельбах М., Шванхойссер Б., Тирфельдер Н., Фанг З., Ханин Р., Раевски Н. (сентябрь 2008 г.). «Широко распространенные изменения в синтезе белка, вызванные микроРНК». Природа . 455 (7209): 58–63. Бибкод : 2008Natur.455...58S . дои : 10.1038/nature07228 . ПМИД 18668040 . S2CID 4429008 .
- ^ Пэк Д., Виллен Дж., Шин С., Камарго Ф.Д., Гиги С.П., Бартель Д.П. (сентябрь 2008 г.). «Влияние микроРНК на выход белка» . Природа . 455 (7209): 64–71. Бибкод : 2008Natur.455...64B . дои : 10.1038/nature07242 . ПМК 2745094 . ПМИД 18668037 .
- ^ Палмеро Э.И., де Кампос С.Г., Кампос М., де Соуза Н.К., Геррейру И.Д., Карвалью А.Л., Маркес М.М. (июль 2011 г.). «Механизмы и роль дерегуляции микроРНК в возникновении и прогрессировании рака» . Генетика и молекулярная биология . 34 (3): 363–70. дои : 10.1590/S1415-47572011000300001 . ПМК 3168173 . ПМИД 21931505 .
- ^ Бернштейн С., Бернштейн Х. (май 2015 г.). «Эпигенетическое снижение репарации ДНК при прогрессировании рака желудочно-кишечного тракта» . Всемирный журнал желудочно-кишечной онкологии . 7 (5): 30–46. дои : 10.4251/wjgo.v7.i5.30 . ПМЦ 4434036 . ПМИД 25987950 .
- ^ Маффиолетти Э., Тардито Д., Дженнарелли М., Боккио-Кьяветто Л. (2014). «Микрошпионы от мозга к периферии: новые данные исследований микроРНК при нервно-психических расстройствах» . Границы клеточной нейронауки . 8 : 75. дои : 10.3389/fncel.2014.00075 . ПМЦ 3949217 . ПМИД 24653674 .
- ^ Меллиос Н., Сур М. (2012). «Новая роль микроРНК при шизофрении и расстройствах аутистического спектра» . Границы в психиатрии . 3 : 39. doi : 10.3389/fpsyt.2012.00039 . ПМК 3336189 . ПМИД 22539927 .
- ^ Гиган М., Кэрнс MJ (август 2015 г.). «МикроРНК и посттранскрипционная дисрегуляция в психиатрии» . Биологическая психиатрия . 78 (4): 231–9. doi : 10.1016/j.biopsych.2014.12.009 . hdl : 1959.13/1335073 . ПМИД 25636176 .
- ^ Барнетт Дж. А. (июль 2004 г.). «История исследований дрожжей 7: ферментативная адаптация и регуляция» . Дрожжи . 21 (9): 703–46. дои : 10.1002/да.1113 . ПМИД 15282797 . S2CID 36606279 .
- ^ Dequéant ML, Pourquié O (май 2008 г.). «Сегментарное паттернирование эмбриональной оси позвоночных». Обзоры природы. Генетика . 9 (5): 370–82. дои : 10.1038/nrg2320 . ПМИД 18414404 . S2CID 2526914 .
- ^ Гилберт С.Ф. (2003). Биология развития, 7-е изд., Сандерленд, Массачусетс: Sinauer Associates, 65–6. ISBN 0-87893-258-5 .
- ^ Нелин Дж.О., Карлберг М., Ронне Х. (ноябрь 1991 г.). «Контроль дрожжевых генов GAL с помощью репрессора MIG1: транскрипционный каскад в ответе на глюкозу» . Журнал ЭМБО . 10 (11): 3373–7. дои : 10.1002/j.1460-2075.1991.tb04901.x . ПМК 453065 . ПМИД 1915298 .
- ^ Чидл С., Фан Дж., Чо-Чунг Ю.С., Вернер Т., Рэй Дж., До Л. и др. (май 2005 г.). «Контроль экспрессии генов во время активации Т-клеток: альтернативное регулирование транскрипции мРНК и стабильности мРНК» . БМК Геномика . 6:75 . дои : 10.1186/1471-2164-6-75 . ПМЦ 1156890 . ПМИД 15907206 .
- ^ Джексон Д.А., Помбо А., Иборра Ф (февраль 2000 г.). «Баланс транскрипции: анализ метаболизма ядерной РНК в клетках млекопитающих» . Журнал ФАСЭБ . 14 (2): 242–54. дои : 10.1096/fasebj.14.2.242 . ПМИД 10657981 . S2CID 23518786 .
- ^ Шванекамп Дж.А., Сартор М.А., Карьяла С., Халблейб Д., Медведович М., Томлинсон Ч.Р. (2006). «Общегеномный анализ показывает, что диоксин по-разному влияет на уровни ядерной и цитоплазматической РНК». Biochimica et Biophysical Acta (BBA) – Структура и экспрессия генов . 1759 (8–9): 388–402. дои : 10.1016/j.bbaexp.2006.07.005 . ПМИД 16962184 .
Библиография
[ редактировать ]- Латчман, Дэвид С. (2005). Регуляция генов: взгляд на эукариоты . Психология Пресс. ISBN 978-0-415-36510-9 .
Внешние ссылки
[ редактировать ]- База данных факторов транскрипции растений и платформа данных и анализа регуляции транскрипции растений
- Регуляция экспрессии генов (MeSH) в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- ChIPBase Открытая база данных для декодирования сетей регуляции транскрипции некодирующих РНК и генов, кодирующих белки, на основе данных ChIP-seq.