Тучная клетка
| Тучная клетка | |
|---|---|
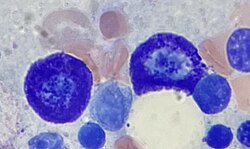 Две тучные клетки в костном мозге | |
| Подробности | |
| Система | Иммунная система |
| Идентификаторы | |
| латинский | мастоцит |
| МеШ | D008407 |
| ТД | Х2.00.03.0.01010 |
| ФМА | 66784 |
| Анатомические термины микроанатомии | |
( Тучная клетка также известная как мастоцит или лаброцит) [ 1 ] ) — резидентная клетка соединительной ткани, содержащая множество гранул, богатых гистамином и гепарином . В частности, это тип гранулоцитов, происходящих из миелоидных стволовых клеток , которые являются частью иммунной и нейроиммунной систем. Тучные клетки были открыты Паулем Эрлихом в 1877 году. [ 2 ] Хотя тучные клетки наиболее известны своей ролью при аллергии и анафилаксии , они также играют важную защитную роль, принимая непосредственное участие в заживлении ран, ангиогенезе , иммунной толерантности , защите от патогенов и проницаемости сосудов при опухолях головного мозга. [ 3 ] [ 4 ]
Тучная клетка очень похожа как по внешнему виду, так и по функциям на базофил , другой тип лейкоцитов . Хотя тучные клетки когда-то считались тканерезидентными базофилами, было показано, что эти две клетки развиваются из разных гемопоэтических линий и, следовательно, не могут быть одними и теми же клетками. [ 5 ]
Структура
[ редактировать ]

Тучные клетки очень похожи на базофильные гранулоциты (класс лейкоцитов ) в крови в том смысле, что оба представляют собой гранулированные клетки , содержащие гистамин и гепарин , антикоагулянт . Их ядра отличаются тем, что ядро базофилов дольчатое , а ядро тучных клеток круглое. Fc -область иммуноглобулина Е (IgE) связывается с тучными клетками и базофилами, и когда паратопы IgE связываются с антигеном, это заставляет клетки высвобождать гистамин и другие медиаторы воспаления. [ 6 ] Эти сходства заставили многих предположить, что тучные клетки — это базофилы, «поселившиеся» в тканях. Более того, они имеют общего предшественника в костном мозге, экспрессирующего молекулу CD34 . Базофилы покидают костный мозг уже зрелыми, тогда как тучные клетки циркулируют в незрелой форме, созревая только один раз в участке ткани. Место расположения незрелой тучной клетки, вероятно, определяет ее точные характеристики. [ 7 ] Впервые in vitro дифференцировка и рост чистой популяции тучных клеток мыши были проведены с использованием кондиционированной среды, полученной из спленоцитов, стимулированных конканавалином А. [ 8 ] Позже было обнаружено, что интерлейкин 3, полученный из Т-клеток, был компонентом, присутствующим в кондиционированной среде, который необходим для дифференцировки и роста тучных клеток. [ 9 ]
Тучные клетки у грызунов классически делят на два подтипа: соединительнотканного тучные клетки типа и тучные клетки слизистой оболочки . Активность последних зависит от Т-клеток . [ 10 ]
Тучные клетки присутствуют в большинстве тканей, обычно окружающих кровеносные сосуды, нервы и лимфатические сосуды. [ 11 ] и особенно выражены вблизи границ между внешним миром и внутренней средой, таких как кожа , слизистая оболочка легких и пищеварительного тракта , а также рот , конъюнктива и нос . [ 7 ]
Функция
[ редактировать ]
Тучные клетки играют ключевую роль в воспалительном процессе. При активации тучная клетка может либо избирательно высвобождать ( по частям дегрануляции ), либо быстро высвобождать ( анафилактическая дегрануляция ) «медиаторы» или соединения, вызывающие воспаление, из запасных гранул в местное микроокружение. [ 3 ] [ 12 ] Тучные клетки могут быть стимулированы к дегрануляции аллергенами структур, связанных с посредством перекрестного связывания с рецепторами иммуноглобулина E (например, FcεRI ), физическим повреждением через рецепторы распознавания образов молекулярных повреждением (DAMP), микробными патогенами посредством рецепторов распознавания образов молекулярных структур, связанных с патогенами. паттерны (PAMP) и различные соединения через связанные с ними рецепторы, связанные с G-белком (например, морфин через опиоидные рецепторы ) или лиганд-управляемые ионные каналы . [ 3 ] [ 12 ] Белки комплемента также могут активировать мембранные рецепторы тучных клеток для выполнения различных функций. [ 7 ]
Тучные клетки экспрессируют рецептор с высоким сродством ( FcεRI ) для Fc-области IgE, наименее распространенного члена антител. Этот рецептор обладает настолько высоким сродством, что связывание молекул IgE практически необратимо. В результате тучные клетки покрываются IgE, который вырабатывается плазматическими клетками (клетками иммунной системы, продуцирующими антитела). Антитела IgE обычно специфичны к одному конкретному антигену .
При аллергических реакциях тучные клетки остаются неактивными до тех пор, пока аллерген не связывается с IgE, уже нанесенным на клетку. Другие события активации мембраны могут либо подготовить тучные клетки к последующей дегрануляции, либо действовать синергично с передачей сигнала FcεRI. [ 13 ] Как правило, аллергены представляют собой белки или полисахариды . Аллерген связывается с сайтами связывания антигена, которые расположены на вариабельных участках молекул IgE, связанных с поверхностью тучных клеток. Похоже, что для активации тучных клеток необходимо связывание двух или более молекул IgE (сшивание). Кластеризация внутриклеточных доменов клеточно-связанных Fc-рецепторов, связанных со сшитыми молекулами IgE, вызывает сложную последовательность реакций внутри тучной клетки, которые приводят к ее активации. Хотя эта реакция наиболее хорошо изучена с точки зрения аллергии, похоже, она развилась как защитная система против паразитов и бактерий. [ 14 ]
Медиаторы тучных клеток
[ редактировать ]Уникальный набор медиаторов тучных клеток, специфичный для стимула, высвобождается в результате дегрануляции после активации рецепторов клеточной поверхности тучных клеток. [ 12 ] Примеры медиаторов, которые высвобождаются во внеклеточную среду во время дегрануляции тучных клеток, включают: [ 7 ] [ 12 ] [ 15 ]
- сериновые протеазы , такие как триптаза и химаза
- гистамин (2–5 пикограмм на тучную клетку)
- серотонин
- протеогликаны , главным образом гепарин (активен как антикоагулянт ) и некоторые протеогликаны хондроитинсульфата.
- аденозинтрифосфат (АТФ)
- лизосомальные ферменты
- новообразованные липидные медиаторы ( эйкозаноиды ):
- цитокины
- активные формы кислорода
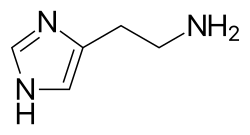
Гистамин расширяет посткапиллярные венулы, активирует эндотелий и увеличивает проницаемость кровеносных сосудов. Это приводит к местному отеку (отечности), повышению температуры, покраснению и привлечению других воспалительных клеток к месту выброса. Он также деполяризует нервные окончания (что приводит к зуду или боли ). Кожные признаки выброса гистамина представляют собой реакцию «вспышки и волдыри ». Шишка и покраснение сразу после укуса комара являются хорошим примером этой реакции, которая возникает через несколько секунд после воздействия аллергена на тучные клетки. [ 7 ]
Другая физиологическая активность тучных клеток изучена гораздо меньше. Некоторые данные свидетельствуют о том, что тучные клетки могут играть довольно фундаментальную роль во врожденном иммунитете : они способны вырабатывать широкий спектр важных цитокинов и других медиаторов воспаления, таких как TNF-α; они экспрессируют множество «рецепторов распознавания образов», которые, как считается, участвуют в распознавании широких классов патогенов; а мыши без тучных клеток, по-видимому, гораздо более восприимчивы к различным инфекциям. [ нужна ссылка ]
Гранулы тучных клеток содержат множество биологически активных химических веществ. Было обнаружено, что эти гранулы передаются соседним клеткам иммунной системы и нейронам в процессе трансгрануляции через псевдоподии тучных клеток . [ 16 ]
В нервной системе
[ редактировать ]В отличие от других гемопоэтических клеток иммунной системы , тучные клетки естественным образом встречаются в мозге человека , где они взаимодействуют с нейроиммунной системой . [ 4 ] В головном мозге тучные клетки расположены в ряде структур, которые опосредуют висцеральные сенсорные (например, болевые) или нейроэндокринные функции или расположены вдоль гемато-спинномозгового барьера , включая ножку гипофиза , шишковидную железу , таламус и гипоталамус , область пострема , сосудистое сплетение и в дуральном слое мозговых оболочек вблизи менингеальных ноцицепторов . [ 4 ] Тучные клетки выполняют одни и те же общие функции в организме и центральной нервной системе, такие как воздействие или регулирование аллергических реакций, врожденного и адаптивного иммунитета, аутоиммунитета и воспаления. [ 4 ] [ 17 ] Во всех системах тучные клетки служат основной эффекторной клеткой , через которую патогены могут влиять на ось кишечник-мозг . [ 18 ] [ 19 ]
В кишечнике
[ редактировать ]В желудочно-кишечном тракте тучные клетки слизистой оболочки расположены в непосредственной близости от чувствительных нервных волокон, которые сообщаются в двух направлениях. [ 20 ] [ 18 ] [ 19 ] Когда эти тучные клетки первоначально дегранулируются, они высвобождают медиаторы (например, гистамин, триптазу и серотонин), которые активируют, сенсибилизируют и усиливают мембранную экспрессию ( ноцицепторов т. е. TRPV1 ) на висцеральных афферентных нейронах через их рецепторы (соответственно HRH1 , HRH2 , HRH3 , PAR2 , 5-HT3 ); [ 20 ] в свою очередь, это приводит к нейрогенному воспалению, висцеральной гиперчувствительности и нарушению перистальтики кишечника (т.е. нарушению перистальтики ). [ 20 ] Активация нейронов индуцирует передачу сигнала нейропептидом ( субстанция P и пептид, родственный гену кальцитонина ) тучным клеткам, где они связываются со связанными с ними рецепторами и запускают дегрануляцию определенного набора медиаторов ( β-гексозаминидаза , цитокины , хемокины , PGD2 , лейкотриены и эоксины ). . [ 20 ] [ 12 ]
Физиология
[ редактировать ]
Структура высокоаффинного рецептора IgE, FcεR1
[ редактировать ]FcεR1 представляет собой IgE-рецептор с высоким сродством, который экспрессируется на поверхности тучных клеток. FcεR1 представляет собой тетрамер, состоящий из одной альфа-(α)-цепи, одной бета-(β)-цепи и двух идентичных дисульфидно-связанных гамма-(γ)-цепей. Сайт связывания IgE образован внеклеточной частью α-цепи, содержащей два домена, сходных с Ig. Один трансмембранный домен содержит остаток аспарагиновой кислоты , а другой — короткий цитоплазматический хвост. [ 21 ] β-цепь содержит единственный мотив активации иммунорецептора на основе тирозина ITAM в цитоплазматической области. Каждая γ-цепь имеет один ITAM в цитоплазматической области. Сигнальный каскад от рецептора инициируется, когда ITAM β- и γ-цепей фосфорилируются тирозинкиназой. Этот сигнал необходим для активации тучных клеток. [ 22 ] Т-хелперы типа 2 ( Th2 ) и многие другие типы клеток лишены β-цепи, поэтому передача сигналов опосредована только γ-цепью. Это связано с тем, что α-цепь содержит сигналы сохранения эндоплазматического ретикулума, что приводит к тому, что α-цепи остаются деградированными в ЭР. Сборка α-цепи с совместно трансфецированными β- и γ-цепями маскирует удержание ЭР и позволяет экспортировать комплекс αβγ в аппарат Гольджи на плазматическую мембрану крыс. У людей только γ-комплекс необходим для уравновешивания удержания ER α-цепи. [ 21 ]
Аллергенный процесс
[ редактировать ]Сигналы перекрестного связывания FcεR1, опосредованные аллергеном, очень похожи на сигнальное событие, приводящее к связыванию антигена с лимфоцитами . Тирозинкиназа Lyn связана с цитоплазматическим концом β - цепи FcεR1. Антиген сшивает молекулы FcεR1, а тирозинкиназа Lyn фосфорилирует ITAM в β- и γ-цепях FcεR1 в цитоплазме. При фосфорилировании тирозинкиназа Syk привлекается к ITAM, расположенным в γ-цепях. Это вызывает активацию тирозинкиназы Syk, вызывая ее фосфорилирование. [ 22 ] Syk действует как сигнал, усиливающий киназную активность, поскольку он воздействует на несколько белков и вызывает их активацию. [ 23 ] Этот антиген стимулировал фосфорилирование, вызывающее активацию других белков в сигнальном каскаде, опосредованном FcεR1. [ 24 ]
Дегрануляция и слияние
[ редактировать ]Важным адаптерным белком, активируемым на этапе фосфорилирования Syk, является линкер активации Т-клеток (LAT). LAT можно модифицировать путем фосфорилирования для создания новых сайтов связывания. [ 23 ] Гамма-фосфолипаза C (PLCγ) фосфорилируется после связывания с LAT, а затем используется для катализа распада фосфатидилинозитолбисфосфата с образованием инозитолтрифосфата (IP3) и диацилглицерина (DAG). IP3 повышает уровень кальция, а DAG активирует протеинкиназу C (PKC). Это не единственный способ изготовления ПКС. Тирозинкиназа FYN фосфорилирует Grb2-связывающий белок 2 (Gab2), который связывается с фосфоинозитид-3-киназой , которая активирует PKC. PKC приводит к активации движения гранул фосфорилирования легкой цепи миозина, что разбирает актин-миозиновые комплексы, позволяя гранулам вступить в контакт с плазматической мембраной. [ 22 ] Гранулы тучных клеток теперь могут сливаться с плазматической мембраной. слитого белка, чувствительного к N-этилмалеимиду рецептора SNARE Этот процесс опосредован растворимым комплексом . Различные белки SNARE взаимодействуют, образуя разные комплексы, катализирующие слияние. Rab3 Гуанозинтрифосфатазы и Rab-ассоциированные киназы и фосфатазы регулируют слияние мембран гранул в покоящихся тучных клетках.
Рецептор тучных клеток MRGPRX2
[ редактировать ]Человеческий специфичный для тучных клеток рецептор MRGPRX2, связанный с G-белком , играет ключевую роль в распознавании молекулярных паттернов, связанных с патогенами (PAMP), и инициировании антибактериального ответа. MRGPRX2 способен связываться со стимулирующим компетентность пептидом (CSP) 1 — молекулой, чувствительной к кворуму (QSM), продуцируемой грамположительными бактериями. [ 25 ] Это приводит к передаче сигнала G-белку и активации тучных клеток. Активация тучных клеток индуцирует высвобождение антибактериальных медиаторов, включая АФК, TNF-α и PRGD2, которые вызывают привлечение других иммунных клеток для ингибирования роста бактерий и образования биопленок .
Рецептор MRGPRX2 является возможной терапевтической мишенью и может быть фармакологически активирован с использованием соединения-агониста 48/80 для контроля бактериальной инфекции. [ 26 ] Также предполагается, что другие QSM и даже сигналы грамотрицательных бактерий могут активировать этот рецептор. Это может особенно иметь место при хронических инфекциях, вызванных бартонеллой , когда в симптоматике человека ясно видно, что у всех этих пациентов имеется синдром активации тучных клеток из-за присутствия еще не определенной молекулы, чувствительной к кворуму (сам базальный гистамин?). Эти пациенты склонны к пищевой непереносимости, обусловленной другим, менее специфическим путем, чем путь рецептора IgE: конечно, путь MRGPRX2. У этих пациентов также наблюдаются циклические кожные патергии и дермографизм каждый раз, когда бактерии выходят из своего скрытого внутриклеточного местоположения.
Ферменты
[ редактировать ]| Фермент | Функция |
|---|---|
| Лин тирозинкиназа | Фосфорилирует ITAM в β- и γ-цепях FcεR1 в цитоплазме. Это заставляет тирозинкиназу Syk рекрутироваться в ITAMS, расположенную на γ-цепях. Это вызывает активацию тирозинкиназы Syk, вызывающую ее фосфорилирование. |
| Больная тирозинкиназа | Нацеливается на несколько белков и вызывает их активацию |
| Фосфолипаза С | Катализирует фосфатидилинозитол-4,5-бисфосфат. |
| Инозитолтрифосфат | Повышает уровень кальция |
| Диацилглицерин | Активирует протеинкиназу С |
| НАХОДИТЬ | Фосфорилаты GAB2 |
| ГАБ2 | Связывается с фосфоинозитид-3-киназой |
| Фосфоинозитид-3-киназа | Активирует протеинкиназу С |
| Протеинкиназа С | Активирует движения гранул фосфорилирования легкой цепи миозина, которые разбирают комплексы актин-миозин. |
| Rab-ассоциированные киназы и фосфатазы | Регулирует слияние мембран клеточных гранул в покоящихся тучных клетках |
Клиническое значение
[ редактировать ]Паразитарные инфекции
[ редактировать ]Тучные клетки активируются в ответ на заражение патогенными паразитами, такими как некоторые гельминты и простейшие , посредством передачи сигналов IgE .
Нарушения активации тучных клеток
[ редактировать ]Нарушения активации тучных клеток ( MCAD ) представляют собой спектр иммунных нарушений , которые не связаны с патогенной инфекцией и включают сходные симптомы, возникающие из-за секретируемых промежуточных продуктов тучных клеток, но незначительно различающиеся по патофизиологии , подходу к лечению и отличительным симптомам. [ 27 ] [ 28 ] Классификация нарушений активации тучных клеток была разработана в 2010 году. [ 27 ] [ 28 ]
Аллергическое заболевание
[ редактировать ]Аллергия опосредуется передачей сигналов IgE , которая запускает дегрануляцию тучных клеток. [ 27 ] В последнее время считается, что IgE-независимые « псевдоаллергические » реакции также опосредуются активацией рецептора MRGPRX2 тучных клеток (например, такими лекарствами, как миорелаксанты , опиоиды , икатибант и фторхинолоны ). [ 29 ]
Многие формы аллергии на коже и слизистых оболочках в значительной степени опосредованы тучными клетками; они играют центральную роль при астме , экземе , зуде (от различных причин), аллергическом рините и аллергическом конъюнктивите . Антигистаминные препараты действуют, блокируя действие гистамина на нервные окончания. Препараты на основе кромогликата (кромогликат натрия, недокромил) блокируют кальциевый канал, необходимый для дегрануляции тучных клеток, стабилизируя клетку и предотвращая высвобождение гистамина и связанных с ним медиаторов. Антагонисты лейкотриенов (такие как монтелукаст и зафирлукаст ) блокируют действие лейкотриеновых медиаторов и все чаще используются при аллергических заболеваниях. [ 7 ]
Кальций запускает секрецию гистамина из тучных клеток после предыдущего воздействия фторида натрия. Секреторный процесс можно разделить на стадию активации фторида и стадию секреции, индуцируемой кальцием. Было замечено, что стадия активации фторида сопровождается повышением уровней циклического аденозинмонофосфата (цАМФ) внутри клеток. Достигнутые высокие уровни цАМФ сохраняются во время высвобождения гистамина. Далее было обнаружено, что катехоламины заметно не изменяют индуцированное фторидом высвобождение гистамина. Было также подтверждено, что теофиллином ингибируется второй, но не первый этап секреции гистамина, индуцированной фторидом натрия. [ 30 ] Расширение сосудов и повышенная проницаемость капилляров являются результатом действия рецепторов как H1, так и H2. [ 31 ]
Стимуляция гистамина активирует гистамин (H2)-чувствительную аденилатциклазу оксинтических клеток, и происходит быстрое увеличение клеточного [цАМФ], который участвует в активации транспорта H+ и других связанных с этим изменениях оксинтических клеток. [ 32 ]
Анафилаксия
[ редактировать ]При анафилаксии (тяжелая системная реакция на аллергены , такие как орехи, укусы пчел или лекарства) дегрануляция тучных клеток по всему телу приводит к расширению сосудов и, в тяжелых случаях, к симптомам опасного для жизни шока . [ нужна ссылка ]
Гистамин – сосудорасширяющее вещество, выделяющееся во время анафилаксии. [ 31 ]
Аутоиммунитет
[ редактировать ]Тучные клетки могут быть вовлечены в патологию, связанную с аутоиммунными воспалительными заболеваниями суставов. Было показано, что они участвуют в привлечении воспалительных клеток в суставы (например, ревматоидный артрит ) и кожу (например, буллезный пемфигоид ), и эта активность зависит от антител и компонентов комплемента. [ 33 ]
Мастоцитоз и клональные нарушения
[ редактировать ]Этот раздел нуждается в расширении . Вы можете помочь, добавив к нему . ( октябрь 2015 г. ) |
Мастоцитоз — редкое клональное заболевание тучных клеток, характеризующееся наличием слишком большого количества тучных клеток ( мастоцитов ) и CD34 + предшественников тучных клеток. [ 34 ] Мутации c-Kit связаны с мастоцитозом. [ 27 ]
Моноклональные расстройства
[ редактировать ]Этот раздел нуждается в расширении . Вы можете помочь, добавив к нему . ( октябрь 2015 г. ) |
Неопластические заболевания
[ редактировать ]Мастоцитомы , или опухоли тучных клеток, могут выделять избыточное количество продуктов дегрануляции. [ 27 ] [ 28 ] Их часто можно увидеть у собак и кошек. [ 35 ] Другие неопластические заболевания, связанные с тучными клетками, включают тучноклеточную саркому и тучноклеточный лейкоз .
Синдром активации тучных клеток
[ редактировать ]Синдром активации тучных клеток (MCAS) представляет собой идиопатическое иммунное заболевание , которое включает в себя рецидивирующую и чрезмерную дегрануляцию тучных клеток и вызывает симптомы, сходные с другими нарушениями активации тучных клеток. [ 27 ] [ 28 ] Синдром диагностируется на основании четырех наборов критериев, включающих ответ на лечение, симптомы, дифференциальный диагноз и биомаркеры дегрануляции тучных клеток. [ 27 ] [ 28 ]
История
[ редактировать ]Тучные клетки были впервые описаны Паулем Эрлихом в его докторской диссертации 1878 года на основании их уникальных характеристик окрашивания и крупных гранул. Эти гранулы также привели его к неправильному убеждению, что они существуют для питания окружающих тканей, поэтому он назвал их Масцеллен (от немецкого Mast «откормление», как у животных). [ 36 ] [ 37 ] Сейчас они считаются частью иммунной системы .
Исследовать
[ редактировать ]Аутизм
[ редактировать ]Исследования иммунологического вклада в развитие аутизма позволяют предположить, что у детей с расстройствами аутистического спектра (РАС) могут наблюдаться «аллергические» проблемы при отсутствии повышенного уровня IgE в сыворотке и хронической крапивницы , что позволяет предположить неаллергическую активацию тучных клеток в ответ на триггеры окружающей среды и стресса. . Эта активация тучных клеток может способствовать воспалению мозга и проблемам развития нервной системы. [ 38 ]
Гистологическое окрашивание
[ редактировать ]Толуидиновый синий : один из наиболее распространенных красителей для кислых мукополисахаридов и гликоаминогликанов , компонентов гранул тучных клеток. [ 39 ]
Бисмарк коричневый: окрашивает гранулы тучных клеток в коричневый цвет. [ 40 ]
Поверхностные маркеры: маркеры клеточной поверхности тучных клеток подробно обсуждались Хенебергом, [ 41 ] утверждая, что тучные клетки могут быть случайно включены в изоляты стволовых клеток или клеток-предшественников, поскольку часть из них положительна по антигену CD34. Классические маркеры тучных клеток включают высокоаффинный рецептор IgE, CD117 (c-Kit) и CD203c (для большинства популяций тучных клеток). Экспрессия некоторых молекул может меняться в ходе активации тучных клеток. [ 42 ]
Другие организмы
[ редактировать ]и энтерохромаффинные клетки являются источником большей части серотонина в желудке грызунов Тучные клетки . [ 43 ]
См. также
[ редактировать ]- Аллергия
- Диаминоксидаза
- Пищевая непереносимость
- Гранулоциты
- Непереносимость гистамина
- Гистамин N-метилтрансфераза или HNMT
- Гистамин
- Список различных типов клеток в организме взрослого человека
- Синдром активации тучных клеток
Ссылки
[ редактировать ]- ^ «лаброциты» . Мемидекс. Архивировано из оригинала 6 ноября 2018 года . Проверено 19 февраля 2011 г.
- ^ Эрлих, Пауль (1878). «Вклад в теорию и практику гистологического окрашивания». Лейпцигский университет .
- ^ Jump up to: а б с да Силва Э.З., Джамур МК, Оливер С. (2014). «Функция тучных клеток: новый взгляд на старую клетку» . Дж. Гистохим. Цитохим . 62 (10): 698–738. дои : 10.1369/0022155414545334 . ПМК 4230976 . ПМИД 25062998 .
Тучные клетки могут распознавать патогены посредством различных механизмов, включая прямое связывание патогенов или их компонентов с рецепторами PAMP на поверхности тучных клеток, связывание антител или бактерий, покрытых комплементом, с рецепторами комплемента или иммуноглобулина или распознавание эндогенных пептидов, продуцируемых инфицированными или поврежденными клетками. (Хофманн и Абрахам, 2009). Характер экспрессии этих рецепторов значительно различается среди разных подтипов тучных клеток. TLR (1–7 и 9), NLR, RLR и рецепторы комплемента ответственны за большинство врожденных реакций тучных клеток.
- ^ Jump up to: а б с д Полизоидис С., Колеца Т., Панагиотиду С., Ашкан К., Теохаридес Т.С. (2015). «Тучные клетки при менингиомах и воспалении головного мозга» . J Нейровоспаление . 12 (1): 170. дои : 10.1186/s12974-015-0388-3 . ПМЦ 4573939 . ПМИД 26377554 .
ТК происходят из предшественника костного мозга и впоследствии приобретают различные характеристики фенотипа локально в тканях. Спектр их функций широк и включает участие в аллергических реакциях, врожденном и адаптивном иммунитете, воспалении и аутоиммунитете [34]. В мозге человека ТК могут располагаться в различных областях, таких как ножка гипофиза, шишковидная железа, постремная область, сосудистое сплетение, таламус, гипоталамус и срединное возвышение [35]. В мозговых оболочках они обнаруживаются внутри дурального слоя в сочетании с сосудами и окончаниями менингеальных ноцицепторов [36]. Отличительной особенностью ТК по сравнению с другими гемопоэтическими клетками является то, что они расположены в головном мозге [37]. ТК содержат многочисленные гранулы и секретируют большое количество заранее сохраненных медиаторов, таких как кортикотропин-рилизинг-гормон (CRH), нейротензин (NT), вещество P (SP), триптаза, химаза, вазоактивный интестинальный пептид (VIP), фактор роста эндотелия сосудов (VEGF). , TNF, простагландины, лейкотриены и разновидности хемокинов и цитокинов, некоторые из которых, как известно, нарушают целостность гематоэнцефалического барьера (ГЭБ) [38–40].
[]Ключевая роль ТК в воспалении [34] и разрушении ГЭБ [41–43] указывает на важные области для исследований в области новой терапии. Все больше данных также указывает на то, что ТК участвуют в нейровоспалении напрямую [44–46] и посредством стимуляции микроглии [47], способствуя патогенезу таких состояний, как головные боли, [48] аутизм [49] и синдром хронической усталости [50]. Фактически, недавний обзор показал, что периферические воспалительные стимулы могут вызывать активацию микроглии [51], таким образом, возможно, вовлекая ТК вне мозга. - ^ Франко CB, Чен CC, Друккер М, Вайсман И.Л., Галли С.Дж. (2010). «Различие дифференцировки тучных клеток и гранулоцитов на уровне отдельных клеток» . Клеточная стволовая клетка . 6 (4): 361–8. дои : 10.1016/j.stem.2010.02.013 . ПМЦ 2852254 . ПМИД 20362540 .
- ^ Мариб Э.Н., Хён К. (2004). Анатомия и физиология человека (6-е изд.). Сан-Франциско: Пирсон Бенджамин Каммингс. п. 805 . ISBN 978-0-321-20413-4 .
- ^ Jump up to: а б с д и ж Пруссин С., Меткалф Д.Д. (февраль 2003 г.). «4. IgE, тучные клетки, базофилы и эозинофилы» . Журнал аллергии и клинической иммунологии . 111 (2 Приложения): S486–94. дои : 10.1067/май.2003.120 . ПМЦ 2847274 . ПМИД 12592295 .
- ^ Разин Э., Кордон-Кардо С. , Гуд Р.А. (апрель 1981 г.). «Выращивание чистой популяции тучных клеток мыши in vitro с использованием кондиционированной среды, полученной из спленоцитов, стимулированных конканавалином А» . Труды Национальной академии наук Соединенных Штатов Америки . 78 (4): 2559–61. Бибкод : 1981PNAS...78.2559R . дои : 10.1073/pnas.78.4.2559 . ПМК 319388 . ПМИД 6166010 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Разин Э., Илье Дж.Н., Селдин Д. и др. (март 1984 г.). «Интерлейкин 3: фактор дифференцировки и роста тучных клеток мыши, содержащий протеогликан хондроитинсульфата Е» . Журнал иммунологии . 132 (3): 1479–86. дои : 10.4049/jimmunol.132.3.1479 . ПМИД 6198393 . S2CID 22811807 . Архивировано из оригинала 14 июня 2018 года . Проверено 28 апреля 2014 г.
- ^ Денбург Дж. А. (1998). Аллергия и аллергические заболевания: новые механизмы и методы лечения . Тотова, Нью-Джерси: Humana Press. ISBN 978-0-89603-404-4 . [ нужна страница ]
- ^ Пал, Сарит; Гашева Ольга Юрьевна; Завея, Дэвид К.; Майнингер, Синтия Дж.; Гашев, Анатолий А. (март 2020 г.). «Гистамин-опосредованная аутокринная передача сигналов в мезентериальных перилимфатических тучных клетках» . Американский журнал физиологии. Регуляторная, интегративная и сравнительная физиология . 318 (3): 590–604 рандов. дои : 10.1152/ajpregu.00255.2019 . ПМК 7099465 . ПМИД 31913658 .
- ^ Jump up to: а б с д и Мун Т.С., Бефус А.Д., Кулка М. (2014). «Медиаторы тучных клеток: их дифференциальное высвобождение и задействованные секреторные пути» . Фронт Иммунол . 5 : 569. дои : 10.3389/fimmu.2014.00569 . ПМК 4231949 . ПМИД 25452755 .
Для MC описаны два типа дегрануляции: частичная дегрануляция (PMD) и анафилактическая дегрануляция (AND) (рис. 1 и 2). И PMD, и AND встречаются in vivo, ex vivo и in vitro в MC у человека (78–82), мыши (83) и крысы (84). ПМД представляет собой селективное высвобождение части содержимого гранулы без слияния мембран гранулы с гранулой и/или гранулы с плазмой. ... В отличие от PMD, AND представляет собой взрывное высвобождение содержимого гранул или целых гранул наружу клеток после слияния мембран гранулы с гранулой и/или гранулы с плазмой (рис. 1 и 2). Ультраструктурные исследования показывают, что AND начинается с набухания гранул и изменения матрикса после соответствующей стимуляции (например, сшивания FcεRI).
Рисунок 1: Высвобождение медиатора из тучных клеток. Архивировано 29 апреля 2018 г. на Wayback Machine.
Рисунок 2: Модель генеза секреторных гранул тучных клеток. Архивировано 29 апреля 2018 г. на Wayback Machine.
Рисунок 3: Биогенез липидных тел. Архивировано 29 апреля 2018 г. на Wayback Machine.
Таблица 2: Высвобождение стимул-селективных медиаторов из тучных клеток. Архивировано 29 апреля 2018 г. на Wayback Machine. - ^ Пулендран Б., Оно С.Дж. (май 2008 г.). «Укол в руку для тучных клеток» . Нат. Мед . 14 (5): 489–90. дои : 10.1038/nm0508-489 . ПМИД 18463655 . S2CID 205378470 .
- ^ Ли Дж., Витч С.Л., Бэрд Б., Холовка Д. (2012). «Молекулярные механизмы спонтанной и направленной подвижности тучных клеток» . Дж. Леукок. Биол . 92 (5): 1029–41. дои : 10.1189/jlb.0212091 . ПМЦ 3476239 . ПМИД 22859829 .
- ^ Эшмол I, Брэддинг П. (май 2013 г.). «Ионные каналы, регулирующие биологию тучных клеток». Клин. Эксп. Аллергия . 43 (5): 491–502. дои : 10.1111/cea.12043 . ПМИД 23600539 . S2CID 1127584 .
Рецепторы P2X представляют собой лиганд-управляемые неселективные катионные каналы, которые активируются внеклеточным АТФ. ... Повышенные локальные концентрации АТФ, вероятно, будут присутствовать вокруг тучных клеток в воспаленных тканях из-за его высвобождения в результате повреждения или гибели клеток и активации тромбоцитов [40]. Более того, сами тучные клетки хранят АТФ в секреторных гранулах, который высвобождается при активации [41]. Таким образом, существует потенциал значительного притока Ca2+ в тучные клетки через рецепторы P2X. Члены семейства P2X различаются как по концентрации АТФ, необходимой им для активации, так и по степени снижения чувствительности после активации агониста [37, 38]. Это открывает возможность того, что, экспрессируя ряд различных рецепторов P2X, тучные клетки смогут адаптировать свой ответ на АТФ в зависимости от концентрации [37].
- ^ Вильгельм М., Сильвер Р., Сильверман А.Дж. (ноябрь 2005 г.). «Нейроны центральной нервной системы приобретают продукты тучных клеток посредством трансгрануляции» . Европейский журнал неврологии . 22 (9): 2238–48. дои : 10.1111/j.1460-9568.2005.04429.x . ПМК 3281766 . ПМИД 16262662 .
- ^ Рен Х, Хан Р, Чен Х, Лю Х, Ван Дж, Ван Л, Ян Х, Ван Дж (май 2020 г.). «Потенциальные терапевтические мишени для воспаления, связанного с внутримозговым кровоизлиянием: обновленная информация» . J Метаболия кровотока головного мозга . 40 (9): 1752–1768. дои : 10.1177/0271678X20923551 . ПМЦ 7446569 . ПМИД 32423330 .
- ^ Jump up to: а б Будзинский Ю, Клопоцка М (2014). «Ось мозг-кишечник в патогенезе инфекции Helicobacter pylori» . Мир Дж. Гастроэнтерол . 20 (18): 5212–25. дои : 10.3748/wjg.v20.i18.5212 . ПМК 4017036 . ПМИД 24833851 .
В пищеварительной ткани H. pylori может изменять передачу сигналов по оси мозг-кишечник тучными клетками, основным эффектором оси мозг-кишечник.
- ^ Jump up to: а б Каработти М., Сирокко А., Маселли М.А., Севери С. (2015). «Ось кишечник-мозг: взаимодействие между кишечной микробиотой, центральной и кишечной нервной системой» . Энн Гастроэнтерол . 28 (2): 203–209. ПМЦ 4367209 . ПМИД 25830558 .
- ^ Jump up to: а б с д Воутерс М.М., Викарио М., Сантос Дж. (2015). «Роль тучных клеток в функциональных расстройствах ЖКТ» . Гут . 65 (1): 155–168. дои : 10.1136/gutjnl-2015-309151 . ПМИД 26194403 .
Функциональные желудочно-кишечные расстройства (ФГИР) характеризуются хроническими жалобами, возникающими из-за дезорганизации взаимодействия мозга и кишечника, что приводит к нарушению моторики и гиперчувствительности. Двумя наиболее распространенными ФГИР, от которых страдают до 16–26% населения мира, являются функциональная диспепсия и синдром раздраженного кишечника. ... Хорошо известно, что активация тучных клеток может вызывать эпителиальную и нервно-мышечную дисфункцию, а также способствовать висцеральной гиперчувствительности и изменению двигательной активности при ФГИР, послеоперационной кишечной непроходимости, пищевой аллергии и воспалительных заболеваниях кишечника.
▸ Тучные клетки играют центральную патофизиологическую роль при СРК и, возможно, при функциональной диспепсии, хотя она еще не четко определена.
▸ Повышенная активация тучных клеток является частым явлением в слизистой оболочке пациентов с функциональными расстройствами ЖКТ. ...
▸ Лечение стабилизаторами тучных клеток представляет собой достаточно безопасный и многообещающий вариант лечения пациентов с СРК, не отвечающих на традиционные подходы, хотя необходимы будущие исследования для оценки эффективности и показаний. - ^ Jump up to: а б Кинет Дж. П. (1999). «Высокоаффинный рецептор IgE (FcεRI): от физиологии к патологии». Ежегодный обзор иммунологии . 17 : 931–72. doi : 10.1146/annurev.immunol.17.1.931 . ПМИД 10358778 .
- ^ Jump up to: а б с Аббас А.К., Лихтман А.Х., Пиллаи С. (2011). «Роль тучных клеток, базофилов и эозинофилов в гиперчувствительности немедленного типа» . Клеточная и молекулярная иммунология (7-е изд.). Нью-Йорк, штат Нью-Йорк: Эльзевир. ISBN 978-1-4377-1528-6 . [ нужна страница ]
- ^ Jump up to: а б Ривера Дж., Кордеро Дж.Р., Фурумото Ю. и др. (сентябрь 2002 г.). «Сигнальные комплексы макромолекулярных белков и реакции тучных клеток: взгляд на организацию IgE-зависимой передачи сигналов тучных клеток». Молекулярная иммунология . 38 (16–18): 1253–8. дои : 10.1016/S0161-5890(02)00072-X . ПМИД 12217392 .
- ^ Ли В., Динин Г.Г., Марголис Б., Шлезингер Дж., Оливер Дж. М. (июль 1992 г.). «FcεR1-опосредованное тирозиновое фосфорилирование нескольких белков, включая фосфолипазу Cγ1 и комплекс рецептора βγ2, в клетках базофильного лейкоза крыс RBL-2H3» . Молекулярная и клеточная биология . 12 (7): 3176–82. дои : 10.1128/MCB.12.7.3176 . ПМЦ 364532 . ПМИД 1535686 .
- ^ Пундир, Приянка; Лю, Руй; Васавда, Чираг; Серхан, Надин; Лимджунявонг, Натачит; Да, Ребекка; Чжан, Инчжуань; Донг, Синьтун; У, Сюэцин; Чжан, Ин; Снайдер, Соломон Х; Гауденцио, Николас; Видаль, Хорхе Э; Донг, Синьчжун (июль 2019 г.). «Рецептор, специфичный для тучных клеток соединительной ткани, обнаруживает молекулы, чувствительные к бактериальному кворуму, и опосредует антибактериальный иммунитет» . Клетка-хозяин и микроб . 26 (1): 114–122. дои : 10.1016/j.chom.2019.06.003 . ПМК 6649664 . ПМИД 31278040 . Проверено 7 июля 2021 г.
- ^ Татемото, Кадзухико; Нодзаки, Юко; Цуда, Рёко; Конно, Синобу; Томура, Кейко; Фуруно, Масахиро; Огасавара, Хироюки; Эдамура, Кодзи; Такаги, Хидео; Ивамура, Хироюки; Ногучи, Масато; Наито, Такаюки (2006). «Иммуноглобулин Е-независимая активация тучных клеток опосредована рецепторами Mrg» . Связь с биохимическими и биофизическими исследованиями . 349 (4): 1322–1328. дои : 10.1016/j.bbrc.2006.08.177 . ПМИД 16979137 . Получено 7 июля.
- ^ Jump up to: а б с д и ж г Фрири М (2018). «Синдром активации тучных клеток». Клин Рев Аллерги Иммунол . 54 (3): 353–365. дои : 10.1007/s12016-015-8487-6 . ПМИД 25944644 . S2CID 5723622 .
Таблица 1
Классификация заболеваний, связанных с активацией тучных клеток, по Akin et al. [14]
1. Первичный
а. Анафилаксия с сопутствующим заболеванием клональных тучных клеток
б. Синдром активации моноклональных тучных клеток (MMAS), объяснение см. в тексте.
2. Вторичный
а. Аллергические расстройства
б. Активация тучных клеток, связанная с хроническими воспалительными или неопластическими заболеваниями
в. Физическая крапивница (требуется первичная стимуляция)
д. Хроническая аутоиммунная крапивница
3. Идиопатический (когда документально подтверждена дегрануляция тучных клеток; может быть как первичным, так и вторичным. Квинке может быть связана с наследственным или приобретенным ангионевротическим отеком, где он может быть независимым от тучных клеток и возникать в результате образования кининов)
а. Анафилаксия
б. отек Квинке
в. Крапивница
д. Синдром активации тучных клеток (MCAS)...
Рецидивирующая идиопатическая анафилаксия проявляется аллергическими признаками и симптомами — крапивницей и ангионевротическим отеком, что является отличительной особенностью — исключает идентифицируемую аллергическую этиологию, предполагает мастоцитоз и карциноидный синдром и лечится антигистаминными препаратами H1 и H2, адреналином и стероидами [21, 22]. - ^ Jump up to: а б с д и Акин С., Валент П., Меткалф Д.Д. (2010). «Синдром активации тучных клеток: предлагаемые диагностические критерии» . Дж. Аллергическая клиника. Иммунол . 126 (6): 1099–104.e4. дои : 10.1016/j.jaci.2010.08.035 . ПМЦ 3753019 . ПМИД 21035176 .
- ^ Кумар М., Дурайсами К., Чоу Б.К. (май 2021 г.). «Раскрытие загадки не-IgE-опосредованных псевдоаллергических реакций с помощью члена X2 рецептора, связанного с G-белком (MRGPRX2)» . Клетки . 10 (5): 1033. doi : 10.3390/cells10051033 . ПМЦ 8146469 . ПМИД 33925682 .
- ^ Альм ЧП (апрель 1983 г.). «Фторид натрия вызывал высвобождение гистамина из тучных клеток. Исследование уровней циклического АМФ и эффектов катехоламинов». Агенты и действия . 13 (2–3): 132–7. дои : 10.1007/bf01967316 . ПМИД 6191542 . S2CID 6977280 .
- ^ Jump up to: а б Дахман В.Д., Бедарида Г., Блашке Т.Ф., Хоффман Б.Б. (март 1994 г.). «Вызванная гистамином венодилятация у людей затрагивает подтипы рецепторов как H1, так и H2» . Журнал аллергии и клинической иммунологии . 93 (3): 606–14. дои : 10.1016/S0091-6749(94)70072-9 . ПМИД 8151062 .
- ^ Мачен Т.Е., Руттен М.Дж., Экблад Э.Б. (февраль 1982 г.). «Гистамин, цАМФ и активация слизистой оболочки желудка поросят». Американский журнал физиологии . 242 (2): G79–84. дои : 10.1152/ajpgi.1982.242.2.G79 . ПМИД 6175225 .
- ^ Ли Д.М., Френд Д.С., Гуриш М.Ф., Бенуа С., Матис Д., Бреннер М.Б. (сентябрь 2002 г.). «Тучные клетки: клеточная связь между аутоантителами и воспалительным артритом». Наука . 297 (5587): 1689–92. Бибкод : 2002Sci...297.1689L . дои : 10.1126/science.1073176 . ПМИД 12215644 . S2CID 38504601 .
- ^ Horny HP, Сотлар К, Валент П (2007). «Мастоцитоз: современное состояние» . Патобиология . 74 (2): 121–32. дои : 10.1159/000101711 . ПМИД 17587883 .
- ^ «Кожные тучные опухоли» . Ветеринарное руководство компании Merck . 2006. Архивировано из оригинала 23 мая 2007 года . Проверено 8 июля 2007 г.
- ^ Эрлих П. (1878). в теорию и практику гистологических красителей ( Вклад диссертация) (на немецком языке). Лейпцигский университет. OCLC 63372150 .
- ^ «Мастоцит – Определение» . Архивировано из оригинала 3 февраля 2010 года . Проверено 16 августа 2010 г. [ нужна полная цитата ]
- ^ Теохаридес Т.С., Ангелиду А., Алисандратос К.Д. и др. (январь 2012 г.). «Активация тучных клеток и аутизм». Биохимия и биофизика Acta (BBA) - Молекулярные основы болезней . 1822 (1): 34–4 дои : 10.1016/j.badis.2010.12.017 . ПМИД 21193035 .
- ^ Блюменкранц Н., Асбо-Хансен Г. (май 1975 г.). «Селективное окрашивание тучных клеток». Гистохимический журнал . 7 (3): 277–82. дои : 10.1007/BF01003596 . ПМИД 47855 . S2CID 32711203 .
- ^ Томов Н.; Димитров, Н. (2017). «Модифицированное окрашивание Бисмарка-коричневого для демонстрации тучных клеток мягких тканей» (PDF) . Тракийский научный журнал . 15 (3): 195–197. дои : 10.15547/tjs.2017.03.001 .
- ^ Хенеберг П. (ноябрь 2011 г.). «Тучные клетки и базофилы: троянские кони обычных изолятов стволовых клеток/клеток-предшественников». Текущий фармацевтический дизайн . 17 (34): 3753–71. дои : 10.2174/138161211798357881 . ПМИД 22103846 .
- ^ Лебдуска П., Корб Дж., Тумова М., Хенеберг П., Драбер П. (декабрь 2007 г.). «Топография сигнальных молекул, обнаруженная с помощью электронной микроскопии на листах плазматической мембраны, выделенных из неприкрепившихся тучных клеток». Журнал иммунологических методов . 328 (1–2): 139–51. дои : 10.1016/j.jim.2007.08.015 . ПМИД 17900607 .
- ^ Фудзимия, Минеко; Инуи, Акио (2000). «Пептидергическая регуляция моторики желудочно-кишечного тракта у грызунов». Пептиды . 21 (10). Эльзевир Б.В .: 1565–1582 гг. дои : 10.1016/s0196-9781(00)00313-2 . ISSN 0196-9781 . ПМИД 11068106 . S2CID 45185196 .
Внешние ссылки
[ редактировать ]- Тучные + клетки Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)