Лечение рака простаты
Эта статья нуждается в более надежных медицинских ссылках для проверки или слишком сильно полагается на первоисточники . ( февраль 2021 г. ) |  |
| Лечение рака простаты | |
|---|---|
| Специальность | онкология |
Лечение рака простаты может включать активное наблюдение , хирургическое вмешательство , лучевую терапию , включая брахитерапию ( брахитерапию простаты ) и внешнюю лучевую терапию , протонную терапию, высокоинтенсивный фокусированный ультразвук (HIFU), криохирургию , гормональную терапию, химиотерапию или некоторую комбинацию. Лечение также распространяется на вмешательства, основанные на выживании. Эти вмешательства сосредоточены на пяти областях, включая: физические симптомы, психологические симптомы, эпиднадзор, укрепление здоровья и координацию ухода. [ 1 ] Однако опубликованный обзор выявил лишь высокий уровень доказательств в отношении мер, направленных на устранение физических и психологических симптомов и укрепление здоровья, без каких-либо обзоров мер по координации ухода или надзору. [ 2 ] Предпочтительный вариант лечения зависит от стадии заболевания, показателя Глисона и уровня ПСА . Другие важные факторы включают возраст мужчины, его общее состояние здоровья и его мнение о потенциальных методах лечения и их возможных побочных эффектах. Поскольку все методы лечения могут иметь серьезные побочные эффекты , такие как эректильная дисфункция и недержание мочи , обсуждения лечения часто сосредотачиваются на балансировании целей терапии с рисками изменения образа жизни.
Если рак распространился за пределы простаты, варианты лечения существенно меняются, поэтому большинство врачей, лечащих рак простаты, используют различные номограммы для прогнозирования вероятности распространения. Лечение путем бдительного ожидания/активного наблюдения, HIFU, дистанционной лучевой терапии, брахитерапии, криохирургии и хирургического вмешательства, как правило, предлагается мужчинам, у которых рак остается в пределах простаты. Клиницисты могут резервировать гормональную терапию и химиотерапию при заболевании, которое распространилось за пределы простаты. Однако есть исключения: лучевая терапия может лечить некоторые поздние опухоли, а гормональная терапия — некоторые опухоли на ранних стадиях. Врачи также могут предложить криотерапию (процесс замораживания опухоли), гормональную терапию или химиотерапию, если первоначальное лечение не помогло и рак прогрессирует. [ 3 ]
Активное наблюдение
[ редактировать ]Активное наблюдение – это наблюдение и регулярный мониторинг без инвазивного лечения. В контексте заболеваний простаты это обычно включает регулярные анализы крови на ПСА и биопсию простаты. Активное наблюдение часто используется при подозрении на раннюю стадию медленно растущего рака простаты. Однако бдительное ожидание также может быть предложено, когда риски хирургического вмешательства, лучевой терапии или гормональной терапии перевешивают возможную пользу. Другие методы лечения можно начать, если развиваются симптомы или появляются признаки ускорения роста рака. [ нужна ссылка ]
Примерно у трети мужчин, выбравших активное наблюдение за опухолями на ранних стадиях, в конечном итоге появляются признаки прогрессирования опухоли, и им, возможно, придется начать лечение в течение трех лет. [ 4 ] Мужчины, выбирающие активное наблюдение, избегают рисков хирургического вмешательства, лучевой терапии и других методов лечения. Риск прогрессирования заболевания и метастазирования (распространения рака) может быть увеличен, но этот риск увеличения кажется небольшим, если строго следовать программе наблюдения, обычно включающей серийные оценки ПСА и повторную биопсию простаты каждые 1–2 года в зависимости от тенденции ПСА. [ нужна медицинская ссылка ]
Результаты исследования 2011 года показывают, что активное наблюдение является лучшим выбором для пожилых пациентов «низкого риска». [ 5 ]
Операция
[ редактировать ]Хирургическое удаление простаты, или простатэктомия , является распространенным методом лечения рака простаты на ранней стадии или рака, который не поддается лучевой терапии. Наиболее распространенным типом является радикальная ретропубическая простатэктомия , когда хирург удаляет простату через разрез брюшной полости. Другой тип — радикальная промежностная простатэктомия , когда хирург удаляет простату через разрез в промежности , коже между мошонкой и задним проходом . Радикальную простатэктомию также можно выполнить лапароскопически через серию небольших (1 см) разрезов в брюшной полости с помощью хирургического робота или без него.
Радикальная простатэктомия
[ редактировать ]Радикальная простатэктомия эффективна при опухолях, не распространившихся за пределы простаты; [ 6 ] Показатели излечения зависят от факторов риска, таких как уровень ПСА и степень Глисона . Однако это может привести к повреждению нервов , что может существенно изменить качество жизни человека, перенесшего рак простаты. Радикальная простатэктомия связана с более значительным снижением сексуальной функции и увеличением недержания мочи (в основном стрессового недержания ), чем дистанционная лучевая терапия, альтернативный метод лечения. [ 7 ]
Радикальная простатэктомия традиционно использовалась отдельно, когда рак локализовался в предстательной железе. [ нужна ссылка ] В случае положительных результатов или местно-распространенного заболевания, обнаруженного при патологии, адъювантная лучевая терапия может улучшить выживаемость. [ нужна ссылка ] Хирургическое вмешательство также может быть предложено, если рак не реагирует на лучевую терапию. Однако, поскольку лучевая терапия вызывает изменения в тканях, простатэктомия после лучевой терапии имеет более высокий риск осложнений.
Чтобы избежать неблагоприятных побочных эффектов радикальной простатэктомии, врачи могут рекомендовать отсроченное лечение, которое может включать наблюдение и паллиативное лечение или активный мониторинг с некоторыми местными методами лечения при необходимости. По сравнению с наблюдением и паллиативным лечением радикальная простатэктомия, вероятно, снижает риск смерти по любой причине, включая смерть от рака простаты. [ 8 ] При радикальной простатэктомии и активном мониторинге риск смерти по любой причине, в том числе от рака простаты, вероятно, одинаков. [ 8 ] Операция также, вероятно, снижает риск распространения рака или его агрессивности. [ 8 ] Проблемы с эрекцией и подтекание мочи, вероятно, более вероятны у пациентов, перенесших хирургическое вмешательство, чем у тех, кто находится под активным наблюдением или наблюдением. [ 8 ]
Лапароскопический подход
[ редактировать ]Лапароскопическая радикальная простатэктомия (ЛРП) – это новый способ хирургического подхода к простате с целью ее лечения. В отличие от открытой хирургической формы операции по поводу рака простаты, лапароскопическая радикальная простатэктомия требует меньшего разреза. Опираясь на современные технологии, такие как миниатюризация , оптоволокно , лапароскопическая радикальная простатэктомия является минимально инвазивным методом лечения рака простаты, но он технически сложен и редко проводится в Соединенных Штатах. [ нужна ссылка ]
Роботизированная помощь
[ редактировать ]Некоторые полагают, что в руках опытного хирурга роботизированная лапароскопическая простатэктомия (RALP) может уменьшить положительные хирургические границы по сравнению с радикальной ретропубической простатэктомией (RRP) среди пациентов с раком простаты, согласно ретроспективному исследованию. [ 9 ] Относительное снижение риска составило 57,7%. Для пациентов с таким же риском, как и в этом исследовании (35,5% пациентов имели положительный хирургический край после RRP), это приводит к абсолютному снижению риска на 20,5%. Чтобы получить пользу, необходимо пройти лечение 4,9 пациентам ( число, необходимое для лечения = 4,9). Другие недавние исследования показали, что RALP приводит к значительно более высокому показателю положительной прибыли. [ 10 ] Другие исследования не выявили различий между роботизированной и открытой хирургией. [ 11 ] В обзоре всесторонне проанализированы данные исследований у мужчин с раком простаты, в которых сравнивалась RALP с открытой радикальной простатэктомией, и не было обнаружено различий в снижении смертности от этого рака, рецидивов или смертности от всех причин. [ 12 ] Качество жизни при обеих процедурах будет одинаковым в отношении мочевой и сексуальной функции, и, похоже, нет различий в послеоперационных хирургических осложнениях. [ 12 ] Роботизированная хирургия может иметь небольшой эффект на послеоперационную боль в период сразу после операции, более короткое пребывание в больнице и меньшую потребность в переливании крови. [ 12 ]
Одной из распространенных проблем, связанных с этой операцией, является недержание мочи или подтекание мочи, которое возникает в течение 6–12 месяцев после удаления катетера, установленного во время операции. При использовании RALP хирурги могут либо действовать стандартным подходом, либо использовать подход, который не разрезает тканевые соединения между передней частью мочевого пузыря и задней частью брюшной стенки, RALP с сохранением Ретциуса. [ 13 ] RALP с сохранением Ретциуса, вероятно, улучшает удержание мочи в течение одной недели после удаления катетера, но с большей вероятностью оставит положительный хирургический край, который может позволить раку вернуться. [ 13 ] Ретциус-сохраняющая RALP также может уменьшить подтекание мочи через 3–6 месяцев после операции, но через 12 месяцев воздержание, вероятно, будет аналогичным. [ 13 ]
Трансуретральная резекция
[ редактировать ]Трансуретральная резекция простаты , обычно называемая «ТУРП», представляет собой хирургическую процедуру, выполняемую, когда трубка, идущая от мочевого пузыря к половому члену ( уретре ), блокируется увеличением простаты. Как правило, ТУРП проводится при доброкачественной гиперплазии предстательной железы и не является окончательным методом лечения рака предстательной железы. Во время ТУРП небольшой инструмент ( цистоскоп ) вводится в половой член и блокирующая простата отсекается прижиганием .
Криохирургия
[ редактировать ]Криохирургия — малоинвазивный метод лечения рака предстательной железы, при котором предстательная железа подвергается воздействию отрицательных температур. [ 14 ] Под контролем УЗИ металлические стержни вводятся через кожу промежности в простату. Для охлаждения стержней используется высокоочищенный газ аргон, замораживающий окружающие ткани при температуре -186° C (-302° F ). Когда вода внутри клеток простаты замерзает, клетки умирают. Уретра теплой защищена от замерзания катетером, наполненным жидкостью. Общая анестезия реже используется при криохирургии, поэтому ее часто можно проводить в амбулаторных условиях клиники. [ 15 ]
Неясно, улучшает ли криохирургия качество жизни и смертность от рака простаты по сравнению с лучевой терапией. [ 15 ] Потенциальные побочные эффекты, связанные с криохирургией, включают задержку мочи, недержание и боль в области промежности, полового члена или мошонки. [ 15 ] Импотенция возникает в девяноста процентах случаев. [ нужна ссылка ] Потенциал серьезных побочных эффектов по сравнению с лучевой терапией не ясен. [ 15 ] Криохирургия менее инвазивна, чем радикальная простатэктомия. [ нужна ссылка ]
Хирургическое удаление яичек
[ редактировать ]При метастатическом заболевании, когда рак распространился за пределы простаты, удаление яичек (так называемая орхиэктомия может быть произведено ), чтобы снизить уровень тестостерона и контролировать рост рака. (См. гормональную терапию ниже).
Осложнения операции
[ редактировать ]Наиболее распространенными серьезными осложнениями хирургического вмешательства являются потеря контроля над мочеиспусканием и импотенция . Сообщаемая частота обоих осложнений широко варьируется в зависимости от того, как они оцениваются, кем и через какое время после операции, а также от условий (например, научные исследования в сравнении с данными, полученными на уровне сообщества или населения). [ нужна ссылка ]
Эректильная дисфункция
[ редактировать ]Хотя чувствительность полового члена и способность достигать оргазма обычно остаются неизменными, эрекция и эякуляция часто нарушаются. Такие лекарства, как силденафил (Виагра), тадалафил (Сиалис) или варденафил (Левитра) могут в некоторой степени восстановить потенцию. Для мужчин, страдающих эрекцией после простатэктомии, регулярный прием лекарств может привести к такой же частоте и качеству эрекций, о которых они сами сообщают, как и прием лекарств по мере необходимости. [ 16 ] Также могут быть одинаковые уровни серьезных нежелательных побочных эффектов для обоих типов использования лекарств. [ 16 ] Большинству мужчин с органо-ограниченным заболеванием более ограниченная «нервосберегающая» техника может помочь уменьшить недержание мочи и импотенцию. [ 17 ] [ 18 ]
Недержание мочи
[ редактировать ]Радикальная простатэктомия, трансуретральная резекция простаты (ТУРП) и лучевая терапия являются основными причинами стрессового недержания мочи у мужчин, причем ведущей причиной является радикальная простатэктомия. [ 19 ] В большинстве случаев недержание проходит в течение 12 месяцев при консервативном лечении. Множество факторов, таких как повреждение сфинктера уретры или нервных пучков, могут играть роль, вызывая в основном стрессовое недержание мочи . [ 20 ] Стрессовое недержание мочи возникает, когда сфинктер уретры (мышечный сфинктер, закрывающий мочевой пузырь) не закрывается должным образом, что приводит к подтеканию мочи в ситуациях, когда внутрибрюшное давление выше обычного, например, при смехе, чихании или кашле.
Консервативное лечение, такое как тренировка мышц тазового дна ( упражнения Кегеля ), было назначено для улучшения удержания мочи; доказательства эффективности у мужчин после радикальной простатэктомии оказались под вопросом. Согласно данным рандомизированного контрольного исследования Men After Prostate Surgery (MAPS), тренировка мышц тазового дна не оказалась терапевтической или экономически эффективной для улучшения удержания мочи. [ 21 ] [ нужен неосновной источник ]
Другие методы лечения включают использование зажимов для полового члена , трансуретральных наполнителей и катетеров , однако наиболее часто используемыми хирургическими методами лечения являются установка уретрального слинга или искусственного мочевого сфинктера . [ 19 ] Для людей со стрессовым недержанием мочи средней и тяжелой степени после операции на предстательной железе искусственный сфинктер мочевого пузыря является методом выбора, когда все другие консервативные меры не помогают. [ 22 ]
Лучевая терапия
[ редактировать ]Лучевая терапия , также известная как лучевая терапия, часто используется для лечения всех стадий рака простаты. Его также часто используют после операции, если операция не принесла успеха в лечении рака. [ нужна ссылка ] Лучевая терапия использует ионизирующее излучение для уничтожения клеток рака простаты. При поглощении тканями ионизирующее излучение, такое как гамма- и рентгеновское излучение, повреждает ДНК раковых клеток, что увеличивает вероятность апоптоза (гибель клеток). Нормальные клетки способны восстанавливать радиационные повреждения, а раковые клетки — нет. Лучевая терапия использует этот факт для лечения рака. Лучевая терапия, используемая при лечении рака простаты, включает дистанционную лучевую терапию и брахитерапию (в частности, брахитерапию простаты ).
Внешняя лучевая терапия
[ редактировать ]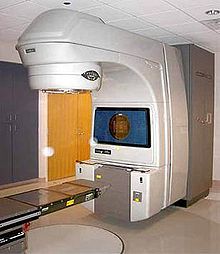
Внешняя лучевая терапия (ДЛТ) использует линейный ускоритель для производства высокоэнергетических рентгеновских лучей, луч которых направляется на простату. Техника, называемая лучевой терапией с модулированной интенсивностью ( IMRT ), может использоваться для регулировки луча излучения в соответствии с формой опухоли, что позволяет назначать более высокие дозы на простату и семенные пузырьки с меньшим повреждением мочевого пузыря и прямой кишки. Дистанционная лучевая терапия обычно проводится в течение нескольких недель с ежедневными посещениями центра лучевой терапии. Новые виды лучевой терапии, такие как IMRT, имеют меньше побочных эффектов, чем традиционное лечение. Однако в краткосрочной перспективе ДЛТ ассоциировалась с резким ухудшением симптомов обструкции мочевыводящих путей и кишечника. Было показано, что эти симптомы со временем уменьшаются. [ 7 ] Тридцать шесть центров в Соединенных Штатах в настоящее время используют протонную терапию рака простаты, при которой для уничтожения раковых клеток используются протоны, а не рентгеновские лучи. [ 23 ] Исследователи также изучают виды стереотаксической лучевой терапии тела (SBRT) для лечения рака простаты. [ нужна медицинская ссылка ]
Брахитерапия
[ редактировать ]Брахитерапия с постоянными имплантатами является популярным методом лечения для пациентов с признаками низкого и среднего риска, может проводиться амбулаторно и связана с хорошими 10-летними результатами при относительно низкой заболеваемости. [ 24 ] Он включает в себя введение около 100 маленьких «семен», содержащих радиоактивный материал (например, йод-125 или палладий-103 ), с помощью иглы через кожу промежности непосредственно в опухоль под спинальной или общей анестезией. Эти семена излучают рентгеновские лучи с более низкой энергией , которые способны распространяться лишь на небольшое расстояние. Хотя семена со временем становятся инертными, они навсегда остаются в простате. Риск заражения других людей от мужчин с имплантированными семенами обычно считается незначительным. [ 25 ] Тем не менее, мужчинам рекомендуется поговорить со своими врачами о любых специальных временных мерах предосторожности в отношении маленьких детей и беременных женщин. [ 26 ]
Использование
[ редактировать ]Лучевая терапия обычно используется при лечении рака простаты. Его можно использовать вместо хирургического вмешательства или после хирургического вмешательства при раке предстательной железы на ранней стадии (адъювантная лучевая терапия). Лучевую терапию также можно сочетать с гормональной терапией при заболеваниях среднего риска, когда хирургическое вмешательство или лучевая терапия сами по себе вряд ли излечат рак. Некоторые онкологи-радиологи сочетают внешнее лучевое облучение и брахитерапию в ситуациях среднего и высокого риска. Лучевая терапия часто используется в сочетании с гормональной терапией у пациентов из группы высокого риска. [ 27 ]
Для мужчин старше 64 лет с раком простаты, ограниченным тазом, использование меньших и более высоких доз радиации ( гифракционирование ) приводит к одинаковым показателям общей выживаемости. [ 28 ] Риск смерти от рака простаты или возникновения острых побочных эффектов со стороны мочевого пузыря может быть таким же, как и при длительном лучевом лечении. [ 28 ] Другие используют «тройную модальную» комбинацию дистанционной лучевой терапии, брахитерапии и гормональной терапии. На поздних стадиях рака простаты радиация используется для лечения болезненных метастазов в костях или уменьшения компрессии спинного мозга.
Лучевая терапия также используется после радикальной простатэктомии либо в случае рецидива рака, либо в случае обнаружения во время операции множественных факторов риска. В двух отдельных рандомизированных исследованиях было продемонстрировано, что лучевая терапия, проводимая сразу после операции при наличии факторов риска (положительный хирургический край, экстракапсулярное расширение, вовлечение семенных пузырьков), уменьшает рецидивы рака, уменьшает отдаленные метастазы и увеличивает общую выживаемость. [ 29 ]
Побочные эффекты
[ редактировать ]Побочные эффекты лучевой терапии могут возникнуть через несколько недель после начала лечения. Оба типа лучевой терапии могут вызвать диарею и легкое ректальное кровотечение из-за радиационного проктита , а также потенциальное недержание мочи и импотенцию. Симптомы имеют тенденцию к улучшению с течением времени, за исключением эрекции, которая с течением времени обычно ухудшается. [ нужна ссылка ]
Новый метод уменьшения радиационного поражения прямой кишки у пациентов с раком простаты предполагает использование рассасывающейся прокладки, помещаемой между простатой и прямой кишкой.

Такие спейсеры коммерчески доступны в некоторых регионах и проходят клинические испытания в других. [ 30 ] Временно изменяя анатомию, эти продукты могут улучшить воздействие на рак, минимизируя при этом риск для соседних здоровых тканей. Спейсеры для прямой кишки простаты должны быть совместимы со всеми методами лучевой терапии рака простаты, включая 3D-конформную, IMRT, стереотаксическую радиацию и брахитерапию. [ нужна ссылка ]
Сравнение с хирургией
[ редактировать ]Множественные ретроспективные анализы показали, что общая выживаемость и безрецидивная выживаемость одинаковы при радикальной простатэктомии, дистанционной лучевой терапии и брахитерапии. [ 31 ] Однако недавнее ретроспективное исследование показывает, что мужчины в возрасте до 60 лет с раком простаты высокой степени имеют более высокие показатели выживаемости после хирургического вмешательства, чем при лучевом облучении. [ 32 ] Показатели импотенции при сравнении лучевой терапии с нервосберегающей хирургией аналогичны. Лучевая терапия приводит к более низким показателям недержания по сравнению с хирургическим вмешательством, но имеет более высокую частоту случайных легких ректальных кровотечений. [ 33 ] Мужчины, прошедшие дистанционную лучевую терапию, могут иметь несколько более высокий риск развития рака толстой кишки и мочевого пузыря в дальнейшем . [ 34 ]
Поскольку рак простаты, как правило, является мультифокальным заболеванием, традиционная простатэктомия устраняет все местные поражения путем удаления всей простаты. Однако была выдвинута гипотеза, что «индексное поражение» может быть ответственным за прогрессирование заболевания. Таким образом, фокальная терапия, направленная на очаговое поражение, может эффективно лечить рак предстательной железы, сохраняя при этом остальную часть железы. Интервенционные радиологи начали лечить рак предстательной железы с помощью минимально инвазивных методов лечения, таких как криоабляция , HIFU , радиочастотная абляция и фотодинамическая терапия, которые позволяют проводить фокальную терапию под контролем изображения. Эти методы лечения все еще находятся на начальной или экспериментальной стадии; однако, поскольку они сохраняют ткани, они потенциально могут снизить неблагоприятные последствия лечения, такие как импотенция и недержание. Небольшое проспективное исследование, опубликованное в журнале European Urology в феврале 2015 года, оценивало очаговое лечение индексных поражений с помощью HIFU у пациентов с мультифокальным раком простаты и обнаружило, что у большинства мужчин функция мочеполовой системы вернулась к исходному уровню, а у 86% мужчин не было клинически значимого рака простаты. в один год. [ 35 ] Небольшие нерандомизированные когортные исследования со средним периодом наблюдения 17–47 месяцев показали, что криоабляция , HIFU и фототерапия связаны с низким уровнем побочных эффектов и уровнем раннего контроля заболевания на уровне 83–100% на основании отрицательных результатов биопсии. [ 36 ]
Люди с раком простаты, которым особенно полезна фокальная терапия с помощью HIFU, — это мужчины с рецидивом рака после удаления железы. Частота рецидивов рака после хирургической резекции может достигать 15–20%. [ нужна ссылка ] МРТ улучшает раннее выявление рака, поэтому терапию под контролем МРТ можно применять для лечения рецидивирующих заболеваний. Кроме того, для мужчин, которые уже потерпели неудачу в спасительной лучевой терапии и у которых остались ограниченные терапевтические возможности, интервенционная терапия может предложить больше шансов потенциально вылечить их болезнь. Хотя недавние исследования продемонстрировали осуществимость этих методов лечения, необходима дополнительная работа для дальнейшей оценки того, какие пациенты лучше всего подходят для этих процедур, и определения долгосрочной эффективности. [ 37 ]
Фокусированный ультразвук высокой интенсивности
[ редактировать ]Фокусированный ультразвук высокой интенсивности (HIFU) впервые был использован в 1940-х и 1950-х годах для разрушения опухолей в центральной нервной системе. С тех пор было доказано, что HIFU эффективен при разрушении злокачественных тканей головного мозга, простаты, селезенки, печени, почек, молочной железы и костей. [ 38 ]
HIFU при раке простаты использует ультразвук для абляции/разрушения ткани простаты. Во время процедуры HIFU звуковые волны используются для нагрева ткани простаты, тем самым разрушая раковые клетки. По сути, ультразвуковые волны фокусируются на определенных участках простаты для устранения рака простаты с минимальным риском воздействия на другие ткани или органы. Температура в точке фокуса звуковых волн может превышать 100 ° C (212 ° F ). [ 38 ] Однако многие исследования HIFU проводились производителями устройств HIFU или членами консультативных групп производителей. [ 39 ]
Противопоказаниями к использованию HIFU при раке простаты являются объем простаты более 40 граммов, что может препятствовать достижению целевых волн HIFU передних и передне-базальных областей простаты, анатомические или патологические состояния, которые могут препятствовать введению или смещению датчика HIFU в прямую кишку и кальциноз большого объема в предстательной железе, что может привести к рассеянию HIFU и ухудшению передачи. [ 40 ]
Британское исследование очагового HIFU в 2012 году на 41 пациенте сообщило об отсутствии гистологических признаков рака у 77% мужчин, прошедших лечение (95% доверительный интервал: 61–89%) при целевой биопсии через 12 месяцев, а также о низкой частоте побочных эффектов со стороны мочеполовой системы. [ 41 ] Однако это не обязательно означает, что 77% мужчин окончательно излечились от рака простаты, поскольку в процессе биопсии присутствуют систематические и случайные ошибки выборки, и поэтому рецидив или ранее невыявленный рак может быть пропущен. [ 42 ]
Гормональная терапия
[ редактировать ]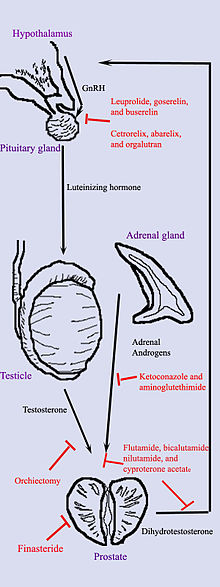
Андрогенная депривационная терапия
[ редактировать ]Гормональная терапия использует лекарства или хирургическое вмешательство, чтобы блокировать получение клетками рака простаты дигидротестостерона (ДГТ), гормона, вырабатываемого в простате и необходимого для роста и распространения большинства клеток рака простаты. Блокирование ДГТ часто приводит к тому, что рак простаты перестает расти и даже уменьшается. Однако гормональная терапия редко излечивает рак простаты, поскольку рак, который первоначально реагирует на гормональную терапию, обычно становится устойчивым через один-два года. Поэтому гормональная терапия обычно используется, когда рак распространился из простаты. Его также можно назначать некоторым мужчинам, проходящим лучевую терапию или операцию, чтобы предотвратить возвращение рака. [ 43 ]
Гормональная терапия рака простаты нацелена на пути, которые организм использует для выработки ДГТ. Петля обратной связи, включающая яички, гипоталамус, гипофиз, надпочечники и предстательную железу, контролирует уровень ДГТ в крови. Во-первых, низкий уровень ДГТ в крови стимулирует гипоталамус вырабатывать гонадотропин-рилизинг гормон (ГнРГ). Затем ГнРГ стимулирует гипофиз к выработке лютеинизирующего гормона (ЛГ), а ЛГ стимулирует яички к выработке тестостерона. Наконец, тестостерон из яичек и дегидроэпиандростерон из надпочечников стимулируют простату вырабатывать больше ДГТ. Гормональная терапия может снизить уровень ДГТ, прерывая этот путь в любой момент. Существует несколько форм гормональной терапии:
- Орхиэктомия , также называемая «кастрацией», представляет собой операцию по удалению яичек. Поскольку яички производят большую часть тестостерона в организме, после орхиэктомии уровень тестостерона падает. Теперь простате не только не хватает стимула тестостерона для выработки ДГТ, но также не хватает тестостерона для преобразования в ДГТ. Орхиэктомия считается золотым стандартом лечения. [ 44 ]
- Антиандрогены — это лекарства, такие как флутамид , нилутамид , бикалутамид , энзалутамид , апалутамид и ципротерона ацетат , которые напрямую блокируют действие тестостерона и ДГТ на клетки рака простаты.
- Мужчинам с метастатическим гормоночувствительным раком простаты врачи могут рекомендовать добавить химиотерапию на основе таксанов ( доцетаксел ). к гормональной терапии [ 45 ] Эта комбинация, вероятно, улучшает общую и онкологическую выживаемость, замедляя распространение рака. Однако химиотерапия на основе таксанов может вызвать усиление побочных эффектов. [ 45 ]
- Лекарства, которые блокируют выработку андрогенов надпочечниками, таких как ДГЭА, включают кетоконазол и аминоглутетимид . Поскольку надпочечники производят лишь около 5% андрогенов в организме, эти препараты обычно используются только в сочетании с другими методами, которые могут блокировать 95% андрогенов, вырабатываемых яичками. Эти комбинированные методы называются полной андрогенной блокадой (ТАБ). TAB также можно достичь с помощью антиандрогенов.
- Действие ГнРГ можно прервать одним из двух способов. Антагонисты ГнРГ, такие как абареликс и дегареликс, подавляют выработку ЛГ напрямую, воздействуя на переднюю долю гипофиза. Агонисты ГнРГ, такие как лейпрорелин и гозерелин, подавляют ЛГ посредством процесса подавления после первоначального эффекта стимуляции, что может вызвать начальную вспышку опухоли. Чтобы предотвратить стимуляцию роста опухоли во время первоначального всплеска ЛГ, за неделю до и через три недели после введения агонистов ГнРГ назначают антиандроген, такой как ципротерона ацетат. Абареликс и дегареликс являются примерами антагонистов ГнРГ, тогда как агонисты ГнРГ включают лейпролид, гозерелин, трипторелин и бусерелин . Первоначально агонисты ГнРГ увеличивают выработку ЛГ. Однако, поскольку постоянное введение лекарства не соответствует естественному ритму выработки организма, выработка как ЛГ, так и ГнРГ снижается через несколько недель. [ 46 ]
- Абиратерона ацетат был одобрен FDA в апреле 2011 года для лечения резистентного к кастрации рака простаты у пациентов, у которых терапия доцетакселом оказалась неэффективной . Абиратерона ацетат ингибирует фермент, известный как CYP17 , который используется в организме для выработки тестостерона. [ 47 ] [ 48 ] Обзор 2020 года показал, что применение абиратерона ацетата в сочетании с гормональной терапией улучшает общую выживаемость мужчин с раком простаты, а также увеличивает риск тяжелых и опасных для жизни побочных эффектов, что приводит к прекращению лечения этими препаратами. [ 49 ]
Наиболее успешными гормональными методами лечения являются орхиэктомия и агонисты ГнРГ. Несмотря на более высокую стоимость, агонисты ГнРГ часто выбирают вместо орхиэктомии по косметическим и эмоциональным причинам. В конце концов, полная андрогенная блокада может оказаться более эффективной, чем орхиэктомия или монотерапия агонистами ГнРГ.
Каждый метод лечения имеет недостатки, которые ограничивают его использование в определенных обстоятельствах. Хотя орхиэктомия представляет собой операцию с низким уровнем риска, психологические последствия удаления яичек могут быть значительными, и бесплодие несомненно. Потеря тестостерона может вызвать приливы жара , увеличение веса, потерю либидо , увеличение груди ( гинекомастия ) , импотенцию, атрофию полового члена и остеопороз . Агонисты ГнРГ в конечном итоге вызывают те же побочные эффекты, что и орхиэктомия, но могут вызывать ухудшение симптомов в начале лечения. При первом применении агонистов ГнРГ выбросы тестостерона могут привести к усилению боли в костях из-за метастатического рака, поэтому для смягчения этих побочных эффектов часто добавляют антиандрогены или абареликс. Эстрогены обычно не используются, поскольку они увеличивают риск сердечно-сосудистых заболеваний и образования тромбов . В целом антиандрогены не вызывают импотенции и обычно вызывают меньшую потерю костной и мышечной массы. Кетоконазол может вызвать повреждение печени при длительном применении, а аминоглутетимид может вызвать повреждение кожи. высыпания .
Когда гормональное лечение целесообразно, врачи могут начать лечение как можно раньше, сразу после постановки диагноза, или подождать, пока рак не начнет расти. Для мужчин с распространенным раком простаты раннее гормональное лечение, вероятно, снижает риск смерти от любой причины, включая смерть от рака простаты, без серьезного влияния на качество жизни. [ 50 ] Однако раннее начало лечения может привести к усилению усталости и сердечной слабости. [ 50 ]
Одно исследование 2021 года, проведенное JAMA Oncology, было направлено на сравнение эффективности и безопасности, определенных в рандомизированных клинических исследованиях системного лечения метастатического рака простаты, чувствительного к кастрации (mCSPC). Исследование показало, что «в качестве дополнительного лечения к АДТ абиратерона ацетат и апалутамид могут обеспечить наибольшие преимущества в общей выживаемости при относительно низких рисках SAE . Хотя энзалутамид может в наибольшей степени улучшить выживаемость без рентгенологического прогрессирования, необходимо более длительное наблюдение». чтобы изучить общие преимущества выживаемости, связанные с энзалутамидом». [ 51 ]
Эстрогенная терапия
[ редактировать ]Высокие дозы эстрогеновой терапии используются при лечении рака простаты. [ 52 ] эстрогены Использованные включают диэтилстильбэстрол , фосфестрол , этинилэстрадиол , сульфонат этинилэстрадиола , полиэстрадиолфосфат и ундецилат эстрадиола , а также двойной эстрогенный и цитостатический агент эстрамустинфосфат . [ 52 ] [ 53 ] новые эстрогены с улучшенной переносимостью и безопасностью, такие как GTx-758 . Также изучались [ 54 ] [ 55 ] Эстрогены эффективны при раке простаты, поскольку они являются функциональными антиандрогенами. [ 53 ] [ 56 ] Они оба подавляют уровень тестостерона до кастрационного уровня благодаря своему антигонадотропному эффекту. [ 53 ] [ 56 ] и они уменьшают долю свободного и биодоступного тестостерона за счет повышения уровня глобулина, связывающего половые гормоны . [ 54 ] [ 56 ] Эстрогены могут также оказывать прямое цитотоксическое действие на предстательную железу . [ 53 ]
Было обнаружено, что эстрогены эквивалентны по эффективности андрогенной депривационной терапии посредством хирургической или медицинской кастрации и нестероидным антиандрогенам . [ 56 ] Кроме того, они предотвращают приливы , сохраняют плотность костной ткани , сохраняют некоторый сексуальный интерес , улучшают качество жизни и являются гораздо менее дорогостоящими, чем традиционная андрогенная депривационная терапия. [ 57 ] [ 58 ] [ 59 ] [ 60 ] [ 61 ] [ 62 ] [ 63 ] Однако эстрогены вызывают феминизацию и гинекомастию в качестве побочных эффектов . [ 58 ] [ 59 ] [ 60 ] [ 62 ] [ 63 ] Более того, в дозировке от 3 до 5 мг/день диэтилстильбестрол может увеличить сердечно-сосудистую смертность , особенно у тех пациентов, у которых уже нарушена сердечно-сосудистая система. Диэтилстильбэстрол в дозе 1–2 мг/день, по-видимому, безопасен и эффективен для пациентов с ХРПЖ, имеющих здоровую сердечно-сосудистую систему и одновременно принимающих низкие дозы аспирина. [ 56 ] Хотя наиболее часто используемые эстрогены, пероральные и синтетические эстрогены, такие как диэтилстильбэстрол и этинилэстрадиол, увеличивают сердечно-сосудистую смертность, некоторые эстрогены, а именно биоидентичные парентеральные эстрогены, такие как полиэстрадиолфосфат и высокие дозы трансдермального эстрадиола , делают это ограниченно или не делают этого вообще; это объясняется разной степенью влияния классов эстрогенов на синтез белка в печени и расширением факторов свертывания крови . [ 56 ]
Фокальная терапия
[ редактировать ]Необратимая электропорация (IRE)
[ редактировать ]Необратимая электропорация (IRE) — это новая фокальная терапия рака простаты, особенно подходящая для небольших опухолей, ограниченных простатой. В отличие от традиционных методов лечения, таких как радикальная простатэктомия или лучевая терапия, которые могут привести к побочным эффектам, таким как недержание мочи и эректильная дисфункция, IRE стремится минимизировать такие риски, точно воздействуя на раковую ткань и сохраняя окружающие нераковые структуры. [ 64 ] [ 65 ]
Представленный клинически в начале 21 века, IRE использует электрические поля для создания нанопор в клеточных мембранах раковых клеток, что приводит к гибели клеток без значительного выделения тепла. Этот нетермический механизм имеет решающее значение для сохранения окружающих нервов и кровеносных сосудов, потенциально уменьшая побочный ущерб, связанный с другими терапевтическими методами. Из-за этих преимуществ IRE исследуется на предмет его полезности для пациентов, которые не могут быть идеальными кандидатами для традиционных методов лечения или для тех, кто отдает приоритет функциональным результатам. [ 66 ]
Исследования, проведенные на сегодняшний день, включая ретроспективную оценку 471 метода лечения IRE, обсуждали осуществимость, безопасность, токсичность и функциональные результаты, предполагая, что IRE может стать стандартным методом лечения рака простаты и средством решения проблем распространенного рака Т4. [ 67 ] Учитывая свой потенциал, IRE является предметом текущих исследований, в том числе многоцентрового регистрового исследования (NCT02255890), поскольку медицинское сообщество работает над установлением своей позиции в стандартах лечения рака простаты. [ 68 ]
Несмотря на свои преимущества, IRE остается экспериментальной терапией, и необходимы более крупные долгосрочные исследования, чтобы полностью понять ее эффективность и профиль безопасности. Как и в случае любого нового метода лечения, отбор пациентов имеет решающее значение, и IRE следует рассматривать в более широком контексте целей лечения отдельного пациента и общего состояния здоровья. [ 69 ] [ 70 ]
Фотодинамическая терапия
[ редактировать ]Фотодинамическая терапия (ФДТ) — это новая фокальная терапия для лечения рака простаты, предлагающая минимально инвазивную альтернативу традиционным методам лечения. ФДТ предполагает введение фотосенсибилизирующего агента , который активируется под воздействием определенного типа света. При активации этот агент вырабатывает активные формы кислорода, которые избирательно уничтожают раковые клетки, сводя к минимуму повреждение окружающих здоровых тканей. [ 71 ] [ 72 ]
Клиническое применение ФДТ при раке простаты продемонстрировало потенциальные преимущества с точки зрения эффективности и безопасности, особенно для пациентов с локализованными опухолями низкого и среднего риска. ФДТ дает преимущество, воздействуя на определенные области простаты, что может помочь сохранить мочевыделительные и сексуальные функции, на которые часто влияют более инвазивные процедуры, такие как хирургическое вмешательство или облучение. [ 73 ]
Несмотря на свои преимущества, ФДТ при раке простаты все еще находится на стадии клинических исследований, при этом продолжаются исследования, направленные на повышение точности терапии, расширение ее применения и установление долгосрочных результатов. Исследователи продолжают изучать возможность интеграции ФДТ с другими методами лечения, такими как химиотерапия и иммунотерапия , для повышения общей эффективности лечения. [ 74 ]
В целом, фотодинамическая терапия представляет собой многообещающее достижение в лечении рака простаты, предоставляя вариант лечения, сочетающий эффективность с качеством жизни. [ 75 ]
Электрохимиотерапия
[ редактировать ]Электрохимиотерапия (ЭСТ) — относительно новый подход в лечении рака, сочетающий использование электрических импульсов с химиотерапией для усиления поглощения лекарств раковыми клетками. Хотя он преимущественно используется для лечения рака кожи и доступных опухолей, его применение при раке простаты остается экспериментальным и находится на стадии клинических исследований. Этот метод включает в себя применение коротких интенсивных электрических импульсов, которые временно увеличивают проницаемость клеточной мембраны, позволяя более высоким концентрациям химиотерапевтических препаратов проникать в клетки. [ 76 ]
В настоящее время использование ЭСТ при раке простаты ограничено клиническими испытаниями и еще не признано стандартным вариантом лечения. Ранние исследования показывают, что ЭСТ потенциально может быть эффективной для лечения локализованного рака простаты, предлагая минимально инвазивную альтернативу традиционным методам лечения, таким как хирургия и лучевая терапия, с меньшим количеством побочных эффектов. Однако необходимы дополнительные исследования для определения оптимальных протоколов и долгосрочной эффективности этого подхода. [ 77 ]
Поскольку исследования продолжаются, электрохимиотерапия может дать новую надежду пациентам с раком простаты, особенно тем, кто ищет менее инвазивные варианты лечения или тем, для кого традиционные методы лечения оказались неэффективными. Клинические результаты и дальнейшие исследования определят будущую роль ЭСТ в лечении рака простаты. [ 78 ]
Изменения образа жизни
[ редактировать ]Увеличение простаты может вызвать трудности с полным опорожнением мочевого пузыря. Эта ситуация, при которой в мочевом пузыре имеется остаточный объем, склонна к таким осложнениям, как цистит и камни в мочевом пузыре , также часто встречается у пациентов с доброкачественной гиперплазией предстательной железы . Часто предлагалось изменить положение мочеиспускания у мужчин с симптомами, однако результаты исследований показали неоднородность . Метаанализ людей с увеличением простаты и здоровых мужчин показал значительное уменьшение остаточного объема, при этом была обнаружена тенденция к улучшению скорости потока мочи и уменьшению времени мочеиспускания. [ 79 ] Считается, что эффект изменения положения возникает в результате расслабления мускулатуры таза, которая сокращается в положении стоя, тем самым влияя на уродинамику.
Есть некоторые доказательства того, что физические упражнения могут быть полезны для людей с раком простаты, однако их эффект неясен. [ 80 ]
Рецидивирующее заболевание
[ редактировать ]После операции или лучевой терапии уровень ПСА может снова начать повышаться, что называется биохимическим рецидивом, если уровень ПСА достигает определенного порога (обычно 0,1 или 0,2 нг/мл при хирургическом вмешательстве). Через 10 лет наблюдения после операции общий риск биохимического рецидива составляет 30–50%, в зависимости от исходного состояния риска, и единственным методом лечения является спасительная лучевая терапия (СЛТ). [ 81 ] СЗТ часто назначают в сочетании с андрогенной депривационной терапией на срок до двух лет. Ретроспективное исследование пациентов, получавших СЗТ в период с 1987 по 2013 год, показало, что у 56% из 2460 пациентов не было биохимических нарушений после 5 лет наблюдения. [ 82 ] Среди тех, у кого ПСА менее 0,2 до СЗТ, это составило 71%.
Обширное заболевание
[ редактировать ]Паллиативная помощь при поздних стадиях рака простаты направлена на продление жизни и облегчение симптомов метастатического заболевания. Как отмечалось выше , абиратерон демонстрирует некоторые перспективы в лечении рака простаты на поздних стадиях. Он вызывает резкое снижение уровня ПСА и размеров опухолей при агрессивном раке простаты на поздних стадиях у 70% пациентов. [ 47 ] [ 48 ] Химиотерапия может быть предложена для замедления прогрессирования заболевания и отсрочки появления симптомов. Наиболее часто используемая схема сочетает химиотерапевтический препарат доцетаксел с кортикостероидом, таким как преднизолон . Одно исследование показало, что лечение доцетакселом с преднизоном продлевало жизнь с 16,5 месяцев для тех, кто принимал митоксантрон и преднизолон, до 18,9 месяцев для тех, кто принимал доцетаксел + преднизолон. [ 83 ] бисфосфонаты, такие как золедроновая кислота, Было показано, что замедляют развитие скелетных осложнений, таких как переломы или необходимость лучевой терапии, у пациентов с гормонорефрактерным метастатическим раком простаты. [ 84 ] Ксофиго — это новый альфа-излучающий фармацевтический препарат, нацеленный на метастазы в кости . Испытания фазы II показывают увеличение продолжительности жизни пациентов, уменьшение боли и улучшение качества жизни.
Боль в костях, вызванная метастатическим заболеванием, лечится опиоидными обезболивающими, такими как морфин и оксикодон . Дистанционная лучевая терапия, направленная на костные метастазы, может облегчить боль . Инъекции некоторых радиоизотопов , таких как стронций-89 , фосфор-32 или самарий-153 , также воздействуют на костные метастазы и могут помочь облегчить боль.
Для мужчин с раком простаты и метастазами в костях золедроновая кислота ( бисфосфонат ) и деносумаб ( ингибитор RANK-лиганда ), по-видимому, являются наиболее эффективными в предотвращении скелетных осложнений. [ 85 ] Однако эти препараты, по-видимому, также вызывают более частые и тяжелые побочные эффекты, включая почечную недостаточность при лечении золедроновой кислотой и остеонекроз челюсти при лечении деносумабом . [ 85 ]
Альтернативные методы лечения
[ редактировать ]В качестве альтернативы активному наблюдению или радикальному лечению также исследуются другие методы лечения рака простаты. Было показано, что уровень ПСА снижается у мужчин с выраженным локализованным раком простаты при использовании веганской диеты (разрешена рыба), регулярных физических упражнениях и снижении стресса. [ 86 ] Эти результаты до сих пор оказались стойкими после двухлетнего лечения. Однако в этом исследовании веганская диета не сравнивалась ни с активным наблюдением, ни с окончательным лечением, и поэтому не может комментировать сравнительную эффективность веганской диеты при лечении рака простаты. [ 87 ]
В краткосрочных исследованиях было показано, что многие другие отдельные агенты снижают уровень ПСА, замедляют время удвоения ПСА или оказывают аналогичное воздействие на вторичные маркеры у мужчин с локализованным раком, например, гранатовый сок или генистеин, изофлавон, содержащийся в различных бобовых. [ 88 ] [ 89 ]
Потенциал совместного использования нескольких таких агентов, не говоря уже о сочетании их с изменением образа жизни, еще не изучен. Опубликован более тщательный обзор естественных подходов к лечению рака простаты. [ 90 ]
Доказано, что нейтроны превосходят рентгеновские лучи при лечении рака предстательной железы. Обоснование заключается в том, что опухоли, содержащие гипоксические клетки (клетки с достаточной концентрацией кислорода, чтобы быть жизнеспособными, но недостаточной для того, чтобы быть радиочувствительными к рентгеновским лучам) и клетки с дефицитом кислорода, устойчивы к уничтожению рентгеновскими лучами. Таким образом, более низкий коэффициент усиления кислорода (OER) нейтронов дает преимущество. Кроме того, нейтроны обладают более высокой относительной биологической эффективностью (ОБЭ) для медленно растущих опухолей, чем рентгеновские лучи, что дает преимущество в уничтожении опухолевых клеток. [ 91 ]
Профилактика
[ редактировать ]Ни селен , ни витамин Е не оказались эффективными в предотвращении рака простаты . [ 92 ]
Компромиссы
[ редактировать ]Дилемма компромисса относится к выбору между ожидаемыми полезными и вредными эффектами с точки зрения выживаемости и качества жизни для конкретного лечения. Примером такого компромисса при лечении рака простаты являются симптомы мочеиспускания и кишечника, а также снижение сексуальной функции . [ 93 ] Насколько распространены эти симптомы и страдания, которые они вызывают, варьируются в зависимости от типа лечения и отдельных людей. [ 94 ]
Один из вариантов — обменять сохранную сексуальную функцию на возможность увеличения продолжительности жизни без радикального лечения. Выбор предполагает компромисс, поэтому для человека и врача крайне важно иметь доступ к информации об установленных преимуществах лечения и побочных эффектах. Шведское исследование показало, что готовность пойти на такой компромисс среди мужчин значительно различается. [ 93 ] В то время как шесть из десяти были готовы рассмотреть компромисс между продолжительностью жизни и сохранностью сексуальной функции, учитывая нынешние знания о преимуществах лечения клинически локализованного рака простаты, четверо из десяти заявили, что они при всех обстоятельствах выберут лечение, независимо от риск снижения сексуальной функции. Доступ к достоверной эмпирической информации имеет решающее значение для принятия таких решений. Ключевыми факторами здесь являются отношение человека к болезни, его эмоциональные ценности и религиозные убеждения. Значительная часть людей и врачей испытывают стресс, пытаясь найти компромисс между различными вариантами лечения и побочными эффектами лечения, что усугубляет стресс от диагностированного рака. Ситуация усугубляется тем, что восемь из десяти человек с раком простаты не имеют кому-то, кому можно доверять, кроме супруга, и каждый пятый живет в полной эмоциональной изоляции . [ 95 ]
Американская урологическая ассоциация (AUA), Американское общество радиационной онкологии (ASTRO) и Общество урологической онкологии (SUO) выпустили совместные рекомендации по совместному принятию решений с пациентами с локализованным раком простаты, чтобы помочь пациентам ориентироваться в этих решениях. [ 96 ] Систематический обзор литературы, проведенный в 2017 году, показал, что, хотя большинство исследований рака простаты сосредоточено на вариантах лечения, ориентированных на выживаемость, было мало доказательств того, что результаты, ориентированные на пациента, оценивались в связи со сравнительной эффективностью лечения. [ 97 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Резник М.Дж., Лаккетти С., Бергман Дж., Хауке Р.Дж., Хоффман К.Э., Кунгель Т.М. и др. (март 2015 г.). «Руководство по уходу за выжившими после рака простаты: одобрение рекомендаций по клинической практике Американского общества клинической онкологии» . Журнал клинической онкологии . 33 (9): 1078–85. дои : 10.1200/JCO.2014.60.2557 . ПМИД 25667275 . S2CID 24355867 .
- ^ Кроуфорд-Уильямс Ф., Марч С., Гудвин Б.С., Ральф Н., Гальван Д.А., Ньютон Р.У. и др. (октябрь 2018 г.). «Вмешательства по выживанию после рака простаты: систематический обзор обзоров» (PDF) . Психоонкология . 27 (10): 2339–2348. дои : 10.1002/пон.4888 . ПМИД 30255558 . S2CID 52823451 .
- ^ «Рак простаты с первого взгляда» . www.shavemagazine.com . Архивировано из оригинала 14 июля 2018 г. Проверено 6 августа 2009 г.
- ^ Ву Х., Сунь Л., Моул Дж.В., Ву Х.И., МакЛеод Д.Г., Амлинг С. и др. (март 2004 г.). «Бдительное ожидание и факторы, прогнозирующие вторичное лечение локализованного рака простаты». Журнал урологии . 171 (3): 1111–6. дои : 10.1097/01.ju.0000113300.74132.8b . ПМИД 14767282 .
- ^ «Активное наблюдение может быть предпочтительным вариантом у некоторых мужчин с раком простаты» . Архивировано из оригинала 3 мая 2011 года.
- ^ Билл-Аксельсон А., Холмберг Л., Рууту М., Хэггман М., Андерссон С.О., Брателл С., Спонгберг А., Буш С., Нордлинг С., Гармо Х., Палмгрен Дж., Адами Х.О., Норлин Б.Дж., Йоханссон Дж.Э. (май 2005 г.). «Радикальная простатэктомия в сравнении с бдительным ожиданием при раннем раке простаты» . Медицинский журнал Новой Англии . 352 (19): 1977–84. doi : 10.1056/NEJMoa043739 . ПМИД 15888698 . S2CID 44790644 .
- ^ Jump up to: а б Чен С, Чен З, Ван К, Ху Л, Сюй Р, Хэ Икс (ноябрь 2017 г.). «Сравнение качества жизни, связанного со здоровьем, при хирургическом вмешательстве и лучевой терапии при локализованном раке простаты: систематический обзор и метаанализ» . Онкотаргет . 8 (58): 99057–65. дои : 10.18632/oncotarget.21519 . ПМЦ 5716791 . ПМИД 29228751 .
- ^ Jump up to: а б с д Верноой Р.В., Ланси М., Клевес А., Дам П., Бангма Ч., Абен К.К. (июнь 2020 г.). «Радикальная простатэктомия в сравнении с отсроченным лечением локализованного рака простаты» . Кокрановская база данных систематических обзоров . 2020 (6): CD006590. дои : 10.1002/14651858.cd006590.pub3 . ПМК 7270852 . ПМИД 32495338 .
- ^ Смит Дж.А., Чан Р.К., Чанг С.С., Херрелл С.Д., Кларк П.Е., Баумгартнер Р., Куксон М.С. (декабрь 2007 г.). «Сравнение частоты и расположения положительных хирургических краев при роботизированной лапароскопической радикальной простатэктомии и открытой позадилонной радикальной простатэктомии». Журнал урологии . 178 (6): 2385–9, обсуждение 2389–90. дои : 10.1016/j.juro.2007.08.008 . ПМИД 17936849 .
- ^ Оу Ю.К., Ян Ч.Р., Ван Дж., Ченг С.Л., Патель В.Р. (май 2009 г.). «Сравнение роботизированной и позадилонной радикальной простатэктомии, выполняемой одним хирургом». Противораковые исследования . 29 (5): 1637–42. ПМИД 19443379 .
- ^ Хэм В.С., Пак С.И., Ра К.Х., Ким В.Т., Чой Ю.Д. (июнь 2009 г.). «Роботизированная радикальная простатэктомия у больных местно-распространенным раком предстательной железы осуществима: результаты моноинституционального исследования». Журнал лапароэндоскопических и передовых хирургических методов. Часть А. 19 (3): 329–32. дои : 10.1089/lap.2008.0344 . ПМИД 19397390 .
- ^ Jump up to: а б с Илич Д., Эванс С.М., Аллан К.А., Юнг Дж.Х., Мерфи Д., Фриденберг М. и др. (Кокрейновская урологическая группа) (сентябрь 2017 г.). «Лапароскопическая и роботизированная простатэктомия в сравнении с открытой радикальной простатэктомией для лечения локализованного рака простаты» . Кокрановская база данных систематических обзоров . 2017 (9): CD009625. дои : 10.1002/14651858.CD009625.pub2 . ПМК 6486168 . ПМИД 28895658 .
- ^ Jump up to: а б с Розенберг Дж.Э., Юнг Дж.Х., Эдгертон З., Ли Х., Ли С., Баккер С.Дж., Дам П. и др. (Кокрейновская урологическая группа) (август 2020 г.). «Ретциус-сохраняющая и стандартная роботизированная лапароскопическая простатэктомия для лечения клинически локализованного рака простаты» . Кокрановская база данных систематических обзоров . 2020 (8): CD013641. дои : 10.1002/14651858.CD013641.pub2 . ПМЦ 7437391 . ПМИД 32813279 .
- ^ PreventProstateCancer.info: Краткий обзор рака простаты. Архивировано 24 сентября 2008 г. в Wayback Machine.
- ^ Jump up to: а б с д Юнг Дж.Х., Риск MC, Гольдфарб Р., Редди Б., Коулз Б., Дам П. и др. (Кокрейновская урологическая группа) (май 2018 г.). «Первичная криотерапия локализованного или местно-распространенного рака простаты» . Кокрановская база данных систематических обзоров . 2018 (5): CD005010. дои : 10.1002/14651858.CD005010.pub3 . ПМК 6494517 . ПМИД 29845595 .
- ^ Jump up to: а б Филиппу Ю.А., Юнг Дж.Х., Стеггалл М.Дж., О'Дрисколл С.Т., Баккер С.Дж., Боди Дж.А., Дам П. и др. (Кокрейновская урологическая группа) (октябрь 2018 г.). «Реабилитация полового члена при эректильной дисфункции после простатэктомии» . Кокрановская база данных систематических обзоров . 2018 (10): CD012414. дои : 10.1002/14651858.CD012414.pub2 . ПМК 6517112 . ПМИД 30352488 .
- ^ Гербер Г.С., Тистед Р.А., Скардино П.Т., Фромюллер Х.Г., Шредер Ф.Х., Полсон Д.Ф. и др. (август 1996 г.). «Результаты радикальной простатэктомии у мужчин с клинически локализованным раком простаты». ДЖАМА . 276 (8): 615–9. дои : 10.1001/jama.276.8.615 . ПМИД 8773633 .
- ^ "Эректильная дисфункция" . Библиотека медицинских концепций Lecturio . Проверено 21 июля 2021 г.
- ^ Jump up to: а б Трост Л., Эллиот Д.С. (2012). «Стрессовое недержание мочи у мужчин: обзор вариантов и результатов хирургического лечения» . Достижения в урологии . 2012 : 287489. doi : 10.1155/2012/287489 . ПМЦ 3356867 . ПМИД 22649446 .
- ^ Хойланд К., Васдев Н., Аброф А., Бустед Г. (2014). «Недержание мочи после радикальной простатэктомии: этиология и профилактика» . Обзоры в Урологии . 16 (4): 181–8. ПМЦ 4274175 . ПМИД 25548545 .
- ^ Глейзер С., Боачи С., Бакли Б. и др. (июль 2011 г.). «Недержание мочи у мужчин после формальной индивидуальной тренировки мышц тазового дна после радикальной простатэктомии или трансуретральной резекции простаты (MAPS): два параллельных рандомизированных контролируемых исследования» . Ланцет . 378 (9788): 328–37. дои : 10.1016/S0140-6736(11)60751-4 . HDL : 2164/2366 . ПМИД 21741700 . S2CID 31399321 .
- ^ Тюрофф Дж.В., Абрамс П., Андерссон К.Е., Артибани В., Чаппл Ч.Р., Дрейк М.Дж. и др. (март 2011 г.). «Руководство ЕАУ по недержанию мочи». Европейская урология . 59 (3): 387–400. дои : 10.1016/j.eururo.2010.11.021 . ПМИД 21130559 . S2CID 9180421 .
- ^ «Центры протонной терапии в США» Национальная ассоциация протонной терапии (NAPT) . Проверено 21 июля 2021 г.
- ^ Наг С., Бейер Д., Фридланд Дж., Гримм П., Нат Р. (июль 1999 г.). «Рекомендации Американского общества брахитерапии (ABS) по трансперинеальной постоянной брахитерапии рака простаты». Международный журнал радиационной онкологии, биологии, физики . 44 (4): 789–99. дои : 10.1016/S0360-3016(99)00069-3 . ПМИД 10386635 .
- ^ Перес К.А., Хэнкс Г.Е., Лейбель С.А., Зитман А.Л., Фукс З., Ли В.Р. (декабрь 1993 г.). «Локализованный рак предстательной железы (стадии T1B, T1C, T2 и T3). Обзор лечения с помощью дистанционной лучевой терапии» . Рак . 72 (11): 3156–73. doi : 10.1002/1097-0142(19931201)72:11<3156::AID-CNCR2820721106>3.0.CO;2-G . ПМИД 7694785 . S2CID 37262788 . Обзор.
- ^ «Лучевая терапия рака простаты: брахитерапия простаты» . Архивировано из оригинала 4 марта 2010 г. Проверено 17 марта 2010 г.
- ^ Д'Амико А.В., Манола Дж., Лоффредо М., Реншоу А.А., ДеллаКроче А., Кантофф П.В. (2004). «6-месячная андрогенная супрессия плюс лучевая терапия против только лучевой терапии для пациентов с клинически локализованным раком простаты: рандомизированное контролируемое исследование». ДЖАМА . 292 (7): 821–27. дои : 10.1001/jama.292.7.821 . ПМИД 15315996 .
- ^ Jump up to: а б Хики Б.Е., Джеймс М.Л., Дейли Т., Со Ф.Ю., Джеффри М. и др. (Кокрейновская урологическая группа) (сентябрь 2019 г.). «Гипофракционирование при клинически локализованном раке предстательной железы» . Кокрановская база данных систематических обзоров . 9 (10): CD011462. дои : 10.1002/14651858.CD011462.pub2 . ПМК 6718288 . ПМИД 31476800 .
- ^ Томпсон И.М., Танген К.М., Парадело Дж. (2009). «Адъювантная лучевая терапия патологического рака предстательной железы T3N0M0 значительно снижает риск метастазов и улучшает выживаемость: долгосрочное наблюдение рандомизированного клинического исследования» . Журнал урологии . 181 (3): 956–62. дои : 10.1016/j.juro.2008.11.032 . ПМЦ 3510761 . ПМИД 19167731 .
- ^ «Продукция – Аугменикс» . Augmenix.com . Проверено 16 февраля 2012 г.
- ^ Купелян П.А., Эльшейх М., Редди К.А., Зиппе С., Кляйн Е.А. (август 2002 г.). «Сравнение эффективности местной терапии локализованного рака простаты в эпоху простатспецифического антигена: большой опыт одного учреждения в области радикальной простатэктомии и дистанционной лучевой терапии». Журнал клинической онкологии . 20 (16): 3376–85. дои : 10.1200/JCO.2002.01.150 . ПМИД 12177097 .
- ^ Хуанг Х., Мускателли С., Наслунд М., Бадиян С.Н., Кайзер А., Сиддики М.М. (январь 2019 г.). «Оценка смертности от рака при хирургическом вмешательстве по сравнению с лучевой терапией в качестве первичной терапии локализованного рака простаты высокой степени злокачественности у мужчин моложе 60 лет». Журнал урологии . 201 (1): 120–28. дои : 10.1016/j.juro.2018.07.049 . ПМИД 30059685 . S2CID 51880099 .
- ^ Лоутон К.А., Вон М., Пилепич М.В., Асбелл С.О., Шипли В.У., Хэнкс Г.Е. и др. (сентябрь 1991 г.). «Отдаленные последствия лечения аденокарциномы предстательной железы внешним лучом: анализ исследований RTOG 7506 и 7706». Международный журнал радиационной онкологии, биологии, физики . 21 (4): 935–9. дои : 10.1016/0360-3016(91)90732-J . ПМИД 1917622 .
- ^ Бреннер DJ, Кертис Р.Э., Холл Э.Дж., Рон Э. (январь 2000 г.). «Вторичные злокачественные новообразования у пациентов с карциномой простаты после лучевой терапии по сравнению с хирургическим вмешательством». Рак . 88 (2): 398–406. CiteSeerX 10.1.1.385.7956 . doi : 10.1002/(SICI)1097-0142(20000115)88:2<398::AID-CNCR22>3.0.CO;2-V . ПМИД 10640974 . S2CID 7508136 .
- ^ Ахмед Х.У., Дикинсон Л., Чарман С., Вейр С., Маккартан Н., Хиндли Р.Г. и др. (декабрь 2015 г.). «Фокальная абляция, направленная на индексное поражение при мультифокальном локализованном раке простаты: исследование перспективного развития». Европейская урология . 68 (6): 927–36. дои : 10.1016/j.eururo.2015.01.030 . ПМИД 25682339 .
- ^ Каравитакис М., Ахмед Х.У., Абель П.Д., Хейзелл С., Винклер М.Х. (январь 2011 г.). «Очаговость опухоли при раке предстательной железы: значение для фокальной терапии». Обзоры природы. Клиническая онкология . 8 (1): 48–55. дои : 10.1038/nrclinonc.2010.190 . ПМИД 21116296 . S2CID 32571574 .
- ^ Общество интервенционной радиологии. «Горячие и холодные методы интервенционной радиологии при рецидивирующем раке простаты» . www.biocompare.com . Biocompare: Руководство для покупателей для ученых-биологов . Проверено 18 апреля 2018 г.
- ^ Jump up to: а б Гарднер Т.А., Кох М.О. (декабрь 2005 г.). «Терапия рака простаты с помощью высокоинтенсивного фокусированного ультразвука». Клинический рак мочеполовой системы . 4 (3): 187–92. дои : 10.3816/CGC.2005.n.031 . ПМИД 16425987 . S2CID 22955796 .
- ^ Пиклз Т., Гольденберг Л., Стейнхофф Г. (2005). «Фокусированный ультразвук высокой интенсивности при раке простаты» (PDF) . Агентство по борьбе с раком Британской Колумбии. Архивировано из оригинала (PDF) 26 августа 2014 г. Проверено 10 ноября 2012 г.
- ^ Баркави AB, Кроуфорд ЭД (2008). «Новая роль HIFU как неинвазивного аблятивного метода лечения локализованного рака простаты» . Онкология . 22 (2): 123–29, обсуждение 129, 133, 137 пассим. ПМИД 18409659 .
- ^ Ахмед Х.У., Хиндли Р.Г., Дикинсон Л., Фриман А., Киркхэм А.П., Саху М. и др. (июнь 2012 г.). «Фокальная терапия локализованного унифокального и мультифокального рака простаты: проспективное исследование развития» . «Ланцет». Онкология . 13 (6): 622–32. дои : 10.1016/S1470-2045(12)70121-3 . ПМЦ 3366323 . ПМИД 22512844 .
- ^ Ахмед Х.У., Мур С., Лекорне Э., Эмбертон М. (май 2010 г.). «Фокальная терапия рака простаты: факторы успеха и неудачи». Журнал эндоурологии . 24 (5): 819–25. дои : 10.1089/конец.2009.0665 . ПМИД 20380513 .
- ^ Робсон М., Доусон Н. (июнь 1996 г.). «Как лучше всего лечить андрогензависимый метастатический рак простаты?». Гематологические/онкологические клиники Северной Америки . 10 (3): 727–47. дои : 10.1016/S0889-8588(05)70364-6 . ПМИД 8773508 . Обзор.
- ^ «Немедленное и отсроченное лечение распространенного рака простаты: первоначальные результаты исследования Совета медицинских исследований. Группа исследователей рабочей группы по раку простаты Совета медицинских исследований» . Британский журнал урологии . 79 (2): 235–46. Февраль 1997 г. doi : 10.1046/j.1464-410x.1997.d01-6840.x . ПМИД 9052476 .
- ^ Jump up to: а б Сатианатен Н.Дж., Филиппу Ю.А., Кунц Г.М., Конети Б.Р., Гупта С., Лэмб А.Д., Дам П. и др. (Кокрейновская урологическая группа) (октябрь 2018 г.). «Хемогормональная терапия на основе таксана при метастатическом гормоночувствительном раке предстательной железы» . Кокрановская база данных систематических обзоров . 2018 (10): CD012816. дои : 10.1002/14651858.CD012816.pub2 . ПМК 6516883 . ПМИД 30320443 .
- ^ Лоблоу Д.А., Мендельсон Д.С., Талкотт Дж.А., Вирго К.С., Сомерфилд М.Р., Бен-Джозеф Э., Миддлтон Р., Портерфилд Х., Шарп С.А., Смит Т.Дж., Таплин М.Е., Фогельзанг Н.Дж., Уэйд Дж.Л. младший, Беннетт К.Л., Шер Х.И., Американское общество клинической онкологии (15 июля 2004 г.). «Рекомендации Американского общества клинической онкологии по начальному гормональному лечению андроген-чувствительного метастатического, рецидивирующего или прогрессирующего рака простаты». Журнал клинической онкологии . 22 (14): 2927–41. дои : 10.1200/JCO.2004.04.579 . ПМИД 15184404 . S2CID 20462746 . (Ошибка: два : 10.1200/JCO.2004.08.943 )
- ^ Jump up to: а б Аттард Г., Рид А.Х., Яп Т.А., Рейно Ф., Доусетт М., Сеттатри С. и др. (октябрь 2008 г.). «Клинические испытания I фазы селективного ингибитора CYP17, абиратерона ацетата, подтверждают, что устойчивый к кастрации рак простаты обычно остается гормонально-зависимым» . Журнал клинической онкологии . 26 (28): 4563–71. дои : 10.1200/JCO.2007.15.9749 . ПМИД 18645193 . (Ошибка: два : 10.1200/JCO.2012.43.7756 )
- ^ Jump up to: а б Уорри Р. (22 июля 2008 г.). «Лекарство от смертельного рака простаты» . Би-би-си . Проверено 23 июля 2008 г.
- ^ Сатианатен Н.Дж., Острайх М.К., Браун С.Дж., Гупта С., Конети Б.Р., Дам П., Кунат Ф. и др. (Кокрейновская урологическая группа) (декабрь 2020 г.). «Абиратерона ацетат в сочетании с андрогендепривационной терапией по сравнению с андрогендепривационной терапией только при метастатическом гормоночувствительном раке предстательной железы» . Кокрановская база данных систематических обзоров . 2020 (12): CD013245. дои : 10.1002/14651858.CD013245.pub2 . ПМК 8092456 . ПМИД 33314020 .
- ^ Jump up to: а б Кунат Ф., Дженсен К., Пинар М., Кальмейер А., Шмидт С., Прайс К.Л. и др. (Кокрейновская урологическая группа) (июнь 2019 г.). «Ранняя и отсроченная стандартная андрогенсупрессивная терапия при распространенном гормоночувствительном раке простаты» . Кокрановская база данных систематических обзоров . 2019 (6): CD003506. дои : 10.1002/14651858.CD003506.pub2 . ПМК 6564091 . ПМИД 31194882 .
- ^ Ван Л., Паллер С.Дж., Хонг Х., Де Феличе А., Александр Г.К., Броули О. (март 2021 г.). «Сравнение системных методов лечения метастатического рака простаты, чувствительного к кастрации: систематический обзор и сетевой метаанализ» . JAMA Онкология . 7 (3): 412–420. дои : 10.1001/jamaoncol.2020.6973 . ПМК 7809610 . ПМИД 33443584 .
- ^ Jump up to: а б Джос ван Бокстел С., Сантосо Б., Эдвардс И.Р. (2008). Польза и риски лекарств: Международный учебник клинической фармакологии . ИОС Пресс. стр. 458–. ISBN 978-1-58603-880-9 .
- ^ Jump up to: а б с д Эттель М., Шиллингер Э. (2012). Эстрогены и антиэстрогены II: фармакология и клиническое применение эстрогенов и антиэстрогенов . Справочник по экспериментальной фармакологии. Том. 135/2. Springer Science & Business Media. стр. 540–42. дои : 10.1007/978-3-642-60107-1 . ISBN 978-3-642-60107-1 . S2CID 35733673 .
- ^ Jump up to: а б Косс CC, Джонс А., Парк Д.Н., Нараянан Р., Барретт С.М., Кирби Дж.Д., Веверка К.А., Миллер Д.Д., Мортон Р.А., Штайнер М.С., Далтон Дж.Т. (март 2012 г.). «Доклиническая характеристика нового селективного агониста ERα дифенилбензамида для гормональной терапии рака простаты» . Эндокринология . 153 (3): 1070–81. дои : 10.1210/en.2011-1608 . ПМИД 22294742 .
- ^ Ю Е.Ю., Гетценберг Р.Х., Косс К.С., Гиттельман М.М., Кин Т., Тутрон Р. и др. (февраль 2015 г.). «Селективный альфа-агонист эстрогеновых рецепторов GTx-758 снижает уровень тестостерона с уменьшенными побочными эффектами андрогенной депривационной терапии у мужчин с распространенным раком простаты». Европейская урология . 67 (2): 334–41. дои : 10.1016/j.eururo.2014.06.011 . ПМИД 24968970 .
- ^ Jump up to: а б с д и ж Хонг В.К., Холланд Дж.Ф. (2010). Холланд-Фрай онкологическая медицина 8 . PMPH-США. стр. 753–. ISBN 978-1-60795-014-1 .
- ^ Али Шах С.И. (2015). «Новый потенциал парентерального эстрогена в качестве андрогенной депривационной терапии рака простаты» . Южноазиатский журнал рака . 4 (2): 95–97. дои : 10.4103/2278-330X.155699 . ПМЦ 4418092 . ПМИД 25992351 .
- ^ Jump up to: а б Рассел Н., Чунг А., Гроссманн М. (август 2017 г.). «Эстрадиол для смягчения побочных эффектов андрогенной депривационной терапии» . Эндокринный рак . 24 (8): Р297–Р313. дои : 10.1530/ERC-17-0153 . ПМИД 28667081 .
- ^ Jump up to: а б Вибово Э., Вассерсуг Р.Дж. (сентябрь 2013 г.). «Влияние эстрогена на сексуальный интерес кастрированных мужчин: последствия для больных раком простаты андроген-депривационной терапии». Критические обзоры по онкологии/гематологии . 87 (3): 224–38. дои : 10.1016/j.critrevonc.2013.01.006 . ПМИД 23484454 .
- ^ Jump up to: а б Вибово Э., Шеллхаммер П., Вассерсуг Р.Дж. (январь 2011 г.). «Роль эстрогена в нормальной мужской функции: клинические последствия для пациентов с раком простаты, находящихся на андрогенной депривационной терапии». Журнал урологии . 185 (1): 17–23. дои : 10.1016/j.juro.2010.08.094 . ПМИД 21074215 .
- ^ Норман Дж., Дин М.Э., Лэнгли Р.Э., Ходжес З.К., Ричи Дж., Пармар М.К., Сайдс М.Р., Абель П., Иствуд А.Дж. (февраль 2008 г.). «Парентеральный эстроген в лечении рака простаты: систематический обзор» . Британский журнал рака . 98 (4): 697–707. дои : 10.1038/sj.bjc.6604230 . ПМК 2259178 . ПМИД 18268497 .
- ^ Jump up to: а б Лисетт Дж.Л., Бланд Л.Б., Гарзотто М., Beer TM (декабрь 2006 г.). «Парентеральные эстрогены при раке простаты: может ли новый способ введения преодолеть старые токсичности?». Клинический рак мочеполовой системы . 5 (3): 198–205. дои : 10.3816/CGC.2006.n.037 . ПМИД 17239273 .
- ^ Jump up to: а б Окрим Дж., Лалани Э.Н., Абель П. (октябрь 2006 г.). «Therapy Insight: парентеральное лечение эстрогенами при раке простаты - новый рассвет старой терапии». Природная клиническая практика. Онкология . 3 (10): 552–63. дои : 10.1038/ncponc0602 . ПМИД 17019433 . S2CID 6847203 .
- ^ Беомонте Зобель, Бруно (25 января 2024 г.). «Необратимая электропорация (IRE) для лечения рака простаты: современное состояние» . Журнал персонализированной медицины . 14 (2): 137. дои : 10.3390/jpm14020137 . ПМК 10890194 . ПМИД 38392571 .
- ^ «Необратимая электропорационная абляция при раке простаты» . Онкологический центр Моффита .
- ^ Грассо, Розарио Франческо (23 августа 2021 г.). «Необратимая электропорация у пациентов с локализованным раком простаты: мнение экспертов об этом универсальном терапевтическом подходе» . Европейский медицинский журнал .
- ^ Беомонте Зобель, Бруно (25 января 2024 г.). «Необратимая электропорация (IRE) для лечения рака простаты: современное состояние» . Журнал персонализированной медицины . 14 (2): 137. дои : 10.3390/jpm14020137 . ПМК 10890194 . ПМИД 38392571 .
- ^ «Необратимая электропорационная абляция при раке простаты» . Онкологический центр Моффита .
- ^ Беомонте Зобель, Бруно (25 января 2024 г.). «Необратимая электропорация (IRE) для лечения рака простаты: современное состояние» . Журнал персонализированной медицины . 14 (2): 137. дои : 10.3390/jpm14020137 . ПМК 10890194 . ПМИД 38392571 .
- ^ «Необратимая электропорационная абляция при раке простаты» . Онкологический центр Моффита .
- ^ Гюлерюз, Б (2021). «Фотодинамическая терапия рака предстательной железы на основе активированных апконверсионными наночастицами ближнего инфракрасного света (UCNP): исследование in vitro» . Фотодиагностика и фотодинамическая терапия . 36 : 102616. doi : 10.1016/j.pdpdt.2021.102616 . ПМИД 34740839 .
- ^ Мур, К. (2006). «Клиническая оценка оптических характеристик простаты у мужчин с раком простаты» . Европейская урология . 5 (Приложение): 131.
- ^ Сенгупта, Дж (2020). «Наносферы PEG-PLGA, наполненные наносцинтилляторами и фотосенсибилизаторами для радиационно-активируемой фотодинамической терапии» . Акта Биоматериалы . 117 : 335–348. doi : 10.1016/j.actbio.2020.09.029 . ПМИД 32956872 .
- ^ Чжу, ТК (2005). «Оптические свойства простаты человека при длине волны 732 нм, измеренные при опосредованной фотодинамической терапии» . Фотохимия и фотобиология . 81 : 96–105. doi : 10.1562/2004-08-06-RA-259.1 (неактивен 29 апреля 2024 г.). ПМИД 15535736 .
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на апрель 2024 г. ( ссылка ) - ^ Финли, Джей Си (2006). «Интерстициальная флуоресцентная спектроскопия в предстательной железе человека во время фотодинамической терапии, опосредованной мотексафином и лютецием» . Фотохимия и фотобиология . 82 (5): 1270–1278. дои : 10.1562/2005-10-04-RA-711 . ПМЦ 4475578 . ПМИД 16808592 .
- ^ Доу, Джон (2022). «Изучение эффективности электрохимиотерапии при лечении рака простаты» . Клиническая онкология . 22 : 445–453. doi : 10.1016/j.clonc.2022.05.003 (неактивен 29 апреля 2024 г.).
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на апрель 2024 г. ( ссылка ) - ^ «Электрохимиотерапия: новые применения в лечении рака» . ClinicalTrials.gov .
- ^ Смит, Эмма (2023). «Будущие направления электрохимиотерапии: потенциал применения рака простаты» . Журнал инновационной онкологии . 5 (1): 12–19.
- ^ де Йонг Й., Пинккерс Дж.Х., тен Бринк Р.М., Ликлама и Ниджехольт А.А., Деккерс О.М. (2014). «Мочеиспускание стоя или сидя: положение имеет значение у мужчин с увеличением простаты. Систематический обзор и метаанализ» . ПЛОС ОДИН . 9 (7): е101320. Бибкод : 2014PLoSO...9j1320D . дои : 10.1371/journal.pone.0101320 . ПМК 4106761 . ПМИД 25051345 .
- ^ Моришита С., Хамауэ И., Фукусима Т., Танака Т., Фу Дж.Б., Накано Дж. (январь 2020 г.). «Влияние физических упражнений на смертность и рецидивы у больных раком: систематический обзор и метаанализ» . Интегративная терапия рака . 19 : 1534735420917462. дои : 10.1177/1534735420917462 . ПМЦ 7273753 . ПМИД 32476493 .
- ^ Ранс К., Берген С., Жониау С., Де Меерлер Г. (март 2020 г.). «Спасительная лучевая терапия рака простаты». Клиническая онкология . 32 (3): 156–162. дои : 10.1016/j.clon.2020.01.003 . ПМИД 32035581 . S2CID 211070763 .
- ^ Тендулкар Р.Д., Агравал С., Гао Т., Эфстатиу Дж.А., Писанский Т.М., Михальски Дж.М. и др. (октябрь 2016 г.). «Современное обновление межведомственной прогностической номограммы для спасительной лучевой терапии после радикальной простатэктомии». Журнал клинической онкологии . 34 (30): 3648–3654. дои : 10.1200/JCO.2016.67.9647 . ПМИД 27528718 .
- ^ Таннок И.Ф., де Вит Р., Берри В.Р., Хорти Дж., Плужанска А., Чи К.Н., Удар С., Теодор С., Джеймс Н.Д., Турессон I, Розенталь М.А., Айзенбергер М.А., Следователи TAX 327 (7 октября 2004 г.). «Доцетаксел плюс преднизолон или митоксантрон плюс преднизолон при распространенном раке простаты» . Медицинский журнал Новой Англии . 351 (15): 1502–12. doi : 10.1056/NEJMoa040720 . ПМИД 15470213 . S2CID 22649502 .
- ^ Саад Ф., Глисон Д.М., Мюррей Р., Чекмедиян С., Веннер П., Лакомб Л., Чин Дж.Л., Винхолс Дж.Дж., Гоас Дж.А., Чен Б. (2002). «Рандомизированное плацебо-контролируемое исследование золедроновой кислоты у пациентов с гормонорефрактерной метастатической карциномой простаты» . Журнал Национального института рака . 94 (19): 1458–68. дои : 10.1093/jnci/94.19.1458 . ПМИД 12359855 .
- ^ Jump up to: а б Якоб Т., Тесфамариам Ю.М., Машери С., Кур К., Адамс А., Монсеф I и др. (Кокрейновская урологическая группа) (декабрь 2020 г.). «Бисфосфонаты или ингибиторы RANK-лиганда для мужчин с раком простаты и метастазами в костях: сетевой метаанализ» . Кокрановская база данных систематических обзоров . 2020 (12): CD013020. дои : 10.1002/14651858.CD013020.pub2 . ПМК 8095056 . ПМИД 33270906 .
- ^ Орниш Д., Вайднер Г., Фэйр В.Р., Марлин Р., Петтенгилл Э.Б., Изюм С.Дж. и др. (сентябрь 2005 г.). «Интенсивные изменения образа жизни могут повлиять на прогрессирование рака простаты» . Журнал урологии . 174 (3): 1065–9, обсуждение 1069–70. дои : 10.1097/01.ju.0000169487.49018.73 . ПМИД 16094059 .
- ^ Фраттароли Дж., Вейднер Г., Днистрян А.М., Кемп С., Добенмир Дж.Дж., Марлин Р.О. и др. (декабрь 2008 г.). «Клинические события в исследовании образа жизни при раке простаты: результаты двухлетнего наблюдения». Урология . 72 (6): 1319–23. doi : 10.1016/j.urology.2008.04.050 . ПМИД 18602144 .
- ^ Пантук А.Дж., Лепперт Дж.Т., Зомородиан Н., Аронсон В., Хонг Дж., Барнард Р.Дж. и др. (июль 2006 г.). «Исследование фазы II гранатового сока у мужчин с повышением уровня простатспецифического антигена после операции или лучевой терапии по поводу рака простаты» . Клинические исследования рака . 12 (13): 4018–26. doi : 10.1158/1078-0432.CCR-05-2290 . ПМИД 16818701 . S2CID 7921887 .
- ^ Кумар Н.Б., Кантор А., Аллен К., Риккарди Д., Бестерман-Дахан К., Сень Дж. и др. (май 2004 г.). «Особая роль изофлавонов в снижении риска рака простаты». Простата . 59 (2): 141–7. дои : 10.1002/pros.10362 . ПМИД 15042614 . S2CID 19319738 .
- ^ Ярнелл Э (1999). «Натуропатический подход к раку простаты. Часть 2: Рекомендации по лечению и профилактике». Альтернативные и дополнительные методы лечения . 5 (6): 360–68. дои : 10.1089/акт.1999.5.360 .
- ^ Холл Э.Дж. (2000). Радиобиология для радиолога . Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уильямс. стр. 432–33 . ISBN 978-0-06-141077-2 .
- ^ Липпман С.М., Кляйн Е.А., Гудман П.Дж. и др. (январь 2009 г.). «Влияние селена и витамина Е на риск рака простаты и других видов рака: исследование по профилактике рака с использованием селена и витамина Е (SELECT)» . ДЖАМА . 301 (1): 39–51. дои : 10.1001/jama.2008.864 . ПМЦ 3682779 . ПМИД 19066370 .
- ^ Jump up to: а б Хельгасон А.Р., Адольфссон Дж., Дикман П., Фредриксон М., Арвер С., Стейнек Г. (1996). «Снижение сексуальной функции – наиболее важное заболевание, специфичное для пациентов с раком простаты» . Британский журнал рака . 73 (11): 1417–21. дои : 10.1038/bjc.1996.268 . ПМК 2074472 . ПМИД 8645589 .
- ^ Хельгасон А.Р., Адольфссон Дж., Дикман П., Фредриксон М., Стейнек Г. (1998). «Дистресс из-за нежелательных побочных эффектов лечения рака простаты связан с ухудшением самочувствия (качества жизни)» . Рак простаты и заболевания предстательной железы . 1 (3): 128–33. дои : 10.1038/sj.pcan.4500226 . ПМИД 12496905 .
- ^ Хельгасон А.Р., Дикман П.В., Адольфссон Дж., Стейнек Г. (2001). «Эмоциональная изоляция: распространенность и влияние на благополучие среди пациентов с раком простаты в возрасте 50–80 лет». Скандинавский журнал урологии и нефрологии . 35 (2): 97–101. CiteSeerX 10.1.1.549.5736 . дои : 10.1080/003655901750170407 . ПМИД 11411666 . S2CID 218865571 .
- ^ «Обновление данных для клиницистов: рак простаты» . www.pcori.org . 2018-03-30 . Проверено 29 января 2020 г.
- ^ Джаядеваппа Р., Чхатре С., Вонг Ю.Н., Виттинк М.Н., Кук Р., Моралес К.Х. и др. (май 2017 г.). «Сравнительная эффективность лечения рака простаты для результатов, ориентированных на пациента: систематический обзор и метаанализ (соответствует PRISMA)» . Лекарство . 96 (18): e6790. дои : 10.1097/MD.0000000000006790 . ПМЦ 5419922 . ПМИД 28471976 .