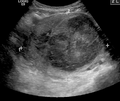
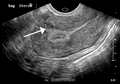
Миома матки
| Миома матки | |
|---|---|
| Другие имена | Лейомиома матки, миома матки, миома, фибромиома, фибролейомиома |
 | |
| Миома матки, наблюдаемая во время лапароскопической операции | |
| Специальность | Гинекология |
| Симптомы | Болезненные или тяжелые менструации [1] |
| Осложнения | Бесплодие [1] |
| Обычное начало | Средний и поздний репродуктивный годы [1] |
| Причины | Неизвестный [1] |
| Факторы риска | Семейный анамнез, ожирение , употребление красного мяса [1] |
| Метод диагностики | Осмотр органов малого таза , медицинская визуализация [1] |
| Дифференциальный диагноз | Лейомиосаркома , беременность , киста яичника , рак яичника [2] |
| Уход | Лекарственные препараты, хирургия, эмболизация маточных артерий [1] |
| Медикамент | Ибупрофен , парацетамол (ацетаминофен), препараты железа , агонист гонадотропин-рилизинг гормона. [1] |
| Прогноз | Улучшение после менопаузы [1] |
| Частота | ~50% женщин к 50 годам [1] |
Миома матки , также известная как лейомиома матки или миома , представляет собой опухоль гладкой мускулатуры матки доброкачественную , части женской репродуктивной системы . [1] У некоторых женщин с миомой нет никаких симптомов, в то время как у других могут быть болезненные или обильные менструации . [1] Если они достаточно большие, они могут давить на мочевой пузырь , вызывая частые позывы к мочеиспусканию . [1] Они также могут вызывать боль во время проникающего секса или боль в пояснице . [1] [3] У женщины может быть одна миома матки или несколько. [1] Редко, но возможно, что миома может затруднить наступление беременности . [1]
Точная причина миомы матки неясна. [1] Однако миома встречается в семьях и, по-видимому, частично определяется уровнем гормонов . [1] Факторы риска включают ожирение и употребление красного мяса . [1] Диагноз можно поставить с помощью гинекологического осмотра или медицинской визуализации . [1]
Лечение обычно не требуется, если нет симптомов. [1] НПВП , такие как ибупрофен , могут помочь при боли и кровотечении, а парацетамол (ацетаминофен) может помочь при боли. [1] [4] Добавки железа могут потребоваться тем, у кого тяжелые менструации. [1] Лекарства класса агонистов гонадотропин-рилизинг-гормона могут уменьшить размер миомы, но они дороги и связаны с побочными эффектами. [1] Если присутствуют более серьезные симптомы, может помочь операция по удалению миомы или матки. [1] Эмболизация маточных артерий также может помочь. [1] Раковые варианты миомы очень редки и известны как лейомиосаркомы . [1] По-видимому, они не развиваются из доброкачественных миом. [1]
Примерно у 20-80% женщин к 50 годам развивается миома. [1] По оценкам, в 2013 году во всем мире пострадал 171 миллион женщин. [5] Обычно они встречаются в среднем и более позднем репродуктивном возрасте. [1] После менопаузы они обычно уменьшаются в размерах. [1] В Соединенных Штатах миома матки является частой причиной хирургического удаления матки . [6]
Признаки и симптомы
[ редактировать ]У некоторых женщин с миомой матки симптомы отсутствуют. Боль в животе, анемия и повышенное кровотечение могут указывать на наличие миомы. [7] Также может возникнуть боль во время полового акта (проникновения), в зависимости от расположения миомы. Во время беременности они также могут стать причиной выкидыша . [8] кровотечение, преждевременные роды или нарушение положения плода. [9] Миома матки может вызвать ректальное давление. Живот может увеличиться, имитируя появление беременности. [1] Некоторые крупные миомы могут распространяться через шейку матки и влагалище. [7]
Хотя миомы распространены, они не являются типичной причиной бесплодия: на их долю приходится около 3% причин, по которым женщина не может иметь ребенка. [10] У большинства женщин с миомой матки исход беременности будет нормальным. [11] В случаях интеркуррентной миомы матки при бесплодии миома обычно располагается в подслизистой оболочке, и считается, что это расположение может влиять на функцию слизистой оболочки и способность эмбриона к имплантации . [10]
Факторы риска
[ редактировать ]Некоторые факторы риска, связанные с развитием миомы матки, поддаются изменению. [12] Фиброиды чаще встречаются у женщин с ожирением. [13] Рост миомы зависит от эстрогена и прогестерона и поэтому актуален только в репродуктивном возрасте.
Диета
[ редактировать ]Диеты с высоким содержанием фруктов и овощей, как правило, снижают риск развития миомы. [12] Клетчатка, витамины А, С и Е, фитоэстрогены, каротиноиды, мясо, рыба и молочные продукты оказывают неясное влияние. [12] Нормальный уровень витамина D в питании может снизить риск развития миомы. [12]
Генетика
[ редактировать ]Пятьдесят процентов миомы матки демонстрируют генетическую аномалию. Часто транслокация обнаруживается в некоторых хромосомах. [7] Фиброиды частично являются генетическими. Если у матери была миома, риск у дочери примерно в три раза выше среднего. [14] У чернокожих женщин вероятность развития миомы матки в 3–9 раз выше, чем у белых женщин. [15] Лишь несколько специфических генов или цитогенетических отклонений связаны с миомой. 80–85% миомы имеют мутацию в гене субъединицы 12 медиаторного комплекса ( MED12 ). [16] [17]
Семейные лейомиомы
[ редактировать ]синдроме ( синдроме Рида ), который вызывает лейомиому матки наряду с лейомиомой кожи и почечно-клеточным раком . Сообщалось о [18] [19] [20] Это связано с мутацией гена, продуцирующего фермент фумаратгидратазу , расположенного на длинном плече хромосомы 1 (1q42.3-43). Наследование аутосомно-доминантное .
Патофизиология
[ редактировать ]
Фиброиды — это разновидность лейомиомы матки . Фиброиды обычно выглядят как круглые, хорошо очерченные (но не инкапсулированные), твердые узелки белого или желтовато-коричневого цвета, имеющие на гистологическом срезе мутовчатый вид. Размер варьирует: от микроскопических до очагов значительных размеров. Обычно поражения размером с грейпфрут или больше ощущаются самой пациенткой через брюшную стенку. [1]

Микроскопически опухолевые клетки напоминают нормальные клетки (удлиненные, веретенообразные, с сигарообразным ядром) и образуют пучки разной направленности (мутовчатые). Эти клетки однородны по размеру и форме, с редкими митозами. Существует три доброкачественных варианта: причудливый (атипичный); сотовый; и митотически активны.
Появление выступающих ядрышек с околоядрышковыми ореолами должно насторожить патологоанатома для изучения возможности чрезвычайно редкого наследственного лейомиоматоза и синдрома почечно-клеточного рака (Рида). [21]
Местоположение и классификация
[ редактировать ]
Рост и расположение являются основными факторами, определяющими, приводит ли миома к симптомам и проблемам. [6] Небольшое поражение может быть симптоматическим, если оно расположено внутри полости матки, тогда как большое поражение снаружи матки может остаться незамеченным. Различные места классифицируются следующим образом:
- Интрамуральная миома расположена внутри мышечной стенки матки и является наиболее распространенным типом. [22] Если они не большие, они могут протекать бессимптомно. Интрамуральная миома начинается с небольших узелков в мышечной стенке матки. Со временем интрамуральные миомы могут расширяться внутрь, вызывая деформацию и удлинение полости матки.
- Субсерозные миомы располагаются на поверхности матки. Они также могут расти наружу от поверхности и оставаться прикрепленными к небольшому кусочку ткани, и тогда их называют миомами на ножке. [1]
- Подслизистые миомы располагаются в мышцах под эндометрием матки и деформируют полость матки; даже небольшие повреждения в этом месте могут привести к кровотечению и бесплодию . Образование на ножке внутри полости называется внутриполостной миомой и может проходить через шейку матки.
- Миома шейки матки расположена в стенке шейки матки (шейке матки). Редко миома обнаруживается в опорных структурах ( круглой связке , широкой связке или маточно-крестцовой связке ) матки, которые также содержат гладкую мышечную ткань.
С 2011 года FIFA опубликовала свой консенсусный документ по классификации миомы, а именно от 0 до 8. Это часть классификации PALM COEIN и наиболее часто используемая в клинической практике и исследованиях. [23] Пожалуйста, продолжайте читать здесь: Классификация FIFA.
- Тип 0: подслизистый на ножке, внутриполостной (т.е. внутри матки).
- Тип 1: подслизистый, <50% интрамурально.
- Тип 2: подслизистый, ≥50% интрамурально.
- Тип 3: контактирует с эндометрием, 100% интрамурально.
- Тип 4: интрамуральный (т.е. полностью внутри стенки матки).
- Тип 5: субсерозный, ≥50% интрамуральный.
- Тип 6: субсерозный, <50% интрамуральный.
- Тип 7: субсерозный на ножке.
- Тип 8: другие (например, шейные, паразитарные)
Существуют также гибридные леймиомы, такие как тип 2-5, которые располагаются как субсерозно, так и подслизисто.
Фиброиды могут быть одиночными или множественными. Большинство миом зарождаются в мышечной стенке матки. При дальнейшем росте некоторые поражения могут развиваться по направлению к внешней стороне матки или во внутреннюю полость. Вторичные изменения, которые могут развиться внутри миомы, включают кровоизлияния, некроз, кальцификацию и кистозные изменения. Они склонны к кальцинированию после менопаузы. [24]
Если в матке их слишком много, чтобы их можно было подсчитать, это называется диффузным лейомиоматозом матки .
Внематочная миома маточного происхождения, метастатическая миома
[ редактировать ]Фиброиды маточного происхождения, расположенные в других частях тела, иногда также называемые паразитическими миомами, исторически встречались крайне редко, но в настоящее время диагностируются все чаще. Они могут быть связаны или идентичны метастазирующей лейомиоме .
В большинстве случаев они по-прежнему гормонозависимы, но при появлении в отдаленных органах могут вызывать опасные для жизни осложнения. Некоторые источники предполагают, что значительная часть случаев может быть поздними осложнениями операций, таких как миомэктомия или гистерэктомия. В частности, лапароскопическая миомэктомия с использованием морцеллятора связана с повышенным риском этого осложнения. [25] [26] [27]
Существует ряд редких состояний, при которых миома метастазирует. Они по-прежнему растут безвредно, но могут быть опасными в зависимости от своего местоположения. [28]
- При лейомиоме с сосудистой инвазией обычная на вид миома прорастает в сосуд, но риск рецидива отсутствует.
- При внутривенном лейомиоматозе лейомиомы растут в венах, источником которых является миома матки. Поражение сердца может быть фатальным.
- При доброкачественной метастазирующей лейомиоме лейомиомы растут в более отдаленных местах, таких как легкие и лимфатические узлы. Источник не совсем ясен. Поражение легких может быть фатальным.
- При диссеминированном внутрибрюшинном лейомиоматозе лейомиомы разрастаются диффузно на поверхности брюшины и сальника, их источником является миома матки. Это может имитировать злокачественную опухоль, но ведет себя доброкачественно.
Патогенез
[ редактировать ]


Фиброиды являются моноклональными опухолями, и примерно в 40–50% случаев обнаруживаются кариотипически обнаруживаемые хромосомные аномалии . Когда присутствуют множественные миомы, они часто имеют несвязанные генетические дефекты. Специфические мутации белка MED12 отмечены в 70 процентах случаев миомы. [29]
Точная причина возникновения миомы не совсем понятна, но в настоящее время рабочая гипотеза заключается в том, что генетическая предрасположенность, внутриутробное воздействие гормонов и воздействие гормонов, факторов роста и ксеноэстрогенов вызывают рост миомы. Известными факторами риска являются африканское происхождение, ожирение , синдром поликистозных яичников , диабет , гипертония и отсутствие родов . [30]
Считается, что эстроген и прогестерон оказывают митогенное действие на клетки лейомиомы, а также действуют, влияя (прямо и косвенно) на большое количество факторов роста , цитокинов и факторов апоптоза, а также на другие гормоны. Более того, действие эстрогена и прогестерона модулируется перекрестной передачей сигналов эстрогена, прогестерона и пролактина , которая контролирует экспрессию соответствующих ядерных рецепторов. Считается, что эстроген способствует росту за счет повышения уровня IGF-1 , EGFR , TGF-beta1 , TGF-beta3 и PDGF , а также способствует аберрантному выживанию клеток лейомиомы за счет снижения уровня p53 , увеличения экспрессии антиапоптотического фактора PCP4 и противодействующие передаче сигналов PPAR-гамма . Считается, что прогестерон способствует росту лейомиомы за счет повышения уровня EGF , TGF-бета1 и TGF-бета3, а также способствует выживанию за счет повышения уровня экспрессии Bcl-2 и снижения уровня TNF-альфа . Считается, что прогестерон противодействует росту, подавляя IGF-1. [31] Экспрессия трансформирующего фактора взаимодействия с ростом (TGIF) увеличивается в лейомиоме по сравнению с миометрием. [32] TGIF является потенциальным репрессором путей TGF-β в клетках миометрия. [32]
Ароматаза и 17-бета-гидроксистероиддегидрогеназа аберрантно экспрессируются в миомах, что указывает на то, что миомы могут превращать циркулирующий андростендион в эстрадиол. [33] Аналогичный механизм действия был выяснен при эндометриозе и других заболеваниях эндометрия. [34] Ингибиторы ароматазы в настоящее время рассматриваются для лечения.в определенных дозах они полностью подавляют выработку эстрогена в миоме, не влияя при этом на выработку эстрогена яичниками (и, следовательно, на его системные уровни). Сверхэкспрессия ароматазы особенно выражена у афроамериканских женщин. [35]
Рассматриваются генетические и наследственные причины, и некоторые эпидемиологические данные указывают на значительное генетическое влияние, особенно в случаях с ранним началом. У родственников первой степени родства риск увеличивается в 2,5 раза, а при рассмотрении случаев раннего начала - почти в 6 раз. Монозиготные близнецы имеют двойную частоту конкордантности при гистерэктомии по сравнению с дизиготными близнецами . [36]
Расширение миомы матки происходит за счет медленной пролиферации клеток в сочетании с выработкой обильного количества внеклеточного матрикса . [35]
Небольшая популяция клеток миомы матки обладает свойствами стволовых клеток или клеток-предшественников и вносит значительный вклад в стероид -зависимый рост миомы яичников. Эти стволовые клетки-предшественники лишены рецептора эстрогена α и рецептора прогестерона и вместо этого полагаются на существенно более высокие уровни этих рецепторов в окружающих дифференцированных клетках, чтобы опосредовать действия эстрогена и прогестерона посредством паракринной передачи сигналов . [35]
Диагностика
[ редактировать ]Физикальное обследование и УЗИ достаточны для диагностики миомы матки у большинства пациенток. Если результаты УЗИ неубедительны, магнитно-резонансная томография (МРТ) в большинстве случаев может подтвердить диагноз миомы матки. Кроме того, с помощью МРТ можно выявить доброкачественные миомы матки с атипичными признаками визуализации и миомы с различными вариантами роста. МРТ может также выявить другие маточные (например, аденомиоз, полипы эндометрия, рак эндометрия) и внематочные (например, доброкачественные и злокачественные опухоли яичников, эндометриоз) заболевания, которые могут имитировать появление миомы матки и/или способствовать развитию симптомов у пациентки. [37] Однако небольшая часть миомы матки может имитировать другие злокачественные опухоли матки (например, лейомиосаркому) при всех доступных методах визуализации (например, УЗИ, КТ, МРТ и ПЭТ-КТ). [37]
Злокачественные опухоли стенки матки (например, лейомиосаркома) встречаются очень редко. Признаки, указывающие на злокачественную опухоль матки, а не на доброкачественную миому, включают быстрый или неожиданный рост (особенно после менопаузы), прерывание/стирание полоски эндометрия, увеличение лимфатических узлов, инвазию в соседние органы и метастазы в отдаленные органы (например, легкие). Данные МРТ, указывающие на злокачественное новообразование, включают узловые/плохо очерченные края опухоли, среднюю/высокую интенсивность Т2-взвешенного сигнала компонентов солидной опухоли, области с высоким сигналом Т1-взвешенных последовательностей, что соответствует подострому кровоизлиянию, тонкое/неуловимое усиление солидного новообразования. части опухоли и ограниченная диффузия при диффузионно-взвешенной визуализации (ДВИ). [37] Биопсия проводится редко, а если и проводится, то редко является диагностической. Если после УЗИ и МРТ диагноз неясен, обычно показано хирургическое вмешательство. [38]
- Очень большая (9 см) миома матки, вызывающая синдром застоя в малом тазу, как видно на КТ.
- Очень большая (9 см) миома матки, вызывающая синдром застоя в малом тазу, как видно на УЗИ.
- Относительно крупная подслизистая лейомиома; он заполняет большую часть полости эндометрия.
- Небольшая миома матки, видимая внутри стенки миометрия на поперечном ультразвуковом снимке.
- Две кальцинированные миомы (в матке)
- Субсерозная миома матки диаметром 5 сантиметров.
- МРТ-изображение при множественных лейомиомах матки
- Гигантские лейомиомы, почти заполняющие брюшную полость
- Гистопатология миомы матки обычно демонстрирует мутовчатую (пучковую) структуру гладких мышц. [39]
- Этот вариант окраски Ван Гизона отличает мышцы (желтые) от соединительной ткани (красные).
- Иммуногистохимия при β-катенина лейомиоме матки дает отрицательный результат, поскольку наблюдается окрашивание только цитоплазмы, но не ядер клеток.
Отрицательное иммуногистохимическое окрашивание на β-катенин в ядрах клеток является постоянным признаком лейомиомы матки и помогает отличить такие опухоли от β-катенин-положительных веретеноклеточных опухолей. [40]
Сопутствующие расстройства
[ редактировать ]Фибромы, которые приводят к обильным вагинальным кровотечениям, приводят к анемии и дефициту железа . желудочно-кишечные проблемы, такие как запоры Из-за воздействия давления возможны и вздутие живота. Сдавление мочеточника может привести к гидронефрозу . Фиброиды могут также присутствовать наряду с эндометриозом , который сам по себе может вызывать бесплодие. Аденомиоз может быть ошибочно принят за миому или сосуществовать с ней.
В очень редких случаях лейомиосаркомы . возможно развитие злокачественных (раковых) разрастаний миометрия — [22] В крайне редких случаях миома матки может проявляться как часть или ранний симптом наследственного лейомиоматоза и синдрома почечно-клеточного рака .
Уход
[ редактировать ]Большинство миом не требуют лечения, если только они не вызывают симптомов. После менопаузы миомы уменьшаются, и они редко вызывают проблемы.
Симптоматическую миому матки можно лечить следующими способами:
- лекарства для контроля симптомов (т. е. симптоматическое лечение)
- лекарства, направленные на уменьшение опухолей
- разрушение миомы ультразвуком
- миомэктомия или радиочастотная абляция
- гистерэктомия
- эмболизация маточных артерий
У тех, у кого есть симптомы, эмболизация маточных артерий и хирургические варианты имеют одинаковые результаты в отношении удовлетворения. [41]
На протяжении десятилетий общепринятым подходом к лечению симптоматической миомы было «либо сделать гистерэктомию, либо подождать, пока менопауза не уменьшит симптомы», но минимально инвазивные и неинвазивные варианты часто не предлагались. [42] Особенно с 2010-х годов все чаще предлагаются минимально инвазивные и неинвазивные варианты, поскольку они продвинулись на своем технологическом пути от новых и необычных до обычной клинической практики. [42]
Медикамент
[ редактировать ]Для контроля симптомов можно использовать ряд лекарств. НПВП можно использовать для уменьшения болезненных менструальных периодов. Для уменьшения маточного кровотечения и спазмов могут быть назначены пероральные противозачаточные таблетки. [10] Анемию можно лечить добавками железа.
Внутриматочные спирали с левоноргестрелом эффективны для ограничения менструального кровотока и улучшения других симптомов. Побочные эффекты обычно немногочисленны, поскольку левоноргестрел ( прогестин ) высвобождается локально в низкой концентрации. [43] Хотя большинство исследований по использованию левогестрела ВМС были сосредоточены на лечении женщин без миомы, в некоторых из них сообщалось о хороших результатах, особенно для женщин с миомой, включая существенную регрессию миомы. [44] [45]
В двух исследованиях было показано, что каберголин в умеренной и хорошо переносимой дозе эффективно уменьшает миому. Механизм действия, ответственный за то, как каберголин уменьшает миому, неясен. [44]
Улипристала ацетат представляет собой синтетический селективный модулятор рецепторов прогестерона (СПРМ), который имеет предварительные доказательства в поддержку его использования для дооперационного лечения миомы матки с низким уровнем побочных эффектов. [46] При длительном лечении миомы УПА наблюдалось уменьшение объема примерно на 70%. [47] В некоторых случаях для облегчения симптомов без хирургического вмешательства используется только УПА. [48] и обеспечить успешную беременность без повторного роста миомы. [49] Действительно, в опухолевых клетках молекула блокирует пролиферацию клеток, индуцирует их апоптоз. [50] [51] и стимулирует ремоделирование обширного фиброза матриксными металлопротеиназами , [52] следовательно, объясняя долгосрочную выгоду. [53] Тем не менее, из-за некоторых редких, но тяжелых повреждений печени после лечения УПА, в 2020 году в ЕС действие лицензии было приостановлено. [54] и добровольно выслан в Канаду. [55]
Даназол — эффективное средство для уменьшения миомы и контроля симптомов. Его применение ограничено неприятными побочными эффектами. Предполагается, что механизм действия заключается в антиэстрогенном эффекте. Недавний опыт показывает, что безопасность и профиль побочных эффектов можно улучшить за счет более осторожного дозирования. [44]
Аналоги гонадотропин-рилизинг-гормона вызывают временную регрессию миомы за счет снижения уровня эстрогена. Из-за ограничений и побочных эффектов этого лекарства его редко рекомендуют, кроме как для предоперационного использования, чтобы уменьшить размер миомы и матки перед операцией. Обычно их используют максимум шесть месяцев или меньше, поскольку после более длительного использования они могут вызвать остеопороз и другие осложнения, типичные для постменопаузы. Основными побочными эффектами являются преходящие симптомы постменопаузы. Во многих случаях миома снова вырастает после прекращения лечения, однако в некоторых случаях значительный положительный эффект может сохраняться гораздо дольше. Возможны несколько вариантов, например, агонисты ГнРГ с схемами прикрытия, предназначенными для уменьшения побочных эффектов дефицита эстрогена. Возможны несколько режимов прикрытия: тиболон , ралоксифен , только прогестагены , только эстроген и комбинированные эстрогены и прогестагены. [44]
Антагонисты прогестерона , такие как мифепристон, были протестированы, есть доказательства того, что они облегчают некоторые симптомы и улучшают качество жизни, но из-за неблагоприятных гистологических изменений, которые наблюдались в нескольких исследованиях, в настоящее время их нельзя рекомендовать за пределами исследовательских целей. [56] Рост миомы возобновился после прекращения лечения антипрогестином. [35]
Ингибиторы ароматазы использовались экспериментально для уменьшения миомы. Считается, что этот эффект частично обусловлен снижением системных уровней эстрогена и частично ингибированием локально сверхэкспрессируемой ароматазы в миомах. [44] Однако после прекращения лечения рост миомы возобновился. [35] Опыт экспериментального лечения эндометриоза ингибиторами ароматазы показывает, что ингибиторы ароматазы могут быть особенно полезны в сочетании с прогестагенным ингибитором овуляции.
Маточная артерия
[ редактировать ]Эмболизация маточных артерий (ЭМА) — это неинвазивная процедура, которая блокирует приток крови к миомам, вызывая их сокращение. [57] Долгосрочные результаты в отношении того, насколько люди довольны этой процедурой, аналогичны результатам хирургического вмешательства. [58] Имеются предварительные данные о том, что традиционная хирургия может привести к улучшению фертильности. [58] Один обзор показал, что ОАЭ удваивают риск выкидыша в будущем . [59] В ОАЭ также требуется больше повторных процедур, чем если бы операция проводилась изначально. [58] Обычно человек восстанавливается после процедуры в течение нескольких дней.
Перевязка маточных артерий, а иногда и лапароскопическая окклюзия маточных артерий являются малоинвазивными методами ограничения кровоснабжения матки путем небольшой операции, которая может выполняться трансвагинально или лапароскопически. Основной механизм действия может быть таким же, как в ОАЭ, но его легче выполнять и ожидается меньше побочных эффектов. [60] [ нужен неосновной источник ] [61] [ нужен неосновной источник ]
В рекомендациях NICE (Национальный институт клинического мастерства – неправительственной общественной организации, которая публикует рекомендации по использованию медицинских технологий и надлежащей клинической практики в Соединенном Королевстве) 2016 года говорится, что ОАЭ/UFE могут быть предложены женщинам с симптоматической миомой (миома обычно >30 мм в размере). Женщины должны быть проинформированы о том, что ЭМА и миомэктомия (хирургическое удаление миомы) потенциально могут позволить им сохранить фертильность. [62]
миомэктомия
[ редактировать ]
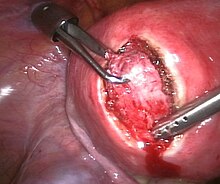
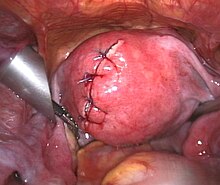
Миомэктомия — это операция по удалению одной или нескольких миом. Обычно его рекомендуют, когда более консервативные варианты лечения не помогают женщинам, которые хотят провести операцию по сохранению фертильности или хотят сохранить матку. [63]
Существует три типа миомэктомии:
- При гистероскопической миомэктомии (также называемой трансцервикальной ) миому можно резекцией удалить либо с помощью резектоскопа, эндоскопического инструмента, вводимого через влагалище и шейку матки, который может использовать высокочастотную электрическую энергию для разрезания тканей, либо с помощью аналогичного устройства. .
- Лапароскопическая миомэктомия проводится через небольшой разрез возле пупка. Врач использует лапароскоп и хирургические инструменты для удаления миомы. Исследования показали, что лапароскопическая миомэктомия приводит к более низким показателям заболеваемости и более быстрому выздоровлению, чем лапаротомная миомэктомия. [64]
- Лапаротомная миомэктомия (также известная как открытая или абдоминальная миомэктомия) является наиболее инвазивной хирургической процедурой по удалению миомы. Врач делает разрез брюшной стенки и удаляет миому матки.
Лапароскопическая миомэктомия менее болезненна и требует более короткого времени пребывания в больнице, чем открытая операция. [65] Анализ 15 000 женщин показал, что тем, кто перенес миомэктомию, потребовалось меньше дополнительных процедур для лечения миомы (включая гистерэктомию) в течение следующих 5 лет, чем тем, у кого была ЭМА. [66] [67]
Гистерэктомия
[ редактировать ]Гистерэктомия была классическим методом лечения миомы матки. Хотя сейчас это рекомендуется только как последний вариант, миома по-прежнему остается основной причиной гистерэктомии в США.
Абляция эндометрия
[ редактировать ]Абляцию эндометрия можно использовать, если миома локализуется только внутри матки, а не интрамурально и относительно небольшая. Ожидается высокая частота неудач и рецидивов при наличии более крупных или интрамуральных миом.
Другие процедуры
[ редактировать ]Радиочастотная абляция — малоинвазивный метод лечения миомы матки. [68] В этом методе миома уменьшается путем введения игольчатого устройства в миому через брюшную полость и нагревания ее радиочастотной (РЧ) электрической энергией, чтобы вызвать некроз клеток. Это лечение является потенциальным вариантом для женщин с миомой матки, родивших детей и желающих избежать гистерэктомии.
Фокусированный ультразвук под магнитно-резонансным контролем — это неинвазивное вмешательство (не требующее разреза), при котором используются сфокусированные ультразвуковые волны высокой интенсивности для разрушения тканей в сочетании с магнитно-резонансной томографией (МРТ), которая направляет и контролирует лечение. Во время процедуры подача сфокусированной ультразвуковой энергии контролируется с помощью МРТ-термографии. [69] Пациенты с симптоматической миомой, желающие получить неинвазивное лечение и не имеющие противопоказаний к МРТ, являются кандидатами на MRgFUS. Около 60% пациентов соответствуют критериям. Это амбулаторная процедура, которая занимает от одного до трех часов в зависимости от размера миомы. Это безопасно и имеет эффективность около 75%. [70] Симптоматическое улучшение сохраняется в течение двух с лишним лет. [71] Потребность в дополнительном лечении варьирует от 16 до 20% и во многом зависит от количества миомы, которую можно безопасно удалить; чем выше удаленный объем, тем ниже частота повторного лечения. [72] В настоящее время нет рандомизированных исследований между MRgFUS и ОАЭ. В настоящее время проводится многоцентровое исследование для изучения эффективности MRgFUS по сравнению с ОАЭ.
Прогноз
[ редактировать ]Примерно 1 из 1000 поражений являются или становятся злокачественными, обычно по гистологическому признаку это лейомиосаркома . [10] Признаком того, что поражение может быть злокачественным, является рост после менопаузы . [10] Среди патологоанатомов нет единого мнения относительно трансформации лейомиомы в саркому.
Метастазирование
[ редактировать ]Существует ряд редких состояний, при которых миома метастазирует. Они по-прежнему растут безвредно, но могут быть опасными в зависимости от своего местоположения. [28]
См. внематочную миому .
Эпидемиология
[ редактировать ]Примерно у 20-80% женщин к 50 годам развивается миома. [12] [1] По оценкам, в 2013 году во всем мире пострадало 171 миллион женщин. [5] Обычно они встречаются в среднем и более позднем репродуктивном возрасте. [1] После менопаузы они обычно уменьшаются в размерах. [1] Операция по удалению миомы матки чаще проводится у женщин из «высших социальных классов». [12] У подростков миома матки развивается гораздо реже, чем у женщин старшего возраста. [7] До 50% женщин с миомой матки не имеют симптомов. Распространенность миомы матки среди подростков составляет 0,4%. [7]
Европа
[ редактировать ]Считается, что заболеваемость миомой матки в Европе ниже, чем в США. [12]
Соединенные Штаты
[ редактировать ], у восьмидесяти процентов афроамериканских женщин к концу 40-х лет развивается доброкачественная миома матки По данным Национального института наук о здоровье окружающей среды . [73] Афроамериканские женщины в два-три раза чаще заболевают миомой, чем женщины европеоидной расы. [12] [13] [74] У афроамериканских женщин миома возникает в более молодом возрасте, растет быстрее и с большей вероятностью вызывает симптомы. [75] Это приводит к более высокому уровню хирургических операций среди афроамериканцев, как миомэктомии, так и гистерэктомии. [76] Повышенный риск миомы у афроамериканцев приводит к тому, что они хуже справляются с лечением бесплодия in vitro и повышают риск преждевременных родов и родов путем кесарева сечения. [76]
Неясно, почему миома чаще встречается у афроамериканских женщин. Некоторые исследования показывают, что чернокожие женщины, страдающие ожирением и высоким кровяным давлением , чаще страдают миомой. [76] Другие предполагаемые причины включают склонность афроамериканских женщин потреблять пищу, в которой содержание витамина D меньше суточной потребности . [12]
Соответствующее законодательство
[ редактировать ]Соединенные Штаты
[ редактировать ]Законопроект S.1289 2005 года был прочитан дважды и передан в комитет по здравоохранению, труду и пенсиям, но так и не был принят на голосование в Сенате или Палате представителей ; в предлагаемом Законе об исследованиях и образовании миомы матки 2005 года упоминается, что ежегодно 5 миллиардов долларов тратится на операции по гистерэктомии , от которых страдают 22% афроамериканок и 7% женщин европеоидной расы. Законопроект также призывает к увеличению финансирования исследовательских и образовательных целей. В нем также говорится, что из 28 миллиардов долларов, выделенных НИЗ, 5 миллионов долларов были выделены на лечение миомы матки в 2004 году. [77]
Другие животные
[ редактировать ]Миома матки редко встречается у других млекопитающих, хотя она наблюдалась у некоторых собак и серых тюленей . [78]
Исследовать
[ редактировать ]Селективные модуляторы рецепторов прогестерона , такие как прогента , находятся под следствием. Другой селективный модулятор рецепторов прогестерона, асоприснил, тестируется с многообещающими результатами в качестве возможного использования для лечения миомы матки, призванного обеспечить преимущества антагонистов прогестерона без их побочных эффектов. [44] Низкое потребление витамина D с пищей связано с развитием миомы матки. [12]
Примечания
[ редактировать ]Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление но из в ах есть также и «Информационный бюллетень по миоме матки» . Управление по здоровью женщин . 15 января 2015 года. Архивировано из оригинала 7 июля 2015 года . Проверено 26 июня 2015 г.
- ^ Ферри ФФ (2010). Дифференциальный диагноз Ферри: практическое руководство по дифференциальной диагностике симптомов, признаков и клинических нарушений (2-е изд.). Филадельфия, Пенсильвания: Эльзевир/Мосби. п. Глава U. ISBN 978-0-323-07699-9 .
- ^ «Миома матки | Фиброиды | MedlinePlus» . Проверено 7 ноября 2018 г.
- ^ Кашани Б.Н., Чентини Дж., Морелли СС, Вайс Дж., Петралья Ф. (июль 2016 г.). «Роль медицинского лечения лейомиомы матки». Лучшая практика Res Clin Obstet Gynaecol . 34 : 85–103. дои : 10.1016/j.bpobgyn.2015.11.016 . hdl : 11365/1031597 . ПМИД 26796059 .
- ^ Перейти обратно: а б Исследование глобального бремени болезней, 2013 г. (5 июня 2015 г.). «Глобальная, региональная и национальная заболеваемость, распространенность и продолжительность жизни с инвалидностью для 301 острого и хронического заболевания и травмы в 188 странах, 1990-2013 гг.: систематический анализ для исследования глобального бремени болезней 2013 г.» . Ланцет . 386 (9995): 743–800. дои : 10.1016/S0140-6736(15)60692-4 . ПМЦ 4561509 . ПМИД 26063472 .
- ^ Перейти обратно: а б Уоллах Э.Э., Влахос Н.Ф. (август 2004 г.). «Миомы матки: обзор развития, клинических особенностей и лечения». Акушерский Гинекол . 104 (2): 393–406. дои : 10.1097/01.AOG.0000136079.62513.39 . ПМИД 15292018 . S2CID 45013410 .
- ^ Перейти обратно: а б с д и Морони Р.М., Виейра К.С., Ферриани Р.А., Рейс Р.М., Ногейра А.А., Брито Л.Г. (январь 2015 г.). «Проявление и лечение лейомиомы матки в подростковом возрасте: систематический обзор» . BMC Женское здоровье . 15 :4. дои : 10.1186/s12905-015-0162-9 . ПМЦ 4308853 . ПМИД 25609056 .
- ^ Метвалли М., Ли ТК (2015). Репродуктивная хирургия в вспомогательном зачатии . Спрингер. п. 107. ИСБН 978-1-4471-4953-8 .
- ^ «Фибромиома матки: симптомы, причины, факторы риска и лечение» . Кливлендская клиника . Проверено 8 октября 2022 г.
- ^ Перейти обратно: а б с д и Буклет для пациентов Американского общества репродуктивной медицины: миома матки , 2003 г. Архивировано 3 июля 2008 г. в Wayback Machine.
- ^ Сегарс Дж.Х., Парротт Э.К., Нагель Дж.Д., Го XC, Гао X, Бирнбаум Л.С. и др. (2014). «Материалы Третьего Международного конгресса Национальных институтов здравоохранения по достижениям в исследованиях лейомиомы матки: всесторонний обзор, резюме конференции и будущие рекомендации» . Хм. Репродукция. Обновлять . 20 (3): 309–33. дои : 10.1093/humupd/dmt058 . ПМЦ 3999378 . ПМИД 24401287 .
- ^ Перейти обратно: а б с д и ж г час я дж Параццини Ф, Ди Мартино М, Кандиани М, Вигано П (2015). «Диетические компоненты и лейомиомы матки: обзор опубликованных данных». Нутр Рак . 67 (4): 569–79. дои : 10.1080/01635581.2015.1015746 . ПМИД 25826470 . S2CID 35376265 .
- ^ Перейти обратно: а б Миома матки в «Руководство по диагностике и терапии Merck» Профессиональном издании
- ^ «Информационный бюллетень по миоме матки» . www.womenshealth.gov. 15 декабря 2016 г. Архивировано из оригинала 9 февраля 2016 г.
- ^ Юнас К., Хадура Э., Майоко Ф., Бунхейла А. (январь 2016 г.). «Обзор научно обоснованного лечения миомы матки» . Акушер-гинеколог . 18 (1): 33–42. дои : 10.1111/тог.12223 .
- ^ Кямпъярви К., Парк М.Дж., Мехине М., Ким Н.Х., Кларк А.Д., Бютцов Р. и др. (сентябрь 2014 г.). «Мутации в экзоне 1 подчеркивают роль MED12 в лейомиоме матки» . Человеческая мутация . 35 (9): 1136–41. дои : 10.1002/humu.22612 . ПМИД 24980722 . S2CID 13931280 .
- ^ Хейнонен Х.Р., Пасанен А., Хейкинхеймо О., Тансканен Т., Пэйлин К., Толванен Дж. и др. (2017). «Множественные клинические характеристики разделяют лейомиомы матки с положительными и отрицательными мутациями MED12» . Научный представитель . 7 (1): 1015. Бибкод : 2017NatSR...7.1015H . дои : 10.1038/s41598-017-01199-0 . ПМК 5430741 . ПМИД 28432313 .
- ^ Толванен Дж., Уимари О., Рюнянен М., Аалтонен Л.А., Вахтеристо П. (2012). «Сильный семейный анамнез лейомиоматоза матки требует скрининга мутаций фумаратгидратазы» . Репродукция человека . 27 (6): 1865–9. дои : 10.1093/humrep/des105 . ПМИД 22473397 .
- ^ Торо Дж.Р., Никерсон М.Л., Вэй М.Х., Уоррен М.Б., Гленн Г.М., Тернер М.Л. и др. (2003). «Мутации в гене фумаратгидратазы вызывают наследственный лейомиоматоз и почечно-клеточный рак в семьях в Северной Америке» . Ам Джей Хум Жене . 73 (1): 95–106. дои : 10.1086/376435 . ПМЦ 1180594 . ПМИД 12772087 .
- ^ «Синдром Рида» . Архивировано из оригинала 24 февраля 2012 г. Проверено 9 апреля 2012 г. [ нужна полная цитата ]
- ^ Гарг К., Тику С.К., Сослоу Р.А., Рейтер В.Е. (2011). «Морфологические особенности лейомиомы матки, связанных с наследственным лейомиоматозом и синдромом почечно-клеточного рака». Американский журнал хирургической патологии . 35 (8): 1235–1237. дои : 10.1097/PAS.0b013e318223ca01 . ПМИД 21753700 . S2CID 1342593 .
- ^ Перейти обратно: а б «Фибромы» . Выбор Национальной службы здравоохранения . Национальная служба здравоохранения Великобритании. 2017-10-19. Архивировано из оригинала 5 мая 2008 г.
- ^ Манро М.Г., Кричли Х.О., Бродер М.С., Фрейзер И.С., Рабочая группа FIFA по менструальным расстройствам (апрель 2011 г.). «Система классификации ФИГО (PALM-COEIN) причин аномальных маточных кровотечений у небеременных женщин репродуктивного возраста» . Международный журнал гинекологии и акушерства . 113 (1): 3–13. дои : 10.1016/j.ijgo.2010.11.011 . ISSN 1879-3479 . ПМИД 21345435 . S2CID 205260568 .
- ^ Импи Л., Чайлд Т. (2016). Акушерство и гинекология . Джон Уайли и сыновья. ISBN 978-1-119-01080-7 .
- ^ Кучинелла Г., Гранезе Р., Каланья Г., Сомильяна Э., Перино А. (2011). «Паразитарные миомы после лапароскопической операции: возникающее осложнение при использовании морцеллятора? Описание четырех случаев» . Фертильность и бесплодие . 96 (2): е90–е96. doi : 10.1016/j.fertnstert.2011.05.095 . hdl : 10447/77912 . ПМИД 21719004 .
- ^ Нежат С, Хо К (2010). «Ятрогенные миомы: новый класс миом?». Журнал минимально инвазивной гинекологии . 17 (5): 544–550. дои : 10.1016/j.jmig.2010.04.004 . ПМИД 20580324 .
- ^ «Обновленная оценка FDA использования лапароскопических морцелляторов для лечения миомы матки» (PDF) . Управление по контролю за продуктами и лекарствами . Проверено 23 декабря 2017 г.
- ^ Перейти обратно: а б Диагностическая гистопатология опухолей Флетчера (3-е изд.). стр. 692–4.
- ^ Мякинен Н., Мехине М., Толванен Дж., Каасинен Э., Ли Ю., Лехтонен Х.Дж. и др. (2011). «MED12, ген субъединицы 12 медиаторного комплекса, мутирует с высокой частотой в лейомиоме матки» . Наука . 334 (6053): 252–255. Бибкод : 2011Sci...334..252M . дои : 10.1126/science.1208930 . ПМИД 21868628 . S2CID 20288929 .
- ^ Около С (2008). «Заболеваемость, этиология и эпидемиология миомы матки». Лучшие практики и исследования. Клиническая акушерство и гинекология . 22 (4): 571–588. дои : 10.1016/j.bpobgyn.2008.04.002 . ПМИД 18534913 .
- ^ Маруо Т., Охара Н., Ван Дж., Мацуо Х. (2004). «Половая стероидная регуляция роста и апоптоза лейомиомы матки» . Обновление репродукции человека . 10 (3): 207–220. дои : 10.1093/humupd/dmh019 . ПМИД 15140868 .
- ^ Перейти обратно: а б Йен-Пин Хо Дж, Ман ВК, Вэнь Ю, Полан МЛ, Ши-Чу Хо Э, Чен Б (июнь 2009 г.). «Преобразование экспрессии факторов, взаимодействующих с ростом, при лейомиоме по сравнению с миометрием» . Плодородный. Стерильный . 94 (3): 1078–83. doi : 10.1016/j.fertnstert.2009.05.001 . ПМЦ 2888713 . ПМИД 19524896 .
- ^ Сёдзу М., Мураками К., Иноуэ М. (2004). «Ароматаза и лейомиома матки». Семинары по репродуктивной медицине . 22 (1): 51–60. дои : 10.1055/s-2004-823027 . ПМИД 15083381 . S2CID 260319833 .
- ^ Булун С.Е. , Ян С., Фанг З., Гуратес Б., Тамура М., Чжоу Дж. и др. (2001). «Роль ароматазы при заболеваниях эндометрия». Журнал биохимии стероидов и молекулярной биологии . 79 (1–5): 19–25. дои : 10.1016/S0960-0760(01)00134-0 . ПМИД 11850203 . S2CID 7642211 .
- ^ Перейти обратно: а б с д и Моравек М.Б., Инь П., Оно М., Кун Дж.С., Дайсон М.Т., Наварро А. и др. (2015). «Стероиды яичников, стволовые клетки и лейомиома матки: терапевтические последствия» . Обновление воспроизведения гула . 21 (1): 1–12. дои : 10.1093/humupd/dmu048 . ПМК 4255606 . ПМИД 25205766 .
- ^ Ходж Дж.К., Мортон CC (2007). «Генетическая гетерогенность лейомиомы матки: понимание злокачественного прогрессирования» . Молекулярная генетика человека . 16 Спецификация № 1: R7–13. дои : 10.1093/hmg/ddm043 . ПМИД 17613550 .
- ^ Перейти обратно: а б с Авиви М.О., Бадави М., Шаабан А.М., Мениас К.О., Горовиц Дж.М., Солиман М. и др. (июль 2022 г.). «Обзор миомы матки: визуализация типичных и атипичных особенностей, вариантов и мимики с акцентом на исследование и классификацию FIFA». Абдом Радиол (Нью-Йорк) . 47 (7): 2468–2485. дои : 10.1007/s00261-022-03545-x . ПМИД 35554629 . S2CID 248725335 .
- ^ «Миома матки – Диагностика и лечение – Клиника Майо» . www.mayoclinic.org . Проверено 8 октября 2022 г.
- ^ Мохамед Мохтар Десуки. «Матка – Стромальные опухоли – Лейомиома» . Очертания патологии . Тема завершена: 1 августа 2011 г. Отредактирована: 15 декабря 2019 г.
- ^ Эль Сабех М., Саха С.К., Африн С., Ислам М.С., Борахай М.А. (2021). «Сигнальный путь Wnt/β-катенин при лейомиоме матки: роль в биологии опухоли и возможности нацеливания» . Мол Клеточная Биохимия . 476 (9): 3513–3536. дои : 10.1007/s11010-021-04174-6 . ПМЦ 9235413 . ПМИД 33999334 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Гупта Дж.К., Синха А., Ламсден М.А., Хики М. (26 декабря 2014 г.). «Эмболизация маточных артерий при симптоматической миоме матки» . Кокрановская база данных систематических обзоров . 12 (12): CD005073. дои : 10.1002/14651858.CD005073.pub4 . ПМЦ 11285296 . ПМИД 25541260 .
- ^ Перейти обратно: а б Саймонс М (11 декабря 2022 г.). «Фибромиома — это серьезно. Хирургическое вмешательство — не единственный способ остановить ее. Многим женщинам не рассказывают о неинвазивных методах лечения, которые не влияют на фертильность. Эксперты хотят изменить это» . Вашингтон Пост . Проверено 11 декабря 2022 г.
- ^ Сапата Л.Б., Уайтман М.К., Теппер Н.К., Джеймисон Д.Д., Марчбэнкс П.А., Кертис К.М. (2010). «Использование внутриматочных спиралей женщинами с миомой матки: систематический обзор ☆». Контрацепция . 82 (1): 41–55. doi : 10.1016/j.contraception.2010.02.011 . ПМИД 20682142 .
- ^ Перейти обратно: а б с д и ж Шанкаран С., Manyonda IT (август 2008 г.). «Медикаментозное лечение миомы». Лучшая практика Res Clin Obstet Gynaecol . 22 (4): 655–76. дои : 10.1016/j.bpobgyn.2008.03.001 . ПМИД 18468953 .
- ^ Кайласам С., Кэхилл Д. (2008). «Обзор безопасности, эффективности и переносимости внутриматочной системы, высвобождающей левоноргестрел» . Предпочтения и приверженность пациентов . 2 : 293–302. дои : 10.2147/ppa.s3464 . ПМК 2770406 . ПМИД 19920976 .
- ^ Талауликар В.С., Маньонда ИТ (август 2012 г.). «Улипристала ацетат: новый вариант медикаментозного лечения симптоматической миомы матки». Адв Тер . 29 (8): 655–63. дои : 10.1007/s12325-012-0042-8 . ПМИД 22903240 . S2CID 25905881 .
- ^ Перес-Лопес, Франция (апрель 2015 г.). «Улипристала ацетат в лечении симптоматической миомы матки: факты и нерешенные проблемы». Климактерический . 18 (2): 177–81. дои : 10.3109/13697137.2014.981133 . ПМИД 25390187 . S2CID 25077228 .
- ^ Доннес Дж., Томашевски Дж., Васкес Ф., Бушар П., Лемещук Б., Баро Ф. и др. (февраль 2012 г.). «Улипристала ацетат по сравнению с лейпролидом ацетатом при миоме матки» . N Engl J Med . 366 (5): 421–32. дои : 10.1056/NEJMoa1103180 . ПМИД 22296076 .
- ^ Люйкс М., Сквиффлет Дж.Л., Джадул П., Вотино Р., Долманс М.М., Доннез Дж. (ноябрь 2014 г.). «Первая серия из 18 беременностей после лечения миомы матки улипристала ацетатом» . Фертильная стерилизация . 102 (5): 1404–9. doi : 10.1016/j.fertnstert.2014.07.1253 . ПМИД 25241376 .
- ^ Куртой Дж., Донне Дж., Марбе Э., Долманс М. М. (август 2015 г.). «Механизмы уменьшения объема миомы матки in vivo при лечении улипристала ацетатом» . Фертильная стерилизация . 104 (2): 426–34.e1. doi : 10.1016/j.fertnstert.2015.04.025 . ПМИД 26003270 .
- ^ Куртой Дж., Донне Дж., Амбруаз Дж., Арриагада П., Луйкс М., Марбе Э. и др. (август 2018 г.). «Изменения экспрессии генов в миомах матки в ответ на лечение улипристала ацетатом». Репрод Биомед Онлайн . 37 (2): 224–233. дои : 10.1016/j.rbmo.2018.04.050 . ПМИД 29807764 . S2CID 44106868 .
- ^ Куртой Дж.Э., Анриет П., Марбе Э., де Кодт М., Луйкс М., Донне Дж. и др. (апрель 2018 г.). «Активность матриксных металлопротеиназ коррелирует с уменьшением объема миомы матки после лечения улипристала ацетатом» . J Clin Эндокринол Метаб . 103 (4): 1566–1573. дои : 10.1210/jc.2017-02295 . ПМИД 29408988 .
- ^ Доннес Дж., Доннес О., Матуле Д., Арендт Х.Дж., Худечек Р., Затик Дж. и др. (январь 2016 г.). «Долгосрочное медикаментозное лечение миомы матки с помощью улипристала ацетата» . Плодородная стерильность . 105 (1): 165–173.e4. doi : 10.1016/j.fertnstert.2015.09.032 . ПМИД 26477496 .
- ^ «Европейское Медикаментозное Агентство» .
- ^ Правительство Канады, Министерство здравоохранения Канады (16 сентября 2020 г.). «Allergan Inc. добровольно отзывает с канадского рынка свой препарат Фибристал, используемый для лечения миомы матки» . healthcanadians.gc.ca . Проверено 17 марта 2021 г.
- ^ Тристан М., Ороско Л.Дж., Стид А., Рамирес-Морера А., Стоун П. (август 2012 г.). «Мифепристон при миоме матки» . Cochrane Database Syst Rev. 2012 (8): CD007687. дои : 10.1002/14651858.CD007687.pub2 . ПМЦ 8212859 . ПМИД 22895965 .
- ^ «Процесс эмболизации» . FEmISA: Эмболизация миомы матки: информация, поддержка, советы. Архивировано из оригинала 31 мая 2014 г.
- ^ Перейти обратно: а б с Гупта Дж.К., Синха А., Ламсден М.А., Хики М. (декабрь 2014 г.). «Эмболизация маточных артерий при симптоматической миоме матки» . Cochrane Database Syst Rev (12): CD005073. дои : 10.1002/14651858.CD005073.pub4 . ПМЦ 11285296 . ПМИД 25541260 .
- ^ Гомер Х., Саридоган Э. (июнь 2010 г.). «Эмболизация маточных артерий при миоме связана с повышенным риском выкидыша» . Фертильная стерилизация . 94 (1): 324–30. doi : 10.1016/j.fertnstert.2009.02.069 . ПМИД 19361799 .
- ^ Лю ВМ, Нг ХТ, Ву ЮК, Йен ЮК, Юань CC (2001). «Лапароскопическая биполярная коагуляция сосудов матки: новый метод лечения симптоматической миомы» . Фертильность и бесплодие . 75 (2): 417–22. дои : 10.1016/S0015-0282(00)01724-6 . ПМИД 11172850 .
- ^ Акинола О.И., Фабамво А.О., Оттун А.Т., Акиннийи О.А. (2005). «Лигирование маточных артерий для лечения миомы матки». Международный журнал гинекологии и акушерства . 91 (2): 137–40. дои : 10.1016/j.ijgo.2005.07.012 . ПМИД 16168993 . S2CID 8042317 .
- ^ «Эмболизация миомы матки в Африке» . 23 февраля 2017 г.
- ^ Метвалли М., Рэйбоулд Дж., Чеонг Ю.К., Хорн А.В. (январь 2020 г.). «Хирургическое лечение миомы матки при бесплодии» . Cochrane Database Syst Rev. 1 (1): CD003857. дои : 10.1002/14651858.CD003857.pub4 . ПМК 6989141 . ПМИД 31995657 .
- ^ Агди М., Туланди Т. (август 2008 г.). «Эндоскопическое лечение миомы матки». Лучшая практика Res Clin Obstet Gynaecol . 22 (4): 707–16. дои : 10.1016/j.bpobgyn.2008.01.011 . ПМИД 18325839 .
- ^ Бхаве Читтавар П., Франк С., Паувер А.В., Фаркухар С. (21 октября 2014 г.). «Минимально инвазивные хирургические методы в сравнении с открытой миомэктомией при миоме матки» . Кокрановская база данных систематических обзоров . 10 (10): CD004638. дои : 10.1002/14651858.CD004638.pub3 . ПМЦ 10961732 . ПМИД 25331441 .
- ^ Амоа А., Куинн С.Д. (1 июня 2023 г.). «Матосохраняющее лечение или повторное вмешательство в гистерэктомию после миомэктомии или эмболизации маточной артерии: ретроспективное когортное исследование долгосрочных результатов» . BJOG: Международный журнал акушерства и гинекологии . 130 (7): 823–831. дои : 10.1111/1471-0528.17412 . ISSN 1470-0328 . ПМИД 36706789 . S2CID 256325720 .
- ^ «Хирургическое удаление миомы имеет лучшие долгосрочные результаты, чем блокирование кровеносных сосудов» . Доказательства НИХР . 22 сентября 2023 г. doi : 10.3310/nihrevidence_59961 . S2CID 262209805 .
- ^ Бек М (20 января 2010 г.). «Новый метод лечения, помогающий женщинам избежать гистерэктомии» . Уолл Стрит Джорнал .
- ^ «FDA одобрило новое устройство для лечения миомы матки» (пресс-релиз). FDA. 22 октября 2004 г. Архивировано из оригинала 9 мая 2008 г. Проверено 26 мая 2008 г.
- ^ Шен С.Х., Феннесси Ф., Макданнольд Н., Джолеш Ф., Темпани С. (апрель 2009 г.). «Тепловая терапия миомы матки под визуальным контролем» . Семин УЗИ КТ МР . 30 (2): 91–104. дои : 10.1053/j.sult.2008.12.002 . ПМЦ 2768544 . ПМИД 19358440 .
- ^ Стюарт Э.А., Рабинович Дж., Темпани С.М., Инбар Ю., Риган Л., Гостут Б. и др. (январь 2006 г.). «Клинические результаты фокусированной ультразвуковой хирургии в лечении миомы матки» . Плодородный. Стерильный . 85 (1): 22–9. doi : 10.1016/j.fertnstert.2005.04.072 . ПМИД 16412721 .
- ^ Курашвили Ж, Степанов А, Кулабучова Е, Батаршина О (2014). «Тезисы 2-го Европейского симпозиума по фокусированной ультразвуковой терапии» . J Тер Ультразвук . 2 (Приложение 1): А1–А25. дои : 10.1186/2050-5736-2-s1-a1 . ПМК 4292016 . ПМИД 25932673 .
- ^ «Помощь чернокожим женщинам в распознавании и лечении миомы» . ЭНЕРГЕТИЧЕСКИЙ ЯДЕРНЫЙ РЕАКТОР . Архивировано из оригинала 22 января 2012 года . Проверено 30 марта 2011 г.
- ^ «Афроамериканские женщины и миомы» . Проект здоровья чернокожих женщин Филадельфии . Архивировано из оригинала 1 апреля 2011 года . Проверено 30 марта 2011 г.
- ^ «Здоровье женщин меньшинств» . Женское здоровье.gov. Архивировано из оригинала 30 августа 2010 г.
- ^ Перейти обратно: а б с «Чернокожие женщины и высокая распространенность миомы» . Коллектив по лечению миомы . 29 ноября 2010 года. Архивировано из оригинала 25 декабря 2010 года . Проверено 30 марта 2011 г.
- ^ Бюджетное управление (PDF). Архивировано 30 сентября 2011 г. в Wayback Machine. [ нужна полная цитата ]
- ^ Бэклин Б.М., Эрикссон Л., Оловссон М. (март 2003 г.). «Гистология лейомиомы матки и ее возникновение в связи с репродуктивной активностью у балтийского серого тюленя (Halichoerus grypus)» . Ветеринар. Патол . 40 (2): 175–80. дои : 10.1354/vp.40-2-175 . ПМИД 12637757 .