Имплантация (эмбриология)
| Имплантация | |
|---|---|
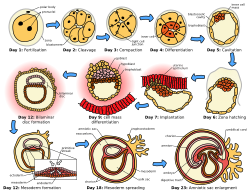 Имплантация как один из ранних этапов эмбрионального развития человека. | |
| Подробности | |
| Этап Карнеги | 3 |
| Дни | 5–9 |
| Дает начало | Гаструла |
| Идентификаторы | |
| МеШ | D010064 |
| Анатомическая терминология | |
Имплантация , также известная как нидация , [1] Это стадия млекопитающих эмбрионального развития , на которой бластоциста вылупляется, прикрепляется, прикрепляется и проникает в эндометрий самки матки . [2] Имплантация — это первый этап беременности , и в случае успеха самка считается беременной . [3] Имплантированный эмбрион обнаруживается по наличию повышенного уровня хорионического гонадотропина человека (ХГЧ) в тесте на беременность . [3] Имплантированный эмбрион будет получать кислород и питательные вещества для своего роста.
Чтобы имплантация состоялась, матка должна стать восприимчивой. Рецептивность матки включает в себя множество перекрестных взаимодействий между эмбрионом и маткой, инициируя изменения в эндометрии. Этот этап дает синхронность, которая открывает окно имплантации, позволяющее успешно имплантировать жизнеспособный эмбрион. [4] Эндоканнабиноидная система играет жизненно важную роль в этой синхронности в матке, влияя на восприимчивость матки и имплантацию эмбриона. [5] Эмбрион экспрессирует каннабиноидные рецепторы на ранних стадиях своего развития, которые реагируют на анандамид (AEA), секретируемый в матке. AEA производится на более высоких уровнях перед имплантацией, а затем его уровень снижается во время имплантации. Эта передача сигналов важна для перекрестных помех между эмбрионом и маткой в регуляции времени имплантации эмбриона и рецептивности матки. Для успешной имплантации необходимы адекватные концентрации AEA, которые не являются ни слишком высокими, ни слишком низкими. [5] [6] [7]
существуют значительные различия в типах клеток трофобласта и структурах плаценты . У разных видов млекопитающих [8] Из пяти признанных стадий имплантации, включая две предимплантационные стадии, предшествующие плацентации , первые четыре одинаковы у всех видов. Пять стадий: миграция и вылупление, предконтакт, прикрепление, адгезия и инвазия. [8] Две предимплантационные стадии связаны с предимплантационным эмбрионом . [9] [10]
У человека после стадии вылупления, которая происходит примерно через четыре-пять дней после оплодотворения , начинается процесс имплантации. К концу первой недели бластоциста поверхностно прикрепляется к эндометрию матки. К концу второй недели имплантация завершилась. [11]
Этапы имплантации
[ редактировать ]Существует пять признанных стадий имплантации у млекопитающих, включая две предимплантационные стадии, которые предшествуют образованию плаценты . Это: миграция и вылупление, преконтакт, прикрепление, адгезия и инвазия. Первые четыре стадии одинаковы для всех видов, при этом процесс инвазии варьируется. [8] [12] Эти три стадии аппозиции , прикрепления и инвазии также альтернативно называются контактом (приложением), адгезией (прикреплением) и проникновением (инвазией). [10] [9] и может произойти только в течение ограниченного периода времени, известного как окно имплантации , когда матка наиболее восприимчива.
Миграция и вылупление
[ редактировать ]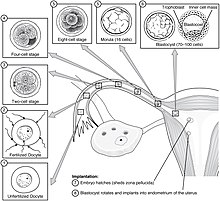
Имплантация включает две стадии миграции: первая — миграция зиготы , а вторая — миграция трофобласта . [13] Оплодотворение яйцеклетки происходит в ампуле фаллопиевой трубы . Реснички на слизистой трубке перемещают зиготу при ее миграции к матке. [13]
Во время этой миграции зигота претерпевает ряд делений клеток , в результате чего образуется клубок из 16 уплотненных бластомеров, называемый морулой . [14] Морула попадает в матку через три или четыре дня, и при этом полость, называемая бластоцелем, в моруле образуется для образования бластоцисты . Бластоциста содержит внутреннюю клеточную массу , которая в дальнейшем разовьется в собственно эмбрион , и внешний клеточный слой трофобластов, который разовьется во внеэмбриональные мембраны ( плодные оболочки ). [15]
Бластоциста все еще заключена в яйцевую оболочку, известную как пеллюцидная зона , и для того, чтобы она могла имплантироваться в стенку матки, она должна избавиться от этого покрытия. Эта стадия известна как хэтчинг зоны , и при достаточном растворении бластоциста может инициировать стадию аппозиции имплантации. Литические факторы в полости матки, а также факторы самой бластоцисты необходимы для разрушения яйцеклетки. На механизмы последнего указывает тот факт, что пеллюцидная оболочка остается интактной, если в тех же условиях в матку помещается неоплодотворенная яйцеклетка. [16]
Среди известных молекулярных регуляторов, способствующих вылуплению, преобладают протеазы , стимулируемые различными факторами роста . [17] Бластоциста также вырабатывает цитокины , как провоспалительные, так и противовоспалительные, которые играют решающую роль во время имплантации и на других стадиях беременности. Оба типа цитокинов модулируют активность протеаз, в том числе ММП , активаторов плазминогена и катепсинов . [17] Неизвестно, являются ли цитокины, участвующие в вылуплении, провоспалительными или противовоспалительными, а также какие протеазы в этом участвуют. Однако общепризнано, что провоспалительные цитокины доминируют во время имплантации. также присутствуют цитокины В маточном молоке , которые могут регулировать развитие и функцию бластоцисты, но нет никаких доказательств, подтверждающих их участие в вылуплении. Фактор ингибирования лейкемии (LIF) представляет собой провоспалительный цитокин, экспрессируемый в эндометрии во время лютеиновой фазы менструального цикла , причем наибольшая экспрессия наблюдается в период имплантации. LIF играет роль в адгезии и инвазии. [17]
Вспомогательное вылупление зоны может иметь место при вспомогательной репродукции, когда для облегчения вылупления пеллюцидную зону можно искусственно проткнуть. [18]
Приложение
[ редактировать ]После вылупления зоны самое первое свободное соединение или контакт между бластоцистой и эндометрием называется аппозицией. Аппозиция обычно производится при наличии небольшого крипта в эндометрии, а также при достаточном разрушении прозрачной зоны, позволяющем трофобласту бластоцисты напрямую контактировать с подлежащим эндометрием. В конечном итоге внутренняя клеточная масса (также эмбриобласт) внутри слоя трофобласта выравнивается ближе всего к децидуальной оболочке . Если внутренняя клеточная масса не выровнена с децидуальной оболочкой при аппозиции, она обладает способностью свободно вращаться внутри трофобласта и достигать этого выравнивания. Аппозиция представляет собой лишь слабое взаимодействие трофэктодермы с эпителием матки, неустойчивое к сдвиговым напряжениям . Аппозиция также обратима, что позволяет изменить положение бластоцисты в матке. [14]
Адгезия
[ редактировать ]Адгезия представляет собой гораздо более прочное прикрепление к эндометрию, чем рыхлая аппозиция. [ нужна ссылка ]
Трофобласты прикрепляются, проникая в эндометрий, с выпячиваниями клеток трофобласта. [ нужна ссылка ]
Эту адгезивную активность осуществляют микроворсинки, находящиеся на трофобласте. Трофобласт имеет соединения связывающих волокон, ламинин, коллаген типа IV и интегрины, которые способствуют процессу адгезии. [19]
Муцин-16 представляет собой трансмембранный муцин, экспрессирующийся на апикальной поверхности эпителия матки. Этот муцин предотвращает имплантацию бластоцисты в нежелательное место на эпителии. Таким образом, MUC-16 ингибирует межклеточную адгезию. его удаление во время формирования пиноподов Было показано, что облегчает инвазию трофобласта in vitro . [20]
Идентичность молекул трофобласта и эпителия эндометрия, которые опосредуют первоначальное взаимодействие между ними, остается неидентифицированной. Однако ряд исследовательских групп предположили, что в этом участвует MUC1 , член семейства гликозилированных белков муцинов . [21] MUC1 представляет собой трансмембранный гликопротеин, экспрессирующийся на апикальной поверхности эпителиальных клеток эндометрия во время окна имплантации у людей, и было показано, что в это время он дифференциально экспрессируется у фертильных и бесплодных субъектов. [21] MUC1 отображает углеводные фрагменты на своем внеклеточном домене, которые являются лигандами L-селектина , молекулы клеточной адгезии на поверхности клеток трофобласта. [22] [23] Модель имплантации in vitro подтвердила гипотезу о том, что L-селектин опосредует прилегание бластоцисты к эпителию матки путем взаимодействия с его лигандами. [24]
Вторжение
[ редактировать ]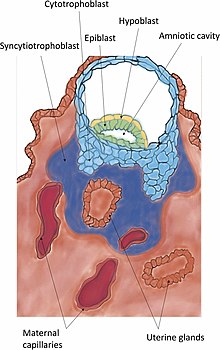
Инвазия – это дальнейшее внедрение бластоцисты в эндометрий. Выпячивания клеток трофобласта, прикрепившиеся к эндометрию, продолжают пролиферировать и проникать в эндометрий с помощью желатиназ А ( ММП-2 ) и В ( ММП-9 ). [25] Трофобласты проникают в матку, пытаясь достичь кровоснабжения матери и создать основу для кровотока плода. [26] Они также секретируют преимплантационный фактор — пептид, который помогает их инвазии и образованию плаценты. [27] По мере проникновения эти трофобласты сливаются со своими соседями, окончательно дифференцируясь в многоядерную , ткань — синцитий известный как синцитиотрофобласт . Между этим слоем и бластоцистой лежит цитотрофобласт . [28] [29]
Когда синцитиотрофобласт достигает базальной мембраны под децидуальными клетками , он вытесняет их для дальнейшего проникновения в строму матки. Смещение осуществляется путем разрушения молекул клеточной адгезии (САМ), которые связывают децидуальные клетки и связанный с ними внеклеточный матрикс . Деградация достигается за счет секреции фактора некроза опухоли-альфа из синцитиотрофобласта, который ингибирует экспрессию САМ и бета-катенина . Внеклеточный матрикс разрушается металлопротеиназами, такими как коллагеназы , желатиназы и матриксные металлопротеиназы , а также сериновыми протеазами . [30] Коллагеназы переваривают типов I , II , III , VII и коллаген X. [30] Желатиназы существуют в двух формах; один переваривает коллаген типа IV и один переваривает желатин . [30] Внеклеточный матрикс разрушается сериновыми эндопептидазами и металлопротеиназами . Синцитиотрофобласт может затем проникнуть в эндометрий, унося с собой эмбрион, где он внедряется. [30] В конце концов синцитиотрофобласт вступает в контакт с материнской кровью и образует ворсинки хориона – начало плацентации . После инвазии разрыв в эпителии матки, образовавшийся в результате входа бластоцисты, закрывается фибриновой пробкой . Фибриновая пробка представляет собой коагуляцию сгустка крови и клеточного мусора. [11]
Вневорсинчатые трофобласты
[ редактировать ]Вневорсинчатые трофобласты представляют собой клетки инвазивных ворсинок, которые мигрируют в миометрий материнской матки. Эти клетки реконструируют спиральные артерии , чтобы улучшить и обеспечить приток материнской крови к растущему эмбриону. Есть также данные о том, что этот процесс происходит с венами матки, стабилизируя их, улучшая отток крови плода и продуктов метаболизма. [31] Также было зарегистрировано, что трофобласты мигрируют в различные ткани матери. В связи с этим трофобласты вовлечены в феномен, известный как фетоматеринский микрохимеризм , когда клетки плода создают клеточные линии в материнских тканях. [32]
Выделения
[ редактировать ]Было показано, что преимплантационные бластоцисты способны секретировать факторы роста, гормоны и трипсиноподобные протеазы для участия в процессе вылупления. [33]
Во время инвазии бластоциста секретирует факторы для множества целей. [33] Он секретирует несколько аутокринных факторов, нацеливаясь на себя и стимулируя дальнейшее проникновение в эндометрий. Хорионический гонадотропин человека (ХГЧ) является аутокринным фактором роста бластоцисты, тогда как инсулиноподобный фактор роста 2 стимулирует его инвазивность. [30] Хорионический гонадотропин человека не только действует как иммунодепрессант, но также сигнализирует матери о том, что она беременна , предотвращая лютеолиз желтого тела и менструацию, поддерживая функцию желтого тела. [30] Секреции отделяют децидуальные клетки друг от друга, предотвращают отторжение эмбриона матерью, запускают окончательную децидуализацию и предотвращают менструацию. Преимплантационный фактор секретируется клетками трофобласта до формирования плаценты. [27]
Иммунодепрессивный
[ редактировать ]Эмбрион отличается от клеток матери и был бы отвергнут иммунной системой матери как паразит, если бы он не выделял иммунодепрессанты . К таким агентам относятся фактор активации тромбоцитов , хорионический гонадотропин человека , фактор ранней беременности , простагландин Е2 , интерлейкин-1 альфа , интерлейкин 6 , интерферон -альфа, фактор ингибирования лейкемии и колониестимулирующий фактор . [ нужна ссылка ]
Другие факторы
[ редактировать ]Другие факторы, секретируемые бластоцистой: [ нужна ссылка ]
- эмбрионального происхождения Высвобождающий гистамин фактор
- Тканевой активатор плазминогена, а также его ингибиторы.
- Эстрадиол
- β1- интегрины
- Фактор роста фибробластов
- Трансформирующий фактор роста альфа
- Ингибин
Восприимчивость матки
[ редактировать ]Чтобы обеспечить имплантацию, матка претерпевает изменения, чтобы иметь возможность принять зачатие. Рецептивность включает изменения клеток эндометрия в виде пиноподий , которые помогают поглощать маточную жидкость; изменение толщины эндометрия и развитие его кровоснабжения, а также формирование децидуальной оболочки . В совокупности эти изменения известны как трансформация плазматической мембраны : они приближают бластоцисты к эндометрию и обездвиживают его. На этом этапе бластоциста все еще может быть удалена путем вымывания из матки. [34] [35]
Успешная имплантация зависит от жизнеспособности эмбриона и восприимчивости матки. [4] Важнейшим фактором является синхронность развития между эмбрионом и маткой. [36] Синхронность дает короткий период восприимчивости, известный как окно имплантации, и на этой стадии включает в себя большое количество перекрестных помех между бластоцистой и эндометрием. [37] [38] [39]
Эндоканнабиноидная система играет жизненно важную роль в этой синхронности в матке, влияя на восприимчивость матки и имплантацию эмбриона. [5] Эмбрион экспрессирует каннабиноидные рецепторы на ранних стадиях своего развития, которые реагируют на анандамид (AEA), секретируемый в матке. Эта передача сигналов важна для перекрестных помех между эмбрионом и маткой в регуляции времени имплантации эмбриона и рецептивности матки. Для успешной имплантации необходимы адекватные концентрации AEA, которые не являются ни слишком высокими, ни слишком низкими. [5] [40] IL-6 и FAAH оба имеют решающее значение для восприимчивости матки, и вместе с AEA наблюдается связь с адекватной толщиной эндометрия, которая поддерживает беременность. [5]
Во время адгезии перекрестные помехи передаются посредством взаимодействий рецептор - лиганд , как интегрин-матрикс, так и протеогликанов. Рецепторы протеогликанов находятся на поверхности децидуальной оболочки, а их аналоги — протеогликаны — вокруг клеток трофобласта бластоцисты. Эта система лиганд-рецептор также присутствует прямо в окне имплантации. [30] Бластоциста сигнализирует эндометрию о необходимости дальнейшей адаптации к ее присутствию, например, путем изменений в цитоскелете децидуальных клеток . Это, в свою очередь, отрывает децидуальные клетки от их связи с подлежащей базальной пластинкой , что позволяет бластоцисте выполнить последующую инвазию. [30]
Окно имплантации
[ редактировать ]Окно имплантации представляет собой ограниченный период времени для успешного прикрепления бластоцисты. [41] У человека рецептивность матки оптимальна на 20-24-й день секреторной фазы менструального цикла , когда уровень лютеинизирующего гормона достигает максимума. [9] [42] В это время происходят перекрестные помехи между эмбрионом и эндометрием. [9] Эндотелиальные эпителиальные клетки, выстилающие матку, являются первыми клетками, которые обнаруживают сигналы от бластоцисты, и они преобразуются в нижестоящие сигнальные пути. [33] У человека окно имплантации доступно только в течение 24–36 часов. [43]
Было показано, что микробиом эндометрия играет важную роль в успешной имплантации, контроле функции клеток эндометрия и функции местной системы иммунитета, которая предотвращает рост патогенов. Это связано с выделением защитных веществ. [44] [45]
Пиноподы
[ редактировать ]Пиноподы образуются в начале окна имплантации и встречаются у многих видов. [46] [41] Они представляют собой грибовидные выпячивания апикальной клеточной мембраны эпителиальных клеток матки. [41] Пиноподы образуются в результате набухания этих эпителиальных клеток и слияния ряда микроворсинок для достижения максимального размера. [46] Они появляются между 19 и 21 днями беременности и полностью формируются к 20 дню. [41] Это соответствует возрасту оплодотворения примерно пять-семь дней, что хорошо соответствует времени имплантации. Пиноподы сохраняются максимум два дня и рассматриваются как ультраструктурные маркеры восприимчивости. [46]
Их развитие усиливается прогестероном и тормозится эстрогенами . Во время окна имплантации межклеточная адгезия ингибируется MUC1, гликопротеином клеточной поверхности, принадлежащим гликокаликсу . Пиноподии выше микроворсинок и выступают через гликокаликс, обеспечивая прямой контакт с прикрепившимся трофобластом. Наиболее важным свойством пинопод является удаление гликопротеинов с клеточной поверхности эпителиальных клеток матки. [9] Также было показано, что MUC16 исчезает с поверхности клеток с развитием пиноподов.В некоторых исследованиях сообщалось, что пиноподы захватывают реснички, что предотвращает движение эмбриона, а во время имплантации обеспечивает тесный контакт и прилипание эмбриона. [41]
Пиноподы переносят маточную жидкость и ее макромолекулы в клетки путем эндоцитоза . При этом уменьшается объем матки, приближая стенки к плавающей в ней бластоцисте. Таким образом, период активных пиноподов может ограничивать окно имплантации. [30] Пиноподы продолжают поглощать жидкость, удаляя большую ее часть на ранних стадиях имплантации. [47]
Предецидуализация
[ редактировать ]Эндометрий увеличивается в толщине, васкуляризируется , а его железы становятся извилистыми и выделяют повышенную секрецию. Эти изменения достигают максимума примерно через семь дней после овуляции . [ нужна ссылка ]
Кроме того, на поверхности эндометрия образуются своеобразные округлые клетки, которые покрывают всю область по направлению к полости матки. Это происходит примерно через 9–10 дней после овуляции. [30] Эти клетки называются децидуальными клетками , что подчеркивает, что весь их слой отслаивается при каждой менструации , если не наступает беременность, точно так же, как листья лиственных деревьев . С другой стороны, активность маточных желез снижается и дегенерируют примерно через 8–9 дней. [30] после овуляции при отсутствии беременности.
Децидуальные клетки происходят из стромальных клеток, которые всегда присутствуют в эндометрии, и составляют новый слой — децидуальную оболочку . Остальная часть эндометрия, кроме того, имеет различия между люминальной и базальной сторонами. Люминальные клетки образуют компактный слой эндометрия, в отличие от базалолатерального губчатого слоя , который состоит из довольно губчатых стромальных клеток. [30]
Децидуализация
[ редактировать ]
Децидуализация расширяется при наступлении беременности, в дальнейшем развивая маточные железы, компактную зону и выстилающий ее эпителий децидуальных клеток. Децидуальные клетки наполняются липидами и гликогеном и принимают характерную для децидуальных клеток многогранную форму. Факторы бластоцисты также запускают окончательное формирование децидуальных клеток в их правильную форму. Напротив, некоторые децидуальные клетки вблизи бластоцисты дегенерируют, обеспечивая ее питательными веществами. [30] Признаком эмбрионального влияния является то, что децидуализация происходит в более высокой степени в циклах зачатия, чем в циклах отсутствия зачатия. [30] Более того, аналогичные изменения наблюдаются при применении стимулов, имитирующих естественное вторжение в эмбрион. [30]
Эмбрион высвобождает сериновые протеазы, которые вызывают деполяризацию мембраны эпителиальных клеток и активируют эпителиальные натриевые каналы . Это вызывает приток ионов кальция (Ca 2+ ) и фосфорилирование CREB. Фосфорилирование CREB усиливает экспрессию COX2 , что приводит к высвобождению простагландина E2 (PGE2) из эпителиальных клеток. PGE2 действует на клетки стромы, активируя пути, связанные с цАМФ, в стромальных клетках, что приводит к децидуализации. [48]
Части децидуальной оболочки
[ редактировать ]Децидуальные оболочки могут быть разделены на отдельные отделы, хотя они имеют одинаковый состав.
- Базальная децидуальная оболочка – это часть децидуальной оболочки, которая после имплантации расположена базальнолатерально по отношению к эмбриону.
- Decidua capsularis – Decidua capsularis растет над эмбрионом на просветной стороне, заключая его в эндометрий. Он окружает зародыш вместе с базальной децидуальной оболочкой.
- Decidua parietalis. Все остальные децидуальные оболочки на поверхности матки относятся к decidua parietalis.
Децидуальная ткань во время беременности
[ редактировать ]После имплантации децидуальная оболочка сохраняется, по крайней мере, в течение первого триместра. [30] Однако наиболее заметное время — на ранних стадиях беременности, во время имплантации. Ее функция окружающей ткани заменяется окончательной плацентой . Однако некоторые элементы децидуализации сохраняются на протяжении всей беременности. [30]
Слои компакты и губки все еще видны под децидуальной оболочкой во время беременности. Железы губчатого слоя продолжают секретировать в течение первого триместра беременности, когда они дегенерируют. Однако до этого исчезновения некоторые железы выделяют неодинаково много секрета. Этот феномен гиперсекреции называется феноменом Ариаса-Стеллы . [30] в честь патологоанатома Хавьера Ариаса-Стеллы .
Маточные железы
[ редактировать ]
| Белки, гликопротеины и пептиды секретируемый маточными железами [30] |
| Матрица -связанная: |
| Фибронектин |
| Ламинин |
| Энтактин |
| Коллаген IV типа |
| Гепарансульфат |
| Протеогликан |
| Интегрины |
| – |
| Другие: |
| Муцины |
| Пролактин |
| ИФРСБ -1 |
| Гликоделин |
| Эндометриальный белок 15 |
| Альбумин |
| Бета-липопротеин |
| Релаксин |
| Фактор роста фибробластов 1 |
| Фактор роста фибробластов 2 |
| Паппализин-1 |
| Белок реакции на стресс 27 (SRP-27) |
| СА-125 |
| Бета-эндорфин |
| Лей- энкефалин |
| Диаминооксидаза |
| Тканевой активатор плазминогена |
| Ренин |
| Прогестерон-зависимая карбоангидраза |
| Лактоферрин |
Трансформируется не только слизистая оболочка матки, но и секрет из ее желез . Это изменение вызвано повышенным уровнем прогестерона в желтом теле . Мишенью секрета является эмбриобласт, который выполняет несколько функций.
Питание
[ редактировать ]Перед имплантацией эмбрион проводит в полости матки около 72 часов. В это время он не может получать питание непосредственно из крови матери и должен полагаться на питательные вещества, секретируемые в полость матки, например железо и жирорастворимые витамины. [30]
Рост и имплантация
[ редактировать ]Помимо питания, эндометрий секретирует несколько стероидозависимых белков, важных для роста и имплантации. холестерин и стероиды. Также секретируются [30] Имплантации дополнительно способствует синтез матриксных веществ, молекул адгезии и поверхностных рецепторов матричных веществ.
Клиническое значение
[ редактировать ]Отказ имплантации
[ редактировать ]Размножение у человека не очень эффективно. Лишь около 30% естественных зачатий заканчиваются успешной беременностью. Около 85% неудачных беременностей происходят из-за неудачной имплантации. [49] Считается, что неудача имплантации в двух третях случаев обусловлена недостаточной рецептивностью матки, а в другой трети – проблемами с самим эмбрионом. [50] Большинство процедур ЭКО терпят неудачу из-за неудачной имплантации, что составляет почти половину всех неудачных попыток беременности. [49]
Неадекватная рецептивность матки может быть вызвана аномальной цитокиновой и гормональной передачей сигналов, а также эпигенетическими изменениями . [51] Рецидивирующая неудача имплантации является причиной женского бесплодия . Следовательно, частота наступления беременности может быть повышена за счет оптимизации восприимчивости эндометрия к имплантации. [51] Оценка маркеров имплантации может помочь предсказать исход беременности и выявить скрытый дефицит имплантации. [51] В рамках «Орган на чипе» программы был разработан эндометрий на чипе для моделирования функционирования эндометрия, который мог бы более четко определить причины неудачной имплантации. [52] Органоиды также были разработаны для моделирования эндометрия и его роли в имплантации. [53]
показал, что у женщин с более чем тремя неудачными имплантациями при вспомогательных репродуктивных технологиях Обзор нескольких небольших рандомизированных контролируемых исследований использование дополнительного низкомолекулярного гепарина повышает частоту живорождения примерно на 80%. [54] Поддержка лютеиновой фазы может включать использование прогестерона и хорионического гонадотропина человека (ХГЧ) для повышения шансов на успешную имплантацию. [55]
Дефицит цинка
[ редактировать ]Цинк имеет решающее значение на этапе до зачатия (и успешной беременности), а его дефицит может привести к некомпетентному развитию бластоцисты. После оплодотворения яйцеклетки цинк высвобождается в виде цинковой искры , что способствует изменениям, включающим затвердевание прозрачной оболочки, предотвращающую полиспермию . [56]
Имплантационное кровотечение
[ редактировать ]Кровотечения и кровянистые выделения часто встречаются во время лютеиновой фазы менструального цикла и на ранних стадиях беременности, но не связаны с имплантацией. Имплантационное кровотечение возникает через 7–14 дней после оплодотворения. [57] и представляет собой небольшое количество легких вагинальных кровотечений или кровянистых выделений, которые могут возникнуть на ранних сроках беременности из-за проникновения бластоцисты в слизистую оболочку матки во время имплантации. [58] [59] [60] К 13-му дню место проникновения в эндометрий обычно закрывается фибриновой пробкой , но усиление притока крови в пространство синцитиотрофобласта иногда может вызвать кровотечение в этом месте. [58] Имплантационное кровотечение может сопровождаться такими симптомами, как спазмы, тошнота, болезненность молочных желез и головные боли. [61] Имплантационное кровотечение можно отличить от менструального кровотечения по цвету, свертываемости, силе и продолжительности течения. [62] [63]
См. также
[ редактировать ]- Каннабиноиды
- Эмбриональная диапауза
- Клетки Хофбауэра
- Гомеостатическая способность
- Человеческое перенаселение
- мембрана Райхерта
Ссылки
[ редактировать ]- ^ «Определение имплантации» . www.merriam-webster.com . Проверено 26 апреля 2023 г.
- ^ Нирингиюмукиза Д.Д., Цай Х., Сян В. (май 2018 г.). «Участие простагландина E2 в женской фертильности млекопитающих: овуляция, оплодотворение, развитие эмбриона и ранняя имплантация» . Репродуктивная биология и эндокринология . 16 (1): 43. дои : 10.1186/s12958-018-0359-5 . ПМЦ 5928575 . ПМИД 29716588 .
- ^ Jump up to: а б Уилкокс А.Дж., Хармон К., Дуди К., Вольф Д.П., Адаши Э.Ю. (апрель 2020 г.). «Преимплантационная потеря оплодотворенных человеческих яйцеклеток: оценка ненаблюдаемого» . Репродукция человека . 35 (4): 743–750. дои : 10.1093/humrep/deaa048 . ПМЦ 8287936 . ПМИД 32296829 .
- ^ Jump up to: а б Ян Ю, Чжу Ци, Лю Дж.Л. (ноябрь 2021 г.). «Расшифровка восприимчивости матки мыши к имплантации эмбрионов с разрешением отдельных клеток» . Пролиферация клеток . 54 (11): e13128. дои : 10.1111/cpr.13128 . ПМК 8560620 . ПМИД 34558134 .
- ^ Jump up to: а б с д и Эзечукву ХК, Дия К.А., Шреста Н., Хрицив Д.Х. (сентябрь 2020 г.). «Роль эндоканнабиноидов на ранних сроках беременности: последние достижения и последствия употребления каннабиса». Американский журнал физиологии. Эндокринология и обмен веществ . 319 (3): E557–E561. дои : 10.1152/ajpendo.00210.2020 . ПМИД 32744098 . S2CID 220943305 .
- ^ Маккарроне М., Валенсис Х., Бари М., Лаззарин Н., Романини С., Финацци-Агро А (2000). «Связь между снижением концентрации анандамидгидролазы в лимфоцитах человека и выкидышем». Ланцет . 355 (9212): 1326–9. дои : 10.1016/S0140-6736(00)02115-2 . ПМИД 10776746 . S2CID 39733100 .
- ^ Деннеди MC, Фрил AM, Хулихан Д.Д., Бродерик В.М., Смит Т., Моррисон Дж.Дж. (январь 2004 г.). «Каннабиноиды и матка человека во время беременности» (PDF) . Американский журнал акушерства и гинекологии . 190 (1): 2–9, обсуждение 3А. дои : 10.1016/j.ajog.2003.07.013 . ПМИД 14749627 .
- ^ Jump up to: а б с Имакава К., Бай Р., Фудзивара Х., Кусама К. (январь 2016 г.). «Имплантация концепции и плацентация: молекулы, связанные с эпителиально-мезенхимальным переходом, возвращением лимфоцитов, эндогенными ретровирусами и экзосомами» . Репродуктивная медицина и биология . 15 (1): 1–11. дои : 10.1007/s12522-015-0215-7 . ПМЦ 5715838 . ПМИД 29259417 .
- ^ Jump up to: а б с д и Ким С.М., Ким Дж.С. (декабрь 2017 г.). «Обзор механизмов имплантации» . Развитие и воспроизводство . 21 (4): 351–359. дои : 10.12717/DR.2017.21.4.351 . ПМК 5769129 . ПМИД 29359200 .
- ^ Jump up to: а б Макгоуэн М.Р., Эрез О., Ромеро Р., Уайлдман Д.Э. (2014). «Эволюция имплантации эмбрионов» . Международный журнал биологии развития . 58 (2–4): 155–161. doi : 10.1387/ijdb.140020dw . ПМК 6053685 . ПМИД 25023681 .
- ^ Jump up to: а б Мур КЛ (2020). Развивающийся человек: клинически ориентированная эмбриология (Одиннадцатое изд.). Эдинбург. стр. 35–42. ISBN 978-0-323-61154-1 .
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) - ^ Чакмак Х., Тейлор Х.С. (март 2011 г.). «Отказ имплантации: молекулярные механизмы и клиническое лечение» . Обновление репродукции человека . 17 (2): 242–253. дои : 10.1093/humupd/dmq037 . ПМК 3039220 . ПМИД 20729534 .
- ^ Jump up to: а б Очоа-Бернал, Массачусетс, Фазлеабас А.Т. (март 2020 г.). «Физиологические события имплантации и децидуализации эмбрионов у человека и нечеловеческих приматов» . Международный журнал молекулярных наук . 21 (6): 1973. doi : 10.3390/ijms21061973 . ПМЦ 7139778 . ПМИД 32183093 .
- ^ Jump up to: а б Гаустер М., Мозер Г., Верницниг С., Куппер Н., Хупперц Б. (июнь 2022 г.). «Раннее развитие трофобласта человека: от морфологии к функции» . Клеточные и молекулярные науки о жизни . 79 (6): 345. дои : 10.1007/s00018-022-04377-0 . ПМЦ 9167809 . ПМИД 35661923 .
- ^ Сэдлер Т.В. (2010). Медицинская эмбриология Лангмана (11-е изд.). Филадельфия: Липпинкотт Уильям и Уилкинс. п. 45. ИСБН 978-0-7817-9069-7 .
- ^ Бор 2004 , с. 1172.
- ^ Jump up to: а б с Сешагири П.Б., Вани В., Мадулика П. (март 2016 г.). «Цитокины и вылупление бластоцист» . Американский журнал репродуктивной иммунологии . 75 (3): 208–17. дои : 10.1111/aji.12464 . ПМИД 26706391 . S2CID 11540123 .
- ^ ЭКО-бесплодие.com
- ^ Сингх Х, Аплин, доктор медицинских наук (июль 2009 г.). «Молекулы адгезии в эпителии эндометрия: целостность ткани и имплантация эмбриона» . Журнал анатомии . 215 (1): 3–13. дои : 10.1111/j.1469-7580.2008.01034.x . ПМЦ 2714633 . ПМИД 19453302 .
- ^ Гипсон И.К., Блэлок Т., Тисдейл А., Сперр-Мишо С., Олкорн С., Ставреус-Эверс А. и др. (январь 2008 г.). «MUC16 теряется с поверхности утеродома (пинопода) восприимчивого эндометрия человека: доказательства in vitro, что MUC16 является барьером для присоединения трофобласта» . Биология размножения . 78 (1): 134–142. дои : 10.1095/biolreprod.106.058347 . ПМИД 17942799 . S2CID 44999196 .
- ^ Jump up to: а б Маргарит Л., Тейлор А., Робертс М.Х., Хопкинс Л., Дэвис С., Брентон А.Г. и др. (декабрь 2010 г.). «MUC1 как дискриминатор между эндометрием фертильных и бесплодных пациентов с СПКЯ и эндометриозом» . Журнал клинической эндокринологии и метаболизма . 95 (12): 5320–5329. дои : 10.1210/jc.2010-0603 . ПМИД 20826587 .
- ^ Карсон Д.Д., Джулиан Дж., Лесси Б.А., Пракобфол А., Фишер С.Дж. (сентябрь 2006 г.). «MUC1 представляет собой каркас для лигандов селектина в матке человека» . Границы бионауки . 11 (1): 2903–2908. дои : 10.2741/2018 . ПМИД 16720361 .
- ^ Фрэнсис Л.В., Яо С.Н., Пауэлл Л.С., Гриффитс С., Беркуанд А., Пьясекки Т. и др. (февраль 2021 г.). «Высоко гликозилированный MUC1 опосредует высокоаффинное связывание L-селектина с поверхностью эндометрия человека» . Журнал нанобиотехнологий . 19 (1): 50. дои : 10.1186/s12951-021-00793-9 . ПМЦ 7890821 . ПМИД 33596915 .
- ^ Генбацев О.Д., Пракобфол А., Фулк Р.А., Кртолица А.Р., Илич Д., Сингер М.С. и др. (январь 2003 г.). «Опосредованная трофобластом L-селектином адгезия на границе раздела мать-плод». Наука . 299 (5605): 405–408. Бибкод : 2003Sci...299..405G . дои : 10.1126/science.1079546 . ПМИД 12532021 . S2CID 15462671 .
- ^ Чжу Цзюй, Пан ЗДжей, Юй Юй (2012). «Регуляция инвазии трофобласта: роль матриксных металлопротеиназ» . Обзоры по акушерству и гинекологии . 5 (3–4): с137–е143. ПМЦ 3594863 . ПМИД 23483768 .
- ^ Картер А.М., Эндерс А.К., Пейненборг Р. (март 2015 г.). «Роль инвазивного трофобласта в имплантации и плацентации приматов» . Философские труды Лондонского королевского общества. Серия Б, Биологические науки . 370 : 20140070.doi : (1663 ) 10.1098/rstb.2014.0070 . ПМК 4305171 . ПМИД 25602074 .
- ^ Jump up to: а б Заре Ф., Сейфати С.М., Дехган-Маншади М., Фесахат Ф. (май 2020 г.). «Преимплантационный фактор (PIF): пептид с различными функциями» . JBRA Assist Репродукция . 24 (2): 214–218. дои : 10.5935/1518-0557.20190082 . ПМК 7169918 . ПМИД 32202400 .
- ^ Гардинер С., Таннетта Д.С., Симмс К.А., Харрисон П., Редман К.В., Сарджент Иллинойс (2011). «Микровезикулы синцитиотрофобластов, высвободившиеся из плаценты при преэклампсии, демонстрируют повышенную активность тканевого фактора» . ПЛОС ОДИН . 6 (10): e26313. Бибкод : 2011PLoSO...626313G . дои : 10.1371/journal.pone.0026313 . ПМК 3194796 . ПМИД 22022598 .
- ^ Циндрова-Дэвис Т., Сферруцци-Перри А.Н. (1 ноября 2022 г.). «Развитие и функция плаценты человека» . Семинары по клеточной биологии и биологии развития . 131 : 66–77. дои : 10.1016/j.semcdb.2022.03.039 . ПМИД 35393235 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п д р с т в Бор В. , Булпап Э. (2004). Медицинская физиология: клеточный и молекулярный подход . Оксфорд : Эльзевир . ISBN 1-4160-2328-3 . OCLC 61527528 . [ нужна страница ]
- ^ Мозер Г., Вайс Г., Сундл М., Гаустер М., Сиветц М., Ланг-Олип И. и др. (март 2017 г.). «Экстраворсинчатые трофобласты проникают не только в маточные артерии: свидетельства инвазии в маточные вены» . Гистохимия и клеточная биология . 147 (3): 353–366. дои : 10.1007/s00418-016-1509-5 . ПМЦ 5344955 . ПМИД 27774579 .
- ^ Дове Г.С., Тан XW, Сяо ZC (январь 2007 г.). «Миграция клеток от ребенка к матери» . Адгезия и миграция клеток . 1 (1): 19–27. дои : 10.4161/cam.4082 . ПМЦ 2633676 . ПМИД 19262088 .
- ^ Jump up to: а б с Хеннес А., Девро Дж., Де Клерк К., Чиприетти М., Хелд К., Луйтен К. и др. (апрель 2023 г.). «Секреция протеазы вторгающейся бластоцистой вызывает колебания кальция в эпителиальных клетках эндометрия через активируемый протеазой рецептор 2» . Репрод Биол Эндокринол . 21 (1): 37. дои : 10.1186/s12958-023-01085-7 . ПМЦ 10105462 . ПМИД 37060079 .
- ^ Мерфи CR (август 2004 г.). «Восприимчивость матки и трансформация плазматической мембраны» . Клеточные исследования . 14 (4): 259–267. дои : 10.1038/sj.cr.7290227 . ПМИД 15353123 . S2CID 24023502 .
- ^ Мерфи CR, Шоу TJ (декабрь 1994 г.). «Трансформация плазматической мембраны: общий ответ эпителиальных клеток матки в периимплантационный период». Международная клеточная биология . 18 (12): 1115–1128. дои : 10.1006/cbir.1994.1038 . ПМИД 7703952 . S2CID 22769575 .
- ^ Тех В.Т., Макбейн Дж., Роджерс П. (ноябрь 2016 г.). «Каков вклад асинхронности эмбриона и эндометрия в неудачу имплантации?» . Журнал вспомогательной репродукции и генетики . 33 (11): 1419–1430. дои : 10.1007/s10815-016-0773-6 . ПМК 5125144 . ПМИД 27480540 .
- ^ Штернберг А.К., Бак В.Ю., Классен-Линке И., Леубе Р.Е. (август 2021 г.). «Как механические силы изменяют эндометрий человека во время менструального цикла при подготовке к имплантации эмбриона» . Клетки . 10 (8): 2008. doi : 10.3390/cells10082008 . ПМЦ 8391722 . ПМИД 34440776 .
- ^ У ХМ, Чен Л.Х., Сюй Л.Т., Лай Ч.Х. (ноябрь 2022 г.). «Иммунная толерантность к имплантации эмбриона и беременности: роль внеклеточных везикул децидуального стромального и эмбрионального происхождения человека» . Int J Mol Sci . 23 (21): 13382. doi : 10.3390/ijms232113382 . ПМЦ 9658721 . ПМИД 36362169 .
- ^ Лян Дж., Ван С., Ван З. (ноябрь 2017 г.). «Роль микроРНК в имплантации эмбриона» . Репрод Биол Эндокринол . 15 (1): 90. дои : 10.1186/s12958-017-0309-7 . ПМК 5699189 . ПМИД 29162091 .
- ^ Маккарроне М., Валенсис Х., Бари М., Лаззарин Н., Романини С., Финацци-Агро А (2000). «Связь между снижением концентрации анандамидгидролазы в лимфоцитах человека и выкидышем». Ланцет . 355 (9212): 1326–9. дои : 10.1016/S0140-6736(00)02115-2 . ПМИД 10776746 . S2CID 39733100 .
- ^ Jump up to: а б с д и Куинн К.Э., Мэтсон BC, Ветендорф М., Кэрон К.М. (февраль 2020 г.). «Пиноподы: последние достижения, текущие перспективы и будущие направления» . Молекулярная и клеточная эндокринология . 501 : 110644. doi : 10.1016/j.mce.2019.110644 . ПМК 6962535 . ПМИД 31738970 .
- ^ Сяо Ю, Сунь Х, Ян Х, Чжан Дж, Сюэ Ц, Цай Б и др. (июнь 2010 г.). «Фактор ингибирования лейкемии нарушается в эндометрии и смывной жидкости матки у пациенток с аденомиозом во время окна имплантации» . Фертильность и бесплодие . 94 (1): 85–89. doi : 10.1016/j.fertnstert.2009.03.012 . ПМИД 19361790 .
- ^ Нг СВ, Норвиц Г.А., Павличев М., Тилбургс Т., Симон С., Норвиц Э.Р. (июнь 2020 г.). «Децидуализация эндометрия: основной фактор здоровья беременности» . Int J Mol Sci . 21 (11): 4092. doi : 10.3390/ijms21114092 . ПМК 7312091 . ПМИД 32521725 .
- ^ Крха И., Вентруба П., Жакова Дж., Йешета М., Пилка Р., Лусова Е. и др. (2019). «Микробиом матки и рецептивность эндометрия». Чешская гинекология . 84 (1): 49–54. ПМИД 31213058 .
- ^ Морено И., Коданьер Ф.М., Вилелья Ф., Вальбуэна Д., Мартинес-Бланш Х.Ф., Хименес-Альмазан Х. и др. (декабрь 2016 г.). «Доказательства того, что микробиота эндометрия влияет на успех или неудачу имплантации» . Американский журнал акушерства и гинекологии . 215 (6): 684–703. дои : 10.1016/j.ajog.2016.09.075 . ПМИД 27717732 .
- ^ Jump up to: а б с Чжао Ю, Хэ Д, Цзэн Х, Луо Дж, Ян С, Чен Дж и др. (сентябрь 2021 г.). «Экспрессия и значение миР-30d-5p и SOCS1 у пациентов с рецидивирующей неудачей имплантации во время окна имплантации» . Репрод Биол Эндокринол . 19 (1): 138. дои : 10.1186/s12958-021-00820-2 . ПМЦ 8425163 . ПМИД 34496883 .
- ^ Шарма А., Кумар П. (январь 2012 г.). «Понимание окна имплантации — важнейшего явления» . J Hum Reprod Sci . 5 (1): 2–6. дои : 10.4103/0974-1208.97777 . ПМК 3409914 . ПМИД 22870007 .
- ^ Руан Ю.К., Го Дж.Х., Лю X, Чжан Р., Цанг Л.Л., Донг Дж.Д. и др. (июль 2012 г.). «Активация эпителиального канала Na+ запускает высвобождение и выработку простагландина E₂, необходимого для имплантации эмбриона». Природная медицина . 18 (7): 1112–1117. дои : 10.1038/нм.2771 . ПМИД 22729284 . S2CID 5116022 .
- ^ Jump up to: а б Ван Ю, Цзян Икс, Цзя Л, Ву Икс, Ву Х, Ван Ю и др. (2022). «Одноклеточная характеристика постимплантационных эмбрионов человека, культивированных in vitro, определяет морфогенез при первичной синцитиализации» . Границы клеточной биологии и биологии развития . 10 : 835445. doi : 10.3389/fcell.2022.835445 . ПМЦ 9240912 . ПМИД 35784461 .
- ^ Мелфорд С.Э., Тейлор А.Х., Конье Дж.К. (2013). «О мышах и (женщинах) мужчинах: факторы, влияющие на успешную имплантацию, включая эндоканнабиноиды» . Обновление репродукции человека . 20 (3): 415–428. дои : 10.1093/humupd/dmt060 . ПМИД 24306146 .
- ^ Jump up to: а б с Чакмак Х., Тейлор Х.С. (2010). «Отказ имплантации: молекулярные механизмы и клиническое лечение» . Обновление репродукции человека . 17 (2): 242–253. дои : 10.1093/humupd/dmq037 . ПМК 3039220 . ПМИД 20729534 .
- ^ Ан Дж., Юн М.Дж., Хонг Ш., Ча Х., Ли Д., Ку Х.С. и др. (сентябрь 2021 г.). «Трехмерный микроинженерный васкуляризированный эндометрий на чипе» . Репродукция человека . 36 (10): 2720–2731. дои : 10.1093/humrep/deab186 . ПМЦ 8450871 . ПМИД 34363466 .
- ^ Роулингс Т.М., Маквана К., Трифонос М., Лукас Э.С. (июль 2021 г.). «Органоиды для моделирования эндометрия: имплантация и не только» . Репродукция Fertil . 2 (3): Р85–Р101. дои : 10.1530/RAF-21-0023 . ПМК 8801025 . ПМИД 35118399 .
- ^ Потдар Н., Гелбая Т.А., Конье Дж.К., Нардо Л.Г. (2013). «Дополнительный низкомолекулярный гепарин для повышения частоты живорождения после повторной неудачной имплантации: систематический обзор и метаанализ» . Обновление репродукции человека . 19 (6): 674–684. дои : 10.1093/humupd/dmt032 . ПМИД 23912476 .
- ^ Фаркуар С., Марджорибанкс Дж. (август 2018 г.). «Вспомогательные репродуктивные технологии: обзор Кокрейновских обзоров» . Кокрановская база данных систематических обзоров . 2018 (8): CD010537. дои : 10.1002/14651858.CD010537.pub5 . ПМЦ 6953328 . ПМИД 30117155 .
- ^ Гарнер Т.Б., Хестер Дж.М., Карозерс А., Диас Ф.Дж. (май 2021 г.). «Роль цинка в женской репродукции» . Биология размножения . 104 (5): 976–994. doi : 10.1093/biolre/ioab023 . ПМЦ 8599883 . ПМИД 33598687 .
- ^ «Имплантационное кровотечение и менструация: как отличить» . Воссоединить Rx . 09.12.2020 . Проверено 29 июля 2021 г.
- ^ Jump up to: а б Сэдлер Т.В. (2010). Медицинская эмбриология Лангмана (11-е изд.). Филадельфия: Липпинкотт Уильям и Уилкинс. стр. 50–51. ISBN 978-0-7817-9069-7 .
- ^ Шейнер Э (2011). Кровотечение во время беременности: подробное руководство . Нью-Йорк: Спрингер. п. 9. ISBN 978-1-4419-9810-1 .
- ^ Харвилл Э.В. , Уилкокс А.Дж., Бэрд Д.Д., Вайнберг Ч.Р. (сентябрь 2003 г.). «Вагинальное кровотечение на очень ранних сроках беременности» . Репродукция человека . 18 (9): 1944–1947. дои : 10.1093/humrep/deg379 . ПМИД 12923154 .
- ^ Хегер, Л. Демосфен Э (ред.). «Как ощущаются спазмы при имплантации? Как отличить имплантацию от менструальных спазмов» . Инсайдер . Проверено 29 июля 2021 г.
- ^ Аггарвал К. (2020). «Вагинальное кровотечение на ранних сроках беременности». В Шарме А (ред.). Чрезвычайные ситуации в родильном зале . Сингапур: Спрингер. стр. 155–161. дои : 10.1007/978-981-10-4953-8_18 . ISBN 978-981-10-4953-8 . S2CID 212812977 .
- ^ «Как узнать, что это имплантационное кровотечение?» . МедицинаНет . Проверено 29 июля 2021 г.
Книги
[ редактировать ]- Бор В. , Булпап Э. (2004). Медицинская физиология: клеточный и молекулярный подход . Оксфорд : Эльзевир . ISBN 1-4160-2328-3 . OCLC 61527528 .