Талассемия
| Талассемия | |
|---|---|
| Другие имена | Талассемия, средиземноморская анемия |
 | |
| Мазок периферической крови человека с дельта-бета-талассемией. | |
| Произношение | |
| Специальность | Гематология |
| Симптомы | Чувство усталости , бледная кожа , увеличенная селезенка , желтоватая кожа , темная моча. [1] |
| Причины | Генетический ( аутосомно-рецессивный ) [2] |
| Метод диагностики | Анализы крови, генетические тесты [3] |
| Уход | Переливание крови , хелатирование железа , фолиевая кислота. [4] |
| Частота | 280 миллионов (2015) [5] |
| Летальные исходы | 16,800 (2015) [6] |
Талассемия — это наследственное заболевание крови , которое приводит к аномальному гемоглобину . [7] Симптомы зависят от типа талассемии и могут варьироваться от отсутствия до тяжелых. [1] Часто наблюдается анемия от легкой до тяжелой степени (низкий уровень эритроцитов или гемоглобина), поскольку талассемия может влиять на выработку эритроцитов, а также на продолжительность жизни эритроцитов. [1] Симптомы анемии включают чувство усталости и бледность кожи . [1] Другие симптомы талассемии включают проблемы с костями, увеличение селезенки , желтоватую кожу , легочную гипертензию и темную мочу. [1] У детей может наблюдаться медленный рост. [1] Симптомы и проявления талассемии могут со временем меняться. Более старые термины включали анемию Кули и средиземноморскую анемию при бета-талассемии. Они были заменены терминами «трансфузионно-зависимая талассемия» (TDT) и «нетрансфузионно-зависимая талассемия» (NTDT). Пациентам с ТДТ требуются регулярные переливания крови, обычно каждые две-пять недель. TDT включают большую бета-талассемию, неделеционную болезнь HbH, выжившую болезнь Hb-Барта и тяжелую HbE/бета-талассемию. [8]
Талассемия является генетическим заболеванием . [2] Существует два основных типа: альфа-талассемия и бета-талассемия . [7] Тяжесть альфа- и бета-талассемии зависит от того, сколько из четырех генов альфа-глобина или двух генов бета-глобина отсутствует. [2] Диагноз обычно ставится на основе анализов крови, включая общий анализ крови , специальные тесты на гемоглобин и генетические тесты. [3] Диагноз может быть поставлен до рождения посредством пренатального тестирования . [9]
Лечение зависит от типа и степени тяжести. [4] Лечение людей с более тяжелым заболеванием часто включает регулярное переливание крови , хелатирование железа и фолиевую кислоту . [4] Хелатирование железа можно проводить с помощью дефероксамина , деферазирокса или деферипрона . [4] [10] Иногда трансплантация костного мозга . вариантом может быть [4] Осложнения могут включать перегрузку железом в результате переливания крови, приводящую к заболеваниям сердца или печени , инфекциям и остеопорозу . [1] Если селезенка чрезмерно увеличивается, хирургическое удаление . может потребоваться [1] Пациенты с талассемией, которые плохо реагируют на переливание крови, могут принимать гидроксимочевину или талидомид , а иногда и их комбинацию. [11] Гидроксимочевина — единственный препарат, одобренный FDA для лечения талассемии. Пациенты, принимавшие гидроксимочевину в дозе 10 мг/кг каждый день в течение года, имели значительно более высокий уровень гемоглобина, и это лечение хорошо переносилось пациентами, которые плохо реагировали на переливание крови. [12] Другие известные индукторы гемоглобина включают талидомид, но он не тестировался в клинических условиях. Комбинация талидомида и гидроксимочевины привела к значительному повышению уровня гемоглобина у трансфузионно-зависимых и нетрансфузионно-зависимых пациентов. [13]
По состоянию на 2015 год талассемия встречается примерно у 280 миллионов человек, из которых около 439 000 страдают тяжелым заболеванием. [14] Это наиболее распространено среди людей греческого , итальянского , ближневосточного , южноазиатского и африканского происхождения. [7] Мужчины и женщины имеют одинаковые показатели заболеваемости. [ нужна ссылка ] В 2015 году это привело к 16 800 смертям по сравнению с 36 000 смертей в 1990 году. [6] [15] Те, у кого есть легкая степень талассемии, как и те, у кого есть серповидноклеточный признак , имеют некоторую защиту от малярии , что объясняет, почему серповидноклеточный признак и талассемия чаще встречаются в регионах мира, где риск малярии выше. [16] По оценкам, 1/3 людей с талассемией страдают «независимой от переливания крови талассемией», и их выживание не зависит от регулярного продолжения переливания крови.
Признаки и симптомы
[ редактировать ]

- Перегрузка железом . Люди с талассемией могут получить перегрузку железа в организме либо из-за самой болезни, либо из-за частых переливаний крови. Слишком много железа может привести к повреждению сердца, печени и эндокринной системы , в том числе желез, вырабатывающих гормоны, регулирующие процессы во всем организме. Повреждение характеризуется чрезмерными отложениями железа. Без адекватной терапии хелаторами железа почти у всех пациентов с бета-талассемией накапливаются потенциально смертельные уровни железа. [17]
- Инфекция. Люди с талассемией имеют повышенный риск заражения. Это особенно актуально, если селезенка была удалена. [18]
- Деформации костей. Талассемия может привести к расширению костного мозга, что приводит к расширению костей. Это может привести к нарушению структуры костей, особенно лица и черепа. Расширение костного мозга также делает кости тонкими и ломкими, что увеличивает риск переломов костей. [19]
- Увеличенная селезенка . Селезенка помогает бороться с инфекцией и фильтрует нежелательный материал, например, старые или поврежденные клетки крови. Талассемия часто сопровождается разрушением большого количества эритроцитов, и задача удаления этих клеток приводит к увеличению селезенки. Спленомегалия может усугубить анемию и сократить жизнь перелитых эритроцитов. Сильное увеличение селезенки может потребовать ее удаления. [20]
- Замедление темпов роста: анемия может привести к замедлению роста ребенка. Половое созревание также может быть задержано у детей с талассемией. [21]
- Проблемы с сердцем: такие заболевания, как застойная сердечная недостаточность и нарушения сердечного ритма, могут быть связаны с тяжелой талассемией. [22]
Структурная биология гемоглобина
[ редактировать ]Нормальные гемоглобины человека представляют собой тетрамерные белки, состоящие из двух пар цепей глобина, каждая из которых содержит одну альфа-подобную (α-подобную) цепь и одну бета-подобную (β-подобную) цепь. Каждая цепь глобина связана с железосодержащим фрагментом гема. В течение жизни синтез альфа-подобных и бета-подобных (также называемых неальфа-подобными) цепей сбалансирован, так что их соотношение относительно постоянно и не происходит избытка того или иного типа. [23]
Специфические альфа- и бета-подобные цепи, входящие в состав гемоглобина, строго регулируются во время развития:
- Эмбриональные гемоглобины экспрессируются уже на четвертой-шестой неделе эмбриогенеза и исчезают примерно на восьмой неделе беременности, когда они замещаются фетальным гемоглобином. [24] [25] Эмбриональные Hbs включают:
- Hb Gower-1, состоящий из двух ζ-глобинов (дзета-глобинов) и двух ε-глобинов (эпсилон-глобинов) (ζ2ε2)
- Hb Gower-2, состоящий из двух альфа-глобинов и двух эпсилон-глобинов (α2ε2).
- Hb Portland I, состоящий из двух зета-глобинов и двух гамма-глобинов (ζ2γ2).
- Hb Portland II, состоящий из двух зета-глобинов и двух бета-глобинов (ζ2β2).
- Фетальный гемоглобин (Hb F) вырабатывается примерно с восьми недель беременности до рождения и составляет примерно 80 процентов гемоглобина у доношенного новорожденного. Он снижается в течение первых нескольких месяцев жизни и в нормальном состоянии составляет <1 процента от общего уровня гемоглобина в раннем детстве и после него. Hb F состоит из двух альфа-глобинов и двух гамма-глобинов (α2γ2). У пациентов с β-талассемией наблюдаются более высокие уровни гамма-глобулина и, следовательно, большее производство Hb F, чтобы противодействовать дисбалансу, связанному с неспособностью производить бета-цепи. [26]
- Взрослый Hb ( Hb A ) вырабатывается в низких уровнях в течение эмбриональной и внутриутробной жизни и является преобладающим гемоглобином у детей в возрасте шести месяцев и старше; он составляет 96-97% от общего гемоглобина у лиц без гемоглобинопатии. Он состоит из двух альфа-глобинов и двух бета-глобинов (α2β2). [ нужна ссылка ]
- Hb A2 представляет собой второстепенный уровень Hb у взрослых, который обычно составляет примерно 2,5–3,5% от общего уровня Hb, начиная с шестимесячного возраста. Он состоит из двух альфа-глобинов и двух дельта-глобинов (α2δ2). [ нужна ссылка ]
Причина
[ редактировать ]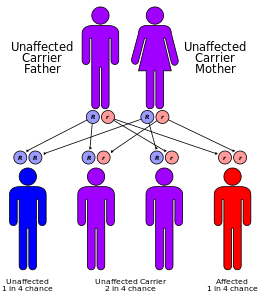
Как α-, так и β-талассемия часто наследуются по аутосомно- рецессивному типу. случаях доминантно Сообщалось о наследуемых α- и β-талассемий, первый из которых произошел в ирландской семье с двумя делециями 4 и 11 п.н. в экзоне 3, прерванными вставкой 5 п.н. в гене β-глобина. При аутосомно-рецессивных формах заболевания оба родителя должны быть носителями, чтобы ребенок мог заболеть. Если оба родителя являются носителями признаков гемоглобинопатии, риск составляет 25% для каждой беременности у больного ребенка. [27]
Гены, участвующие в талассемии, контролируют выработку здорового гемоглобина. Гемоглобин связывает кислород в легких и высвобождает его, когда эритроциты достигают периферических тканей, таких как печень. Связывание и высвобождение кислорода гемоглобином необходимы для выживания. [ нужна ссылка ]
Эволюция
[ редактировать ]Наличие единственного генетического варианта талассемии может защитить от малярии и, таким образом, может быть преимуществом. [28]
Люди с диагнозом гетерозиготной (носительницы) β-талассемии имеют некоторую защиту от ишемической болезни сердца . [29]
Патофизиология
[ редактировать ]В норме большая часть взрослого гемоглобина ( HbA ) состоит из четырех белковых цепей, двух α- и двух β-цепей глобина, образующих гетеротетрамер . При талассемии у пациентов наблюдаются дефекты в некодирующей области генов альфа- или бета-глобина, вызывающие неэффективное производство нормальных цепей альфа- или бета-глобина, что может привести к неэффективному эритропоэзу, преждевременному разрушению эритроцитов и анемии. [8]
Талассемии классифицируют в зависимости от того, какая цепь молекулы гемоглобина поражена. При α-талассемиях нарушается выработка цепи α-глобина, тогда как при β-талассемии нарушается выработка цепи β-глобина. [30]
Цепи β-глобина кодируются одним геном на хромосоме 11 ; Цепи α-глобина кодируются двумя тесно связанными генами на хромосоме 16 . [31] Таким образом, у здорового человека, имеющего две копии каждой хромосомы, два локуса кодируют β-цепь, а четыре локуса кодируют α-цепь. Делеция одного из α-локусов широко распространена у людей африканского или азиатского происхождения, что повышает вероятность развития α-талассемии. β-талассемия распространена не только у африканцев , но также у греков и турок . [ нужна ссылка ]
Альфа-талассемия
[ редактировать ]В α-талассемии участвуют гены HBA1. [32] и HBA2 , [33] наследуется по менделевскому рецессивному типу. Существует два генных локуса и, следовательно, четыре аллели. Для α-глобина существуют два генетических локуса, таким образом, в диплоидных клетках присутствуют четыре аллеля. Два аллеля имеют материнское происхождение, а два аллеля — отцовское. Тяжесть α-талассемий коррелирует с количеством пораженного α-глобина; аллели: чем больше, тем тяжелее будут проявления заболевания. [34] Альфа-талассемия приводит к снижению выработки альфа-глобина; следовательно, образуется меньше цепей альфа-глобина, что приводит к избытку β-цепей у взрослых и избытку γ-цепей у новорожденных. Избыточные β-цепи образуют нестабильные тетрамеры (называемые гемоглобином H или HbH из 4 бета-цепей), которые имеют аномальные кривые диссоциации кислорода. Альфа-талассемия часто встречается у людей из Юго-Восточной Азии, Ближнего Востока, Китая и у лиц африканского происхождения. [35]
| # недостающих аллелей | Виды альфа-талассемии [34] | Симптомы |
|---|---|---|
| 1 | Тихий носитель | Никаких симптомов |
| 2 | Признак альфа-талассемии | Незначительная анемия |
| 3 | Болезнь гемоглобина H | Легкая и умеренная анемия; может вести нормальную жизнь |
| 4 | Водянка плода | Смерть обычно наступает внутриутробно или при рождении. |
Бета-талассемия
[ редактировать ]Бета-талассемия возникает из-за мутаций гена HBB на хромосоме 11. [36] также наследуется по аутосомно-рецессивному типу. Тяжесть заболевания зависит от характера мутации и наличия мутаций в одном или обоих аллелях.
Мутировавшие аллели называются β. + когда частичная функция сохранена (либо белок имеет сниженную функцию, либо он функционирует нормально, но производится в уменьшенном количестве) или β тот , когда не вырабатывается функционирующий белок.
Положение обоих аллелей определяет клиническую картину:
- Большая β-талассемия ( средиземноморская анемия или анемия Кули ) вызывается β- талассемией. тот /б тот генотип. Функциональные β-цепи не образуются, и, следовательно, гемоглобин А не может быть собран. Это наиболее тяжелая форма β-талассемии;
- Промежуточная β-талассемия вызывается β + /б тот или β + /б + генотип. В этой форме вырабатывается некоторое количество гемоглобина А;
- Малая β-талассемия вызывается β/β тот или β/β + генотип. Только один из двух аллелей β-глобина содержит мутацию, поэтому выработка β-цепи не сильно нарушена, и пациенты могут протекать относительно бессимптомно.
Бета-талассемия чаще всего встречается у людей средиземноморского происхождения. В меньшей степени могут пострадать китайцы, другие азиаты и афроамериканцы. [35]
Дельта-талассемия
[ редактировать ]Помимо альфа- и бета-цепей, присутствующих в гемоглобине, около 3% гемоглобина взрослого человека состоит из альфа- и дельта-цепей. Как и в случае с бета-талассемией, могут возникать мутации, влияющие на способность этого гена производить дельта-цепи. [37] [38]
Комбинированные гемоглобинопатии
[ редактировать ]Талассемия может сосуществовать с другими гемоглобинопатиями . Наиболее распространенными из них являются:
- Гемоглобин Е /талассемия: распространен в Камбодже , Таиланде и некоторых частях Индии , клинически подобен большой β-талассемии или промежуточной талассемии. [ нужна ссылка ]
- Гемоглобин S /талассемия: распространена среди населения Африки и Средиземноморья , клинически похожа на серповидноклеточную анемию с дополнительным признаком спленомегалии . [ нужна ссылка ]
- Гемоглобин C /талассемия: распространен в средиземноморском и африканском населении, гемоглобин C/β. тот талассемия вызывает умеренно тяжелую гемолитическую анемию со спленомегалией; гемоглобин C/β + талассемия вызывает более легкое заболевание. [ нужна ссылка ]
- Гемоглобин D /талассемия: распространена в северо-западной части Индии и Пакистана ( регион Пенджаб ). [39]
Диагностика
[ редактировать ]Талассемию можно диагностировать с помощью общего анализа крови , электрофореза гемоглобина или высокоэффективной жидкостной хроматографии , а также анализа ДНК. [40] [41] Электрофорез гемоглобина не широко доступен в развивающихся странах, но индекс Ментцера также можно использовать для диагностики талассемии; это не окончательный тест, но он может указывать на возможность талассемии. Индекс Ментцера можно рассчитать на основании общего анализа крови . [42]
Эндокринные осложнения при талассемии
1) Гипогонадизм: перегрузка железом в гонадотропных клетках гипофиза вызывает снижение секреции гонадотропинов, что приводит к задержке, замедлению или остановке полового созревания.
2) Гипопаратиреоз: хроническая анемия вызывает нарушение кроветворения, что приводит к реабсорбции кости, что снижает секрецию паращитовидной железы.
3) Надпочечниковая недостаточность: снижение роста лобковых и подмышечных волос у подростков-пациентов ТМ. Это происходит из-за избыточного отложения железа, которое вызывает дисфункцию надпочечников.
4) Гипотиреоз: увеличение веса и задержка роста у подростков. Вторичный гипотиреоз встречается редко, и большинство страдает от первичного гипотиреоза.
Управление
[ редактировать ]Учитывая диапазон тяжести заболевания, некоторые люди не нуждаются в лечении (те, у кого нет симптомов), в то время как некоторым для выживания требуется регулярное переливание крови. [43] Людям с тяжелой формой талассемии требуется медицинское лечение, и основным лечением обычно является переливание эритроцитов.
Переливание эритроцитов
[ редактировать ]Переливание крови является основным методом лечения, позволяющим продлить жизнь. [44] Необходимый подход и частота варьируются у каждого человека в зависимости от тяжести заболевания, возраста, задержки роста, наличия экстрамедуллярного эритропоэза (педиатрия), беременности и состояния сердца. Переливание крови сопряжено с рисками, включая усугубление перегрузки железом, риск инфекций, риск образования антител к эритроцитам, повышенный риск развития реакций гиперчувствительности и риск воспаления желчного пузыря ( холецистита ). [43]
Многократные переливания крови могут привести к перегрузке железом. Перегрузку железом, связанную с талассемией, можно лечить с помощью хелаторной терапии с использованием препаратов дефероксамина , деферипрона или деферазирокса . [45] [46] [47] Эти методы лечения привели к увеличению продолжительности жизни людей с большой талассемией. [45] Дефероксамин эффективен только при ежедневной инъекции, что усложняет его длительное применение. Однако это недорого и безопасно. Побочные эффекты включают первичные кожные реакции вокруг места инъекции и потерю слуха . [45] Деферазирокс и деферипрон являются пероральными препаратами, общие побочные эффекты которых включают тошноту, рвоту и диарею. При сравнении эффективности нет доказательств превосходства деферазирокса или деферипрона, однако долгосрочное сравнение не проводилось. [47] Деферасирокс не эффективен для всех пациентов и может не подойти тем, у кого серьезные проблемы с сердцем, связанные с перегрузкой железом, в то время как деферипрон, по-видимому, является наиболее эффективным средством при поражении сердца. Кроме того, стоимость деферазирокса также значительна. [45] Сочетание блокаторов кальциевых каналов с терапией хелатирования железа находится в стадии изучения, однако польза от проведенных клинических испытаний не очевидна. [48]
Терапия гормоном роста
[ редактировать ]Есть некоторые доказательства того, что заместительная терапия гормоном роста может помочь увеличить скорость роста детей с талассемией. [49]
Трансплантация костного мозга
[ редактировать ]Трансплантация костного мозга может дать возможность излечения молодых людей, имеющих HLA -совместимого донора. [50] Показатели успеха достигли диапазона 80–90%. [50] Смертность от процедуры составляет около 3%. [51] Рандомизированных контролируемых исследований, в которых проверялась бы безопасность и эффективность трансплантации костного мозга неидентичных доноров у лиц с β-талассемией, зависимых от переливания крови, не проводилось. [52]
Болезни «трансплантат против хозяина» (РТПХ) являются одним из важных побочных эффектов трансплантации костного мозга. Необходимы дальнейшие исследования, чтобы оценить, можно ли использовать мезенхимальные стромальные клетки в качестве профилактики или лечения РТПХ. [53]
Если у человека нет совместимого по HLA донора, можно попытаться провести трансплантацию костного мозга от гаплоидентичной матери ребенку (несовместимому донору). В исследовании с участием 31 человека выживаемость без талассемии составила 70%, отторжение — 23%, а смертность — 7%. Наиболее положительные результаты обычно наблюдаются у очень молодых людей. [54]
Генная терапия
[ редактировать ]Betibeglogene autotemcel , продаваемый под торговой маркой Zynteglo, представляет собой генную терапию для лечения бета-талассемии. [55] Он был одобрен для медицинского использования в Европейском Союзе в мае 2019 года. [56] и в США в августе 2022 года. [57] [58] Бетибеглоген аутотемцел показан для лечения людей двенадцати лет и старше с трансфузионно-зависимой бета-талассемией, у которых нет генотипа β0/β0, для которых подходит трансплантация гемопоэтических стволовых клеток (HSC), но соответствующий человеческий лейкоцитарный антиген (HLA). родственный донор HSC недоступен.
Процедура включает сбор гемопоэтических стволовых клеток (ГСК) из крови больного. Затем к ЗКП добавляют ген бета-глобина с использованием лентивирусного вектора . После разрушения костного мозга больного человека дозой химиотерапии (режим миелоаблативного кондиционирования) измененные ЗКП вводятся обратно в организм больного, где они приживляются в костном мозге и размножаются. Это потенциально приводит к постепенному увеличению синтеза гемоглобина А2 во всех последующих развивающихся эритроцитах, что приводит к разрешению анемии. [59]
Индукция HbF
[ редактировать ]Exagamglogene autotemcel , продаваемый под торговой маркой Casgevy, представляет собой генную терапию для лечения трансфузионно-зависимой бета-талассемии . Его разработали Vertex Pharmaceuticals и CRISPR Therapeutics . [60]
В ноябре 2023 года препарат был одобрен в Великобритании для лечения трансфузионно-зависимой бета-талассемии. [61] [62] [63] и в США в январе 2024 года. [64] [65] [66]
Exagamglogene autotemcel — это первый метод клеточной генной терапии с использованием технологии редактирования генов CRISPR/Cas9, одобренный Управлением по контролю за продуктами и лекарствами США (FDA). [64]
Генная терапия производится из собственных стволовых клеток крови реципиента, которые модифицируются и передаются обратно в виде однократной инфузии одной дозы в рамках трансплантации гемопоэтических стволовых клеток . Перед лечением собирают собственные стволовые клетки реципиента, а затем реципиент должен пройти миелоаблативное кондиционирование (высокодозную химиотерапию), процесс, который удаляет клетки из костного мозга, чтобы их можно было заменить модифицированными клетками в эксагамглогенном аутотемцеле . Модифицированные стволовые клетки крови трансплантируются обратно реципиенту, где они приживаются в костном мозге и увеличивают выработку фетального гемоглобина (HbF), типа гемоглобина, который облегчает доставку кислорода.
Другие методы лечения
[ редактировать ]Лечение гидроксимочевиной с целью реактивации гамма-генов для производства HbF не имеет доказательств высокого качества, подтверждающих его эффективность. [67]
нет доказательств В результате рандомизированных контролируемых исследований в поддержку приема добавок цинка у больных талассемией. [68] Компьютерные программы или мобильные приложения были предложены в качестве инструментов, помогающих людям управлять талассемией и следовать лечению, включая терапию хелатированием железа. Эффективность этих приложений недостаточно исследована. [69]
Люди с талассемией подвергаются более высокому риску развития остеопороза. [70] Варианты лечения включают бисфосфонаты, а иногда и добавление гормональной терапии. Были предложены другие методы лечения, включая кальцитонин, цинк, гидроксимочевину и добавки кальция. Эффективность бисфосфонатов и цинка не ясна, и необходимы дальнейшие исследования. [70]
Стоматологическая помощь
[ редактировать ]Помощь людям с талассемией в уходе за зубами и лечении стоматологических проблем может быть сложной задачей из-за основного заболевания. Перегрузка железом из-за переливания крови может привести к отложению железа в зубах и изменению их цвета, а также существует повышенный риск заражения. [71] Варианты лечения людей с талассемией необходимо изменить, чтобы обеспечить учет потребностей человека, а также настоятельно рекомендуется раннее выявление и раннее лечение любых проблем, чтобы снизить риск того, что человеку потребуется более сложное стоматологическое лечение. [71] Доказательства, подтверждающие эффективность стоматологического лечения у людей с талассемией, слабы, и необходимы более качественные клинические исследования. [71]
Легкая талассемия
[ редактировать ]Люди с признаками талассемии не нуждаются в медицинской или последующей помощи после постановки первоначального диагноза. [44] Людей с признаком β-талассемии следует предупредить, что их состояние может быть ошибочно принято за более распространенную железодефицитную анемию . Им следует избегать регулярного приема добавок железа , но дефицит железа может развиться во время беременности или в результате хронического кровотечения. [72] Генетическое консультирование показано всем лицам с генетическими нарушениями, особенно если в семье существует риск тяжелой формы заболевания, которую можно предотвратить. [73]
Профилактика
[ редактировать ]Американский колледж акушеров и гинекологов рекомендует всем людям, планирующим беременность, пройти тестирование на наличие талассемии. [74] Генетическое консультирование и генетическое тестирование рекомендуются семьям, имеющим признаки талассемии. [27] Мы надеемся, что понимание генетического риска, в идеале до создания семьи, позволит семьям больше понять об этом заболевании и принять обоснованное решение, которое лучше всего подходит для их семьи. [27]
существует политика скрининга, На Кипре направленная на снижение заболеваемости талассемией, которая с момента реализации программы в 1970-х годах (включая пренатальный скрининг и аборты) сократила количество детей, рожденных с этим заболеванием, с одного из каждых 158 рождений почти до нуля. . [75] В Греции также существует программа скрининга для выявления людей, являющихся носителями. [76]
В Иране в качестве добрачного скрининга сначала проверяются показатели эритроцитов мужчины. Если у него имеется микроцитоз ( средний гемоглобин в клетке < 27 пг или средний объем эритроцитов < 80 мкл), женщину обследуют. Когда оба являются микроцитарными, гемоглобина А2 измеряют концентрацию . Если у обоих концентрация превышает 3,5% (диагностический признак талассемии), их направляют в местный назначенный медицинский пункт для генетического консультирования . [77]
организуются масштабные информационные кампании. В Индии [78] как правительственными, так и неправительственными организациями для содействия добровольному добрачному скринингу, при этом браки между носителями категорически не поощряются.
Эпидемиология
[ редактировать ]Бета-форма талассемии особенно распространена среди народов Средиземноморья , и это географическое объединение дало ей первоначальное название. [79] Талассемия привела к 25 000 смертей в 2013 году по сравнению с 36 000 смертей в 1990 году. [15]
В Европе самые высокие концентрации заболевания наблюдаются в Греции , прибрежных регионах Турции (особенно в Эгейском регионе , таком как Измир , Балыкесир , Айдын , Мугла , и средиземноморском регионе , таком как Анталья , Адана , Мерсин ), на юге Испании, в части Италии , особенно южная Италия . За исключением Балеарских островов крупные средиземноморские острова, такие как Сицилия , Сардиния , Мальта , Корсика , Кипр и Крит , сильно пострадали . Другие народы Средиземноморья, а также народы, проживающие вблизи Средиземноморья, также имеют высокий уровень талассемии, включая людей из Северной Африки и Западной Азии . Вдали от Средиземноморья страдают также жители Южной Азии , при этом самая высокая в мире концентрация носителей (16–18% населения) приходится на Мальдивы . [80]
Заболевание также встречается у населения, живущего в Африке, Америке, а также у народа тару в регионе Тераи в Непале и Индии . [81] Считается, что именно она является причиной гораздо более низких показателей заболеваемости и смертности от малярии. [82] что объясняет историческую способность тарусов выживать в районах с сильным заражением малярией, в то время как другие не могли этого сделать. Талассемия особенно связана с людьми средиземноморского происхождения, арабами (особенно палестинцами и людьми палестинского происхождения) и азиатами. [83] По оценкам, распространенность составляет 16% у жителей Кипра , 1% [84] в Таиланде и 3–8% среди населения Бангладеш , Китая , Индии , Малайзии и Пакистана .
По оценкам, примерно 1,5% мирового населения (80–90 миллионов человек) являются носителями β-талассемии. [85] Однако точные данные о распространенности носителей во многих группах населения отсутствуют, особенно в развивающихся регионах мира, которые, как известно или ожидаются, будут сильно затронуты. [86] [87] Из-за распространенности заболевания в странах, где о талассемии мало что известно, доступ к правильному лечению и диагностике может быть затруднен. [88] Хотя в развивающихся странах существуют некоторые диагностические и лечебные учреждения, в большинстве случаев они не предоставляются государственными службами и доступны только тем пациентам, которые могут себе это позволить. В целом, более бедные слои населения имеют доступ лишь к ограниченным диагностическим средствам и средствам переливания крови. В некоторых развивающихся странах практически нет средств для диагностики и лечения талассемии. [88]
Этимология и синоним
[ редактировать ]Слово талассемия ( / θælɪˈs греческого » , iː ) m iə / ( ) происходит от слова таласса θάλασσα , «море [89] и неолатинский -emia (от греческой составной основы - аимия (-αιμία), от haima (αἷμα), «кровь»). [90] Оно было придумано потому, что состояние, называемое «средиземноморской анемией», было впервые описано у людей средиземноморских национальностей. «Средиземноморская анемия» была переименована в большую талассемию , когда генетика стала лучше изучена. Слово талассемия впервые было использовано в 1932 году. [79] : 877 [91]
Исследовать
[ редактировать ]Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г час «Каковы признаки и симптомы талассемии?» . НХЛБИ . 3 июля 2012 года. Архивировано из оригинала 16 сентября 2016 года . Проверено 5 сентября 2016 г.
- ^ Перейти обратно: а б с «Что вызывает талассемию?» . НХЛБИ . 3 июля 2012 года. Архивировано из оригинала 26 августа 2016 года . Проверено 5 сентября 2016 г.
- ^ Перейти обратно: а б «Как диагностируется талассемия?» . НХЛБИ . 3 июля 2012 года. Архивировано из оригинала 16 сентября 2016 года . Проверено 5 сентября 2016 г.
- ^ Перейти обратно: а б с д и «Как лечат талассемию?» . НХЛБИ . 3 июля 2012 года. Архивировано из оригинала 16 сентября 2016 года . Проверено 5 сентября 2016 г.
- ^ ГББ, 2015 г., «Заболеваемость и распространенность заболеваний и травм» (8 октября 2016 г.). «Глобальная, региональная и национальная заболеваемость, распространенность и продолжительность жизни с инвалидностью по 310 заболеваниям и травмам, 1990–2015 гг.: систематический анализ для исследования глобального бремени болезней, 2015 г.» . Ланцет . 388 (10053): 1545–1602. дои : 10.1016/S0140-6736(16)31678-6 . ПМК 5055577 . ПМИД 27733282 .
{{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ Перейти обратно: а б ГББ, 2015 г. Смертность и причины смерти (8 октября 2016 г.). «Глобальная, региональная и национальная продолжительность жизни, смертность от всех причин и смертность от конкретных причин по 249 причинам смерти, 1980–2015 гг.: систематический анализ для исследования глобального бремени болезней, 2015 г.» . Ланцет . 388 (10053): 1459–1544. дои : 10.1016/s0140-6736(16)31012-1 . ПМЦ 5388903 . ПМИД 27733281 .
{{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ Перейти обратно: а б с «Что такое талассемия?» . НХЛБИ . 3 июля 2012 года. Архивировано из оригинала 26 августа 2016 года . Проверено 5 сентября 2016 г.
- ^ Перейти обратно: а б Бэрд, округ Колумбия, Баттен С.Х., Спаркс СК. Альфа- и бета-талассемия: быстрый обзор фактических данных. Я известный врач. 1 марта 2022 г.; 105(3): 272–280. PMID: 35289581.
- ^ «Как можно предотвратить талассемию?» . НХЛБИ . 3 июля 2012 года. Архивировано из оригинала 16 сентября 2016 года . Проверено 5 сентября 2016 г.
- ^ «Хелирование железа» . Проверено 15 июля 2020 г.
- ^ Шах, Сандип; Шет, Радхика; Шах, Камлеш; Патель, Киннари (февраль 2020 г.). «Безопасность и эффективность комбинации талидомида и гидроксимочевины при средней и большой β-талассемии: ретроспективное пилотное исследование» . Британский журнал гематологии . 188 (3): e18–e21. дои : 10.1111/bjh.16272 . ISSN 0007-1048 . ПМИД 31710694 . S2CID 207940189 .
- ^ Кейхаи, Биджан (2015). «Клинические и гематологические эффекты гидроксимочевины у пациентов с промежуточной β-талассемией» . Журнал клинических и диагностических исследований . 9 (10): ОМ01-3. дои : 10.7860/JCDR/2015/14807.6660 . ПМЦ 4625280 . ПМИД 26557561 .
- ^ Мазера, Николетта; Тавеккья, Луиза; Капра, Мариетта; Каццанига, Джованни; Вимеркати, Кьяра; Поцци, Лорена; Бионди, Андреа; Мазера, Джузеппе (2010). «Оптимальный ответ на талидомид у пациента с большой талассемией, резистентного к традиционной терапии» . Переливание крови . 8 (1): 63–5. дои : 10.2450/2009.0102-09 . ISSN 1723-2007 . ПМК 2809513 . ПМИД 20104280 .
- ^ Исследование глобального бремени болезней, 2013 г. (22 августа 2015 г.). «Глобальная, региональная и национальная заболеваемость, распространенность и количество лет жизни с инвалидностью для 301 острого и хронического заболевания и травмы в 188 странах, 1990–2013 гг.: систематический анализ для исследования глобального бремени болезней 2013 г.» . Ланцет . 386 (9995): 743–800. дои : 10.1016/s0140-6736(15)60692-4 . ПМЦ 4561509 . ПМИД 26063472 .
{{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ Перейти обратно: а б ГББ 2013 Смертность и причины смерти (17 декабря 2014 г.). «Глобальная, региональная и национальная смертность от всех причин и по конкретным причинам в разбивке по возрасту и по конкретным причинам по 240 причинам смерти, 1990–2013 гг.: систематический анализ для исследования глобального бремени болезней, 2013 г.» . Ланцет . 385 (9963): 117–71. дои : 10.1016/S0140-6736(14)61682-2 . hdl : 11655/15525 . ПМК 4340604 . ПМИД 25530442 .
{{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ Уэзералл, диджей (2015). «Талассемия: нарушения синтеза глобина» . Гематология Уильямса (9-е изд.). МакГроу Хилл Профессионал. п. 725. ИСБН 9780071833011 .
- ^ Чианчулли П. (октябрь 2008 г.). «Лечение перегрузки железом при талассемии». Педиатр Эндокринол Ред . 6 (Приложение 1): 208–13. ПМИД 19337180 .
- ^ «Талассемия – Симптомы и причины» . Клиника Мэйо . Архивировано из оригинала 20 ноября 2016 года . Проверено 4 апреля 2017 г.
- ^ Вогиаци, Мария Г; Маклин, Эрик А; Фунг, Эллен Б; Чунг, Анджела М; Вичинский, Эллиот; Оливьери, Нэнси; Кирби, Мелани; Квятковски, Джанет Л; Каннингем, Мелоди; Холм, Ингрид А; Лейн, Джозеф; Шнайдер, Роберт; Флейшер, Мартин; Грейди, Роберт В.; Петерсон, Чарльз С; Джардина, Патрисия Дж (март 2009 г.). «Заболевания костей при талассемии: частая и до сих пор нерешенная проблема» . Журнал исследований костей и минералов . 24 (3): 543–557. дои : 10.1359/jbmr.080505 . ISSN 0884-0431 . ПМК 3276604 . ПМИД 18505376 .
- ^ «Симптомы и причины – Увеличение селезенки (спленомегалия) – Клиника Майо» . www.mayoclinic.org . Архивировано из оригинала 19 ноября 2016 года . Проверено 2 февраля 2017 г.
- ^ Солиман, Ашраф Т; Калра, Санджай; Де Санктис, Винченцо (1 ноября 2014 г.). «Анемия и рост» . Индийский журнал эндокринологии и метаболизма . 18 (7): С1–5. дои : 10.4103/2230-8210.145038 . ПМЦ 4266864 . ПМИД 25538873 .
- ^ «Осложнения талассемии» . Талассемия . Открытое издательство. Архивировано из оригинала 3 октября 2011 года . Проверено 27 сентября 2011 г.
- ^ Weatherall DJ. Новая генетика и клиническая практика, Oxford University Press, Оксфорд, 1991.
- ^ Хьюсман Т.Д. Строение и функции нормальных и аномальных гемоглобинов. В: Клиническая гематология Байера, Хиггс Д.Р., Weatherall DJ (редакторы), WB Saunders, Лондон, 1993. стр.1.
- ^ Натараджан К., Таунс Т.М., Кутлар А. Нарушения структуры гемоглобина: серповидноклеточная анемия и связанные с ней аномалии. В: Гематология Уильямса, 8-е изд., Каушанский К., Лихтман М.А., Бойтлер Э. и др. (Ред.), McGraw-Hill, 2010. стр. 48.
- ^ Вай Фэн Лим, Логесваран Мунианди, Элизабет Джордж, Джамила Сатар, Лай Куан Тех и Мэй И Лай (2015) HbF при HbE/β-талассемии: клиническая и лабораторная корреляция, Гематология, 20:6, 349-353, DOI: 10.1179/1607845414Y.0000000203
- ^ Перейти обратно: а б с Хусейн, Норита; Хеннеман, Лидевий; Кай, Джо; Куреши, Надим (11 октября 2021 г.). Кокрейновская группа по муковисцидозу и генетическим заболеваниям (ред.). «Оценка риска развития талассемии, серповидно-клеточной анемии, муковисцидоза и болезни Тея-Сакса до зачатия» . Кокрейновская база данных систематических обзоров . 2021 (10): CD010849. дои : 10.1002/14651858.CD010849.pub4 . ПМЦ 8504980 . ПМИД 34634131 .
- ^ Вамбуа С; Мванги, Табита В.; Корток, Моисей; Уйога, Софи М.; Махария, Алекс В.; Мвачаро, Джедида К.; Уэзералл, Дэвид Дж.; Сноу, Роберт В.; Марш, Кевин; Уильямс, Томас Н. (май 2006 г.). «Влияние α +-талассемии на заболеваемость малярией и другими заболеваниями у детей, живущих на побережье Кении» . ПЛОС Медицина . 3 (5): е158. doi : 10.1371/journal.pmed.0030158 . ПМЦ 1435778 . PMID 16605300 .
- ^ Тассиопулос С; Дефтереос, Спирос; Константинопулос, Костас; Фармакис, Димитрис; Цирони, Мария; Кириакидис, Михалис; Эссоп, Афанассиос (2005). «Дает ли гетерозиготная бета-талассемия защиту от ишемической болезни сердца?». Анналы Нью-Йоркской академии наук . 1054 (1): 467–70. Бибкод : 2005NYASA1054..467T . дои : 10.1196/анналы.1345.068 . ПМИД 16339699 . S2CID 71993591 .
- ^ Герберт Л. Манси-младший; Кэмпбелл, Джеймс С. (15 августа 2009 г.). «Альфа и бета-талассемия» . Американский семейный врач . 80 (4): 339–344. ПМИД 19678601 .
- ^ Основная патология Роббинса, страница №: 428.
- ^ Интернет-менделевское наследование у человека (OMIM): Гемоглобин - альфа-локус 1; HBA1 - 141800
- ^ Онлайн-менделевское наследование у человека (OMIM): Гемоглобин - альфа-локус 2; HBA2 - 141850
- ^ Перейти обратно: а б Галанелло, Ренцо; Цао, Антонио (5 января 2011 г.). «Альфа-талассемия» . Генетика в медицине . 13 (2): 83–88. дои : 10.1097/GIM.0b013e3181fcb468 . ISSN 1098-3600 . ПМИД 21381239 .
- ^ Перейти обратно: а б «Основы анемии» . ВебМД . Проверено 9 мая 2019 г.
- ^ Интернет-менделевское наследование у человека (OMIM): Гемоглобин - бета-локус; ГББ - 141900
- ^ «Дельта-бета-талассемия» . Сирота . Проверено 16 сентября 2016 г.
- ^ «HBD – субъединица гемоглобина дельта» . Сирота . Проверено 17 сентября 2016 г.
- ^ Торрес Лде С (март 2015 г.). «Гемоглобин D-Пенджаб: происхождение, распространение и лабораторная диагностика» . Бразильский обзор гематологии и гемотерапии . 37 (2): 120–126. дои : 10.1016/j.bjhh.2015.02.007 . ПМЦ 4382585 . ПМИД 25818823 .
- ^ «Как диагностируется талассемия? - NHLBI, NIH» . www.nhlbi.nih.gov . Архивировано из оригинала 28 июля 2017 года . Проверено 6 сентября 2017 г.
- ^ Кеохан, Э; Смит, Л; Валенга, Дж (2015). Гематология Родака: клинические принципы и приложения (5-е изд.). Elsevier Науки о здоровье. стр. 467–9. ISBN 978-0-323-23906-6 .
- ^ Коттке-Марчант, К; Дэвис, Б. (2012). Лабораторная гематологическая практика (1-е изд.). Джон Уайли и сыновья. п. 569. ИСБН 978-1-4443-9857-1 .
- ^ Перейти обратно: а б Фунг, Вай Ченг; Лох, К Хай; Хо, Жаклин Дж; Лау, Дорис СК (13 января 2023 г.). Кокрейновская группа по муковисцидозу и генетическим заболеваниям (ред.). «Индукторы фетального гемоглобина для снижения переливания крови при нетрансфузионно-зависимых бета-талассемиях» . Кокрейновская база данных систематических обзоров . 2023 (1): CD013767. дои : 10.1002/14651858.CD013767.pub2 . ПМЦ 9837847 . ПМИД 36637054 .
- ^ Перейти обратно: а б Лечение детской талассемии в eMedicine
- ^ Перейти обратно: а б с д Нойфельд, Э.Дж. (2010). «Обновленная информация о хелаторах железа при талассемии» . Гематология . 2010 : 451–5. дои : 10.1182/asheducation-2010.1.451 . ПМИД 21239834 .
- ^ Фишер, Шейла А.; Бранскилл, Сьюзен Дж.; Дори, Кэролайн; Чоудхури, Онима; Гудинг, Сара; Робертс, Дэвид Дж. (21 августа 2013 г.). «Оральный деферипрон для хелирования железа у людей с талассемией» . Кокрейновская база данных систематических обзоров (8): CD004839. дои : 10.1002/14651858.CD004839.pub3 . ISSN 1469-493X . ПМИД 23966105 .
- ^ Перейти обратно: а б Боллиг, Клаудия; Шелл, Лиза К.; Рюкер, Герта; Аллерт, Роман; Мотшалл, Эдит; Нимейер, Шарлотта М.; Басслер, Дирк; Меерполь, Йорг Дж. (15 августа 2017 г.). «Деферасирокс для борьбы с перегрузкой железом у людей с талассемией» . Кокрановская база данных систематических обзоров . 2017 (8): CD007476. дои : 10.1002/14651858.CD007476.pub3 . ISSN 1469-493X . ПМК 6483623 . ПМИД 28809446 .
- ^ Садаф, Алина; Хасан, Бабар; Дас, Джай К; Колан, Стивен; Алви, Наджвин (12 июля 2018 г.). Кокрейновская группа по муковисцидозу и генетическим заболеваниям (ред.). «Блокаторы кальциевых каналов для профилактики кардиомиопатии из-за перегрузки железом у людей с трансфузионно-зависимой бета-талассемией» . Кокрейновская база данных систематических обзоров . 2018 (7): CD011626. дои : 10.1002/14651858.CD011626.pub2 . ПМК 6513605 . ПМИД 29998494 .
- ^ Нгим, CF; Лай, Нью-Мексико; Хонг, JY; Тан, СЛ; Рамадас, А; Мутукумарасами, П; Тонг, МК (28 мая 2020 г.). «Терапия гормоном роста для людей с талассемией» . Кокрановская база данных систематических обзоров . 2020 (5): CD012284. дои : 10.1002/14651858.CD012284.pub3 . ПМЦ 7387677 . ПМИД 32463488 .
- ^ Перейти обратно: а б Газиев Дж.; Лукарелли, Дж. (июнь 2011 г.). «Трансплантация гемопоэтических стволовых клеток при талассемии». Современные исследования и терапия стволовыми клетками . 6 (2): 162–9. дои : 10.2174/157488811795495413 . ПМИД 21190532 .
- ^ Саблофф, М; Чанди, М; Ван, З; Логан, БР; Гавамзаде, А; Лизать; Ирфан, С.М.; Бредесон, Китай; и др. (2011). «Трансплантация HLA-совместимого брата и сестры костного мозга при большой β-талассемии» . Кровь . 117 (5): 1745–50. дои : 10.1182/blood-2010-09-306829 . ПМК 3056598 . ПМИД 21119108 .
- ^ Шарма, Акшай; Джаганнатх, Ванита А.; Пури, Латика (21 апреля 2021 г.). «Трансплантация гемопоэтических стволовых клеток людям с β-талассемией» . Кокрановская база данных систематических обзоров . 2021 (4): CD008708. дои : 10.1002/14651858.CD008708.pub5 . ISSN 1469-493X . ПМК 8078520 . ПМИД 33880750 .
- ^ Фишер, Шейла А; Катлер, Энтони; Дори, Кэролайн; Бранскилл, Сьюзен Дж; Стэнворт, Саймон Дж; Наваррете, Кристина; Гердлстоун, Джон (30 января 2019 г.). Кокрейновская группа по гематологическим злокачественным новообразованиям (ред.). «Мезенхимальные стромальные клетки как лечение или профилактика острой или хронической реакции трансплантат против хозяина у реципиентов трансплантата гемопоэтических стволовых клеток (ТГСК) с гематологическими заболеваниями» . Кокрейновская база данных систематических обзоров . 1 (1): CD009768. дои : 10.1002/14651858.CD009768.pub2 . ПМК 6353308 . ПМИД 30697701 .
- ^ Содани, П; Исгро, А; Газиев Дж.; Пачиарони, К; Марциали, М; Симона, доктор медицины; Роведа, А; Де Анджелис, Дж; и др. (2011). «Трансплантация hla-гаплоидентичных стволовых клеток с обеднением Т-клеток молодым пациентам с талассемией» . Педиатрические отчеты . 3 (Дополнение 2): e13. дои : 10.4081/pr.2011.s2.e13 . ПМК 3206538 . ПМИД 22053275 .
- ^ Негре, Оливье; Эггиманн, Анн-Вирджини; Безар, Ив; Рибей, Жан-Антуан; Бурже, Филипп; Борворнпиньо, Супарерк; Хонгэн, Сурадей; Хасейн-бей, Салима; Каваццана, Марина; Лебульш, Филипп; Пайен, Эммануэль (февраль 2016 г.). «Генная терапия β-гемоглобинопатий путем лентивирусного переноса β – гена» . Генная терапия человека . 27 (2): 148–165. дои : 10.1089/hum.2016.007 . ПМЦ 4779296 . ПМИД 26886832 .
- ^ «Зинтегло ЭПАР» . Европейское агентство лекарственных средств (EMA) . 25 марта 2019 года. Архивировано из оригинала 16 августа 2019 года . Проверено 16 августа 2019 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ «Зинтегло» . Управление по контролю за продуктами и лекарствами США . 17 августа 2022 года. Архивировано из оригинала 26 августа 2022 года . Проверено 26 августа 2022 г.
- ^ «FDA одобрило первую клеточную генную терапию для лечения взрослых и детей с бета-талассемией, которым требуется регулярное переливание крови» . США Управление по контролю за продуктами и лекарствами (FDA) (пресс-релиз). 17 августа 2022 года. Архивировано из оригинала 21 августа 2022 года . Проверено 20 августа 2022 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе . - ^ Биффи, А. (19 апреля 2018 г.). «Генная терапия как вариант лечения β-талассемии». Медицинский журнал Новой Англии . 378 (16): 1551–1552. дои : 10.1056/NEJMe1802169 . ПМИД 29669229 .
- ^ Штейн Р. (31 октября 2023 г.). «Консультанты FDA не видят препятствий для лечения серповидноклеточной анемии с помощью редактирования генов» . ЭНЕРГЕТИЧЕСКИЙ ЯДЕРНЫЙ РЕАКТОР . Архивировано из оригинала 4 декабря 2023 года . Проверено 4 декабря 2023 г.
- ^ «MHRA санкционирует первую в мире генную терапию, целью которой является лечение серповидно-клеточной анемии и трансфузионно-зависимой β-талассемии» . Агентство по регулированию лекарственных средств и товаров медицинского назначения (MHRA) (пресс-релиз). 16 ноября 2023 года. Архивировано из оригинала 25 ноября 2023 года . Проверено 8 декабря 2023 г.
- ^ Шеридан С. (ноябрь 2023 г.). «Первая в мире терапия CRISPR одобрена: кто ее получит?» . Природная биотехнология . 42 (1): 3–4. дои : 10.1038/d41587-023-00016-6 . ПМИД 37989785 . S2CID 265350318 . Архивировано из оригинала 4 декабря 2023 года . Проверено 4 декабря 2023 г.
- ^ «Vertex и CRISPR Therapeutics объявляют о разрешении MHRA Соединенного Королевства первого препарата с измененным геном CRISPR/Cas9, Casgevy (exagamglogene autotemcel) для лечения серповидно-клеточной анемии и трансфузионно-зависимой бета-талассемии» (пресс-релиз). Вертекс Фармасьютикалс. 16 ноября 2023 года. Архивировано из оригинала 22 ноября 2023 года . Проверено 9 декабря 2023 г. - через Business Wire.
- ^ Перейти обратно: а б «FDA одобрило первый метод генной терапии для лечения пациентов с серповидноклеточной анемией» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 8 декабря 2023 года. Архивировано из оригинала 8 декабря 2023 года . Проверено 8 декабря 2023 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе . - ^ «Vertex и CRISPR Therapeutics объявляют об одобрении FDA США препарата Casgevy (exagamglogene autotemcel) для лечения серповидноклеточной анемии» (пресс-релиз). Вертекс Фармасьютикалс. 8 декабря 2023 года. Архивировано из оригинала 9 декабря 2023 года . Проверено 9 декабря 2023 г. - через Business Wire.
- ^ Комиссар Управления (16 января 2024 г.). «Сводка новостей FDA: 16 января 2024 г.» . FDA . Проверено 19 января 2024 г.
- ^ Ансари, Сакиб Х; Ласси, Зохра С; Ховаджа, Салима М; Адиль, Сайед Омайр; Шамси, Тахир С. (16 марта 2019 г.). Кокрейновская группа по муковисцидозу и генетическим заболеваниям (ред.). «Гидроксимочевина (гидроксикарбамид) при трансфузионно-зависимой β-талассемии» . Кокрейновская база данных систематических обзоров . 3 (3): CD012064. дои : 10.1002/14651858.CD012064.pub2 . ПМК 6421980 . ПМИД 30882896 .
- ^ Ке Мон Мин Све (2013). «Пищевые добавки цинка для лечения талассемии и серповидноклеточной анемии» . Кокрейновская база данных систематических обзоров . 2013 (6): CD009415. дои : 10.1002/14651858.CD009415.pub2 . ПМЦ 9964104 . ПМИД 23807756 .
- ^ Мулимани, Прити; Абас, Адинегара Б.Л.; Карант, Лакшминараян; Коломбатти, Рафаэлла; Кулкарни, Пална (2 августа 2019 г.). Кокрейновская группа по муковисцидозу и генетическим заболеваниям (ред.). «Лечение стоматологических и ортодонтических осложнений при талассемии» . Кокрейновская база данных систематических обзоров . 8 (8): CD012969. дои : 10.1002/14651858.CD012969.pub2 . ПМК 6699676 . ПМИД 31425614 .
- ^ Перейти обратно: а б Бхардвадж, Амит; Шве, Ке Мон Мин; Синха, Нирмал К.; Осункво, Ифейинва (10 марта 2016 г.). «Лечение остеопороза у людей с β-талассемией». Кокрановская база данных систематических обзоров . 3 : CD010429. дои : 10.1002/14651858.CD010429.pub2 . ISSN 1469-493X . ПМИД 26964506 .
- ^ Перейти обратно: а б с Мулимани, Прити; Абас, Адинегара Б.Л.; Карант, Лакшминараян; Коломбатти, Рафаэлла; Кулкарни, Пална (2 февраля 2023 г.). Кокрейновская группа по муковисцидозу и генетическим заболеваниям (ред.). «Лечение стоматологических и ортодонтических осложнений при талассемии» . Кокрейновская база данных систематических обзоров . 2023 (2): CD012969. дои : 10.1002/14651858.CD012969.pub3 . ПМЦ 9893875 . ПМИД 36732291 .
- ^ Бердик, Колорадо; Нтайос, Г.; Ратод, Д. (март 2009 г.). «Разделение признаков талассемии и дефицита железа простым осмотром» . Являюсь. Дж. Клин. Патол . 131 (3): 444, ответ автора 445. doi : 10.1309/AJCPC09VRAXEASMH . ПМИД 19228649 .
- ^ Принципы внутренней медицины Харрисона (17-е изд.). МакГроу-Хилл медицинский. Сентябрь 2008. с. 776. ИСБН 978-0-07-164114-2 .
- ^ «Скрининг носительства в эпоху геномной медицины – ACOG» . www.acog.org . Архивировано из оригинала 25 февраля 2017 года . Проверено 24 февраля 2017 г.
- ^ Люнг, Теннесси; Лау ТК; Чунг ТХ (апрель 2005 г.). «Скрининг талассемии во время беременности». Современное мнение в акушерстве и гинекологии . 17 (2): 129–34. дои : 10.1097/01.gco.0000162180.22984.a3 . ПМИД 15758603 . S2CID 41877258 .
- ^ Лукопулос, Д. (октябрь 2011 г.). «Гемоглобинопатии в Греции: программа профилактики за последние 35 лет» . Индийский журнал медицинских исследований . 134 (4): 572–6. ПМЦ 3237258 . ПМИД 22089622 .
- ^ Самават А, Модель Б (ноябрь 2004 г.). «Иранская национальная программа скрининга талассемии» . BMJ (Клинические исследования под ред.) . 329 (7475): 1134–7. дои : 10.1136/bmj.329.7475.1134 . ПМК 527686 . ПМИД 15539666 .
- ^ Петру, Мэри (1 января 2010 г.). «Скрининг бета-талассемии» . Индийский журнал генетики человека . 16 (1): 1–5. doi : 10.4103/0971-6866.64934 (неактивен 7 февраля 2024 г.). ПМЦ 2927788 . ПМИД 20838484 .
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на февраль 2024 г. ( ссылка ) [ постоянная мертвая ссылка ] - ^ Перейти обратно: а б Грир, Джон П.; Арбер, Дэниел А.; Глэйдер, Бертиль; Лист, Алан Ф.; Минс-младший, Роберт Т.; Параскевас, Фриксос; Роджерс, Джордж М.; Ферстер, Джон (2013). Клиническая гематология Винтроба . Уолтерс Клювер, Липпинкотт Уильямс и Уилкинс Хелс. ISBN 9781451172683 .
- ^ Вахид, Фазила; Фистер, Коллин; Авофесо, АвоНийи; Стэнли, Дэвид (июль 2016 г.). «Скрининг носительства бета-талассемии на Мальдивах: мнение родителей больных детей, не принимавших участие в скрининге, и его последствия» . Журнал общественной генетики . 7 (3): 243–253. дои : 10.1007/s12687-016-0273-5 . ПМК 4960032 . ПМИД 27393346 .
- ^ Модиано, Дж.; Морпурго, Дж; Терренато, Л; Новеллетто, А; Ди Риенцо, А; Коломбо, Б; Пурпура, М; Мариани, М; и др. (1991). «Защита от заболеваемости малярией: почти фиксация гена α-талассемии в непальском населении» . Американский журнал генетики человека . 48 (2): 390–7. ПМК 1683029 . ПМИД 1990845 .
- ^ Терренато, Л; Шреста, С; Диксит, Калифорния; Луццато, Л; Модиано, Дж; Морпурго, Дж; Арезе, П. (февраль 1988 г.). «Снижение заболеваемости малярией среди населения Тару по сравнению с симпатрическим населением Непала». Анналы тропической медицины и паразитологии . 82 (1): 1–11. дои : 10.1080/00034983.1988.11812202 . ПМИД 3041928 .
- ^ Э. Гольян, Патология, 2-е изд. Mosby Elsevier, серия Rapid Review. [ нужна страница ]
- ^ «Талассемия» (на тайском языке). Департамент медицинских наук. Сентябрь 2011 г. Архивировано из оригинала 25 сентября 2011 г.
- ^ Галанелло, Ренцо; Орига, Рафаэлла (2010). «Бета-талассемия» . Сиротский журнал редких заболеваний . 5 (1): 11. дои : 10.1186/1750-1172-5-11 . ПМЦ 2893117 . ПМИД 20492708 .
- ^ Галанелло, Ренцо; Орига, Рафаэлла (2010). «Бета-талассемия» . Сиротский журнал редких заболеваний . 5 (1): 11. дои : 10.1186/1750-1172-5-11 . ПМЦ 2893117 . ПМИД 20492708 .
- ^ Вичинский, Эллиотт П. (1 ноября 2005 г.). «Изменение моделей талассемии во всем мире». Анналы Нью-Йоркской академии наук . 1054 (1): 18–24. Бибкод : 2005NYASA1054...18V . дои : 10.1196/анналы.1345.003 . ISSN 1749-6632 . ПМИД 16339647 . S2CID 26329509 .
- ^ Перейти обратно: а б Уэзералл, Дэвид Дж. (ноябрь 2005 г.). «Основной доклад: Проблема талассемии для развивающихся стран». Анналы Нью-Йоркской академии наук . 1054 (1): 11–17. Бибкод : 2005NYASA1054...11W . дои : 10.1196/анналы.1345.002 . ПМИД 16339646 . S2CID 45770891 .
- ^ θάλασσα . Лидделл, Генри Джордж ; Скотт, Роберт ; Греко-английский лексикон в проекте «Персей» .
- ^ кровь у Лидделла и Скотта .
- ^ Уиппл, GH; Брэдфорд, Висконсин (1932). «Расовая или семейная анемия детей, связанная с фундаментальными нарушениями метаболизма костей и пигментов (Кули-Фон Якш)». Американский журнал болезней детей . 44 : 336–365. дои : 10.1001/archpedi.1932.01950090074009 .
- 85. https://journals.lww.com/indjem/fulltext/2013/17010/Growth_and_endocrine_disorders_in_thalassemia__The.3.aspx
- О святых, Винченцо; Солиман, Ашраф Т. 1 ; Эльседфи, Хеба 2 ; Скордис, Никос 3 ; Каттамис, Христос 4 ; Ангастиниотис, Майкл 5 ; Карими, Мехран 6 ; Ясин, Мохд Абдель Даем Мохд 7 ; Эль-Авва, Ахмед 1 ; Стоева, Ива 8 ; Райола, Джузеппе 9 ; Галац, Мария Кончетта 10 ; Бедер, Эльсаид М. 11 ; Фишина, Бернадетт 12 ; Эль Холи, Мохамед 2 Информация для автора Индийский журнал эндокринологии и метаболизма 17(1): стр. 8–18, январь – февраль 2013 г. | DOI: 10.4103/2230-8210.107808.
Внешние ссылки
[ редактировать ]- Талассемия в Керли
- «Изучение талассемии», опубликованное Национальным институтом исследования генома человека.