Химия организма

Химия органотина - это научное исследование синтеза и свойств органических соединений или стананов , которые представляют собой органометаллические соединения, содержащие связи с олова - углеродные связи. Первым соединением организма был диэтилтин -диодид ( (Ch 3 CH 2 ) 2 SNI 2 ), обнаруженная Эдвардом Франклендом в 1849 году. [ 1 ] Район быстро рос в 1900 -х годах, особенно после открытия реагентов Гриньяра , которые полезны для создания связей SN - C. Область остается богатой, благодаря множеству применений в промышленности и постоянной деятельности в исследовательской лаборатории. [ 2 ]
Структура
[ редактировать ]Соединения организма обычно классифицируются в соответствии с их состояниями окисления. Соединения олова (IV) гораздо более распространены и более полезны.
Органические производные олова (IV)
[ редактировать ]Производные тетраоргано неизменно тетраэдрические. Соединения типа snrr'r'r '' 'были разрешены в отдельных энантиомеров. [ 3 ]
Органотиновые галогениды
[ редактировать ]Хлориды организма имеют формулу R 4 - N SNCL N для значений N до 3. Бромиды, йодиды и фториды также известны, но менее важны. Эти соединения известны для многих групп R. Они всегда тетраэдрические. Три- и дихалиды образуют аддукты с хорошими базами Льюиса, такими как пиридин . Фтоориды имеют тенденцию ассоциироваться так, чтобы диметилтиновые дифторидные формы, подобные листообразным полимерам. Ди- и особенно галогениды триготина, например, хлорид трибутилтина , демонстрируют токсичность, приближающуюся к токсичности цианида водорода . [ 4 ]
Органотиновые гидриды
[ редактировать ]Гидриды организма имеют формулу R 4 - N SNH N для значений n до 3. Родительский член этой серии, Stannane ( SNH 4 ), это нестабильный бесцветный газ. Стабильность коррелирует с количеством органических заместителей. Гидрид Tributyltin используется в качестве источника гидридного радикала в некоторых органических реакциях.
Оксиды организма и гидроксиды
[ редактировать ]Оксиды органотинов и гидроксиды являются общими продуктами из гидролиза галогенидов органотина. В отличие от соответствующих производных кремния и германия, оксиды олова и гидроксиды часто принимают структуры с пентами и даже шестиуординанированными оловянными центрами, особенно для производных диоргано- и монургано. Группа С IV −o - sn IV называется Stannoxane (который является аналогом эфиров ) , а группа С IV −o - H также называется Stannanol (который является оловянным аналогом спиртов ). [ 5 ] Структурно простыми из оксидов и гидроксидов являются производные триорганотина. Коммерчески важным гидроксидом триорганотина является акарицида цигексатин (также называемый Plictran, трициклогекксилтин гидроксид и трициклогексилстананол), (( C 6 H 11 ) 3 Snoh . Такие гидроксиды триорганотина существуют в равновесии с дистаноксанами:
- 2 r 3 snoh ⇌ r 3 snosnr 3 + h 2 o
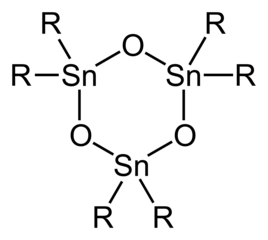
С только двумя органическими заместителями в каждом центре SN, оксиды диорганотина и гидроксиды структурно более сложны, чем производные триоргано. [ 6 ] Простые жестяные гемины ( R 2 Sn (OH) 2 , TIN Analoges of Geminal Diols R 2 C (OH) 2 ) и мономерные стананоны ( R 2 sn = o , аналоги кетонов R 2 C = O ) неизвестны. Оксиды диорганотина ( R 2 sno ) являются полимерами, за исключением случаев, когда органические заместители очень громоздкие, и в этом случае циклические тримеры или, в случае, где r CH (Si (Ch 3 ) 3 ) 2 димера , с Sn 3 o 3 и SN 2 O 2 кольца. Дистанкансаны существуют в виде димеров с формулой [R 2 snx] 2 o 2 , где x группы (например, хлорид - Cl, гидроксид -OH, карбоксилат RCO 2 - ) может быть терминальным или мостовым (см. Таблицу). Гидролиз моноорганотиновых тригалидов может генерировать станановые кислоты, RSNO 2 часа . Что касается оксидов диорганотина/гидроксидов, виды монорганотина образуют структурно сложные из -за возникновения дегидратации/гидратации, агрегации. Иллюстративным является гидролиз трихлорида бутилтина, чтобы дать [(Ch 3 (Ch 2 ) 3 SN) 12 O 14 (OH) 6 ] 2+ .
-
Идеализированная структура тримерного оксида диорготина.
-
Модель мяча и шарика для ( (CH 3 ) 3 C) 2 SNO) 3 .
-
Структура оксида диорготина, подчеркивая обширную межмолекулярную связь.
Гиперкоординированный Станнаны
[ редактировать ]В отличие от аналогов углерода (IV), но в некоторой степени как кремниевые соединения, олово (IV) также может быть координирована с пятью и даже шестью атомами вместо обычных четырех. Эти гиперкоординированные соединения обычно имеют электроотрицательные заместители. Многочисленные примеры гиперкоординированных соединений предоставляются оксидами организма и связанными с ними карбоксилатами и родственными псевдогалидными производными. [ 6 ] Галогениды органотина для аддуктов, например (Ch 3 ) 2 SNCL 2 ( бипиридин ).
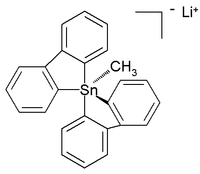
Всеорганические пента и гексаорганостанаты (IV) даже были охарактеризованы, [ 7 ] в то время как в последующем году сообщалось о соединении с шестью координированными тетраорготином. [ 8 ] Кристаллическая структура стабильной температуры в комнате (в аргоне ) всеуглеродистого пентаорганостаната (IV) была зарегистрирована как литиевая соль с этой структурой: [ 9 ]
В этой искаженной тригональной бипирамидальной структуре углеродные длина связей (2,26 Å апикальная , 2,17 Å экваториальная) длиннее обычных связей C-Sn (2,14 Å), отражающих его гиперкоординированную природу.
Триорготиновые катионы
[ редактировать ]Некоторые реакции галогенидов триорганотина указывают на роль R 3 Sn + промежуточные. Такие катионы аналогичны карбокациям . Они были охарактеризованы кристаллографически, когда органические заместители большие, такие как 2,4,6-тризопропилфенил. [ 10 ]
Оловянные радикалы (органические производные олова (III))
[ редактировать ]Оловянные радикалы, с формулой R 3 SN , называются станиловыми радикалами . [ 2 ] Они являются типом радикала тетра и вызываются в качестве промежуточных продуктов в определенных реакциях переноса атома. Например, гидрид Tributyltin (TRIS ( N -Бутил) Станнан) служит полезным источником «атомов водорода» из -за стабильности радикала трибутитина. [ 11 ]
Органические производные олова (II)
[ редактировать ]Соединения органотина (II) несколько редки. Соединения с эмпирической формулой SNR 2 несколько хрупкие и существуют в виде колец или полимеров, когда R не является громоздким. Полимеры, называемые полистаннанами , имеют формулу (SNR 2 ) n .
В принципе, можно ожидать, что соединения олова (II) сформируют аналоги алкенов с формальной двойной связью между двумя атомами олова ( R 2 sn = snr 2 ) или между атомом олова и атом углеродной группы (например, R 2 sn = cr 2 и R 2 sn = сэр 2 ). Действительно, соединения с формулой R 2 SN = SNR 2 , называемые дистаннами или дистаниленами , которые являются аналогами олова этилена R 2 C = Cr 2 , известны для определенных органических заместителей. Центры SN в Stannenes являются тригональными. Но, в отличие от центров C в алкенах, которые являются тригональными планарными , центры SN в Stannenes имеют тенденцию быть высоко пирамидальным . Мономерные соединения с формулой SNR 2 , TIN Analoges of Carbenes CR 2 также известны в нескольких случаях. Один пример Sn (сэр 3 ) 2 , где r - очень громоздкий CH (Si (Ch 3 ) 3 ) 2 . Такие виды обратимо димеризируются в дистанилен при кристаллизации: [ 12 ]
- 2 r 2 sn ⇌ r 2 sn = snr 2
Stannenes , соединения с оловянными двойными связями, иллюстрируются производными Stannabenzene . Станолы , структурные аналоги циклопентадиена . , демонстрируют маленький характер двойной связи C-Sn
Органические производные олова (i)
[ редактировать ]Соединения Sn (I) редки и наблюдаются только с очень громоздкими лигандами. Доступ к одному известному семейству клеток путем пиролиза 2,6-диэтилфенил-замещенного тристанилена [SN (C 6 H 3 -2,6-ET 2 ) 2 ] 3 , который дает кластер типа кубин и Присман . Эти клетки содержат SN (I) и имеют формулу [SN (C 6 H 3 -2,6 -ET 2 )] n , где n = 8, 10 и ET обозначает этильную группу . [ 13 ] Stannyne содержит атом оловянного атомного атомного атома ( например, R - sn®c - r и R -sn®si -r ), а и отдаленность - тройная связь между двумя атомами олова ( R - sn®sn - r ). Дистанины существуют только для чрезвычайно громоздких заместителей. В отличие от Алкинес , C -SNспеющим ядро этих дистаннинов нелинейно, хотя они плоские. Расстояние SN-SN составляет 3,066 (1) Å, а углы SN-SN-C составляют 99,25 (14) °. Такие соединения готовятся путем восстановления громоздких галогенидов арилтина (II). [ 14 ]

Серые шарики: c
Пурпурный (самый большой) шарики: sn
Структура AR 10 SN 10 "PRISMANE", соединение, содержащее SN (I) (AR = 2,6-диэтилфенил).
Подготовка
[ редактировать ]Соединения организма могут быть синтезированы многочисленными методами. [ 15 ] Классика - это реакция реагента Grignard с олова галогенидов, например, оловянного тетрахлорида . Пример приведен синтезом тетраэтилтина: [ 16 ]
- 4 ch 3 ch 2 mgbr + sncl 4 → (ch 3 ch 2 ) 4 sn + 4 mgclbr
Симметричные соединения тетраорганотина, особенно тетраалкильные производные, могут затем быть преобразованы в различные смешанные хлориды путем реакций перераспределения (также известного как «композиция Кохешкова» в случае органических соединений):
- 3 R 4 SW + SNLS 4 → 4 R 3 DNC
- R 4 SN + SNCL 4 → 2 R 2 SNCL 2
- R 4 Sn + 3 Sncl 4 → 4 RSNCl 3
Связанный метод включает в себя перераспределение галогенидов олова с помощью органоалуминия соединений . [ 2 ] : 45–47
В принципе, алкилтиновые галогениды могут быть сформированы из прямой введения металла в углеродную связь. Тем не менее, такие реакции являются темпераментными, как правило, требуется очень слабая углерод-галогенная связь (например, алкил йодид или аллил галогенид) или соляный катализатор с комплексным металлом. Кислоты Льюиса или ионный растворитель могут также способствовать реакции. [ 2 ] : 51–52
Смешанные органо-хало-олово-оловы могут быть преобразованы в смешанные органические производные, как показано синтезом дибутилдивинилтина: [ 17 ]
- Bu 2 sncl 2 + 2 ch 2 = chmgbr → bu 2 sn (ch = ch 2 ) 2 + 2 mgbrcl
Гидриды организма генерируются путем восстановления смешанных алкилхлоридов. Например, обработка дивититилтина дихлорида литиевым алюминиевым гидридом дает дивитилтин дигидрид , бесцветное дистиллеруемое масло: [ 18 ]
- 2 bu 2 sncl 2 + li [alh 4 ] → 2 bu 2 snh 2 + li [alcl 4 ]
Вюрцподобное соединение алкильных натриевых соединений с олово галогенидами дает соединения тетраорганотина.
Гидростанилирование включает в себя катализируемое металлом добавление оловянных гидридов по ненасыщенным субстратам. [ 19 ]
В качестве альтернативы, Stannides атакуют органические электрофилы, чтобы дать органостаннаны, например: [ 2 ] : 49
- LSD 3 + CCL 4 → C (SME 3 ) 4 + LCL.
Реакция
[ редактировать ]Важные реакции, обсуждаемые выше, обычно фокусируются на галогенидах организма и псевдогалидах с нуклеофилами . Все-алкильные органические соединения обычно не гидролизуются , кроме как в концентрированной кислоте ; Основным исключением являются оловянные ацетилиды . [ 20 ] Заполнение органостаннана -это нуклеофильное аллил -Аленил альдегидам -или пропаргилстанннаны к , и иминами добавление [ Цитация необходима ] тогда как гидростанилирование удобно уменьшает только неполяризованные множественные связи. [ 21 ]
Гидриды организма нестабильны к сильному основанию, непропорционаруются газовым водороду и дистаннанам. [ 2 ] : 295 Последний уравновешивается с соответствующими радикалами только в продолжающемся присутствии основания или, если сильно стерически затруднен. [ 2 ] : 299, 334–335 И наоборот, минеральные кислоты расщепляют дистаннанты на галогенид органотина и больше газового водорода. [ 2 ] : 300
В «чистом» органическом синтезе ключевым методом рассматривается реакция STILLE является связи . В реакции Стиль, sp 2 -гибридизированные органические галогениды (например, винилхлорид CH 2 = CHCL ) катализируется Palladium :
- Ведущий 1 −x + r 2 −SN (r 3 ) 3 Ведущий 1 −r 2 + X - sn (r 3 ) 3
Соединения организма также широко используются в радикальной химии (например, радикальные циклизации , дезоксигенация Бартон -Мккомби , декарбоксилирование Бартон и т. Д.).
Приложения
[ редактировать ]Соединение организма коммерчески применяется в качестве стабилизаторов в поливинилхлориде . В этом качестве они подавляют деградацию, удаляя аллиловые хлоридные группы [ нужно разъяснения ] и путем поглощения хлорида водорода . Это приложение потребляет около 20 000 тонн олова каждый год. Основным классом органических соединений является дитиолаты дириганотина с формулой дитиолаты R 2 Sn (Sr ') 2 . Связь SN-S является реактивным компонентом. Диорганотин карбоксилаты, например, дибутитилтин дилуарат используются в качестве катализаторов для образования полиуретанов , для вулканизации силиконов , и переэтерификации . [ 2 ]
N -Бутилтин трихлорид используется при производстве слоев диоксида олова на стеклянных бутылках путем химического отложения паров .
Биологические применения
[ редактировать ]« Твибутилтины » используются в качестве промышленных биоцидов , например, в качестве противогрибковых агентов в текстиле и бумаге, деревянной целлюлозной и бумажной фабрике, пивоваренных заводах и системах промышленного охлаждения. Производители трифенилтина используются в качестве активных компонентов противогрибковых красок и сельскохозяйственных фунгицидов. Другие триорганотины используются в качестве митицидов и акарицидов . Оксид трибутилтина широко используется в качестве консерванта из дерева . [ 2 ]
Соединения Tributyltin когда-то широко использовались в качестве морских анти- биологических агентов для повышения эффективности океанских кораблей. Опасения по поводу токсичности [ 22 ] Из этих соединений (в некоторых сообщениях описывается биологические эффекты морской жизни на концентрации 1 нанограммы на литр) приводили к мировому запрету международной морской организации . В качестве противогарных соединений соединения организма были заменены дихлороктилизотиазолиноном . [ 23 ]
- Соединения организма
-
Некрасивое масло тетрабутилин , предшественник других соединений бутила-тина
-
Оксид трибутилтина , бесцветная или бледно -желтая жидкость, используемая в сохранении древесины
-
Ацетат трифенилтина , не совсем белое кристаллическое твердое вещество, используемое как инсектицид и фунгицид
-
Хлорид трифенилтина , высокотоксичное белое твердое вещество, используемое в качестве биоцида
-
Хлорид триметилтина , токсичное белое твердое вещество, когда -то используемое в качестве биоцида
-
Гидроксид трифенилтина , не совсем белый порошок, используемый в качестве фунгицида
-
Азоциклотин длительного действия , белое твердое вещество, используемое в качестве акарицида для борьбы с пауками на растениях
-
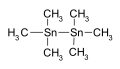
Гексаметидитин используется в качестве промежуточного звена химического синтеза
-
Тетраэтилтин , точка кипения 63–65 ° /12 мм [ нужно разъяснения ] это катализатор. [ 24 ] Символ «ET» означает этильную группу .
Токсичность
[ редактировать ]Токсичность соединений производных трибутилтина и трифенилтина сопоставима с тотаном цианида водорода . Кроме того, три -алкилтины являются фитотоксичными и, следовательно, не могут использоваться в сельском хозяйстве. В зависимости от органических групп, они могут быть мощными бактерицидами и фунгицидами . Отражая их высокую биологическую активность, «трибутилтины» когда-то использовались в морской анти-плавающей краске . [ 2 ]
В отличие от соединений триорганотина, соединений Monoorgano, Diorgano- и тетраорганотина гораздо менее опасны, являются гораздо менее опасными, являются гораздо менее опасными, являются гораздо менее опасными, являются гораздо менее опасными, [ 4 ] Хотя DBT может быть иммунотоксичным. [ 25 ]
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Caseri, Walter (2014). «Первоначальная химия организма». Журнал органометаллической химии . 751 : 20–24. doi : 10.1016/j.jorganchem.2013.08.009 .
- ^ Jump up to: а беременный в дюймовый и фон глин час я Дж k Дэвис, Алвин Джордж. (2004) Химия организма, 2-е издание Вайнхайм: Wiley-VCH. ISBN 978-3-527-31023-4
- ^ Гилен, Марсель (1973). «От кинетики до синтеза хиральных тетраорганотиновых соединений». Акк. Химический Резерв 6 (6): 198–202. doi : 10.1021/ar50066a004 .
- ^ Jump up to: а беременный GG Graf (2005). «Олово, жестяные сплавы и жестяные соединения». Энциклопедия промышленной химии Уллмана . Вейнхайм: Wiley-VCH. doi : 10.1002/14356007.a27_049 . ISBN 978-3527306732 .
- ^ "Станнанол | h4osn | chemspider" .
- ^ Jump up to: а беременный Чандрасекхар, Вадапалли; Нагендран, Сельвараджан; Баскар, Вишванатан (2002). «Сборки организма, содержащие связи SN/O». Обзоры координационной химии . 235 : 1–52. doi : 10.1016/s0010-8545 (02) 00178-9 .
- ^ Рейх, Ганс Дж.; Филлипс, Нэнси Х. (1986). «Реакции литий-металлоидного обмена. Наблюдение за комплексами лития пентаалкил/арил олово». J. Am. Химический Соц 108 (8): 2102–2103. doi : 10.1021/ja00268a067 .
- ^ В.Г. Кумар Дас; Ло Конг Мун; Чен Вэй; Томас CW Mak (1987). «Синтез, спектроскопическое исследование и рентгеновская кристаллическая структура Bis [3- (2-пиридил) -2-тиенил-C, N] дифенилтина (IV): первый пример шестикоординатного соединения тетраорготина». Органометаллики . 6 : 10–14. doi : 10.1021/om00144a003 .
- ^ Магия - это Сайто; Sanaae Imaizaumi; Томайюки Таджима; Kazuya Ishimura & Shigeru Nagase (2007). «Синтез и структурный пентагинастанат, имеющий пять заместителей углерода» J. Am. Химический Соц 129 (36): 10974–1 Doi : 10.1021/j072478 + 17705378PMID
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2 -е изд.). Баттерворт-Хейнеманн . ISBN 978-0-08-037941-8 .
- ^ TV Rajanbabu, PCB Page Br Buckley "Tri-N-Butylstannane" в энциклопедии реагентов E-Eeros для органического синтеза, 2004. doi : 10.1002/047084289x.rt181.pub2
- ^ Холмен, Арнольд Фредерик; Wiberg, Egon (2001), Wiberg, Nils (ed.), Неорганическая химия , переведенная Иглсоном, Мэри; Брюер, Уильям, Сан -Диего/Берлин: Академическая Пресса/Де Грюйтер, ISBN 0-12-352651-5
- ^ Сита, Лоуренс Р. (1994). «Тяжелая металлическая органическая химия: строительство с оловом». Акк. Химический Резерв 27 (7): 191–197. doi : 10.1021/ar00043a002 .
- ^ Пауэр, Филипп П. (2007). «Связывание и реакционная способность более тяжелых элементов группы 14 аналогов алкинов». Органометаллики . 26 (18): 4362–4372. doi : 10.1021/om700365p .
- ^ Сандер HL Thoonen; Причал Ян Дилман; Джерард Ван Котен (2004). «Синтетические аспекты тетраорганотинов и галогенидов органотина (IV)» (PDF) . Журнал органической химии (689): 2145–2157.
- ^ Der Cook, GJM Van; Luikten, JGA (1956). "Тетраэтилттин" Орг Синтезатор 36 : 86 doi : 15227/Orgsyn .
- ^ Сейферт, Дитмар (1959). «Доивильвинилтин». Орг ynth 39 : 10. doi : 10.1527/ords.039.0010 .
- ^ «Органометаллические синтезы: соединения без трансляции» Джон Эйш, изд. Академическая пресса: Нью -Йорк, 1981. ISBN 0122349504 .
- ^ Смит, Николас Д.; Манкусо, Джон; Lautens, Mark (2000). «Катализируемые металлом гидростаннации». Химические обзоры . 100 (8): 3257–3282. doi : 10.1021/cr9902695 . PMID 11749320 .
- ^ Eisch 1981 , с. 156, 169.
- ^ Elschenbroich, Christoph (2006) [2005]. Органометаллики . Перевод Оливейры, Хосе; Эльшенбройх, Кристоф (3 -е изд.). Уайли. п. 310. ISBN 978-3-527-29390-2 .
- ^ Gajda, M.; Jancso, A. (2010). «Органотины, формирование, использование, видообразование и токсикология». Металлические ионы в науках о жизни . 7, Органометаллики в окружающей среде и токсикологии. Кембридж: RSC Publishing: 111–151. doi : 10.1039/9781849730822-00111 . ISBN 9781847551771 .
- ^ Сильва, Вания; Сильва, Катия; Soares, Pedro; Гарридо, Э. Мануэла; Борхес, Фернанда; Гарридо, Хорхе (2020). «Изотиазолинон Боциды: химические, биологические профили и токсичность» . Молекулы . 25 (4): 991. doi : 10.3390/molecules25040991 . PMC 7070760 . PMID 32102175 .
- ^ Органические синтезы , Coll. Тол. 4, с.881 (1963); Тол. 36, с.86 (1956). Связь
- ^ C Gumy; и др. (2008). «Дибутитилтин нарушает функцию глюкокортикоидного рецептора и нарушает индуцированную глюкокортикоидом подавление продукции цитокинов» . Plos один . 3 (10): E3545. Bibcode : 2008ploso ... 3.3545g . doi : 10.1371/journal.pone.0003545 . PMC 2568824 . PMID 18958157 .










![Тетраэтилтин, температура кипения 63–65 ° /12 мм [необходимо разъяснение] является катализатором. [24] Символ «ET» означает этильную группу.](http://upload.wikimedia.org/wikipedia/commons/thumb/1/1e/Tetraethyltin.svg/120px-Tetraethyltin.svg.png)