Аденокарцинома легкого
| Аденокарцинома легкого | |
|---|---|
| Другие имена | Аденокарцинома легких |
 | |
| Грубый патологический образец аденокарциномы легкого, удаленный при лобэктомии . | |
| Специальность | онкология |
Аденокарцинома легких является наиболее распространенным типом рака легких и, как и другие формы рака легких , характеризуется отчетливыми клеточными и молекулярными особенностями. [1] Его классифицируют как один из нескольких видов немелкоклеточного рака легких (НМРЛ), чтобы отличить его от мелкоклеточного рака легких , который имеет другое поведение и прогноз. Аденокарцинома легких подразделяется на несколько подтипов и вариантов. [2] Признаки и симптомы этого конкретного типа рака легких аналогичны симптомам других форм рака легких, и пациенты чаще всего жалуются на постоянный кашель и одышку.
Аденокарцинома чаще встречается у пациентов, курящих сигареты в анамнезе, и является наиболее распространенной формой рака легких у молодых женщин и азиатских групп населения. Патофизиология аденокарциномы сложна, но обычно следует гистологическому прогрессированию от клеток, обнаруженных в здоровых легких, до явно дисморфных или неправильных клеток. Существует несколько различных молекулярных и генетических путей, которые способствуют этому прогрессированию. Как и многие виды рака легких, аденокарцинома легких к моменту постановки диагноза часто находится на поздних стадиях. После того, как поражение или опухоль выявлены с помощью различных методов визуализации, таких как компьютерная томография (КТ) или рентген , для подтверждения диагноза требуется биопсия.
Лечение этого рака легких зависит от конкретного подтипа и степени распространения первичной опухоли. Хирургическая резекция, химиотерапия , лучевая терапия , таргетная терапия и иммунотерапия используются в попытке искоренить раковые клетки на основе этих факторов. [3]
Признаки и симптомы
[ редактировать ]У большинства пациентов с диагнозом рак легких обычно наблюдается местно-распространенное или метастатическое заболевание. Лишь около трети пациентов на момент постановки диагноза имеют I стадию заболевания. [4] Симптомы, которые проявляет пациент, обычно отражают степень распространения рака. Рак легких, обнаруженный на ранней стадии, может вызывать симптомы, локализованные в дыхательной системе. Однако при запущенном раке легких у пациентов появляются дополнительные признаки и симптомы, вторичные по отношению к распространению рака на другие системы органов. [5] К наиболее частым признакам рака легких в порядке убывания частоты относятся: [6]
- кашель, который не проходит или ухудшается
- потеря веса
- одышка (одышка или затрудненное дыхание)
- боль в груди, которая может усиливаться при глубоком дыхании, кашле или смехе
- кровохарканье (кашель с кровью или мокротой ржавого цвета) [7]
- боль в костях
- клубная жизнь
- высокая температура
- обычно чувствую усталость или слабость
- Обструкция верхней полой вены – отек лица, шеи, верхней части туловища. Это вызвано сдавлением сосудов опухолью легкого, что ограничивает возврат крови из верхней части тела. [4]
- дисфагия (проблемы с глотанием или ощущение, что что-то застряло в горле) и охриплость голоса
- новое появление хрипов без астмы в анамнезе
Клиницисты должны иметь высокий уровень подозрения на рак легких, особенно у пациентов с курением. Пациентов с рецидивирующими или неизлечимыми инфекциями легких (например, бронхитом и пневмонией), не реагирующими на антибиотики, также следует дополнительно обследовать на предмет рака легких. У некурящих женщин и жителей Восточной Азии чаще появляются симптомы основного рака легких в более молодом возрасте. [5] Важно отметить, что многие из этих признаков обычно вызваны другими причинами, не являющимися раком. [6]
Внелегочные проявления
[ редактировать ]Ниже описаны наиболее распространенные паранеопластические синдромы, связанные с аденокарциномой легкого:
- Гиперкальциемия злокачественных новообразований чаще встречается при плоскоклеточном раке легкого, но может встречаться и при аденокарциноме. Пептид, родственный паратиреоидному гормону (ПТГрП), вырабатывается опухолевыми клетками и действует аналогично паратиреоидному гормону (ПТГ). Производство этого гормонально активного пептида раковыми клетками вызывает повышенную резорбцию кости за счет активации остеокластов, одной из клеток, ответственных за ремоделирование кости. Когда кость разрушается, кальций выбрасывается в кровоток, что приводит к гиперкальциемии. Признаки и симптомы повышенного содержания кальция в крови включают: жажду, усталость, запор, полиурию (учащение мочеиспускания) и тошноту. Важно исключить костные метастазы у пациентов с НМРЛ, поскольку они также сопровождаются гиперкальциемией.
- Гипертрофическая легочная остеоартропатия (ГПО) при аденокарциноме встречается довольно редко. Менее чем у 1% пациентов с аденокарциномой легкого будет обнаружена эта находка, но когда она все же возникает, это плохой прогностический фактор. Точный механизм ГПО неизвестен, но считается, что он имеет гормональную или нейрогенную этиологию. Триада ГПО включает дистальную булаву, артрит и двустороннее симметричное периостальное образование. [4]
Причины
[ редактировать ]Факторы риска
[ редактировать ]По данным исследования здоровья медсестер , риск развития аденокарциномы легких существенно возрастает после длительного курения табака : у курильщиков с предыдущим стажем курения 30–40 лет более чем в два раза выше вероятность развития аденокарциномы легких по сравнению с никогда не курившими ( относительный риск примерно 2,4); продолжительность более 40 лет увеличивает относительный риск до 5. [8]
Этот рак обычно наблюдается на периферии легких, в отличие от мелкоклеточного рака легких и плоскоклеточного рака легких, которые имеют тенденцию располагаться более центрально. [9] [10] хотя это может также произойти как центральные поражения. [10] По неизвестным причинам оно часто возникает по отношению к периферическим рубцам легких. Текущая теория состоит в том, что рубец, вероятно, возник вторично по отношению к опухоли, а не стал ее причиной. [10] Аденокарцинома чаще встречается у курильщиков и является наиболее распространенным типом рака легких, наблюдаемым у некурящих и женщин. [10] Более глубокое вдыхание сигаретного дыма приводит к периферическим поражениям, которые часто наблюдаются при аденокарциномах легких. Как правило, аденокарцинома растет медленнее и образует меньшие массы, чем другие подтипы. [10] Однако он имеет тенденцию к метастазированию на ранней стадии. [10]
Механизм
[ редактировать ]Патогенез
[ редактировать ]

Крупномасштабные исследования, такие как Атлас генома рака (TCGA), систематически характеризовали рецидивирующие соматические изменения, которые, вероятно, способствуют возникновению и развитию аденокарциномы легких. [11]
Генные мутации и изменения числа копий
[ редактировать ]Поскольку курение является сильным мутагенным фактором, аденокарцинома легких относится к числу опухолей с наибольшим количеством мутаций. [12] Распространенные соматические мутации при аденокарциноме легкого затрагивают многие онкогены и гены-супрессоры опухолей , включая TP53 (мутантный в 46% случаев), EGFR (27%), KRAS (32%), KEAP1 , STK11 и NF1 . [3] Мутации EGFR и KRAS имеют тенденцию проявляться взаимоисключающим образом. Мутации KRAS связаны с привычкой к курению, тогда как мутации EGFR чаще встречаются у женщин, людей азиатской национальности и никогда не куривших. [2]
амплификации числа копий в онкогенах, таких как TERT , Mdm2 , EGFR, MET и Myc Сообщалось об , а также об делециях генов-супрессоров опухолей, таких как CDKN2A . [11]
Частые изменения происходят в генах, принадлежащих к пути рецепторной тирозинкиназы , наиболее ярким примером которых является EGFR. Этот путь участвует в пролиферации и выживании клеток, и его регуляция часто нарушается при раке. Как следствие, были разработаны таргетные методы лечения для ингибирования компонентов мутантного пути. [11] [13]
Хромосомные перестройки
[ редактировать ]Три мембраносвязанных тирозинкиназных рецептора периодически участвуют в слияниях или перегруппировках при аденокарциномах : ALK , ROS1 и RET ; также сообщалось о более чем восьмидесяти других транслокациях при аденокарциномах легких. [14]
При реаранжировках ALK наиболее распространенным геном-партнером является EML4. [3]
Патофизиология
[ редактировать ]Дыхательные пути можно разделить на два основных компонента: проводящие дыхательные пути и воздухообменные пути. Газообменные дыхательные пути состоят из альвеол , небольших микроскопических воздушных мешочков, которые отвечают за обмен кислорода и углекислого газа во время нормального дыхания . Альвеолы состоят из двух типов клеток: пневмоцитов типа I и типа II. Пневмоциты I типа покрывают 95% альвеолярных поверхностей и не способны к регенерации. Пневмоциты типа II встречаются чаще, составляя 60% клеток альвеолярного эпителия, но составляют только 3% альвеолярной поверхности. [15]
Существует несколько факторов, которые способствуют трансформации нормального альвеолярного эпителия в диспластические или предраковые поражения. Аденокарцинома легкого развивается поэтапно, поскольку пневмоциты типа II претерпевают последовательные молекулярные изменения, которые нарушают нормальную регуляцию и обмен клеток. Атипичная аденоматозная гиперплазия (ААГ) считается предраковым поражением и, как полагают, в дальнейшем прогрессирует до аденокарциномы in situ и инвазивной аденокарциномы легкого. Очаги ААГ имеют размер <5 мм, могут быть одиночными или множественными и на КТ имеют вид «матового стекла». По мере накопления большего количества генетических мутаций и нарушения регуляции сигнальных путей нормальных клеток ААГ может прогрессировать до аденокарциномы in situ (АИС). Поражения АИС классифицируются как небольшие опухоли <3 см с аномальным ростом клеток пневмоцитов II типа, который ограничен альвеолярным пространством, т.е. без инвазии в строму, плевру или сосудистую сеть. Этот тип роста называется «лепидным» и характерен для аденокарциномы легкого на самых ранних стадиях. [15]
Диагностика
[ редактировать ]Диагноз рака легких можно заподозрить на основании типичных симптомов , особенно у человека с историей курения. Такие симптомы, как кашель с кровью и непреднамеренная потеря веса, могут потребовать дальнейшего обследования, например, медицинской визуализации .
Классификация
[ редактировать ]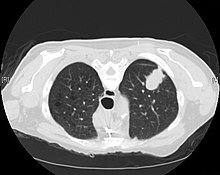
Большинство видов рака легких можно охарактеризовать как мелкоклеточный рак легких (МРЛ) или немелкоклеточный рак легких (НМРЛ). Аденокарцинома легких является одним из трех основных подтипов НМРЛ, которые также включают плоскоклеточный рак и крупноклеточный рак . [15]
Исторически сложилось так, что было много споров о наиболее точном методе описания аденокарциномы легкого, и было опубликовано несколько пересмотренных систем классификации. Совсем недавно, в 2011 году, была опубликована Международная междисциплинарная классификация аденокарциномы легких, которая представляет собой консенсус нескольких организаций по более точному описанию этого конкретного типа рака легких. [2] Существующая система классификации направлена на более надежное прогнозирование и определение терапевтического лечения. [4]
При классификации учитываются размер опухоли, характер роста клеток и глубина инвазии клеток в нормальную легочную ткань. Следующие названия представляют собой поэтапное патологическое прогрессирование естественного течения развития аденокарциномы; Аденокарцинома in situ (АИС), минимально инвазивная аденокарцинома (МИА) и инвазивная аденокарцинома. [15] Инвазивная аденокарцинома легкого включает гетерогенную смесь подтипов и вариантов.
Консенсус 2011 года описывает пять подтипов инвазивных аденокарцином на основе наиболее преобладающего клеточного рисунка. Эти подтипы описаны ниже:



- лепидный преобладает [18]
- ацинарный преобладает [19]
- папиллярный преобладающий [20]
- микропапиллярный преобладает [21]
- твердый преобладает с продукцией муцина [22]
Структура клеток, определяющая подтипы, связана с прогнозом: от благоприятного (лепидный) до промежуточного (ацинарный и папиллярный) и плохого (микропапиллярный и солидный). [2]
четыре дискретных варианта В текущую классификацию также включены инвазивных аденокарцином, не относящихся к этим пяти подтипам:
- инвазивная муцинозная аденокарцинома [23]
- коллоидная аденокарцинома [24]
- аденокарцинома плода [25]
- первичная легочная кишечная аденокарцинома [26] [4]
Визуализация
[ редактировать ]КТ обеспечивает лучшую оценку легких, имеет более высокую чувствительность и специфичность в отношении рака легких по сравнению с рентгенографией грудной клетки (хотя по-прежнему остается значительный процент ложноположительных результатов). [27] ). Компьютерная томография (КТ) , специально предназначенная для оценки рака легких, включает грудную клетку и верхнюю часть живота. Это позволяет оценить другие важные анатомические структуры, такие как близлежащие лимфатические узлы, надпочечники, печень и кости, которые могут свидетельствовать о метастатическом распространении заболевания. [4] Действительно, Рабочая группа по профилактическим услугам США рекомендует ежегодно проводить скрининг с помощью низкодозной КТ у взрослых в возрасте от 55 до 80 лет, которые имеют стаж курения 30 пачек лет и в настоящее время курят или бросили курить в течение последних 15 лет, с некоторыми оговорками (см . скрининг рака ). [28]
Визуализация ядерной медицины, такая как ПЭТ/КТ и сканирование костей , также может быть полезна для диагностики и обнаружения метастатического заболевания в других частях тела. [7] ПЭТ/КТ использует метаболически активный индикатор, который позволяет врачам выявлять области тела с гиперметаболизмом. Повышенное поглощение индикатора происходит в злокачественных клетках и областях воспаления или инфекции. Объединение изображений, отражающих метаболическую активность, с обычными КТ-изображениями обеспечивает более высокую чувствительность и специфичность по сравнению с только ПЭТ . [4]
МРТ предназначена для пациентов с запущенным заболеванием, при котором вероятно поражение внутричерепных структур или головного мозга. Это также полезно для оценки степени поражения грудной стенки, диафрагмы, плечевого сплетения (например, в случае опухолей верхней борозды ) или позвоночника. [4]
Гистопатология
[ редактировать ]Если возможно, биопсия любой подозреваемой опухоли легкого для микроскопической оценки пораженных клеток, что в конечном итоге необходимо для подтверждения диагноза. проводится [7] При отдаленных очагах сначала следует попытаться провести биопсию, чтобы установить гистологический диагноз и одновременно подтвердить стадию метастазирования. Материал биопсии также используется для анализа того, экспрессирует ли опухоль какие-либо специфические мутации, подходящие для таргетной терапии (например, мутация EGFR или мутация ALK). Биопсия может быть выполнена с помощью бронхоскопии, трансторакальной игольной биопсии и видеоторакоскопической хирургии (VATS). [4]
Хотя цитология мокроты, как было показано, имеет ограниченную полезность, торакоцентез или аспирацию плевральной жидкости с помощью иглы под ультразвуковым следует выполнять плеврального выпота при наличии контролем. Когда злокачественные клетки выявляются в плевральном аспирате у пациентов с высоким подозрением на рак легких, устанавливается окончательный диагноз и стадия (аденокарцинома легких IV стадии). [4]
Аденокарцинома легкого имеет тенденцию окрашивать муцин положительным, поскольку она происходит из продуцирующих слизь желез легких. Подобно другим аденокарциномам, если эта опухоль хорошо дифференцирована (низкая степень), она будет напоминать нормальную железистую структуру. Низкодифференцированная аденокарцинома не будет напоминать нормальные железы (высокая степень злокачественности) и будет обнаружена при положительном окрашивании на муцин (который производят железы). Аденокарциному также можно отличить по окрашиванию на TTF-1 , клеточный маркер аденокарциномы. [29]
Как обсуждалось ранее, категория аденокарциномы включает ряд подтипов, и любая опухоль имеет тенденцию быть гетерогенной по составу. Несколько основных подтипов в настоящее время признаны Всемирной организацией здравоохранения (ВОЗ). [1] и Международная ассоциация по изучению рака легких (IASLC)/ Американское торакальное общество (ATS)/ Европейское респираторное общество (ERS): [30] [31] [32] лепидная преобладающая аденокарцинома, ацинарная преобладающая аденокарцинома, папиллярная преобладающая аденокарцинома, микропапиллярная преобладающая аденокарцинома, солидная преобладающая аденокарцинома и солидная преобладающая аденокарцинома с продукцией муцина. В 80% этих опухолей будут распознаваться компоненты более чем одного подтипа. Опухоли, удаленные хирургическим путем, следует классифицировать с помощью комплексного гистологического подтипирования с описанием характера поражения с шагом 5%. Преобладающий гистологический подтип затем используется для классификации опухоли в целом. [2] Преобладающий подтип является прогностическим для выживания после полной резекции. [33]
Чтобы выявить аденокарциноматозную линию солидного варианта, можно продемонстрировать внутриклеточную продукцию муцина. Очаги плоскоклеточной метаплазии и дисплазии могут присутствовать в эпителии проксимальнее аденокарциномы, но они не являются предшественниками этой опухоли. Скорее, предшественник периферических аденокарцином был назван атипической аденоматозной гиперплазией (ААГ). [10] Микроскопически ААГ представляет собой хорошо отграниченный очаг пролиферации эпителия, содержащий клетки от кубической до низкостолбчатой формы, напоминающие булавовидные клетки или пневмоциты II типа . [10] Они демонстрируют различную степень цитологической атипии, включая гиперхромазию , плеоморфизм , выраженные ядрышки . [10] Однако атипия не столь выражена, как при явных аденокарциномах. [10] Поражения AAH являются моноклональными и имеют многие молекулярные аберрации (например, мутации KRAS ), которые связаны с аденокарциномами. [10]
Перстень с печаткой и светлоклеточная аденокарцинома больше не являются гистологическими подтипами, а скорее цитологическими особенностями, которые могут встречаться в опухолевых клетках нескольких гистологических подтипов, чаще всего солидной аденокарциномы. [30]
Уход
[ редактировать ]Лечение аденокарциномы легкого зависит от нескольких факторов, включая стадию , резектабельность, состояние здоровья , гистологию и геномные изменения, приобретенные отдельной опухолью. [34]
Операция
[ редактировать ]Аденокарциномы легких на ранних стадиях (I, II и IIIA) обычно лечат хирургическим путем с целью удаления опухоли с помощью пневмонэктомии или лобэктомии , если с помощью визуализирующих исследований и биопсии оказывается, что опухоль операбельна, и если пациент считается способным переносить хирургическое вмешательство. [10] Часто применяется видеоторакоскопическая хирургия (VATS), которая заключается во введении торакоскопа в небольшой разрез, сделанный на грудной клетке; долю можно удалить с помощью эндоскопа через этот небольшой разрез. [34]

Химиотерапия
[ редактировать ]При запущенных (стадия IV) и неоперабельных опухолях легких терапией первой линии является двойная химиотерапия на основе платины, сочетающая цисплатин или карбоплатин с другим цитотоксическим агентом. [3] Схемы сильно зависят от состояния здоровья и реакции каждого пациента, и когда риск нежелательных явлений может значительно ухудшить качество жизни, более рекомендуется базовая поддерживающая терапия. Химиотерапия также используется в качестве адъювантной терапии после операции для уничтожения оставшихся раковых клеток у пациентов с НМРЛ стадий IIA, IIB и IIIA. [34]
Лучевая терапия
[ редактировать ]Аденокарцинома — это немелкоклеточный рак легкого , который не так чувствителен к лучевой терапии по сравнению с мелкоклеточным раком легкого . [10] Однако лучевая терапия может использоваться в качестве адъювантной терапии для пациентов, перенесших резекционную операцию, чтобы снизить риск рецидива рака легких. Это также может принести пользу неоперабельным опухолям, локализованным в грудной клетке, и быть частью паллиативной помощи для улучшения качества жизни пациентов, не реагирующих на хирургическое вмешательство или химиотерапию. [34]
Таргетная терапия
[ редактировать ]Таргетная терапия доступна для аденокарцином легких с определенными молекулярными характеристиками. Ингибиторы тирозинкиназы (ИТК) были разработаны для воздействия на мутантные компоненты пути рецепторной тирозинкиназы, такие как EGFR, ALK. [36] и ROS1, которые демонстрируют частые изменения при аденокарциномах легких.
ИТК EGFR первого поколения, включая гефитиниб и эрлотиниб Было показано, что , более эффективны при лечении пациентов с мутацией EGFR по сравнению с цитотоксической химиотерапией. Ингибиторы второго поколения, такие как афатиниб и дакомитиниб, обеспечили более широкую сферу применения, поскольку они способны воздействовать не только на сам белок EGFR , но и на других членов семейства EGFR , таких как HER2 и HER4 (также известные как ERBB2 и ERBB4). и они показали лучшую выживаемость без прогрессирования заболевания по сравнению с гефитинибом. Поскольку наиболее распространенной причиной приобретенной устойчивости к ИТК первого поколения является вторая мутация EGFR в кодоне 790, был разработан ИТК EGFR третьего поколения, осимертиниб , также направленный на эту новую мутацию. [3] Амплификация МЕТ — еще один известный механизм приобретенной устойчивости. [2]
Ингибиторы ALK, такие как кризотиниб, оказались эффективными против опухолей, содержащих слитые ALK. Большинству пациентов, ранее получавших кризотиниб, были полезны ингибиторы АЛК второго поколения, включая церитиниб , алектиниб и бригатиниб . Устойчивость к ингибиторам ALK может возникнуть в результате новых приобретенных мутаций или амплификаций ALK. [3]
Также ROS1-положительные опухоли показали высокую чувствительность к ингибиторам ALK из-за высокой гомологии между киназными доменами ROS1 и ALK. [3]
Иммунотерапия
[ редактировать ]Ингибиторы иммунных контрольных точек были одобрены для лечения НМРЛ, включая ниволумаб против PD-1 и пембролизумаб . Агенты против PD-1 используются у пациентов с распространенным НМРЛ, у которых опухоли прогрессируют после цитотоксической химиотерапии первой линии. Пембролизумаб был признан новым стандартом лечения пациентов с распространенным или метастатическим НМРЛ с высоким уровнем экспрессии PD-L1, причем ответы еще более выражены для опухолей с высокой мутационной нагрузкой (т.е. с повышенным количеством мутаций). [3]
По состоянию на 2018 год терапевтические подходы, сочетающие несколько ингибиторов иммунных контрольных точек или один ингибитор иммунных контрольных точек и цитотоксический агент, проходят клинические испытания. [3] [37] Однако в исследовании III фазы KEYNOTE-598 в 2021 году сообщалось, что добавление ипилимумаба к пембролизумабу у пациентов с НМРЛ с показателем доли опухоли PD-L1 ≥50% не дает какого-либо преимущества в эффективности, но может привести к большей токсичности. [38] Также исследуется потенциальная роль анти-PD-1-агентов в качестве неоадъювантной терапии резектабельных НМРЛ. [39]
Эпидемиология
[ редактировать ]Что касается других подтипов рака легких, заболеваемость аденокарциномой легких тесно связана с курением.
За последние несколько десятилетий заболеваемость аденокарциномой легких росла во многих развитых западных странах, и по состоянию на 2012 год ее доля достигла 43,3% от всех случаев рака легких в США. [40] таким образом, заменив плоскоклеточный рак легких как наиболее распространенный тип рака легких. Во многом это можно объяснить снижением уровня курения, что благоприятствует гистологии аденокарциномы. Действительно, хотя курение по-прежнему является самым сильным фактором риска, аденокарцинома легких на сегодняшний день является наиболее распространенной среди некурящих в течение всей жизни (<100 сигарет в течение жизни). [41]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б Трэвис В.Д., Брамбилла Э., Мюллер-Гермелинк Х.К., Харрис CC, ред. (2004). Патология и генетика опухолей легких, плевры, тимуса и сердца (PDF) . Классификация опухолей Всемирной организации здравоохранения. Лион: МАИР Пресс. ISBN 978-92-832-2418-1 . Архивировано из оригинала (PDF) 23 августа 2009 г. Проверено 27 марта 2010 г.
- ^ Перейти обратно: а б с д и ж Трэвис В.Д., Брамбилла Э., Ногучи М., Николсон А.Г., Гейзингер К.Р., Ятабе Ю. и др. (февраль 2011 г.). «Международная ассоциация по изучению рака легких/Американское торакальное общество/Европейское респираторное общество, международная междисциплинарная классификация аденокарциномы легких» . Журнал торакальной онкологии . 6 (2): 244–285. дои : 10.1097/JTO.0b013e318206a221 . ПМЦ 4513953 . ПМИД 21252716 .
- ^ Перейти обратно: а б с д и ж г час я Хербст Р.С., Моргенштерн Д., Бошофф К. (январь 2018 г.). «Биология и лечение немелкоклеточного рака легких». Природа . 553 (7689): 446–454. Бибкод : 2018Natur.553..446H . дои : 10.1038/nature25183 . ПМИД 29364287 . S2CID 4463109 .
- ^ Перейти обратно: а б с д и ж г час я дж Фишман Дж.А., Котлофф Р., Гриппи М.А., Пак А.И., Старший Р.М., Элиас Дж.А. (14 апреля 2015 г.). Гриппи М.А. (ред.). Легочные заболевания и расстройства Фишмана . Макгроу-Хилл Образование. ISBN 9780071807289 . OCLC 898053564 .
- ^ Перейти обратно: а б Хорн Л., Пао В., Джонсон Д.Х. (2012). «Глава 89». В Лонго Д.Л., Каспер Д.Л., Джеймсон Дж.Л., Фаучи А.С., Хаузер С.Л., Лоскальцо Дж. (ред.). Принципы внутренней медицины Харрисона (18-е изд.). МакГроу-Хилл. ISBN 978-0-07-174889-6 .
- ^ Перейти обратно: а б «Признаки и симптомы немелкоклеточного рака легких» . Рак.орг . Американское онкологическое общество. 16 мая 2016 г. Проверено 11 марта 2018 г.
- ^ Перейти обратно: а б с «Тесты на немелкоклеточный рак легких» . Американское онкологическое общество. 23 июня 2017 г. Проверено 11 марта 2018 г.
- ^ Кенфилд С.А., Вэй Е.К., Стампфер М.Дж., Рознер Б.А., Кольдиц Г.А. (июнь 2008 г.). «Сравнение аспектов курения среди четырех гистологических типов рака легких» . Контроль над табаком . 17 (3): 198–204. дои : 10.1136/tc.2007.022582 . ПМК 3044470 . ПМИД 18390646 .
- ^ Трэвис В.Д., Трэвис Л.Б., Девеса С.С. (январь 1995 г.). «Рак легких». Рак . 75 (1 приложение): 191–202. doi : 10.1002/1097-0142(19950101)75:1+<191::AID-CNCR2820751307>3.0.CO;2-Y . ПМИД 8000996 . S2CID 221577784 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м Митчелл Р.С., Кумар В., Аббас А.К., Фаусто Н. (2007). «Глава 13, вставка о морфологии аденокарциномы». Основная патология Роббинса (8-е изд.). Филадельфия: Сондерс. ISBN 978-1-4160-2973-1 .
- ^ Перейти обратно: а б с Сеть исследований Атласа генома рака; и др. (июль 2014 г.). «Комплексное молекулярное профилирование аденокарциномы легких» . Природа . 511 (7511): 543–550. Бибкод : 2014Natur.511..543T . дои : 10.1038/nature13385 . ПМЦ 4231481 . ПМИД 25079552 .
- ^ Эллротт К., Бэйли М.Х., Саксена Г., Ковингтон К.Р., Кандот С., Стюарт С. и др. (март 2018 г.). «Масштабируемый открытый научный подход к вызову мутаций опухолевых экзомов с использованием нескольких геномных конвейеров» . Клеточные системы . 6 (3): 271–281.e7. дои : 10.1016/j.cels.2018.03.002 . ПМК 6075717 . ПМИД 29596782 .
- ^ «Рак легких» . Домашний справочник по генетике . Проверено 6 мая 2019 г.
- ^ «Легкие: транслокации при аденокарциноме» . Атлас генетики и цитогенетики в онкологии и гематологии .
- ^ Перейти обратно: а б с д Бруникарди (2014). Принципы хирургии Шварца (10-е изд.). МакГроу-Хилл. OCLC 941117341 .
- ^ Чен CL, Чен CC, Ю WH, Чен SH, Чанг YC, Сюй TI; и др. (2021). «Подход к патологической классификации типов рака легких без аннотаций с использованием глубокого обучения» . Нат Коммун . 12 (1): 1193. doi : 10.1038/s41467-021-21467-y . ПМЦ 7896045 . ПМИД 33608558 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )
- «Эта статья доступна по международной лицензии Creative Commons Attribution 4.0». - ^ Ли, Мэн; Ву, Нин; Чжан, Ли; Сунь, Вэй; Ван, Цзяньвэй; Льв, Льв; Рен, Цзяньсун; Линь, Дунмей (2017). «Патологический статус N0 при клинической аденокарциноме легкого T1N0M0 предсказуем по доле твердого компонента с помощью количественного анализа чисел КТ» . Научные отчеты . 7 (1). дои : 10.1038/s41598-017-16701-x . ISSN 2045-2322 . ПМК 5711838 .
- Международная лицензия Creative Commons с указанием авторства 4.0. - ^ Вираккоди, Юранга. «Аденокарцинома легкого с преобладанием лепидоза | Справочная статья по радиологии | Radiopaedia.org» . Радиопедия . Проверено 21 января 2022 г.
- ^ Вираккоди, Юранга. «Ацинарно-преобладающая аденокарцинома легкого | Справочная статья по радиологии | Radiopaedia.org» . Радиопедия . Проверено 21 января 2022 г.
- ^ Вираккоди, Юранга. «Папиллярно-преобладающая аденокарцинома легкого | Справочная статья по радиологии | Radiopaedia.org» . Радиопедия . Проверено 21 января 2022 г.
- ^ Муцио, Бруно Ди. «Микропапиллярная аденокарцинома легкого | Справочная статья по радиологии | Radiopaedia.org» . Радиопедия . Проверено 21 января 2022 г.
- ^ Муцио, Бруно Ди. «Солидно-преобладающая аденокарцинома легкого с продукцией муцина | Справочная статья по радиологии | Radiopaedia.org» . Радиопедия . Проверено 21 января 2022 г.
- ^ Вираккоди, Юранга. «Инвазивная муцинозная аденокарцинома легкого | Справочная статья по радиологии | Radiopaedia.org» . Радиопедия . Проверено 21 января 2022 г.
- ^ Вираккоди, Юранга. «Коллоидная аденокарцинома легкого | Справочная статья по радиологии | Radiopaedia.org» . Радиопедия . Проверено 21 января 2022 г.
- ^ Вираккоди, Юранга. «Аденокарцинома легких плода | Справочная статья по радиологии | Radiopaedia.org» . Радиопедия . Проверено 21 января 2022 г.
- ^ Вираккоди, Юранга. «Первичная легочная кишечная аденокарцинома | Справочная статья по радиологии | Radiopaedia.org» . Радиопедия . Проверено 21 января 2022 г.
- ^ Госснер Дж. (апрель 2014 г.). «Скрининг рака легких – не забудьте рентгенограмму грудной клетки» . Всемирный журнал радиологии . 6 (4): 116–118. дои : 10.4329/wjr.v6.i4.116 . ПМК 4000607 . ПМИД 24778773 .
- ^ Рабочая группа США по профилактическим услугам (декабрь 2016 г.). «Заключительная рекомендация: Рак легких: скрининг» . Проверено 10 марта 2018 г.
- ^ Всемирный доклад о раке, 2014 год . Всемирная организация здравоохранения. 2014. С. Глава 5.1. ISBN 978-9283204299 .
- ^ Перейти обратно: а б Ван Шил П.Е., Асамура Х., Раш В.В., Мицудоми Т., Цубои М., Брамбилла Э., Трэвис В.Д. (февраль 2012 г.). «Хирургические последствия новой классификации аденокарциномы IASLC/ATS/ERS» . Европейский респираторный журнал . 39 (2): 478–486. дои : 10.1183/09031936.00027511 . ПМИД 21828029 .
- ^ Трэвис В.Д., Брамбилла Э., Ван Шил П., Скальотти Г.В., Хубер Р.М., Скулиер Дж.П. и др. (август 2011 г.). «Сдвиги парадигмы рака легких, как это определено в новой классификации аденокарциномы легких IASLC/ATS/ERS» . Европейский респираторный журнал . 38 (2): 239–243. дои : 10.1183/09031936.00026711 . ПМИД 21804158 .
- ^ Васкес М., Картер Д., Брамбилла Е., Газдар А., Ногучи М., Трэвис В.Д. и др. (Исследователи Международной программы действий по раннему раку легких) (май 2009 г.). «Одиночные и множественные удаленные аденокарциномы после КТ-скрининга рака легких: гистопатологические особенности и их прогностическое значение» . Рак легких . 64 (2): 148–154. дои : 10.1016/j.lungcan.2008.08.009 . ПМЦ 2849638 . ПМИД 18951650 .
- ^ Рассел П.А., Вайнер З., Райт ГМ, Дэниелс М., Конрон М., Уильямс Р.А. (сентябрь 2011 г.). «Предсказывает ли подтип аденокарциномы легких выживаемость пациентов?: Клинико-патологическое исследование, основанное на новой международной междисциплинарной классификации аденокарциномы легких Международной ассоциации по изучению рака легких/Американского торакального общества/Европейского респираторного общества» . Журнал торакальной онкологии . 6 (9): 1496–1504. дои : 10.1097/JTO.0b013e318221f701 . ПМИД 21642859 . S2CID 26574271 .
- ^ Перейти обратно: а б с д Заппа С., Муса С.А. (июнь 2016 г.). «Немелкоклеточный рак легких: современное лечение и будущие достижения» . Трансляционное исследование рака легких . 5 (3): 288–300. дои : 10.21037/tlcr.2016.06.07 . ПМЦ 4931124 . ПМИД 27413711 .
- ^ Курильщики определяются как нынешние или бывшие курильщики со стажем более 1 года. См. страницу изображения в Commons, чтобы узнать проценты в числах. Ссылка:
- Таблица 2 в: Кенфилд С.А., Вэй Е.К., Стампфер М.Дж., Рознер Б.А., Кольдиц Г.А. (июнь 2008 г.). «Сравнение аспектов курения среди четырех гистологических типов рака легких» . Контроль над табаком . 17 (3): 198–204. дои : 10.1136/tc.2007.022582 . ПМК 3044470 . ПМИД 18390646 .
- ^ Арбор К.С., Рили Г.Дж. (февраль 2017 г.). «Диагностика и лечение киназо-положительного немелкоклеточного рака легких анапластической лимфомы» . Гематологические/онкологические клиники Северной Америки . 31 (1): 101–111. дои : 10.1016/j.hoc.2016.08.012 . ПМК 5154547 . ПМИД 27912826 .
- ^ Хеллманн, доктор медицинских наук, Чуляну Т.Е., Плужански А., Ли Дж.С., Оттерсон Г.А., Одижье-Валетт С. и др. (май 2018 г.). «Ниволумаб плюс ипилимумаб при раке легких с высокой мутационной нагрузкой опухоли» . Медицинский журнал Новой Англии . 378 (22): 2093–2104. дои : 10.1056/NEJMoa1801946 . ПМЦ 7193684 . ПМИД 29658845 .
- ^ Бойер М, Шендур М, Родригес-Абреу Д, Парк К, Ли Д.Х., Чичин И, Юмук П.Ф., Орланди Ф.Дж., Леал Т.А., Молинье О, Сопараттанапайсарн Н., Ланглебен А., Калифано Р., Медгясзай Б., Ся Т.С., Оттерсон Г.А., Сюй Л, Пиперди Б, Самкари А, Рек М (июль 2021 г.). «Пембролизумаб плюс ипилимумаб или плацебо при метастатическом немелкоклеточном раке легких с показателем доли опухоли PD-L1 ≥ 50%: рандомизированное двойное слепое исследование III фазы KEYNOTE-598» . Дж. Клин Онкол . 39 (20): 2327–2338. дои : 10.1200/jco.20.03579 . ПМИД 33513313 . S2CID 231754357 .
- ^ Форд П.М., Чафт Дж.Э., Смит К.Н., Анагносту В., Коттрелл Т.Р., Хеллманн, доктор медицинских наук и др. (май 2018 г.). «Неоадъювантная блокада PD-1 при резектабельном раке легких» . Медицинский журнал Новой Англии . 378 (21): 1976–1986. дои : 10.1056/NEJMoa1716078 . ПМК 6223617 . ПМИД 29658848 .
- ^ «Просмотрите таблицы и рисунки — Обзор статистики рака (CSR) SEER за 1975–2012 годы» . ПРОИДЧИК . Проверено 22 февраля 2019 г.
- ^ Гандара Д.Р., Хаммерман П.С., Сос М.Л., Лара П.Н., Хирш Ф.Р. (май 2015 г.). «Плоскоклеточный рак легкого: от геномики опухолей к терапии рака» . Клинические исследования рака . 21 (10): 2236–2243. дои : 10.1158/1078-0432.CCR-14-3039 . ПМЦ 4862209 . ПМИД 25979930 .