Болезнь базальных ганглиев
| Болезнь базальных ганглиев | |
|---|---|
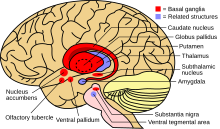 | |
| Базальные ганглии и родственные структуры | |
| Специальность | Неврология |
| Типы | 8 |
Заболевания базальных ганглиев — это группа физических проблем, которые возникают, когда группа ядер головного мозга, известная как базальные ганглии, не может должным образом подавить нежелательные движения или должным образом активировать цепи верхних мотонейронов для запуска двигательной функции. [1] Исследования показывают, что повышенная активность базальных ганглиев подавляет работу таламокортикальных проекционных нейронов . Правильная активация или деактивация этих нейронов является неотъемлемым компонентом правильного движения. Если что-то вызывает чрезмерную активность базальных ганглиев, то нейроны вентральной передней (VA) и вентральной латеральной (VL) таламокортикальной проекции становятся слишком заторможенными, и человек не может инициировать произвольные движения. Эти расстройства известны как гипокинетические расстройства . Однако нарушение, приводящее к аномально низкому выходному сигналу базальных ганглиев, приводит к снижению торможения и, следовательно, возбуждения таламокортикальных проекционных нейронов (VA и VL), которые образуют синапсы в коре. Такая ситуация приводит к невозможности подавить нежелательные движения. Эти расстройства известны как гиперкинетические расстройства. [2]
Причины аномального увеличения или уменьшения активности базальных ганглиев еще недостаточно изучены. Одним из возможных факторов может быть естественное накопление железа в базальных ганглиях, вызывающее нейродегенерацию из-за его участия в токсических реакциях со свободными радикалами . [3] Хотя двигательные расстройства чаще всего связаны с базальными ганглиями, недавние исследования показывают, что нарушения базальных ганглиев могут привести к другим дисфункциям, таким как обсессивно-компульсивное расстройство (ОКР) и синдром Туретта . [4]
Цепи базальных ганглиев
[ редактировать ]

Базальные ганглии — это коллективная группа структур головного мозга. К ним относятся полосатое тело (состоящее из скорлупы и хвостатого ядра ), бледный шар , черная субстанция и субталамическое ядро . Наряду с другими структурами, базальные ганглии являются частью нейронной цепи , которая является неотъемлемой частью произвольной двигательной функции. [1] Когда-то считалось, что основная функция базальных ганглиев заключалась в интеграции проекций из коры головного мозга и передаче информации через таламус в моторную кору . Исследования показали, что базальные ганглии можно смоделировать как группу компонентов параллельных реентерабельных корково-подкорковых цепей, которые берут начало в корковых областях, пересекают базальные ганглии и заканчиваются в определенных областях лобной доли. [4] Считается, что эти области контролируют не только двигательную функцию, но также глазодвигательные , префронтальные , ассоциативные и лимбические области. [2] Понимание этих цепей привело к прорыву в понимании заболеваний базальных ганглиев.
Прямой путь
[ редактировать ]Из всех цепей двигательная цепь является наиболее изученной из-за ее важности для двигательных нарушений. моторной Прямой путь цепи — это путь, при котором проекции из коры головного мозга направляются в скорлупу непосредственно во внутренний сегмент бледного шара (GPi, также известный как GP-Media) или в черную субстанцию , сетчатую часть (SNr), а затем направлен к вентральному переднему ядру (ВА), вентральному латеральному ядру таламуса (ВЛ) и ствола мозга. [2] [4] Посредством этого пути базальные ганглии способны инициировать произвольные движения, растормаживая нейроны таламуса, которые управляют верхними мотонейронами. [1] Этот процесс регулируется дофамином, секретируемым полосатым телом на дофаминовый рецептор D1 на SNc. Дофамин возбуждает нейроны полосатого тела по прямому пути. [5] Правильное высвобождение дофамина в полосатом теле является неотъемлемой частью подавления активности базальных ганглиев, которое необходимо для повышения активности нейронов таламуса. [2] Эта активность ядер таламуса является неотъемлемым компонентом произвольного движения.
Косвенный путь
[ редактировать ]двигательной Считается, что непрямой путь цепи проецируется из коры в скорлупу, а также в таламус и ствол мозга опосредованно, проходя через внешний сегмент бледного шара (GPe), затем через субталамическое ядро (STN), прежде чем вернуться обратно к внутренний сегмент бледного шара (GPi). [4] Косвенный путь отвечает за прекращение движения. Косвенный путь ингибирует нежелательные движения за счет одновременного увеличения возбуждающего воздействия на другие нейроны GPi и SNr. [4] Подобно прямому пути, непрямой путь регулируется дофамином полосатого тела. D2 Рецепторы дофамина ингибируют передачу непрямым путем. D2 Рецепторы ингибируют нейроны полосатого тела непрямым, тормозным путем. [5] Это ингибирующее действие дофамина на непрямой путь выполняет ту же функцию, что и его возбуждающее действие на прямой путь, заключающееся в уменьшении активности базальных ганглиев, что приводит к растормаживанию мотонейронов. [2]
Сопутствующие расстройства
[ редактировать ]Гипокинетические расстройства
[ редактировать ]Гипокинетические расстройства – это двигательные расстройства, которые характеризуются снижением двигательной функции. Обычно это объясняется более высокой, чем обычно, активностью базальных ганглиев, вызывающей торможение таламокортикальных мотонейронов.
паркинсонизм
[ редактировать ]Мышечная ригидность, тремор в покое и замедленность начала и выполнения движений, которые являются основными двигательными симптомами болезни Паркинсона, объясняются снижением дофаминергической активности в двигательных областях базальных ганглиев, особенно скорлупы, из-за постепенного снижения иннервации от компактная часть черной субстанции. [6] Считается, что другие двигательные дефициты и общие немоторные особенности болезни Паркинсона, такие как вегетативная дисфункция, когнитивные нарушения и трудности с походкой/балансом, являются результатом широко распространенных прогрессирующих патологических изменений, начинающихся в нижних отделах ствола мозга и поднимающихся к среднему мозгу, миндалевидному телу, таламусу и в конечном итоге кора головного мозга. [4]
Гиперкинетические расстройства
[ редактировать ]Гиперкинетические расстройства – двигательные расстройства, характеризующиеся усилением неконтролируемой двигательной функции. Они вызваны снижением активности базальных ганглиев, что вызывает усиление таламокортикальной функции, что приводит к неспособности остановить нежелательные движения.
болезнь Хантингтона
[ редактировать ]Болезнь Хантингтона — наследственное заболевание, вызывающее дефекты поведения, когнитивных функций и неконтролируемые быстрые, судорожные движения. [1] Болезнь Хантингтона возникает из-за дефекта, который состоит из расширенного повтора CAG в гене хантингтина (HTT), расположенном на коротком плече p хромосомы 4 . [7] Данные показывают, что в базальных ганглиях у пациентов с болезнью Хантингтона наблюдается снижение активности митохондриального пути , комплекса II-III. Такие недостатки часто связаны с дегенерацией базальных ганглиев. [8] Эта дегенерация нейронов полосатого тела, проецирующихся на GPe, приводит к растормаживанию непрямого пути, усилению торможения субталамического ядра и, следовательно, к снижению продукции базальных ганглиев. [2] Дегенерация нейронов в конечном итоге приводит к смерти в течение 10–20 лет.
Дистония
[ редактировать ]Дистония — это гиперкинетическое двигательное расстройство, которое характеризуется непроизвольными движениями и замедлением преднамеренных движений. Хотя известны причины дистонии, такие как метаболические, сосудистые и структурные нарушения, все еще встречаются пациенты с дистонией без видимой причины. Дистония может возникать как гиперкинетическое расстройство или как побочный эффект гипокинетических расстройств, таких как болезнь Паркинсона. [9] До недавнего времени считалось, что дистония, вероятно, вызвана крайним нарушением функции прямого пути между скорлупой и GPi. Опять же, считалось, что эта дисфункция приводит к уменьшению активности базальных ганглиев в таламусе и, как следствие, к усилению растормаживания таламических проекций в премоторную и моторную кору. [10] Однако недавние модели на мышах показывают, что дисфункция мозжечка может играть равную роль в дистонии. [11]
гемибаллизм
[ редактировать ]Гемибаллизм – это гиперкинетическое двигательное расстройство, вызывающее неконтролируемые движения одной стороны тела. Обычно это вызвано повреждением субталамического ядра (STN). Поскольку внутренний сегмент бледного шара (GPi) является связующим звеном в цепи между STN и таламической проекцией, разрушение локализованных клеток мозга в GPi посредством паллидотомии оказалось полезным средством лечения гемибализма. [9]
Другие заболевания базальных ганглиев
[ редактировать ]Следующие заболевания, которые обычно поражают базальные ганглии, не относятся ни к гипо-, ни к гиперкинетическим заболеваниям.
Эпилепсия
[ редактировать ]Черная субстанция pars reticulata и ее прямая входная структура, субталамическое ядро, играют роль в схеме распространения приступов и были описаны как ядра, закрывающие приступ. Ингибирование этих ядер подавляет судороги в различных экспериментальных моделях эпилепсии. У пациентов с судорогами наблюдается ненормальная электрофизиологическая активность и структурные изменения, такие как атрофия, изменение перфузии крови и метаболизма в базальных ганглиях. В нескольких отчетах о клинических случаях описывается, что глубокая стимуляция субталамического ядра мозга оказалась успешной в уменьшении приступов. Другие подходы к таргетному лечению ограничивались экспериментальными условиями и включали местные инфузии лекарств и трансплантацию клеток. [12]
Синдром Туретта/обсессивно-компульсивное расстройство
[ редактировать ]Синдром Туретта — расстройство, которое характеризуется поведенческими и двигательными тиками, ОКР и синдромом дефицита внимания и гиперактивности (СДВГ). По этой причине принято считать, что вероятны патологии, затрагивающие лимбический, ассоциативный и моторный контуры базальных ганглиев. С момента осознания того, что такие синдромы, как синдром Туретта и ОКР, вызваны дисфункцией немоторных петель базальных ганглиев, разрабатываются новые методы лечения этих расстройств, основанные на методах лечения, первоначально предназначенных для лечения двигательных расстройств. [4]
хорея Сиденхема
[ редактировать ]Хорея Сиденхема — заболевание, характеризующееся быстрыми, нескоординированными подергиваниями, поражающими преимущественно лицо, руки и ноги. [13] Это результат аутоиммунного ответа, возникающего после заражения β-гемолитическим стрептококком группы А (БГСА). [14] разрушает клетки полосатого тела базальных ганглиев . [15] [14] [16]
ПАНДА
[ редактировать ]PANDAS представляет собой спорную гипотезу о том, что существует подгруппа детей с быстрым началом обсессивно-компульсивного расстройства (ОКР) или тиковых расстройств и что эти симптомы вызваны инфекциями β-гемолитического стрептококка группы А (БГСА). [17] [18] [19] Предполагаемая связь между инфекцией и этими расстройствами заключается в том, что первоначальная аутоиммунная реакция на инфекцию GABHS вырабатывает антитела, которые нарушают функцию базальных ганглиев , вызывая обострение симптомов. Было высказано предположение, что этот аутоиммунный ответ может привести к широкому спектру нейропсихиатрических симптомов. [20] [21]
Дискинетический церебральный паралич
[ редактировать ]Дискинетический детский церебральный паралич — разновидность детского церебрального паралича, связанная преимущественно с поражением базальных ганглиев в виде поражений , возникающих в процессе развития головного мозга вследствие билирубиновой энцефалопатии и гипоксически-ишемического головного мозга . поражения [22] Симптомы включают медленные, неконтролируемые движения конечностей и туловища. [23] и небольшие, быстрые, случайные и повторяющиеся, неконтролируемые движения, известные как хорея . [24] Непроизвольные движения часто усиливаются в периоды эмоционального напряжения или волнения и исчезают, когда больной спит или отвлекается. [24]
Атимгормический синдром
[ редактировать ]Атимгормический синдром — редкий психопатологический и неврологический синдром, характеризующийся крайней пассивностью, апатией , притуплением аффекта и глубокой генерализованной потерей самомотивации. Считается, что синдром возникает из-за повреждения областей базальных ганглиев или лобной коры , в частности полосатого тела и бледного шара , ответственных за мотивацию и исполнительные функции. [25]
Синдром Леша-Нихана
[ редактировать ]Синдром Леша-Нихана — редкое Х-сцепленное рецессивное заболевание, вызванное дефицитом фермента гипоксантин -гуанинфосфорибозилтрансферазы (HGPRT), что приводит к мочевой кислоты и дефициту продукции дофамина. накоплению [26] В течение первых нескольких лет жизни экстрапирамидное поражение вызывает аномальные непроизвольные сокращения мышц, такие как потеря двигательного контроля ( дистония ), корчи ( хореоатетоз ) и выгибание позвоночника ( опистотонус ). Сходство с дискинетическим церебральным параличом очевидно, и в результате у большинства людей первоначально диагностируется церебральный паралич. Психологическое поведение может включать отказ от желаемых угощений или путешествий, ответную благодарность за доброту холодностью или гневом, неспособность правильно ответить на вопросы теста, несмотря на учебу и желание добиться успеха, или провоцирование гнева со стороны лиц, осуществляющих уход, когда ласка желательна. [27]
болезнь Вильсона
[ редактировать ]Болезнь Вильсона — это аутосомно-рецессивное генетическое заболевание, вызванное мутацией гена транспорта меди ATP7B , что приводит к избыточному накоплению меди. Около половины заболевших имеют неврологические симптомы, включая паркинсонизм (чаще всего ригидность зубчатого колеса , брадикинезию или замедление движений и отсутствие равновесия). [28] с типичным тремором рук или без него , замаскированной мимикой, невнятной речью, атаксией или дистонией . [29]
Болезнь Фара и кальцификаты
[ редактировать ]Болезнь Фара — редкое, генетически доминантное , наследственное неврологическое заболевание, характеризующееся аномальными отложениями кальция , преимущественно в базальных ганглиях . [30] Около 0,3–1,5% людей имеют бессимптомную кальцификацию базальных ганглиев . [31]
Блефароспазм
[ редактировать ]Блефароспазм – это любое аномальное сокращение или подергивание века. Блефароспазм может возникнуть из-за аномального функционирования базальных ганглиев головного мозга. [32]
Исследовать
[ редактировать ]Генная терапия
[ редактировать ]Многие нарушения базальных ганглиев обусловлены дисфункцией локализованного участка. По этой причине генная терапия кажется жизнеспособной при нейродегенеративных заболеваниях. Генная терапия проводится путем замены больных фенотипов новым генетическим материалом. Этот процесс все еще находится на ранних стадиях, но первые результаты обнадеживают. Примером такой терапии может быть имплантация клеток, генетически модифицированных для экспрессии тирозингидроксилазы, которая в организме может превращаться в дофамин. Повышение уровня дофамина в базальных ганглиях может компенсировать последствия болезни Паркинсона. [1]
Абляция
[ редактировать ]Поражение — это преднамеренное разрушение нейрональных клеток в определенной области, используемое в терапевтических целях. Хотя это кажется опасным, у пациентов с двигательными расстройствами были достигнуты значительные улучшения. [33] Точный процесс обычно включает одностороннее поражение сенсомоторной территории GPi. Этот процесс называется паллидотомией . Считается, что успех паллидотомии в уменьшении последствий двигательных расстройств может быть результатом прерывания аномальной активности нейронов в GPi. Эту технику абляции можно рассматривать как простое удаление неисправного участка цепи. После удаления поврежденного участка цепи здоровый участок цепи может продолжать нормально функционировать. [9]
Глубокая стимуляция мозга
[ редактировать ]Глубокая стимуляция мозга включает в себя введение электродов с помощью стереотаксической хирургии в сенсомоторную область мозга. [1] [4] Эти электроды излучают высокочастотную стимуляцию имплантированных областей. [4] Двусторонняя имплантация необходима для получения симметричных результатов, а также для возможности уменьшения интенсивности и продолжительности периодов отдыха, а также увеличения продолжительности периодов включения. [1] [4] Наиболее эффективными структурами, используемыми для имплантации для глубокой стимуляции мозга, являются внутренний бледный шар (GPi) и субталамическое ядро (STN). Это связано с тем, что безопаснее и эффективнее изменить влияние базальных ганглиев на ядра таламокортика, чем напрямую изменять нейронную активность в цепях верхних мотонейронов . [1] Глубокая стимуляция мозга — более сложный процесс, чем другие методы лечения, такие как абляция. Имеющиеся данные свидетельствуют о том, что преимущества глубокой стимуляции мозга STN обусловлены активацией эфферентов и модуляцией паттернов разрядов в GPi, которые распространяются по таламокортикальным путям. [4] Возможность корректировки протоколов стимуляции позволяет использовать этот метод лечения при различных расстройствах благодаря его способности изменять активность цепей базальных ганглиев. [1]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час я Первс, Д.; Августин, Г.; Фитцпатрик, Д.; Холл, В.; ЛаМанита, А.-С.; Макнамара, Дж.; и др. (2008). Нейронаука (4-е изд.). Сандерленд, Массачусетс: Sinauer Associates.
- ^ Jump up to: а б с д и ж Вичманн Т., Делонг М.Р. (декабрь 1996 г.). «Функциональные и патофизиологические модели базальных ганглиев». Курс. Мнение. Нейробиол . 6 (6): 751–8. дои : 10.1016/S0959-4388(96)80024-9 . ПМИД 9000030 . S2CID 30435859 .
- ^ Кертис А.Р., Фей С., Моррис С.М. и др. (август 2001 г.). «Мутация в гене, кодирующем легкий полипептид ферритина, вызывает доминантное заболевание базальных ганглиев у взрослых». Нат. Жене . 28 (4): 350–4. дои : 10.1038/ng571 . ПМИД 11438811 . S2CID 25483839 .
- ^ Jump up to: а б с д и ж г час я дж к Делонг М.Р., Вичманн Т. (январь 2007 г.). «Цепи и нарушения контуров базальных ганглиев» . Арх. Нейрол . 64 (1): 20–4. дои : 10.1001/archneur.64.1.20 . ПМИД 17210805 .
- ^ Jump up to: а б Намбу А. (декабрь 2008 г.). «Семь проблем по базальным ганглиям». Курс. Мнение. Нейробиол . 18 (6): 595–604. дои : 10.1016/j.conb.2008.11.001 . ПМИД 19081243 . S2CID 24956799 .
- ^ Хайнц Штайнер; Куэй Ю. Ценг (4 января 2010 г.). Справочник по структуре и функциям базальных ганглиев . Академическая пресса. п. 663. ИСБН 978-0-12-374767-9 . Проверено 20 апреля 2012 г.
- ^ Уокер, Ф.О. (20 января 2007 г.). «Болезнь Хантингтона». Ланцет . 369 (9557): 218–28. дои : 10.1016/S0140-6736(07)60111-1 . ПМИД 17240289 . S2CID 46151626 .
- ^ Бил М.Ф. (август 1998 г.). «Митохондриальная дисфункция при нейродегенеративных заболеваниях» . Биохим. Биофиз. Акта . 1366 (1–2): 211–23. дои : 10.1016/s0005-2728(98)00114-5 . ПМЦ 3422529 . ПМИД 9714810 .
- ^ Jump up to: а б с Витек Дж.Л., Чоккан В., Чжан Дж.Ю. и др. (июль 1999 г.). «Нейрональная активность базальных ганглиев у больных генерализованной дистонией и гемибаллизмом». Энн. Нейрол . 46 (1): 22–35. doi : 10.1002/1531-8249(199907)46:1<22::AID-ANA6>3.0.CO;2-Z . ПМИД 10401777 . S2CID 422281 .
- ^ Янавс Дж.Л., Аминофф М.Ю. (октябрь 1998 г.). «Дистония и хорея при приобретенных системных заболеваниях» . Дж. Нейрол. Нейрохирургия. Психиатрия . 65 (4): 436–45. дои : 10.1136/jnnp.65.4.436 . ПМК 2170280 . ПМИД 9771763 .
- ^ Нейчев В.К., Фан Х, Митев В.И., Хесс Э.Дж., Джинна Х.А. (сентябрь 2008 г.). «Базальные ганглии и мозжечок взаимодействуют при выражении дистонических движений» . Мозг . 131 (Часть 9): 2499–509. дои : 10.1093/brain/awn168 . ПМК 2724906 . ПМИД 18669484 .
- ^ Брёр, Соня (2020). «Не часть височной доли, но все еще имеет значение? Черная субстанция и субталамическое ядро при эпилепсии» . Границы системной нейронауки . 14 : 581826. дои : 10.3389/fnsys.2020.581826 . ISSN 1662-5137 . ПМЦ 7768985 . ПМИД 33381016 .
- ^ «Информационная страница Сиденхемской хореи». Архивировано 22 июля 2010 г. в Wayback Machine Saint Vitus Dance, ревматический энцефалит из Национального института неврологических расстройств и инсульта. По состоянию на 26 апреля 2008 г.
- ^ Jump up to: а б Симптомы хореи Сиденхэма . Доступ 24 сентября 2009 г. Архивировано 18 апреля 2008 г. в Wayback Machine.
- ^ Сведо С.Е., Леонард Х.Л., Шапиро М.Б. (1993). «Хорея Сиденхэма: физические и психологические симптомы танца Святого Витта». Педиатрия . 91 (4): 706–713. ПМИД 8464654 .
- ^ Фаустино П.С., Террери М.Т., Роша А.Дж. и др. (2003). «Клинические, лабораторные, психиатрические и магнитно-резонансные данные у больных хореей Сиденгама». Нейрорадиология . 45 (7): 456–462. дои : 10.1007/s00234-003-0999-8 . ПМИД 12811441 . S2CID 23605799 .
- ^ Уилбур С., Битнун А., Кроненберг С., Лаксер Р.М., Леви Д.М., Логан В.Дж., Шоулдис М., Йе Е.А. (май 2019 г.). «ПАНДЫ/ПАНЫ в детстве: Споры и доказательства» . Педиатр по здоровью детей . 24 (2): 85–91. дои : 10.1093/pch/pxy145 . ПМК 6462125 . ПМИД 30996598 .
- ^ Сигра С, Хессельмарк Е, Бежеро С (март 2018 г.). «Лечение PANDAS и PANS: систематический обзор» . Neurosci Biobehav Rev. 86 : 51–65. doi : 10.1016/j.neubiorev.2018.01.001 . ПМИД 29309797 . S2CID 40827012 .
- ^ Моретти Дж., Паскини М., Мандарелли Дж., Тарситани Л., Бионди М. (2008). «Что должен знать каждый психиатр о ПАНДАХ: обзор» . Clin Pract Epidemiol Ment Health . 4 (1): 13. дои : 10.1186/1745-0179-4-13 . ПМК 2413218 . ПМИД 18495013 .
- ^ де Оливейра СК, Пелайо CF (март 2010 г.). «Детские аутоиммунные нервно-психические расстройства, связанные со стрептококковой инфекцией (PANDAS): спорный диагноз». Curr Infect Dis Rep . 12 (2): 103–9. дои : 10.1007/s11908-010-0082-7 . ПМИД 21308506 . S2CID 30969859 .
- ^ Буало Б (2011). «Обзор обсессивно-компульсивного расстройства у детей и подростков» . Диалоги Клин Неврологии . 13 (4): 401–11. doi : 10.31887/DCNS.2011.13.4/bboileau . ПМЦ 3263388 . ПМИД 22275846 .
- ^ Хоу, М; Чжао, Дж; Ю, Р (2006). «Последние достижения в области дискинетического церебрального паралича» (PDF) . Мировой журнал педиатров . 2 (1): 23–28. Архивировано из оригинала (PDF) 4 марта 2016 г. Проверено 29 января 2020 г.
- ^ «Атетоидный дискинетик» . Своп, Роданте, Пенсильвания . Проверено 31 октября 2012 г.
- ^ Jump up to: а б Хоу, М; Чжао, Дж; Ю, Р (2006). «Последние достижения в области дискинетического церебрального паралича» (PDF) . Мировой журнал педиатров . 2 (1): 23–28. Архивировано из оригинала (PDF) 4 марта 2016 г. Проверено 29 января 2020 г.
- ^ Богославский Ю.; Каммингс, Дж. Л. (2000). Расстройства поведения и настроения при очаговых поражениях головного мозга . Издательство Кембриджского университета. ISBN 9780521774826 .
- ^ Синдром Леша-Нихана. Домашний справочник по генетике. Проверено 24 мая 2007 г.
- ^ Гуальтьери, К. Томас (2002). Черепно-мозговая травма и умственная отсталость: психофармакология и нейропсихиатрия , с. 257. Липпинкотт Уильямс и Уилкинс. ISBN 0-7817-3473-8 . [1]
- ^ Лоринц М.Т. (2010). «Неврологическая болезнь Вильсона» (PDF) . Анналы Нью-Йоркской академии наук . 1184 (1): 173–87. Бибкод : 2010NYASA1184..173L . дои : 10.1111/j.1749-6632.2009.05109.x . hdl : 2027.42/78731 . ПМИД 20146697 . S2CID 2989668 .
- ^ Ала А., Уокер А.П., Ашкан К., Дули Дж.С., Шильски М.Л. (2007). «Болезнь Вильсона». Ланцет . 369 (9559): 397–408. дои : 10.1016/S0140-6736(07)60196-2 . ПМИД 17276780 . S2CID 24663871 .
- ^ «Синдром Шавани-Брюнеса» . Архивировано из оригинала 11 мая 2009 г. Проверено 13 июня 2009 г.
- ^ Верулашвили ИВ, Глонти ЛШ, Миминошвили ДК, Мания МН, Мдивани КС (2006). «[Кальцификация базальных ганглиев: клинические проявления и диагностическая оценка]». Грузинские Мед Новости (на русском языке) (140): 39–43. ПМИД 17179586 .
- ^ «Доброкачественный эссенциальный блефароспазм» . НОРД (Национальная организация по редким заболеваниям) . Проверено 29 января 2020 г.
- ^ Барон М.С., Витек Дж.Л., Бакай Р.А. и др. (сентябрь 1996 г.). «Лечение прогрессирующей болезни Паркинсона путем задней паллидотомии GPi: результаты пилотного исследования за 1 год». Энн. Нейрол . 40 (3): 355–66. дои : 10.1002/ana.410400305 . ПМИД 8797525 . S2CID 10245634 .