Нейродегенерация, связанная с пантотенаткиназой
| Нейродегенерация, связанная с пантотенаткиназой | |
|---|---|
| Другие имена | Нейродегенерация с накоплением железа в мозге 1 |
 | |
| Пантен | |
| Специальность | Неврология |
| Симптомы | Дистония, паркинсонизм, деменция |
| Обычное начало | До 10 лет (классический), Более 10 лет (атипичный) |
| Типы | Классический, нетипичный |
| Причины | PANK2 Мутация |
| Частота | 1–3 на 1 миллион человек |
Пантотенат-киназа-ассоциированная нейродегенерация ( PKAN ), ранее называемая синдромом Халлервордена-Шпатца, [1] Это генетическое дегенеративное заболевание головного мозга , которое может привести к паркинсонизму , дистонии , слабоумию и, в конечном итоге, к смерти. Нейродегенерация при ПКАН сопровождается избытком железа , которое постепенно накапливается в мозге.
PKAN вызван потерей функции фермента PANK2 из-за биаллельных генетических мутаций . Это следует за аутосомно-рецессивным наследованием. Этот фермент является первым шагом на пути превращения витамина B5 в коэнзим А. В настоящее время не существует методов лечения, которые изменяют течение заболевания, хотя существует ряд лекарств и методов лечения, которые могут помочь улучшить симптомы, и ведутся активные исследования методов лечения. [2]
Признаки и симптомы
[ редактировать ]Симптомы обычно начинаются в детстве и прогрессируют, часто приводя к смерти в раннем взрослом возрасте. Симптомы ПКАН начинаются до среднего детства и чаще всего наблюдаются в возрасте до десяти лет. Симптомы включают в себя: [ нужна ссылка ]
- дистония (повторяющиеся неконтролируемые сокращения мышц, которые могут вызывать подергивания или скручивания определенных групп мышц)
- дисфагия и дизартрия из-за вовлечения групп мышц, участвующих в речи
- ригидность /жесткость конечностей
- тремор
- извивающиеся движения
- деменция
- спастичность
- слабость
- судороги (редко)
- ходьба на цыпочках
- Пигментный ретинит человека , еще одно дегенеративное заболевание, поражающее сетчатку , часто вызывающее изменение цвета сетчатки и прогрессирующее ухудшение состояния сетчатки, сначала вызывающее куриную слепоту , а затем приводящее к полной потере зрения.
У 25% людей наблюдается нехарактерная форма ПКАН, которая развивается после 10 лет и имеет более медленный и постепенный темп ухудшения, чем у детей до 10 лет. Эти люди сталкиваются со значительными нарушениями речи, а также психическими и поведенческими нарушениями. [ нужна ссылка ]
Будучи прогрессирующим дегенеративным заболеванием нервов, ПКАН приводит к ранней обездвиженности и часто к смерти в раннем взрослом возрасте. Смерть наступает преждевременно из-за таких инфекций, как пневмония, и само по себе заболевание технически не ограничивает жизнь. [ нужна ссылка ]
Генетика
[ редактировать ]ПКАН является аутосомно- рецессивным заболеванием. Оба родителя больного ребенка должны быть гетерозиготными носителями заболевания и, следовательно, нести один мутантный аллель . Поскольку это аутосомное заболевание, у гетерозиготных людей по этому заболеванию могут не проявляться какие-либо атипичные характеристики, которые считаются указывающими на заболевание, однако сообщалось о случаях сложной гетерозиготности, при которых у гетерозиготных людей действительно развивается классическая форма заболевания. [3] [4]
Заболевание вызвано мутантным геном PANK2, расположенным в хромосомном локусе : 20p13-p12.3. PANK2 отвечает за кодирование белка пантотенаткиназы 2. PANK2 кодирует фермент пантотенаткиназы, а мутации в гене приводят к врожденной ошибке метаболизма витамина B5 (пантотената). Витамин B5 необходим для производства кофермента А в клетках. Нарушение работы этого фермента влияет на энергетический и липидный обмен и может привести к накоплению потенциально вредных соединений в мозге, включая железо. [ нужна ссылка ]
PANK2 кодирует транскрипт размером 1,85 КБ, который происходит из семи экзонов, покрывающих общую длину геномной ДНК примерно 3,5 МБ. Ген PANK2 также кодирует белок массой 50,5 кДа, который является функциональной пантотенаткиназой , важным регуляторным ферментом биосинтеза кофермента А (КоА) и катализирует фосфорилирование пантотената ( витамина B 5 ), N-пантотеноилцистеина и пантетеина ( ОМИМ).
Мутантные белки, кодируемые геном PANK2, часто возникают в результате нулевых или миссенс-мутаций, в первую очередь делеции 7 п.о. в последовательности, кодирующей ген PANK2 . [ нужна ссылка ]
Об этом расстройстве сообщалось в определенных сообществах, основанных на внутриобщинных браках, где оба родителя ребенка являются носителями одной и той же мутации. Одной из сообщенных общин является община Агравал (Агарвал), которая в основном базируется в северной части Индии. Известная мутация в сообществе Агарвал — это патогенная мутация 1c.215_216insA в гене PANK2. В некоторых лабораториях это также кодируется как chr20:3870292-3870293insA. Это приводит к сдвигу рамки считывания и преждевременному усечению белка на 47 аминокислот ниже кодона 183 (p.Arg183GlufsTer47; ENST00000316562). [5] [6]
Диагностика
[ редактировать ]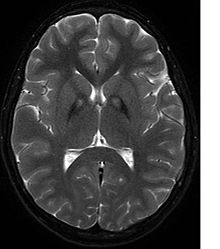
Неврологическое обследование покажет признаки мышечной ригидности; слабость; а также ненормальные позы, движения и тремор. Если другие члены семьи также поражены, это может помочь определить диагноз. Генетические тесты могут подтвердить аномальный ген, вызывающий заболевание. Однако этот тест еще не получил широкого распространения. Необходимо исключить другие двигательные расстройства и заболевания. Людей, у которых проявляются какие-либо из перечисленных выше симптомов, часто проверяют с помощью МРТ (магнитно-резонансной томографии) на ряд нервных расстройств. МРТ обычно показывает отложения железа в базальных ганглиях . Разработка диагностических критериев продолжается в надежде на дальнейшее отделение ПКАН от других форм нейродегенеративных заболеваний, сопровождающихся НБИА. [ нужна ссылка ]
Невропатология
[ редактировать ]Микроскопические признаки ПКАН включают высокий уровень железа в бледном шаре и сетчатой части черной субстанции , что проявляется в характерном ржаво-коричневом цвете. [7] в узоре, называемом знаком «глаз тигра»; [8] липофусцин и нейромеланин концентрируются в зонах накопления железа; овальные, безъядерные структуры, представляющие собой опухшие аксоны, цитоплазма которых набухает с вакуолями , называемые сфероидами , аксонными схолленами или нейроаксональной дистрофией ; и тела Леви . [7]
Уход
[ редактировать ]Было показано, что фосфопантотенат лечит ПКАН у человека, замедляя его прогрессирование, а также на мышиной модели заболевания от ПКАН не существует лекарства. Пантетин (предшественник пантетеина ) был изучен и показал свою эффективность на мышах и на плодовых мушках . модели заболевания [9] [10] [11]
Прогноз
[ редактировать ]Выживаемость пациентов с диагнозом типичной ПКАН, оставшихся без лечения, составляет 11,18 года со стандартным отклонением 7,8 года. Было проведено исследование, в котором сообщалось о хороших результатах у одного пациента с поздним началом ПКАН. [10]
Эпидемиология
[ редактировать ]Данные о распространенности этого расстройства остаются неполными, однако, по оценкам, от 1 из 1 000 000 до 3 из 1 000 000 человек будут страдать этим расстройством (на основе наблюдаемых случаев в популяции), но, опять же, это только оценка, поскольку заболевание настолько редок, что его трудно установить статистически и точно. [ нужна ссылка ]
История
[ редактировать ]ПКАН был впервые описан Халлерворденом и Спатцем (1922). Их открытие было связано с диагнозом семьи из 12 человек, в которой у пяти сестер наблюдалась прогрессирующая деменция и дизартрия. Вскрытие выявило коричневые изменения цвета в различных областях мозга (особенно интерес представляли области бледного шара и черной субстанции). Дальнейшее исследование и описание были проведены Мейером (1958), который диагностировал 30 отдельных случаев ПКАН. За Мейером (1958) последовали Elejalde et al. (1978), который описал 5 затронутых членов семьи и предположил, что расстройство возникло в Центральной Европе , подкрепив свою гипотезу клиническим и генетическим анализом. Дальнейшие исследования и выводы были предоставлены Мальмстремом-Гротом и Кристенсоном (1982). [12] и Янкович и др. (1985). [13]
Диагностика ПКАН стала важной вехой благодаря доступности МРТ, а также подробным описаниям этих МРТ, предоставленным Литтрупом и Гебарски (1985). [14] Танфани и др. (1987), [15] Сети и др. (1988), [16] Анджелини и др. (1992), [17] Кастелс и др. (1994), [18] и Маландрини и др. (1995). [19] Ген был локализован в хромосоме 20p Taylor et al. (1996) [20] который предложил называть это расстройство нейродегенерацией с накоплением железа в мозге (NBIA1), чтобы избежать нежелательного эпонима. [21] Халлерворден-Шпац. Заболевание было переименовано Zhou et al. в «нейродегенерацию, связанную с пантотенаткиназой» или PKAN. (2001) [3] который предложил это название, чтобы избежать неправильного толкования и лучше отразить истинную природу расстройства. Совсем недавно Pellecchia et al. (2005) опубликовали отчет о 16 пациентах с ПКАН, подтвержденный генетическим анализом. [22]
Ссылки
[ редактировать ]- ^ Харпер, Питер С. (1996). «Именование синдромов и неэтичных действий: дело Халлервордена и Спатца». Ланцет . 348 (9036): 1224–1225. дои : 10.1016/S0140-6736(96)05222-1 . ISSN 0140-6736 . ПМИД 8898043 . S2CID 11594905 .
- ^ Сполл, Роберт В.В.; Су, Одри КС; Хогарт, Пенелопа; Хейфлик, Сьюзен Дж.; Куриан, Манджу А. (24 ноября 2021 г.). «На пути к прецизионной терапии наследственных заболеваний нейродегенерации с накоплением железа в мозгу» . Тремор и другие гиперкинетические движения . 11 (1): 51. дои : 10,5334/том.661 . ПМЦ 8641530 . ПМИД 34909266 .
- ^ Jump up to: а б Чжоу Б., Вестэуэй С.К., Левинсон Б., Джонсон М.А., Гитшир Дж., Хейфлик С.Дж. (2001). «Новый ген пантотенаткиназы (PANK2) дефектен при синдроме Халлервордена-Шпатца». Нат. Жене . 28 (4): 345–9. дои : 10.1038/ng572 . ПМИД 11479594 . S2CID 20400095 .
- ^ Бэй-ша, Тан; и др. (2005). «Новые сложные гетерозиготные мутации в гене PANK2 у китайского пациента с атипичной нейродегенерацией, связанной с пантотенаткиназой» . Двигательные расстройства . 20 (7): 819–21. дои : 10.1002/mds.20408 . ПМК 2105744 . ПМИД 15747360 .
- ^ "PANK2_Агарвал" .
- ^ «Мутация-основатель гена PANK у детей Агравала с нейродегенерацией с накоплением железа в мозгу (NBIA). :: Анналы Индийской академии неврологии :: 2007 - Интернет-энциклопедия Britannica» . Архивировано из оригинала 12 февраля 2011 г. Проверено 24 августа 2011 г.
- ^ Jump up to: а б Ханна, Филип А. «Нейродегенерация, связанная с пантотенаткиназой (PKAN)» . Медскейп . Проверено 6 марта 2020 г.
- ^ «Нейродегенерация, связанная с пантотенаткиназой» . Домашний справочник по генетике . Национальные институты здравоохранения Национальная медицинская библиотека . Проверено 6 марта 2020 г.
- ^ Брунетти Д., Дуси С., Джордано С., Ламперти С., Морбин М., Фугнанези В., Марше С., Фаджиолари Г., Сибон О., Моджио М., д'Амати Г., Тиранти В. (2014). «Лечение пантетином эффективно в восстановлении фенотипа заболевания, вызванного кетогенной диетой, на мышиной модели нейродегенерации, связанной с пантотенаткиназой» . Мозг . 137 (Часть 1): 57–68. дои : 10.1093/brain/awt325 . ПМЦ 3891449 . ПМИД 24316510 .
- ^ Jump up to: а б Кристу Ю.П., Тантелес Г.А., Кколоу Е., Ормистон А., Константопулос К., Бекони М., Маршалл Р.Д., Плоткин Х., Клеопа К.А. (2017). «Открытый фосметпантотенат, заместительная терапия фосфопантотенатом у одного пациента с атипичным ПКАН» . Представитель компании Neurol Med . 2017 : 3247034. doi : 10.1155/2017/3247034 . ПМЦ 5439260 . ПМИД 28567317 .
- ^ Зано С.П., Пейт С., Фрэнк М., Рок СО, Джековски С. (2015). «Коррекция генетического дефицита пантотенаткиназы 1 с помощью заместительной терапии фосфопантотенатом» . Мол Генет Метаб . 116 (4): 281–8. дои : 10.1016/j.ymgme.2015.10.011 . ПМЦ 4764103 . ПМИД 26549575 .
- ^ Мальмстрем-Грот А.Г., Кристенсон К. (1982). «Нейроаксональная дистрофия в детстве. Сообщение о двух троюродных братьях и сестрах с ПКАН и случае болезни Зейтельбергера». Acta Paediatrica Scandinavica . 71 (6): 1045–9. дои : 10.1111/j.1651-2227.1982.tb09574.x . ПМИД 7158329 . S2CID 35574844 .
- ^ Янкович Дж., Киркпатрик Дж.Б., Бломквист К.А., Лангле П.Дж., Берд Э.Д. (февраль 1985 г.). «Болезнь Халлервордена-Шпатца с поздним началом, проявляющаяся как семейный паркинсонизм». Неврология . 35 (2): 227–34. дои : 10.1159/000153550 . ПМИД 3969211 .
- ^ Янкович Дж., Киркпатрик Дж.Б., Бломквист К.А., Лангле П.Дж., Берд ЭД (1985). «Болезнь Халлервордена-Шпатца с поздним началом, проявляющаяся как семейный паркинсонизм». Неврология . 35 (2): 227–34. дои : 10.1159/000153550 . ПМИД 3969211 .
- ^ Танфани Г., Маскальчи М., Даль Поццо Г.К., Таверни Н., Сайя А., Тревизан С. (1987). «МРТ при болезни Халлервордена-Шпатца». Журнал компьютерной томографии . 11 (6): 1057–8. дои : 10.1097/00004728-198711000-00027 . ПМИД 3680689 .
- ^ Сетхи К.Д., Адамс Р.Дж., Лоринг Д.В., Эль Гаммал Т. (1988). «Синдром Халлервордена-Шпатца: корреляция клинической и магнитно-резонансной томографии». Энн. Нейрол . 24 (5): 692–4. дои : 10.1002/ana.410240519 . ПМИД 3202617 . S2CID 10181478 .
- ^ Анджелини Л., Нардоччи Н., Руми В., Зорзи С., Страда Л., Савоярдо М. (1992). «Болезнь Халлервордена-Шпатца: клиническое и МРТ-исследование 11 случаев, диагностированных при жизни». Дж. Нейрол . 239 (8): 417–25. дои : 10.1007/BF00856805 . ПМИД 1447570 . S2CID 11403203 .
- ^ Кастелс И., Спайлс В., Суиннен Т. и др. (1994). «Атрофия зрительного нерва как признак синдрома Халлервордена-Шпатца». Нейропедиатрия . 25 (5): 265–7. дои : 10.1055/s-2008-1073034 . ПМИД 7885538 . S2CID 260241219 .
- ^ Маландрини А., Бонуччелли У., Парротта Е., Чераволо Р., Берти Г., Гуацци Г.К. (1995). «Миопатическое поражение в двух случаях болезни Халлервордена-Шпатца». Мозговой разработчик 17 (4): 286–90. дои : 10.1016/0387-7604(95)00039-E . ПМИД 7503394 . S2CID 37031359 .
- ^ Тейлор Т.Д., Литт М., Крамер П., Пандольфо М., Анджелини Л., Нардоччи Н., Дэвис С., Пинеда М., Хаттори Х., Флетт П.Дж., Силио М.Р., Бертини Э., Хейфлик С.Дж. (1996). «Картирование гомозиготности синдрома Халлервордена-Шпатца по хромосоме 20p12.3-p13». Нат. Жене . 14 (4): 479–81. дои : 10.1038/ng1296-479 . ПМИД 8944032 . S2CID 21893195 .
- ↑ Юлиус Халлерворден и Хьюго Спатц были членами нацистской партии и использовали казнённых политических заключённых в медицинских исследованиях.
- ^ Пеллеккья М.Т., Валенте Э.М., Сиф Л. и др. (2005). «Разнообразный фенотип и генотип нейродегенерации, связанной с пантотенаткиназой». Неврология . 64 (10): 1810–2. doi : 10.1212/01.WNL.0000161843.52641.EC . ПМИД 15911822 . S2CID 23003382 .