Селективный модулятор глюкокортикоидных рецепторов
| Селективный модулятор глюкокортикоидных рецепторов | |
|---|---|
| Класс препарата | |
 | |
| Идентификаторы классов | |
| Синонимы | СЕГРМ; ПОБЕДИТЬ; СЕГРАМ; ДИГРА |
| Использовать | Потенциально атопический дерматит , глаукома , катаракта , глазные инфекции и другие. |
| Биологическая цель | Глюкокортикоидный рецептор |
| Химический класс | Стероидный ; нестероидный |
| Юридический статус | |
| В Викиданных | |
Селективные модуляторы глюкокортикоидных рецепторов ( SEGRM ) и селективные агонисты глюкокортикоидных рецепторов ( SEGRA ), ранее известные как диссоциированные агонисты глюкокортикоидных рецепторов ( DIGRA ), представляют собой класс экспериментальных препаратов, разработанных для того, чтобы обладать многими желательными противовоспалительными , иммуносупрессивными или противораковыми свойствами классических глюкокортикоидов. лекарства, но с меньшим количеством побочных эффектов, таких как кожные атрофия . Хотя доклинические данные о противовоспалительном действии SEGRAMs уже достигли кульминации, [ 2 ] в настоящее время эффективность этих SEGRAM при раке в значительной степени неизвестна.
Селективные агонисты глюкокортикоидных рецепторов (SEGRA) исторически имеют стероидную структуру, тогда как селективные модуляторы глюкокортикоидных рецепторов (SEGRM) обычно являются нестероидными . Комбинированное сокращение селективного агониста и модулятора глюкокортикоидных рецепторов — SEGRAM . [ 2 ] Ряд таких лигандов был разработан и проходит доклинические и клинические испытания.
SEGRAM достигают своей селективности, запуская только часть глюкокортикоидных рецепторов . механизмов действия [ 3 ] [ 4 ]
История
[ редактировать ]Синтетические стероиды со свойствами, подобными SEGRA, были обнаружены уже в конце 1990-х годов. [ 5 ] В 2000-е годы было синтезировано множество потенциальных SEGRAM, большинство из которых имели нестероидную структуру. В исследованиях in vitro на клеточных моделях эти молекулы SEGRAM связываются с глюкокортикоидными рецепторами со сродством, сходным с дексаметазоном , мощным глюкокортикоидом, и способностью подавлять выработку медиаторов воспаления, таких как интерлейкин 6 и простагландин Е2 . [ 6 ] Более того, in vitro конкретный SEGRAM может способствовать апоптозу при раке простаты. [ 7 ] и лейкемия . [ 8 ]
Исследования in vivo на мышах и крысах показали, что местное применение SEGRAM ингибирует активность пероксидазы и образование отеков , оба показателя противовоспалительной активности, по сравнению с преднизолоном . Системное введение мышам или крысам показывает, что SEGRAMs могут уменьшить острые инфекции , ревматоидный артрит , астму и колит . [ 2 ] Доказательства in vivo о том, могут ли определенные SEGRAM вызывать эффекты, аналогичные классическим глюкокортикоидам, при раковых патологиях, в настоящее время отсутствуют. Текущие доклинические испытания показывают, что доступные на данный момент SEGRAM будут вызывать меньше побочных эффектов или, по крайней мере, менее серьезные побочные эффекты, чем классические глюкокортикоиды. [ 2 ] Например, в исследовании с использованием SEGRAM Mapracorat атрофия кожи у крыс была значительно менее выражена, чем при приеме преднизолона , а метаболические эффекты, такие как увеличение веса или повышение уровня глюкозы в крови , практически отсутствовали. [ 9 ]
Механизм действия
[ редактировать ]
Как неселективные глюкокортикоиды, так и селективные агонисты глюкокортикоидных рецепторов действуют путем связывания и активации глюкокортикоидного рецептора (ГР). В отличие от глюкокортикоидов, которые активируют ГР через (по крайней мере) два передачи сигнала , пути [ 10 ] SEGRAM активируют GR таким образом, что он действует только по одному из двух основных возможных путей. [ 11 ]
В отсутствие глюкокортикоидов ГР находится в цитозоле в неактивном состоянии в комплексе с белками теплового шока (HSP) и иммунофилинами . Связывание глюкокортикоидов с GR активирует рецептор, вызывая конформационные изменения GR и, таким образом, диссоциацию связанных HSP. Активированный GR может затем регулировать экспрессию генов одним из двух путей: [ 10 ]
- Трансактивация
- Первый (прямой) путь называется трансактивацией, при котором активированный GR димеризуется , транслоцируется в ядро и связывается со специфическими последовательностями ДНК, называемыми элементами глюкокортикоидного ответа (GRE). Комплекс GR/ДНК рекрутирует другие белки, которые транскрибируют ДНК в мРНК и, в конечном итоге, в белок . Примеры генов, чувствительных к глюкокортикоидам, включают те, которые кодируют аннексин A1 , TSC22D3 (также известный как GILZ), ангиотензинпревращающий фермент , нейтральную эндопептидазу и другие противовоспалительные белки.
- Трансрепрессия
- Второй (непрямой) путь называется трансрепрессией , при котором активированный мономерный GR связывается с другими факторами транскрипции, такими как NF-κB и AP-1, и не позволяет им повышать регуляцию экспрессии генов-мишеней. Эти гены-мишени кодируют такие белки, как циклооксигеназа , NO-синтаза , фосфолипаза А2 , фактор некроза опухоли , трансформирующий фактор роста бета , ICAM-1 и ряд других провоспалительных белков.

Следовательно, противовоспалительное действие глюкокортикоидов является результатом как трансактивации, так и трансрепрессии. Напротив, исследования на крысах и мышах показали, что большинство побочных эффектов глюкокортикоидов, таких как диабетогенная активность, остеопороз , а также атрофия кожи, в основном вызваны трансактивацией. [ 9 ] [ 12 ] [ 13 ] Селективный глюкокортикоид, способный трансрепрессировать без трансактивации, должен сохранять многие из желательных терапевтических противовоспалительных эффектов и минимизировать эти конкретные нежелательные побочные эффекты. [ 11 ]
Первоначальные доказательства того, что одной транспрессии может быть достаточно для противовоспалительного ответа, были получены путем введения точечной мутации в GR мышей, которая предотвращала димеризацию GR и связывание с ДНК и тем самым блокировала трансактивацию. [ 14 ] [ 15 ] В то же время эта мутация не препятствовала трансрепрессии. Хотя GR необходим для выживания, эти мыши все еще жизнеспособны. [ 14 ] Однако когда этих мышей лечили синтетическим глюкокортикоидом дексаметазоном, повышения уровня глюкозы не наблюдалось. Эти мыши, получавшие дексаметазон, были устойчивы к воспалительному раздражителю. [ 15 ] Следовательно, эти мыши были чувствительны к противовоспалительному действию дексаметазона, но были устойчивы, по крайней мере, к некоторым побочным эффектам.
Как и глюкокортикоиды, SEGRAM связываются с GR и активируют его. Однако, в отличие от глюкокортикоидов, SEGRAM избирательно активируют ГР таким образом, что они обеспечивают улучшенный терапевтический эффект. Как правило, при определенных заболеваниях, связанных с воспалением, SEGRAM должны более сильно трансрепрессировать, чем трансактивировать, или, что еще лучше, исключительно трансрепрессировать и не трансактивироваться. Этот тип избирательной активации ГР должен приводить к меньшему количеству побочных эффектов, чем ожидаемые побочные эффекты, возникающие при длительном лечении классическими глюкокортикоидами. [ 16 ]
Клинические испытания
[ редактировать ]Клинические испытания фазы II с одним из соединений-кандидатов, мапракоратом (кодовые названия BOL-303242-X и ZK 245186). [ 17 ] ), началось летом 2009 года. Одно из них представляло собой двойное слепое исследование по подбору дозы мази против атопического дерматита, проведенное компанией Intendis , частью Bayer HealthCare Pharmaceuticals, специализирующейся на дерматологии . [ 18 ] В ноябре 2010 года началось исследование фазы III по оценке офтальмологической суспензии для лечения воспаления после операции по удалению катаракты, проводимое компанией Bausch & Lomb . [ 19 ]
Испытание фазы II с другим диссоциированным глюкокортикоидом ( - PF 00251802 фосдагрокоратом (PF-04171327) (пролекарством фосфатного эфира дагрокората ) [ 20 ] [ 21 ] ) для лечения ревматоидного артрита была запущена в 2011 году компанией Pfizer . [ 22 ]
Результаты этих клинических испытаний еще не были раскрыты, и ни один SEGRAM еще не был одобрен для клинического использования.
Возможные применения
[ редактировать ]При хронических воспалительных заболеваниях, таких как атопический дерматит (кожа), ревматоидный артрит (суставы)... побочные эффекты кортикостероидов проблематичны из-за необходимости длительного лечения. Поэтому SEGRAM исследуются в качестве альтернативного местного лечения. Системное длительное лечение воспалений кортикостероидами особенно склонно вызывать метаболические побочные эффекты, что делает разработку пероральных SEGRAMs интересной целью. [ 23 ] Еще неизвестно, действительно ли селективные агонисты или модуляторы рецепторов вызывают значительно меньше побочных эффектов, чем классические кортикоиды при клиническом применении.
Полезный атрофический эффект
[ редактировать ]Следует отметить, что атрофические эффекты глюкокортикоидов не всегда являются недостатком. Это свойство используется при лечении гиперпролиферативных заболеваний, таких как псориаз. [ 24 ] SEGRAM, вероятно, будут менее эффективны в таких условиях. Недавние достижения показали, что первое стремление к полному разделению трансрепрессии и трансактивации GR с помощью SEGRAM заслуживает уточнения, поскольку противовоспалительные гены, стимулируемые трансактивацией GR, такие как GILZ и DUSP1 , по-видимому, играют важную роль. [ 25 ] [ 26 ] Тем не менее, более избирательный характер этих SEGRAM по-прежнему снижает количество побочных эффектов, опосредованных GR, и заслуживает дальнейших клинических испытаний.
Химия
[ редактировать ]

Ранние SEGRA представляли собой синтетические стероиды. Примером может служить RU 24858, одно из первых опубликованных соединений такого типа. [ 5 ] Многие новые SEGRA имеют другую структуру, хотя сходство со стероидами все еще можно увидеть в таких молекулах, как бензопиранохинолин A 276575 или в производных октагидрофенантрен-2,7-диола. Было показано, что все эти соединения проявляют свойства SEGRA на клеточных или животных моделях. [ 3 ]
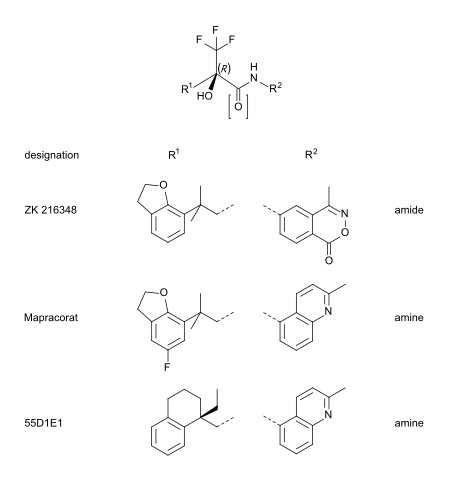
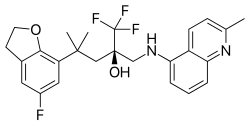
Мапракорат является одним из ряда трифторпропаноламинов и -амидов, структура которых менее стероидоподобна. Другими типичными примерами этой группы являются ZK 216348. [ 9 ] и 55Д1Е1. [ 4 ] Объемные бициклические ароматические заместители (R 1 и Р 2 ) объясняют структурное сходство с кортикоидами. асимметричного R -конформация атома углерода , по-видимому, важна для сродства к GR. [ 9 ]
Список SEGRM
[ редактировать ]- Дагрокорат (PF-00251802, PF-251802)
- Фосдагрокорат (PF-04171327, PF-4171327)
- Мапракорат (BOL-303242-X, ZK-245186)
См. также
[ редактировать ]- Селективный модулятор рецепторов
- Селективный модулятор андрогенных рецепторов
- Селективный модулятор рецепторов эстрогена
- Селективный модулятор рецепторов прогестерона
Ссылки
[ редактировать ]- ^ Мили Н; Дулсат С (2009). «36-е ежегодное собрание Ассоциации дерматологических исследований (ADF)». Наркотики Фут . 34 (4): 341.
- ^ Jump up to: а б с д Сундал Н., Бриделанс Дж., Либерт С., Де Босшер К., Бек И.М. (май 2015 г.). «Селективная модуляция глюкокортикоидных рецепторов: новые направления с помощью нестероидных каркасов» . Фармакология и терапия . 152 : 28–41. doi : 10.1016/j.pharmthera.2015.05.001 . hdl : 1854/LU-6896362 . ПМИД 25958032 .
- ^ Jump up to: а б с Робинсон Р.П., Бакбиндер Л., Хаугето А.И., Макнифф П.А., Миллхэм М.Л., Риз М.Р., Шефер Дж.Ф., Абрамов Ю.А., Борднер Дж., Чантиньи Ю.А., Кляйнман Э.Ф., Лэрд Э.Р., Морган Б.П., Мюррей Дж.К., Солтер Э.Д., Вессель М.Д., Йокум С.А. (март 2009 г.). «Аналоги октагидрофенантрен-2,7-диола как диссоциированные агонисты глюкокортикоидных рецепторов: открытие и ведущие исследования». Журнал медицинской химии . 52 (6): 1731–43. дои : 10.1021/jm801512v . ПМИД 19239259 .
- ^ Jump up to: а б Биггадайк К., Буджелал М., Клакерс М., Коу Д.М., Демейн Д.А., Харди Г.В., Хамфрис Д., Инглис Г.Г., Джонстон М.Дж., Джонс Х.Т., Хаус Д., Луазо Р., Нидхэм Д., Сконе П.А., Уингс И., Вейтч Г., Вайнгартен Г.Г. , Маклей И.М., Макдональд С.Дж. (декабрь 2007 г.). «Нестероидные агонисты глюкокортикоидов: тетрагидронафталины с альтернативными стероидными миметиками А-кольца, обладающими диссоциированной (трансрепрессией / трансактивацией) селективной эффективностью». Журнал медицинской химии . 50 (26): 6519–34. дои : 10.1021/jm070778w . ПМИД 18038970 .
- ^ Jump up to: а б с Вайсьер Б.М., Дюпон С., Шоквар А., Пети Ф., Гарсия Т., Маршадо С., Гронемейер Х., Реше-Ригон М. (август 1997 г.). «Синтетические глюкокортикоиды, которые диссоциируют трансактивацию и трансрепрессию AP-1, проявляют противовоспалительную активность in vivo» . Молекулярная эндокринология . 11 (9): 1245–55. дои : 10.1210/mend.11.9.9979 . ПМИД 9259316 . S2CID 28436574 .
- ^ Jump up to: а б Лин С.В., Накане М., Сташко М., Фолс Д., Кук Дж., Миллер Л., Хуанг Р., Тайри С., Майнер Дж.Н., Розен Дж., Ким PR, Коглан М.Дж., Картер Дж., Лейн BC (август 2002 г.). «Транс-активация и репрессивные свойства нового лиганда нестероидного глюкокортикоидного рецептора 2,5-дигидро-9-гидрокси-10-метокси-2,2,4-триметил-5-(1-метилциклогексен-3-y1)-1H- [1]бензопирано[3,4-f]хинолин (A276575) и его четыре стереоизомера». Молекулярная фармакология . 62 (2): 297–303. дои : 10.1124/моль.62.2.297 . ПМИД 12130681 .
- ^ Емельянов А., Чворног Дж., Гера Л., Джоши С., Чаттертон Р.Т., Будунова И. (июнь 2008 г.). «Новое соединение-фитомодулятор стероидных рецепторов А ингибирует рост и выживание клеток рака простаты» . Исследования рака . 68 (12): 4763–73. дои : 10.1158/0008-5472.CAN-07-6104 . ПМИД 18559523 .
- ^ Лесовая Е.А., Емельянов А.Ю., Кирсанов К.И., Якубовская М.Г., Будунова И.В. (ноябрь 2011 г.). «Противоопухолевое действие лиганда нестероидного глюкокортикоидного рецептора CpdA на клеточные линии лейкемии CEM и K562» (PDF) . Биохимия. Биохимия . 76 (11): 1242–52. дои : 10.1134/S000629791111006X . ПМИД 22117551 . S2CID 35234449 . Архивировано из оригинала (PDF) 11 марта 2016 г. Проверено 28 мая 2015 г.
- ^ Jump up to: а б с д Шеке Х, Шоттелиус А, Дёкке ВД, Стрелке П, Ярох С, Шмис Н, Ревинкель Х, Хеннекес Х, Асадулла К (январь 2004 г.). «Отделение трансактивации от трансрепрессии селективным агонистом глюкокортикоидных рецепторов приводит к отделению терапевтических эффектов от побочных эффектов» . Труды Национальной академии наук Соединенных Штатов Америки . 101 (1): 227–32. Бибкод : 2004PNAS..101..227S . дои : 10.1073/pnas.0300372101 . ПМК 314167 . ПМИД 14694204 .
- ^ Jump up to: а б Рен Т., Цидловски Дж. А. (октябрь 2005 г.). «Противовоспалительное действие глюкокортикоидов - новые механизмы старых лекарств». Медицинский журнал Новой Англии . 353 (16): 1711–23. дои : 10.1056/NEJMra050541 . ПМИД 16236742 . S2CID 5744727 .
- ^ Jump up to: а б Ньютон Р., Холден Н.С. (октябрь 2007 г.). «Разделение трансрепрессии и трансактивации: печальный развод для глюкокортикоидного рецептора?». Молекулярная фармакология . 72 (4): 799–809. дои : 10.1124/моль.107.038794 . ПМИД 17622575 . S2CID 52803631 .
- ^ Хайнеманн А, Шулигой Р (2008). «Глюкокортикоиды – сильные и спорные» [Глюкокортикоиды – сильные и спорные]. Австрийская фармацевтическая газета (на немецком языке). 62 (23). [ постоянная мертвая ссылка ]
- ^ Коглан М.Дж., Джейкобсон П.Б., Лейн Б., Накане М., Лин К.В., Элмор С.В., Ким П.Р., Люли Дж.Р., Картер Г.В., Тернер Р., Тайри СМ, Ху Дж., Элгорт М., Розен Дж., Майнер Дж.Н. (май 2003 г.). «Новое противовоспалительное средство поддерживает эффективность глюкокортикоидов при уменьшении побочных эффектов». Молекулярная эндокринология . 17 (5): 860–9. дои : 10.1210/me.2002-0355 . ПМИД 12586843 . S2CID 10888190 .
- ^ Jump up to: а б Райхардт Х.М., Кестнер К.Х., Такерманн Дж., Крец О., Вессели О., Бок Р., Гасс П., Шмид В., Херрлих П., Анхель П., Шютц Г. (май 1998 г.). «Связывание ДНК с глюкокортикоидным рецептором не является необходимым для выживания» . Клетка . 93 (4): 531–41. дои : 10.1016/S0092-8674(00)81183-6 . ПМИД 9604929 . S2CID 6524157 .
- ^ Jump up to: а б Райхардт Х.М., Тронш Ф., Бауэр А., Шютц Г. (2000). «Молекулярно-генетический анализ передачи сигналов глюкокортикоидов с использованием системы Cre / loxP». Биологическая химия . 381 (9–10): 961–4. дои : 10.1515/BC.2000.118 . ПМИД 11076028 . S2CID 37837380 .
- ^ Шеке Х., Бергер М., Ревинкель Х., Асадулла К. (сентябрь 2007 г.). «Селективные агонисты глюкокортикоидных рецепторов (SEGRA): новые лиганды с улучшенным терапевтическим индексом» (PDF) . Молекулярная и клеточная эндокринология . 275 (1–2): 109–17. дои : 10.1016/j.mce.2007.05.014 . ПМИД 17630119 . S2CID 46020217 .
- ^ Кавет М.Э., Харрингтон К.Л., Уорд К.В., Чжан Дж.З. (2010). «Мапракорат, новый селективный агонист глюкокортикоидных рецепторов, ингибирует гиперосмолярно-индуцированное высвобождение цитокинов и пути МАРК в эпителиальных клетках роговицы человека» . Молекулярное видение . 16 : 1791–800. ПМЦ 2932489 . ПМИД 20824100 .
- ^ Номер клинического исследования NCT00944632 «Повышение дозы различных концентраций ZK 245186 при атопическом дерматите» на сайте ClinicalTrials.gov.
- ^ Номер клинического исследования NCT01230125 «Офтальмологическая суспензия Мапракората для лечения воспаления глаз после операции по удалению катаракты» на сайте ClinicalTrials.gov.
- ^ Сток Т., Флейшакер Д., Мукерджи А., Ле В., Сюй Дж., Зейхер Б. (2009). «Оценка безопасности, фармакокинетики и фармакодинамики селективного модулятора глюкокортикоидных рецепторов (SGRM) у здоровых добровольцев» . Ревмирующий артрит . 60 (Приложение 10): 420. doi : 10.1002/art.25503 (неактивно 13 сентября 2024 г.). Архивировано из оригинала 3 марта 2016 г.
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на сентябрь 2024 г. ( ссылка ) - ^ Ху Х, Ду С., Тунка С., Брейден Т., Лонг КР, Ли Дж., Уэбб Э.Г., Дитц Дж.Д., Хаммерт С., Роу С., Хегде С.Г., Уэббер Р.К., Обукович М.Г. (август 2011 г.). «Антагонисты, но не частичные агонисты лигандов глюкокортикоидных рецепторов, демонстрируют значительную диссоциацию побочных эффектов» . Эндокринология . 152 (8): 3123–34. дои : 10.1210/en.2010-1447 . ПМИД 21558312 .
- ^ Номер клинического исследования NCT01393639 «Исследование сравнения доз экспериментального глюкокортикоидного соединения с преднизолоном и плацебо при ревматоидном артрите» на ClinicalTrials.gov
- ^ Шеке Х, Хеннекес Х, Шоттелиус А, Ярох С, Леманн М, Шмис Н, Ревинкель Х, Асадулла К (2002). «SEGRA: новый класс противовоспалительных соединений». В Cato AC, Schäcke H, Asadullah K (ред.). Последние достижения в области действия глюкокортикоидных рецепторов . Семинар Исследовательского фонда Эрнста Шеринга. Том. 40. Спрингер. стр. 357–71. дои : 10.1007/978-3-662-04660-9_20 . ISBN 978-3-662-04662-3 . ПМИД 12355726 .
- ^ Кершер М.Дж., Харт Х., Кортинг Х.К., Сталлейкен Д. (апрель 1995 г.). «Оценка атрофогенной активности мометазона фуроата in vivo, недавно разработанного хлорированного сильнодействующего глюкокортикоида для местного применения по сравнению с другими старыми и новыми глюкокортикоидами для местного применения». Международный журнал клинической фармакологии и терапии . 33 (4): 187–9. ПМИД 7620686 .
- ^ Шах С., Кинг Э.М., Чандрасекхар А., Ньютон Р. (май 2014 г.). «Роль митоген-активируемой протеинкиназы (MAPK) фосфатазы, DUSP1, в контроле по обратной связи экспрессии воспалительных генов и репрессии дексаметазоном» . Журнал биологической химии . 289 (19): 13667–79. дои : 10.1074/jbc.M113.540799 . ПМК 4036371 . ПМИД 24692548 .
- ^ Айрольди Э., Маккиаруло А., Риккарди С. (декабрь 2014 г.). «Нацеливание на побочные эффекты глюкокортикоидов: селективный модулятор глюкокортикоидных рецепторов или лейциновая застежка-молния, индуцированная глюкокортикоидами? Перспектива» . Журнал ФАСЭБ . 28 (12): 5055–70. дои : 10.1096/fj.14-254755 . ПМИД 25205742 . S2CID 40874311 .
Дальнейшее чтение
[ редактировать ]- Хобсон, Адриан (2023). Медицинская химия модуляторов глюкокортикоидных рецепторов . Спрингер Природа. ISBN 978-3-031-28732-9 .