Аминоацил тРНК синтетаза
| Антикодонсвязывающий домен тРНК | |||
|---|---|---|---|
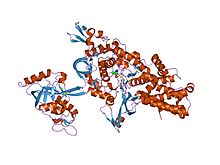 лейцил-тРНК-синтетаза из Thermus Thermophilus, комплексной с помощью аналога пост-переноса подложки. | |||
| Идентификаторы | |||
| Символ | Anticodon_2 | ||
| Pfam | PF08264 | ||
| InterPro | IPR013155 | ||
| Краткое содержание | 1IVS / SCOPE / SUPFAM | ||
| |||
| DALR Anticodon -связывающий домен 1 1 | |||
|---|---|---|---|
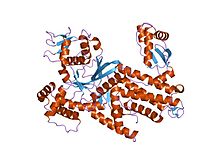 Thermus thermophilus arginyl-тРНК-синтетаза | |||
| Идентификаторы | |||
| Символ | DALR_1 | ||
| Pfam | PF05746 | ||
| PFAM клан | CL0258 | ||
| InterPro | IPR008909 | ||
| Краткое содержание | 1bs2 / scope / supfam | ||
| |||
| DALR Anticodon -связывающий домен 2 | |||
|---|---|---|---|
 Кристаллическая структура бинарного комплекса цистеинил-тРНК с тРНК Cys | |||
| Идентификаторы | |||
| Символ | DALR_2 | ||
| Pfam | PF09190 | ||
| PFAM клан | CL0258 | ||
| InterPro | IPR015273 | ||
| |||
Аминоацил -тРНК-синтетаза ( AARS или ARS ), также называемая тРНК-лигазой, представляет собой фермент , который прикрепляет соответствующую аминокислоту к соответствующей тРНК . Это делает это путем катализирования трансэтерификации специфической родственной аминокислоты или ее предшественника на одну из всех его совместимых родственных тРНК с образованием аминоацил-тРНК . У людей 20 различных типов AA-тРНК производятся 20 различными аминоацил-тРНК-синтетазами, по одному для каждой аминокислоты генетического кода .
Это иногда называют «зарядкой» или «загрузкой» тРНК аминокислотой. Как только тРНК заряжается, рибосома может перенести аминокислоту из тРНК на растущий пептид , согласно генетическому коде. Следовательно, аминоацил тРНК играет важную роль в трансляции РНК , экспрессии генов для создания белков.
Механизм
[ редактировать ]Синтетаза АТФ сначала связывает . и соответствующую аминокислоту (или ее предшественник ) с образованием аминоацил-аденилата, высвобождая неорганический пирофосфат (PPI) связывает Затем комплекс аденилат-аарс подходящую DIM молекулы молекулы тРНК , а аминокислота переносится из AA-AMP в 2'- или 3'-OH из последней тРНК-нуклеотида (A76) на 3'- конец .
Механизм может быть обобщен в следующей серии реакций:
Суммируя реакции, очень эксергоническая общая реакция заключается в следующем:
- Аминокислота + тРНК + АТФ → Аминоацил-трна + ампер + PPI
Некоторые синтетазы также опосредуют реакцию редактирования , чтобы обеспечить высокую точность зарядки тРНК. Если добавлена неправильная тРНК (он же, как установлено, что тРНК является неправильно заряженной), аминоацил-тРНК гидролизуется . Это может произойти, когда две аминокислоты обладают разными свойствами, даже если они имеют сходные формы - как и в случае с валином и треонином .
Точность аминоацил-тРНК-синтетазы настолько высока, что часто она соединена с словом «супер-специфичность», когда она сравнивается с другими ферментами, которые участвуют в метаболизме. Хотя не все синтетазы имеют домен с единственной целью редактирования, они делают. для этого, имея специфическое связывание и активация их аффилированных аминокислот. Аминоацил-тРНК синтетаза и ее родственная тРНК. [ 1 ] [ 2 ]
Классы
[ редактировать ]Существует два класса аминоацил -синтетазы, каждый из которых состоит из десяти ферментов: [ 3 ] [ 4 ]
- У класса I два высококонсервативных мотива последовательности. Он аминоацилатирует в 2'-OH терминального аденозин -нуклеотида на тРНК, и обычно он является мономерным или димерным (одна или две субъединицы соответственно).
- Класс II имеет три высококонсервативных мотива последовательности. Он аминоацилатирует в 3'-OH терминального аденозина на тРНК и обычно является димерным или тетрамерным (две или четыре субъединицы соответственно). Хотя фенилаланин-тРНК-синтетаза представляет собой класс II, она аминоацилирует в 2'-OH.
Аминокислоты прикреплены к гидроксильной (-OH) группе аденозина через карбоксильную (-coOH) группу.
Независимо от того, где аминоацил изначально прикреплен к нуклеотиду, 2'- O- аминоацил-трна в конечном итоге будет мигрировать в 3 'позицию посредством переэтерификации .
Бактериальные аминоацил-тРНК-синтетазы могут быть сгруппированы следующим образом: [ 5 ]
| Сорт | Аминокислоты |
|---|---|
| я | Arg, cys, gln, glu, il, leu, met, trp, tyr, val |
| II | Ala, Asn, Asp, Gly, His, Lys, Pro, Phe, Ser, Thr |
Аминокислоты, которые используют AAR класса II, кажутся эволюционно старше. [ 6 ]


Структуры
[ редактировать ]Оба класса аминоацил-тРНК-синтетаз представляют собой многодоменные белки. В типичном сценарии AARS состоит из каталитического домена (где происходят и вышеупомянутые реакции) и антикодонного связывающего домена (который взаимодействует в основном с антикодонной областью тРНК). Переносные РНК для различных аминокислот различаются не только по их антикодону, но и в других точках, что дает им немного разные общие конфигурации. Аминоацил-тРНК синтетазы распознают правильные тРНК, прежде всего, через их общую конфигурацию, а не только через их антикодон. [ 7 ] Кроме того, некоторые AARS имеют дополнительные домены связывания РНК и домены редактирования [ 8 ] которые расщепляют неправильно парные молекулы аминоацил-тРНК.
Каталитические домены всех AARS данного класса обнаружены гомологичны друг другу, тогда как AARS класса I и класса II не связаны друг с другом. AARSS класса I оснащена цитидидилтрансферазоподобной Rossmann Fold , наблюдаемой в белках, таких как глицерол-3-фосфат цитидидилтрансфераза, никотинамид нуклеотид адениланттрансфераза и архаальная синтаза FAD, где у Aars класса II есть уникальная складка, связанные с биотинами и липатоататоаттеаттеаза.
Альфа -спиральный антикодон -связывающий домен аргинил-, глицил- и цистеинил-тРНК-синтетаз известен как домен DALR после характерных консервативных аминокислот . [ 9 ]
Аминоацил-тРНК-синтетазы были кинетически изучены, показывая, что Mg 2+ Ионы играют активную каталитическую роль, и, следовательно, AAR имеют степень зависимости магния. Увеличение Mg 2+ Концентрация приводит к увеличению констант равновесия для реакций аминоацил-тРНК синтетаз. Хотя эта тенденция была замечена как в синтетазах класса I, так и в классе II, зависимость магния для двух классов очень отличается. Синтетазы класса II имеют два или (чаще) три мг 2+ ионы, в то время как класс I требует только одного мг 2+ ион [ 10 ] [ 11 ]
Помимо отсутствия общего сходства последовательностей и структуры, синтетазы I и класса II класса имеют различные механизмы распознавания АТФ. В то время как класс I связывается с помощью взаимодействий, опосредованных водородными связями, класс II использует пару остатков аргинина для установления солевых мостов в его АТФ -лиганд. Эта оппозиционная реализация проявляется в двух структурных мотивах: скобки из основных целей и пинцет Arginine, которые наблюдаются во всех структурах класса I и класса II, соответственно. Высокая структурная сохранение этих мотивов предполагает, что они должны присутствовать с древних времен. [ 12 ]
Эволюция
[ редактировать ]Большая часть AARS данной специфичности эволюционно ближе друг к другу, чем к AARS другой специфичности. Однако группа ASNRS и GLNRS в ASPRS и GLURS соответственно. Большинство AARS данной специфичности также принадлежат к одному классу. Тем не менее, есть две отдельные версии лиср - одна принадлежащая к семье класса I, а другая принадлежат к семье класса II. [ Цитация необходима ]
Молекулярные филогения AARS часто не согласуются с общепринятыми организмом филогениями . То есть они нарушают так называемую каноническую филогенетическую картину, показанную большинством других ферментов для трех доменов жизни - археи , бактерий и эукарья . Кроме того, филогения, выведенные для AARS различных аминокислот, часто не согласны друг с другом. Кроме того, паралоги AARS в одном и том же виде показывают высокую степень дивергенции между ними. Это четкие признаки того, что горизонтальный перенос произошел несколько раз в течение эволюционной истории AARS. [ 13 ]
Широко распространенная вера в эволюционную стабильность этой суперсемейства, а это означает, что каждый организм имеет все AARS для соответствующих аминокислот, неправильно. Крупномасштабный геномный анализ на ~ 2500 прокариотических геномах показал, что многие из них пропускают один или несколько генов AARS, тогда как многие геномы имеют 1 или более паралогов. [ 14 ] Alars, Glyrs, Leurs, Ilers и Valrs являются наиболее эволюционно стабильными членами семьи. Глюки, лисры и CysR часто имеют паралоги, тогда как ASNR, GLNR, PYLR и SEPR часто отсутствуют во многих геномах.
За исключением Alars, было обнаружено, что 19 из 20 человеческих AARS добавили хотя бы один новый домен или мотив. [ 15 ] Эти новые области и мотивы различаются по функции и наблюдаются в различных формах жизни. Общая новая функция в AARS человека обеспечивает дополнительную регуляцию биологических процессов. Существует теория, что растущее число AARS, которые добавляют домены, обусловлено непрерывной эволюцией более высоких организмов с более сложными и эффективными строительными блоками и биологическими механизмами. Одним из ключевых доказательств этой теории является то, что после добавления нового домена в AARS домен становится полностью интегрированным. Функциональность этой новой области сохраняется с этого момента. [ 16 ]
Поскольку генетическая эффективность развивалась в более высоких организмах, были добавлены 13 новых доменов без очевидной связи с каталитической активностью генов AARSS.
Применение в биотехнологии
[ редактировать ]В некоторых аминоацил -синтетазах полость, которая удерживает аминокислоту, может быть мутирована и модифицирована для переноса неестественных аминокислот, синтезированных в лаборатории, и прикрепить их к специфическим тРНК. Это расширяет генетический код, помимо двадцати канонических аминокислот, обнаруженных в природе, также включает в себя неестественную аминокислоту. Неестественная аминокислота кодируется бессмысленной (TAG, TGA, TAA) триплетом, кодоном четырехлета или в некоторых случаях избыточным редким кодоном. Организм, который экспрессирует мутантную синтетазу, может быть генетически запрограммирован, чтобы включить неестественную аминокислоту в любое желаемое положение в любом интересующем белке, позволяя биохимикам или структурным биологам исследовать или изменять функцию белка. Например, можно начать с гена для белка, который связывает определенную последовательность ДНК, и, направляя неестественную аминокислоту с реактивной боковой цепью в сайт связывания, создайте новый белок, который разрезает ДНК в мишени -Пусенция, а не связывать ее.
Мутирующими аминоациль-синтетазы, химики расширили генетические коды различных организмов, чтобы включить аминокислоты с синтезированными лабораториями со всеми видами полезных свойств: фотореактивные, металлические, ксеноновые, черновые, сшивающие, спин-резонанс, флуоресцент, биотинилированный и ксеновой окислительно-активный аминокислоты. [ 17 ] Другое использование - вводить аминокислоты, несущие реактивные функциональные группы для химической модификации целевого белка.
Причиния определенных заболеваний (такие как патологии нейронов, рак, нарушенные метаболические состояния и аутоиммунные расстройства) были коррелированы со специфическими мутациями аминоацил-тРНК-синтетаз. Charcot-Marie-Tooth (CMT) является наиболее частым наследственным заболеванием периферической нервной системы (заболевания нейронов) и вызвано наследственной мутацией в гликол-тРНК и тирозил-трНК. [ 18 ] Диабет, метаболическое заболевание, вызывает окислительный стресс, который запускает нарастание митохондриальных мутаций тРНК. Также было обнаружено, что тРНК -синтетазы могут частично участвовать в этиологии рака. [ 19 ] Высокий уровень выражения или модификации AARS наблюдался в рамках рака. Распространенным результатом мутаций AARS является нарушение формы/формирования димера, которое имеет прямую связь с ее функцией. Эти корреляции между AARS и некоторыми заболеваниями открыли новую дверь для синтеза терапии. [ 20 ]
Некаталитические домены
[ редактировать ]Новые дополнения домена к генам AARS являются аккретивными и прогрессивными в дереве жизни . [ 21 ] [ 22 ] [ 23 ] Сильное эволюционное давление для этих небольших некаталитических белковых доменов предполагало их важность. [ 24 ] Результаты, начиная с 1999 года, а затем выявили ранее не признанный слой биологии: эти белки контролируют экспрессию генов в клетках происхождения и при высвобождении гомеостатического и контроля развития у специфических типов клеток человека, тканей и органов во время развития взрослых или плода или оба, оба, оба, оба, оба, оба, оба, оба, оба, оба, оба, оба, оба, оба, оба, оба, оба. включая пути, связанные с ангиогенезом , воспалением , иммунным ответом , механистической мишенью передачи сигналов рапамицина (MTOR), апоптоза , онкогенеза и интерферон гамма (IFN- γ ) и передача сигналов p53 . [ 25 ] [ 26 ] [ 27 ] [ 28 ] [ 29 ] [ 30 ] [ 31 ] [ 32 ] [ 33 ]
Истощение субстрата
[ редактировать ]В 2022 году было обнаружено, что аминоацил-тРНК-синтетазы могут включать альтернативные аминокислоты во время нехватки их предшественников. В частности, триптофанил -синтетаза ( Wars1 ) будет включать фенилаланин во время истощения триптофана, по существу, вызывая переназначение кодона . [ 34 ] Истощение другого субстрата аминоацил-тРНК-синтетаз, родственной тРНК, может иметь отношение к определенным заболеваниям, например, болезнь Чаркота-мари-подзащита . Было показано, что варианты CMT-мутантной глицил-тРНК-синтетазы по-прежнему способны связывать тРНК-гла кодоны глицина во время перевода мРНК. [ 35 ]
Клинический
[ редактировать ]Мутации в митохондриальном ферменте были связаны с рядом генетических нарушений, включая синдром Ли , Синдром Запада и Cagss ( катаракта , дефицит гормона роста , сенсорную невропатию , сенсорнорную потерю слуха и синдром скелетной дисплазии). [ 36 ]
Серверы прогнозирования
[ редактировать ]- ICAARS : B. Pawar и GPS Raghava (2010) Прогнозирование и классификация аминоацил -синтетаз с использованием доменов Prosite. BMC Genomics 2010, 11: 507
- Marspred : Panwar B, Raghava GP (май 2012 г.). «Прогнозирование субклеточной локализации тРНК-синтетаз из их первичных структур». Аминокислоты . 42 (5): 1703–13. doi : 10.1007/s00726-011-0872-8 . PMID 21400228 . S2CID 2996097 .
- AARS Прокариотическая база данных : Chliotis, et. (Февраль 2017 г.). "История Коллекса . Нуклеиновые кислоты Res 45 (3): 1059–1 doi : /nar1 10.1093 PMC 53388404 . PMID 28180287 .
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ McClain WH (ноябрь 1993 г.). «Правила, которые регулируют идентичность тРНК в синтезе белка». Журнал молекулярной биологии . 234 (2): 257–80. doi : 10.1006/jmbi.1993.1582 . PMID 8230212 .
- ^ Swanson R, Hoben P, Sumner-Smith M, Uemura H, Watson L, Söll D (декабрь 1988 г.). «Точность аминоацилирования in vivo требует надлежащего баланса тРНК и аминоацил-тРНК синтетазы». Наука . 242 (4885): 1548–51. Bibcode : 1988sci ... 242.1548s . doi : 10.1126/science.3144042 . PMID 3144042 .
- ^ «ТНК -синтетазы» . Архивировано с оригинала 2012-08-04 . Получено 2007-08-18 .
- ^ Делару, М. (1995). «Аминоацил-трна синтетазы». Структурная биология . 5 (1): 48–55. doi : 10.1016/0959-440x (95) 80008-O . PMID 7773747 .
- ^ Получил, Дональд; Голос, Джудит Дж. (2011). Биохимия (4 -е изд.). Хобокен, Нью -Джерси: Уайли. ISBN 978-0-470-57095-1 .
- ^ Трифонов, Э. Н. (2000-12-30). «Консенсус -временный порядок аминокислот и эволюция триплетного кода» . Ген . Документы, представленные на семинаре Антон Дорн. 261 (1): 139–151. doi : 10.1016/s0378-1119 (00) 00476-5 . ISSN 0378-1119 . PMID 11164045 .
- ^ Schimmel P, Giegé R, Moras D, Yokoyama S (октябрь 1993). «Операционный код РНК для аминокислот и возможная связь с генетическим кодом» . Труды Национальной академии наук Соединенных Штатов Америки . 90 (19): 8763–8. Bibcode : 1993pnas ... 90.8763s . doi : 10.1073/pnas.90.19.8763 . PMC 47440 . PMID 7692438 .
- ^ «Молекула месяца: аминоацил-тРНК синтетазы высокая точность» . Архивировано с оригинала 2013-10-20 . Получено 2013-08-04 .
- ^ Вольф Йи, Аравинд Л., Гришин Н.В., Кунин Э.В. (август 1999). «Эволюция аминоацил-тРНК-синтетаз-анализ уникальных доменных архитектур и филогенетических деревьев выявляет сложную историю горизонтальных событий переноса генов» . Исследование генома . 9 (8): 689–710. doi : 10.1101/gr.9.8.689 . PMID 10447505 .
- ^ Airas RK (декабрь 2007 г.). «Магниевая зависимость измеренных равновесных константов аминоацил-тРНК-синтетаз». Биофизическая химия . 131 (1–3): 29–35. doi : 10.1016/j.bpc.2007.08.006 . PMID 17889423 .
- ^ Франклин С., Мусьер-Форсит К, Мартинис С.А. (сентябрь 1997 г.). «Аминоацил-тРНК синтетазы в биологии и болезнях: новые данные структурного и функционального разнообразия в древнем семействе ферментов» . РНК . 3 (9): 954–60. PMC 1369542 . PMID 9292495 .
- ^ Kaiser F, Bittrich S, Salentin S, Leberecht C, Haupt VJ, Krautwurst S, Schroeder M, Labudde D (апрель 2018 г.). «Кроншеты магистрали и аргининовые пинцетки определяют аминоациль -синтетазы класса I и класса II» . PLOS Computational Biology . 14 (4): E1006101. BIBCODE : 2018PLSCB..14E6101K . doi : 10.1371/journal.pcbi.1006101 . PMC 5919687 . PMID 29659563 .
- ^ Woese CR, Olsen GJ, Ibba M, Söll D (март 2000 г.). «Аминоацил-тРНК-синтетазы, генетический код и эволюционный процесс» . Микробиология и молекулярная биология обзоры . 64 (1): 202–36. doi : 10.1128/mmbr.64.1.202-236.2000 . PMC 98992 . PMID 10704480 .
- ^ Чалиотис А., Властаридис П., Моссиалос Д., Ибба М., Беккер Х.Д., Статопулос С., Амутциас Г.Д. (февраль 2017 г.). «Сложная эволюционная история аминоацил-тРНК-синтетаз» . Исследование нуклеиновых кислот . 45 (3): 1059–1068. doi : 10.1093/nar/gkw1182 . PMC 5388404 . PMID 28180287 .
- ^ Го М., Ян XL, Шиммель П (сентябрь 2010 г.). «Новые функции аминоацил-тРНК-синтетаз за пределами перевода» . Природа обзор молекулярной клеточной биологии . 11 (9): 668–74. doi : 10.1038/nrm2956 . PMC 3042954 . PMID 20700144 .
- ^ Lee SW, Cho BH, Park SG, Kim S (август 2004 г.). «Аминоацил-тРНК-синтетазы комплексы: за пределами перевода» . Журнал сотовой науки . 117 (Pt 17): 3725–34. doi : 10.1242/jcs.01342 . PMID 15286174 . S2CID 29447608 .
- ^ Питер Г. Шульц , расширение генетического кода
- ^ Xie W, Schimmel P, Yang XL (декабрь 2006 г.). «Кристаллизация и предварительный рентгеновский анализ нативной синтетазы тРНК человека, аллельные варианты которых связаны с болезнью чарко-мари-зуба» . Acta Crystallographica Раздел f . 62 (Pt 12): 1243–6. doi : 10.1107/s1744309106046434 . PMC 2225372 . PMID 17142907 .
- ^ Квон Н.Х., Кан Т., Ли Дж.Ю., Ким Х.Х., Ким Х.Р., Хонг Дж, О.С., Хан Дж. М., Ку М.Дж., Ли Си, Ким С. (декабрь 2011 г.). «Двойная роль метиониел-тРНК-синтетазы в регуляции трансляции и активности супрессора опухоли аминоацил-тРНК-синтетазы, интрактирующего многофункциональный белок-3» . Труды Национальной академии наук Соединенных Штатов Америки . 108 (49): 19635–40. Bibcode : 2011pnas..10819635K . doi : 10.1073/pnas.1103922108 . PMC 3241768 . PMID 22106287 .
- ^ Park SG, Schimmel P, Kim S (август 2008 г.). «Аминоациль -тРНК синтетазы и их связи с болезнью» . Труды Национальной академии наук Соединенных Штатов Америки . 105 (32): 11043–9. BIBCODE : 2008PNAS..10511043P . doi : 10.1073/pnas.0802862105 . PMC 2516211 . PMID 18682559 .
- ^ Ludmerer SW, Schimmel P (август 1987 г.). «Строительство и анализ делеций в аминоконцевом расширении глутаминовой тРНК-синтетазы Saccharomyces cerevisiae» . Журнал биологической химии . 262 (22): 10807–13. doi : 10.1016/s0021-9258 (18) 61035-x . PMID 3301842 .
- ^ Eriani G, Delarue M, Poch O, Gangloff J, Moras D (сентябрь 1990). «Разделение тРНК -синтетаз на два класса на основе взаимоисключающих наборов мотивов последовательности». Природа . 347 (6289): 203–6. Bibcode : 1990natur.347..203e . doi : 10.1038/347203A0 . PMID 2203971 . S2CID 4324290 .
- ^ Cusack S (декабрь 1997 г.). «Аминоацил-трна синтетазы». Современное мнение в структурной биологии . 7 (6): 881–9. doi : 10.1016/s0959-440x (97) 80161-3 . PMID 9434910 .
- ^ Lo WS, Gardiner E, Xu Z, Lau CF, Wang F, Zhou JJ, Mendlein JD, Nangle LA, Chiang KP, Yang XL, AU KF, Wong WH, Guo M, Zhang M, Schimmel P (июль 2014 г.). «Человеческая тРНК -синтетаза каталитические нули с разнообразными функциями» . Наука . 345 (6194): 328–32. Bibcode : 2014sci ... 345..328L . doi : 10.1126/science.1252943 . PMC 4188629 . PMID 25035493 .
- ^ Вакасуги К., Шиммель П (апрель 1999 г.). «Два различных цитокина, высвобождаемых из человеческой аминоацил-тРНК-синтетазы». Наука . 284 (5411): 147–51. Bibcode : 1999sci ... 284..147W . doi : 10.1126/science.284.5411.147 . PMID 10102815 .
- ^ Lareau LF, Green Re, Bhatnagar RS, Brenner SE (июнь 2004 г.). «Развивающиеся роли альтернативного сплайсинга». Современное мнение в структурной биологии . 14 (3): 273–82. doi : 10.1016/j.sbi.2004.05.002 . PMID 15193306 .
- ^ Вакасуги К., Слике Б.М., Худ Дж., Отани А., Эвальт К.Л., Фридлендер М., Шереш Д.А., Шиммель П (январь 2002 г.). «Человеческая аминоацил-тРНК-синтетаза как регулятор ангиогенеза» . Труды Национальной академии наук Соединенных Штатов Америки . 99 (1): 173–7. Bibcode : 2002pnas ... 99..173W . doi : 10.1073/pnas.012602099 . PMC 117534 . PMID 11773626 .
- ^ Цима Е., Читатель Дж.С., Ирани-Терани М., Эвальт К.Л., Шварц М.А., Шиммель П (январь 2005 г.). «Ve-Cadherin связывает цитокин тРНК-синтетазы с антиангиогенной функцией» . Журнал биологической химии . 280 (4): 2405–8. doi : 10.1074/jbc.c400431200 . PMID 15579907 . S2CID 6943506 .
- ^ Kawahara A, Stainier Dy (август 2009 г.). «Неканоническая активность серил-переносной РНК-синтетазы и сосудистого развития» . Тенденции в сердечно -сосудистой медицине . 19 (6): 179–82. doi : 10.1016/j.tcm.2009.11.001 . PMC 2846333 . PMID 20211432 .
- ^ Zhou Q, Kapoor M, Guo M, Belani R, Xu X, Kiosses WB, Hanan M, Park C, Armor E, Do MH, Nangle LA, Schimmel P, Yang XL (январь 2010 г.). «Ортогональное использование активного сайта тРНК -синтетазы человека для достижения многофункциональности» . Природа структурная и молекулярная биология . 17 (1): 57–61. doi : 10.1038/nsmb.1706 . PMC 3042952 . PMID 20010843 .
- ^ Park SG, Kim HJ, Min YH, Choi EC, Shin YK, Park BJ, Lee SW, Kim S (май 2005 г.). «Человеческая лизил-тРНК-синтетаза секретируется для запуска провоспалительного ответа» . Труды Национальной академии наук Соединенных Штатов Америки . 102 (18): 6356–61. doi : 10.1073/pnas.0500226102 . PMC 1088368 . PMID 15851690 .
- ^ Ариф А., Цзя Дж, Мэдт Р.А., Дикорлето П.Е., Фокс П.Л. (январь 2011). «Фосфорилирование глутамилпролил-тРНК-синтетазы с помощью циклин-зависимой киназы 5 диктует транскриптив-селективную трансляционную контроль» . Труды Национальной академии наук Соединенных Штатов Америки . 108 (4): 1415–20. Bibcode : 2011pnas..108.1415a . doi : 10.1073/pnas.1011275108 . PMC 3029695 . PMID 21220307 .
- ^ Guo M, Schimmel P (март 2013 г.). «Основные нетрансляционные функции синтетаз тРНК» . Природная химическая биология . 9 (3): 145–53. doi : 10.1038/nchembio.1158 . PMC 3773598 . PMID 23416400 .
- ^ Патаскар, Абхихет; Шампанское, Жюльен; Нагель, Ремко; Кенски, Джулиана; Лаос, Маарджа; Михаук, Джастин; Пак, Хуэй Сонг; Bleijerveld, Onno B.; Мортенте, Келли; Наварро, Жасмин Черногория; БЛОМАЕРТ, Наоми (2022-03-09). «Истощение триптофана приводит к заместителям триптофана к фенилаланинам» . Природа . 603 (7902): 721–727. Bibcode : 2022natur.603..721p . doi : 10.1038/s41586-022-04499-2 . ISSN 1476-4687 . PMC 8942854 . PMID 35264796 .
- ^ Зуко, Амила; Маллик, Мусхами; Томпсон, Робин; Сполдинг, Эмили Л.; Wienand, Anne R.; Был марием; Таденв, Абигейл Л.Д.; Ван Бакель, Ник; Sijlmans, Céline; Сантос, Леонардо А.; Буссманн, Джулия; Катиноцци, Марика; Дас, Сарада; Кулшреста, Дивита; Берджесс, Роберт В.; Игнатова, Зоя; Storkebaum, Erik (2021-09-03). «Сверхэкспрессия тРНК спасает периферическую невропатию, вызванную мутациями в синтетазе тРНК» . Наука . 373 (6559): 1161–1166. Bibcode : 2021sci ... 373.1161Z . doi : 10.1126/science.abb3356 . ISSN 1095-9203 . PMC 8856733 . PMID 34516840 .
- ^ Vona B, Maroofian R, Bellacchio E, Najafi M, Thompson K, Alahmad A, He L, Ahangari N, Rad A, Shahrokhzadeh S, Exodus P, Mittag F, Traub F, Movaffaggh J, Amiri N, Dosti M, Boostani R, Traub F, Movaffagg ,. Schmids M, Taylor RW, Karimiani EG (2018). «Расширение клинического фенотипа митохндриального заболевания, связанного с IARS2, » BMC Med Genet 19 (1): 196. doi : 10.1186/ s12881-018-0709-3 6233262PMC 30419932PMID
Внешние ссылки
[ редактировать ]- Амино+ацил-тРНА+синтетазы в Национальной библиотеке Медицинской библиотеки Медицинской библиотеки (Mesh)
- AARS человеческого гена в браузере UCSC Genome .
- ААРС ЧЕЛОВЕКА ДЕНЬ ГЕНА В БРОВЕРЕ Генома UCSC .