Ион
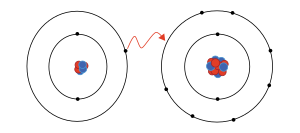
Ион ( / ˈ aɪ . ɒ n , - ən / ) [1] представляет собой атом или молекулу с чистым электрическим зарядом . Заряд электрона по соглашению считается отрицательным, и этот заряд равен и противоположен заряду протона , который по соглашению считается положительным. Суммарный заряд иона не равен нулю, поскольку общее количество его электронов не равно общему числу протонов.
Катион . – это положительно заряженный ион, у которого меньше электронов, чем у протонов [2] в то время как анион представляет собой отрицательно заряженный ион с большим количеством электронов, чем протонов. [3] Противоположные электрические заряды притягиваются друг к другу под действием электростатической силы , поэтому катионы и анионы притягиваются друг к другу и легко образуют ионные соединения .
Ионы, состоящие только из одного атома, называются атомарными или одноатомными ионами , а два или более атомов образуют молекулярные ионы или многоатомные ионы . В случае физической ионизации в жидкости (газе или жидкости) «ионные пары» создаются в результате спонтанных столкновений молекул, где каждая генерируемая пара состоит из свободного электрона и положительного иона. [4] Ионы также создаются в результате химических взаимодействий, таких как растворение соли в жидкостях , или другими способами, такими как прохождение постоянного тока через проводящий раствор, растворение анода посредством ионизации .
История открытия
Слово ион произошло от причастия настоящего времени среднего рода. Греческое ἰέναι ( иенай ), что означает «идти». Катион — это то, что движется вниз ( греч . κάτω , kato , что означает «вниз»), а анион — это то, что движется вверх ( греч . ἄνω , ano , что означает «вверх»). Они называются так потому, что ионы движутся к электроду противоположного заряда. Этот термин был введен (по предложению английского эрудита Уильяма Уэвелла ) [5] английским физиком и химиком Майклом Фарадеем в 1834 году для неизвестных тогда видов, которые переходят от одного электрода к другому через водную среду. [6] [7] Фарадей не знал природы этих видов, но он знал, что, поскольку металлы растворялись и попадали в раствор на одном электроде, а новый металл выделялся из раствора на другом электроде; что какое-то вещество прошло через раствор током. Это переносит материю из одного места в другое. В переписке с Фарадеем Уэвелл также ввел слова анод и катод , а также анион и катион как ионы, которые притягиваются к соответствующим электродам. [5]
Сванте Аррениус в своей диссертации 1884 года предложил объяснение того факта, что твердые кристаллические соли при растворении диссоциируют на парные заряженные частицы, за что он получил Нобелевскую премию по химии 1903 года. [8] Объяснение Аррениуса заключалось в том, что при образовании раствора соль диссоциирует на ионы Фарадея. Он предположил, что ионы образуются даже в отсутствие электрического тока. [9] [10] [11]
Характеристики
Ионы в газоподобном состоянии обладают высокой реакционной способностью и быстро взаимодействуют с ионами противоположного заряда, образуя нейтральные молекулы или ионные соли. Ионы также образуются в жидком или твердом состоянии, когда соли взаимодействуют с растворителями (например, водой) с образованием сольватированных ионов , которые более стабильны по причинам, связанным с сочетанием изменений энергии и энтропии по мере удаления ионов друг от друга. взаимодействовать с жидкостью. Эти стабилизированные виды чаще встречаются в окружающей среде при низких температурах. Типичным примером являются ионы, присутствующие в морской воде и образующиеся из растворенных солей.
Как заряженные объекты, ионы притягиваются к противоположным электрическим зарядам (от положительного к отрицательному и наоборот) и отталкиваются одноименными зарядами. Когда они движутся, их траектории могут отклоняться магнитным полем .
Электроны из-за своей меньшей массы и, следовательно, большей способности заполнять пространство как волны материи , определяют размер атомов и молекул, которые вообще обладают электронами. Таким образом, анионы (отрицательно заряженные ионы) больше, чем исходная молекула или атом, поскольку лишние электроны отталкивают друг друга и увеличивают физический размер иона, поскольку его размер определяется его электронным облаком . Катионы меньше соответствующего родительского атома или молекулы из-за меньшего размера электронного облака. Один конкретный катион (водорода) не содержит электронов и, следовательно, состоит из одного протона — намного меньше , чем исходный атом водорода.
Анионы и катионы
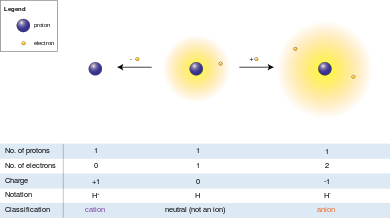
Анион (-) и катион (+) обозначают суммарный электрический заряд иона. Ион, у которого электронов больше, чем протонов, что придает ему суммарный отрицательный заряд, называется анионом, а знак минус «Анион (-)» указывает на отрицательный заряд. С катионом все наоборот: у него меньше электронов, чем у протонов, что придает ему чистый положительный заряд, отсюда и обозначение «катион (+)».
Поскольку электрический заряд протона по величине равен заряду электрона, суммарный электрический заряд иона равен числу протонов в ионе минус количество электронов.
Ан анион (-) ( / ˈ æ n ˌ aɪ . ən / ANN -eye-ən , от греческого слова ἄνω ( ánō ), что означает «вверх» [12] ) — это ион, в котором электронов больше, чем протонов, что придает ему суммарный отрицательный заряд (поскольку электроны заряжены отрицательно, а протоны заряжены положительно). [13]
А катион (+) ( / ˈ k æ t ˌ aɪ . ən / KAT -eye-ən , от греческого слова κάτω ( káto ), означающего «вниз» [14] ) — ион с меньшим количеством электронов, чем протонов, что придает ему положительный заряд. [15]
Есть дополнительные названия, используемые для ионов с несколькими зарядами. Например, ион с зарядом -2 известен как дианион , а ион с зарядом +2 известен как дикатион . Цвиттер -ион — это нейтральная молекула с положительными и отрицательными зарядами в разных местах внутри этой молекулы. [16]
Катионы и анионы измеряются по их ионному радиусу и различаются относительными размерами: «Катионы малы, большинство из них менее 10 −10 м (10 −8 см) в радиусе. Но большинство анионов имеют большие размеры, как и наиболее распространенный на Земле анион кислорода . Из этого факта видно, что большую часть пространства кристалла занимает анион, а катионы занимают промежутки между ними». [17]
Термины анион и катион (для ионов, которые соответственно перемещаются к аноду и катоду во время электролиза) были введены Майклом Фарадеем в 1834 году после его консультации с Уильямом Уэвеллом .
Природные явления
Ионы повсеместно распространены в природе Земли и ответственны за разнообразные явления — от свечения Солнца до существования ионосферы . Атомы в ионном состоянии могут иметь цвет, отличный от нейтральных атомов, поэтому поглощение света ионами металлов придает цвет драгоценным камням . Как в неорганической, так и в органической химии (в том числе в биохимии) взаимодействие воды и ионов имеет чрезвычайно важное значение. [ нужна ссылка ] ; примером является энергия, которая приводит к распаду аденозинтрифосфата ( АТФ ). [ нужны разъяснения ]
Сопутствующая технология
Ионы можно получить нехимическим путем с использованием различных источников ионов , обычно с использованием высокого напряжения или температуры. Они используются во множестве устройств, таких как масс-спектрометры , оптические эмиссионные спектрометры , ускорители частиц , имплантаторы ионов и ионные двигатели .
В качестве реактивных заряженных частиц они также используются для очистки воздуха путем уничтожения микробов, а также в предметах домашнего обихода, таких как детекторы дыма .
Поскольку передача сигналов и метаболизм в организмах контролируются точным ионным градиентом через мембраны , нарушение этого градиента способствует гибели клеток. Это общий механизм, используемый природными и искусственными биоцидами , в том числе ) ионных каналов грамицидином и амфотерицином ( фунгицидом .
Неорганические растворенные ионы являются компонентом общего количества растворенных твердых веществ и являются широко известным индикатором качества воды .
Обнаружение ионизирующего излучения
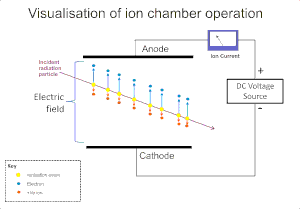
Ионизирующее воздействие излучения на газ широко используется для обнаружения таких излучений, как альфа , бета , гамма и рентгеновское излучение . Исходное событие ионизации в этих инструментах приводит к образованию «ионной пары»; положительный ион и свободный электрон в результате воздействия иона излучением на молекулы газа. Ионизационная камера является самым простым из этих детекторов и собирает все заряды, созданные в результате прямой ионизации газа посредством приложения электрического поля. [4]
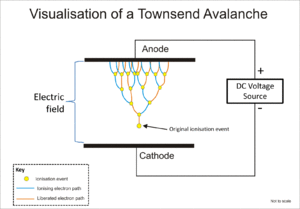
Трубка Гейгера -Мюллера и пропорциональный счетчик используют явление, известное как лавина Таунсенда, для умножения эффекта первоначального ионизирующего события посредством каскадного эффекта, при котором свободные электроны получают достаточную энергию от электрического поля, чтобы высвободить дальнейшие электроны путем ионное воздействие.
Химия
Обозначая заряженное состояние
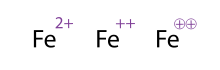
При написании химической формулы иона его суммарный заряд записывается в верхнем индексе сразу после химической структуры молекулы/атома. Чистый заряд записывается с указанием величины перед знаком; то есть двухзарядный катион обозначается как 2+ вместо +2 . Однако для однозарядных молекул/атомов величина заряда не указана; например, катион натрия обозначается как Уже + и не Уже 1+ .
Альтернативный (и приемлемый) способ показать молекулу/атом с несколькими зарядами — это многократное рисование знаков, это часто наблюдается с переходными металлами. Химики иногда обводят знак; это просто украшение и не меняет химического значения. Все три представления Фе 2+ , Фе ++ , и Фе ⊕⊕ показанные на рисунке, таким образом, эквивалентны.

Одноатомные ионы иногда обозначают также римскими цифрами , особенно в спектроскопии ; например, Фе 2+ (положительно заряженный дважды) пример, показанный выше, называется Fe(III) , Фе III или Fe III (Fe I для нейтрального атома Fe, Fe II для однократно ионизованного иона Fe). Римская цифра обозначает формальную степень окисления элемента, тогда как индо-арабские цифры в верхнем индексе обозначают чистый заряд. Таким образом, эти два обозначения можно заменить для одноатомных ионов, но римские цифры нельзя применять к многоатомным ионам. Однако можно смешать обозначения отдельного металлоцентра с многоатомным комплексом, как показано на примере иона уранила.
Подклассы
Если ион содержит неспаренные электроны , его называют ион- радикалом . Как и незаряженные радикалы, ион-радикалы очень реакционноспособны. Многоатомные ионы, содержащие кислород, такие как карбонат и сульфат, называются оксианионами . Молекулярные ионы, содержащие хотя бы одну углерод-водородную связь, называются органическими ионами . Если заряд органического иона формально сосредоточен на углероде, его называют карбокатионом (если заряжен положительно) или карбанионом (если заряжен отрицательно).
Формирование
Образование одноатомных ионов
Одноатомные ионы образуются в результате приобретения или потери электронов на валентной оболочке (самой внешней электронной оболочке) атома. Внутренние оболочки атома заполнены электронами, которые прочно связаны с положительно заряженным атомным ядром и поэтому не участвуют в такого рода химическом взаимодействии. Процесс приобретения или потери электронов нейтральным атомом или молекулой называется ионизацией .
Атомы могут быть ионизированы бомбардировкой излучением , но более обычным процессом ионизации, встречающимся в химии, является перенос электронов между атомами или молекулами. Этот перенос обычно обусловлен достижением стабильных («закрытых оболочек») электронных конфигураций . Атомы будут приобретать или терять электроны в зависимости от того, какое действие требует наименьшего количества энергии.
Например, атом натрия Na имеет один электрон в своей валентной оболочке, окружающей две стабильные, заполненные внутренние оболочки из 2 и 8 электронов. Поскольку эти заполненные оболочки очень стабильны, атом натрия имеет тенденцию терять свой лишний электрон и достигать этой стабильной конфигурации, становясь при этом катионом натрия.
С другой стороны, атом хлора Cl имеет 7 электронов в своей валентной оболочке, что на один меньше, чем в стабильной заполненной оболочке с 8 электронами. Таким образом, атом хлора стремится получить дополнительный электрон и достичь стабильной 8- электронной конфигурации , становясь при этом хлорид-анионом:
Эта движущая сила заставляет натрий и хлор вступать в химическую реакцию, в которой «лишний» электрон передается от натрия к хлору, образуя катионы натрия и анионы хлорида. Будучи противоположно заряженными, эти катионы и анионы образуют ионные связи и объединяются с образованием хлорида натрия NaCl, более известного как поваренная соль.
Образование многоатомных и молекулярных ионов

Многоатомные и молекулярные ионы часто образуются в результате приобретения или потери элементарных ионов, таких как протон, ЧАС + , в нейтральных молекулах. Например, аммиак когда NH 3 , принимает протон, ЧАС + — процесс, называемый протонированием — образует ион аммония , НХ + 4 . Аммиак и аммоний имеют одинаковое количество электронов, по существу, в одной и той же электронной конфигурации , но у аммония есть дополнительный протон, который придает ему чистый положительный заряд.
Аммиак также может потерять электрон, чтобы получить положительный заряд, образуя ион. НХ + 3 . Однако этот ион нестабилен, поскольку он имеет неполную валентную оболочку вокруг атома азота, что делает его очень реакционноспособным ион- радикалом .
Из-за нестабильности ион-радикалов многоатомные и молекулярные ионы обычно образуются путем приобретения или потери элементарных ионов, таких как ЧАС + , а не приобретать или терять электроны. Это позволяет молекуле сохранять стабильную электронную конфигурацию, приобретая при этом электрический заряд.
Ионизационный потенциал
Энергия , необходимая для отделения электрона в его низшем энергетическом состоянии от атома или молекулы газа с меньшим чистым электрическим зарядом, называется потенциалом ионизации , или энергией ионизации . энергия n-я ионизации атома — это энергия, необходимая для отрыва его n- го электрона после того, как первые n - 1 электронов уже оторвались.
Каждая последующая энергия ионизации заметно больше предыдущей. Особенно большое увеличение происходит после того, как какой-либо блок атомных орбиталей исчерпывается электронами. По этой причине ионы имеют тенденцию образовываться таким образом, что у них остаются полные орбитальные блоки. Например, натрий имеет один валентный электрон в своей внешней оболочке, поэтому в ионизированной форме он обычно встречается с одним потерянным электроном, как Уже + . На другой стороне таблицы Менделеева хлор имеет семь валентных электронов, поэтому в ионизированной форме он обычно встречается с одним присоединенным электроном, как кл. − . Цезий имеет самую низкую измеренную энергию ионизации из всех элементов, а гелий - самую большую. [18] В общем, энергия ионизации металлов намного ниже, чем энергия ионизации неметаллов , поэтому, как правило, металлы теряют электроны, образуя положительно заряженные ионы, а неметаллы приобретают электроны, образуя отрицательно заряженные ионы.
Ионная связь
Ионная связь – это разновидность химической связи , возникающая в результате взаимного притяжения противоположно заряженных ионов. Ионы одинакового заряда отталкиваются, а ионы противоположного заряда притягиваются. Следовательно, ионы обычно не существуют сами по себе, а связываются с ионами противоположного заряда, образуя кристаллическую решетку . Полученное соединение называется ионным соединением и, как говорят, удерживается вместе за счет ионной связи . В ионных соединениях между соседями ионов возникают характерные расстояния, из которых можно определить пространственную протяженность и ионный радиус отдельных ионов.
Наиболее распространенный тип ионной связи наблюдается в соединениях металлов и неметаллов (кроме благородных газов , которые редко образуют химические соединения). Металлы характеризуются наличием небольшого количества электронов сверх стабильной электронной конфигурации с закрытой оболочкой . Таким образом, они имеют тенденцию терять лишние электроны, чтобы достичь стабильной конфигурации. Это свойство известно как электроположительность . С другой стороны, неметаллы характеризуются наличием электронной конфигурации, которая всего на несколько электронов меньше стабильной конфигурации. Таким образом, они имеют тенденцию приобретать больше электронов для достижения стабильной конфигурации. Эта тенденция известна как электроотрицательность . Когда высокоэлектроположительный металл соединяется с высокоэлектроотрицательным неметаллом, лишние электроны от атомов металла передаются атомам неметалла с дефицитом электронов. В результате этой реакции образуются катионы металлов и анионы неметаллов, которые притягиваются друг к другу, образуя соль .
Общие ионы
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
См. также
Ссылки
- ^ «ион» . CollinsDictionary.com . ХарперКоллинз . Архивировано 24 декабря 2013 г. в Wayback Machine .
- ^ «катион» . Словарь Merriam-Webster.com . Проверено 6 октября 2021 г. Архивировано 6 октября 2021 г. в Wayback Machine .
- ^ «анион» . Словарь Merriam-Webster.com . Проверено 6 октября 2021 г. Архивировано 6 октября 2021 г. в Wayback Machine .
- ^ Jump up to: а б с Нолл, Гленн Ф. (1999). Обнаружение и измерение радиации (3-е изд.). Нью-Йорк: Уайли . ISBN 978-0-471-07338-3 .
- ^ Jump up to: а б Фрэнк Эй Джей Джеймс, изд. (1991). Переписка Майкла Фарадея, Том. 2: 1832–1840 . п. 183. ИСБН 9780863412493 . Архивировано из оригинала 14 апреля 2021 г. Проверено 16 октября 2020 г.
- ^ Майкл Фарадей (1791–1867) . Великобритания: Би-би-си .
- ^ «Интернет-словарь этимологии» . Архивировано из оригинала 14 мая 2011 г. Проверено 7 января 2011 г.
- ^ «Нобелевская премия по химии 1903 года» . nobelprize.org . Архивировано из оригинала 8 июля 2018 г. Проверено 13 июня 2017 г.
- ^ Харрис, Уильям; Леви, Джудит, ред. (1976). Энциклопедия Новой Колумбии (4-е изд.). Нью-Йорк: Колумбийский университет . п. 155 . ISBN 978-0-231-03572-9 .
- ^ Гетц, Филип В. (1992). МакГенри, Чарльз (ред.). Новая Британская энциклопедия . Том. 1 (15 изд.). Чикаго: Британская энциклопедия, Inc., стр. 587. Бибкод : 1991неб..книга.....Г . ISBN 978-0-85229-553-3 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Силлиспи, Чарльз, изд. (1970). Словарь научной биографии (1-е изд.). Нью-Йорк: Сыновья Чарльза Скрибнера . стр. 296–302. ISBN 978-0-684-10112-5 .
- ^ Издательство Оксфордского университета (2013). «Оксфордский справочник: ОБЗОР анионов» . oxfordreference.com. Архивировано из оригинала 18 января 2017 г. Проверено 15 января 2017 г.
- ^ Университет Колорадо в Боулдере (21 ноября 2013 г.). «Атомы и элементы, изотопы и ионы» . Колорадо.edu. Архивировано из оригинала 2 февраля 2015 года . Проверено 22 ноября 2013 г.
- ^ Издательство Оксфордского университета (2013). «Оксфордский справочник: ОБЗОР катионов» . oxfordreference.com. Архивировано из оригинала 18 января 2017 г. Проверено 15 января 2017 г.
- ^ Дуглас В. Хейвик, доктор философии; Университет Южной Алабамы (2007–2008 гг.). «Элементарная химия» (PDF) . usouthal.edu. Архивировано (PDF) из оригинала 4 декабря 2011 г. Проверено 22 ноября 2013 г.
- ^ Университет Пердью (21 ноября 2013 г.). «Аминокислоты» . Purdue.edu. Архивировано из оригинала 13 июля 2011 года . Проверено 22 ноября 2013 г.
- ^ Пресс, Фрэнк; Зивер, Раймонд (1986). Земля (14-е изд.). Нью-Йорк: WH Freeman and Company . п. 63. ИСБН 0-7167-1743-3 . OCLC 12556840 .
- ^ Химические элементы, перечисленные по энергии ионизации. Архивировано 30 марта 2009 г. в Wayback Machine . Lenntech.com
- ^ Jump up to: а б с «Обычные ионы и их заряды» (PDF) . Научный фанат . Архивировано (PDF) из оригинала 18 февраля 2018 г. Проверено 11 мая 2018 г.



