Обратный зооноз
Обратный zoon зооноз , также известный как зооантропоноз (греч. « животное», anthropos «человек», nosos « болезнь») или антропоноз , [ 1 ] представляет собой патоген , накапливающийся в организме человека и способный передаваться животным, не являющимся человеком . [ 2 ]
Терминология
[ редактировать ]Антропоноз относится к патогенам, источником которых является человек, и может включать передачу от человека к животному, а также от человека к человеку. Термин «зооноз» технически относится к заболеванию, передающемуся от любого животного к другому животному, человеку или нечеловеку, без усмотрения, а также определяется как заболевание, передающееся от животного к человеку и наоборот . [ 2 ] Тем не менее, из-за медицинских предубеждений, ориентированных на человека, зооноз, как правило, используется так же, как и антропозооноз, который конкретно относится к патогенам, хранящимся в животных, кроме человека, которые могут передаваться человеку. [ 2 ]
Дополнительная путаница, связанная с тем, что ученые часто используют термины «антропозооноз» и «зооантропоноз» как синонимы, была разрешена во время заседания Объединенного комитета по продовольствию и сельскому хозяйству и Всемирной организации здравоохранения в 1967 году , которое рекомендовало использовать термин «зооноз» для описания двунаправленного обмена инфекционными патогенами между животными и животными. люди. [ 3 ] [ 2 ]
Кроме того, поскольку люди редко находятся в прямом контакте с дикими животными и заносят патогены посредством «мягкого контакта», необходимо ввести термин «сапронотические агенты». Сапронозы (от греч. sapros «разложение») относятся к болезням человека, которые обладают способностью расти и размножаться (а не просто выживать или загрязнять) в абиотических средах, таких как почва, вода, разлагающиеся растения, трупы животных, экскременты и другие субстраты. [ 2 ] Кроме того, сапрозоонозы можно охарактеризовать как имеющие как живого хозяина, так и неживотное место развития в виде органического вещества, почвы или растений. [ 2 ] Облигатные внутриклеточные паразиты, которые не могут размножаться вне клеток и репродуктивная функция которых полностью зависит от проникновения в клетку для использования внутриклеточных ресурсов, такие как вирусы, риккетсии, хламидии и Cryptosporidium parvum, не могут быть сапронотическими агентами. [ 2 ]
Этимологические подводные камни
[ редактировать ]Разделение болезней на эпидемиологические классы по предполагаемому источнику инфекции или направлению передачи вызывает ряд противоречий, которые можно разрешить с помощью циклических моделей. [ нужна ссылка ] См. следующие сценарии:
Зооноз против обратного зооноза против антропоноза
[ редактировать ]В случае заболеваний, передающихся от членистоногих -переносчиков, таких как городская желтая лихорадка , лихорадка денге , эпидемический тиф , клещевой возвратный тиф , лихорадка Зика и малярия , [ 2 ] различие между терминами становится все более туманным. Например, человека, зараженного малярией, кусает комар, который впоследствии тоже заражается. Это случай обратного зооноза (от человека к животному). Однако вновь зараженный комар затем заражает другого человека. Это может быть случай зооноза (от животного к человеку), если первоначальным источником считается комар, или антропоноза (от человека к человеку), если первоначальным источником считается человек. Если бы этот инфицированный комар вместо этого заразил примата, не являющегося человеком, это можно было бы рассматривать как случай обратного зооноза/зооантропоноза (от человека к животному), если первичным источником считается человек, или просто зооноза (от животного к животному), если считается, что комар первоисточник.
Зооноз против антропоноза
[ редактировать ]Аналогичным образом, ВИЧ, возникший у обезьян (кроссовер из-за употребления человеком мяса диких ) шимпанзе и вирусы гриппа А , возникшие у птиц (кроссовер из-за антигенного сдвига), первоначально могли рассматриваться как зоонозный перенос, поскольку инфекции впервые произошли от позвоночных животных, но могли в настоящее время рассматривается как антропоноз из-за его способности передаваться от человека к человеку.
Сапроноз против сапрозооноза
[ редактировать ]Типичными примерами сапронотических агентов являются грибы, такие как кокцидиоидомикоз , гистоплазмоз , аспергиллез , криптококкоз , Microsporum gypseum . Некоторые из них могут быть бактериальными, от спорулирующих клостридий и бацилл до Rhodococcus equi, Burkholderia pseudomallei, Listeria , Erysipelothrix , Yersinia pseudotuberculosis, легионеллеза, понтиакской лихорадки и нетуберкулезных микобактериозов. Другие сапронозы являются амебными, как и при первичном амебном менингоэнцефалите . И снова трудности в классификации возникают в случае спорулирующих бактерий, инфекционные споры которых образуются только после значительного периода неактивного вегетативного роста в абиотической среде, однако это все равно считается случаем сапронозов. [ 2 ] Однако случаи зоосапронозов с участием Listeria , Erysipelothrix , Yersinia pseudotuberculosis , Burkholderia pseudomallei и Rhodococcus equi могут передаваться животным или абиотическим субстратом, но обычно происходят фекально-оральным путем между человеком и другими животными. [ 4 ]
Случаи со способами передачи
[ редактировать ]Векторы членистоногих
[ редактировать ]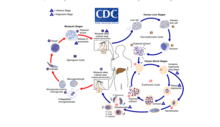
Малярия
[ редактировать ]Малярия предполагает циклическое заражение животных (человека и нечеловека) и комаров рода Anopheles рядом видов Plasmodium . Паразит Plasmodium передается комару, когда он питается кровью зараженного животного, после чего начинается спорогенный в кишечнике комара цикл, который заражает другое животное при следующем приеме крови. По-видимому, паразитарная инфекция не оказывает никакого вредного воздействия на комаров. [ 5 ] Паразит Plasmodium brasilianum, обычно встречающийся у приматов, морфологически похож на вызывающий малярию Plasmodium malariae, который чаще встречается у людей, и спорен вопрос о том, являются ли эти два вида на самом деле разными видами. [ 6 ] Тем не менее, появилось 12 сообщений о малярии в отдаленных общинах коренных народов яномами венесуэльской Амазонки , где неожиданно было обнаружено, что она вызвана штаммом P. brasilianum, на 100% идентичным последовательностям, обнаруженным у Alouatta seniculus . обезьян [ 7 ] Это предполагает явный зооноз и высокую вероятность обратного распространения в группы приматов, не относящихся к человеку, в виде обратных зоонозов. [ нужна ссылка ]

Африканская сонная болезнь
[ редактировать ]Trypanosoma brucei gambiense (T. b. gambiense) — это вид африканских трипаносом , представляющих собой простейших гемофлагелляты , ответственных за трипаносомоз (более известный как африканская сонная болезнь ) у людей и других животных. Простейшие передаются через мух цеце , где они размножаются и могут передаваться другому животному-хозяину во время кормления мухи кровью. [ 8 ] Вспышки сонной болезни в некоторых человеческих сообществах были ликвидированы, но лишь временно, поскольку постоянная реинтродуция из неизвестных источников статистически предполагает наличие нечеловеческого резервуара, где обратный поток возбудителя поддерживается в лесном цикле и повторно заносится в городскую среду. цикл. [ 9 ] Наличие Т. б. gambiense обнаруживался отдельно у людей и домашнего скота. Это стимулировало молекулярное исследование, сравнивающее реактивность сыворотки свиней , коз и коров человека с сывороткой , где наблюдалось заметное сходство во всех образцах, но особенно в образцах свиней. [ 10 ] В совокупности эти данные указывают на обратную зоонозную передачу вируса от человека к животному.
Арбовирусы
[ редактировать ]
Вирусы желтой лихорадки, вирусы лихорадки Денге и вирусы Зика относятся к флавивирусов родам , а Чикунгунья вирус — к родам альфавирусов . Все они считаются арбовирусами, что указывает на их способность передаваться через членистоногих-переносчиков. [ 11 ] [ 12 ] Сильватические циклы передачи арбовирусов в сообществах приматов, не являющихся людьми, могут перерасти в городской цикл среди людей, где люди могут оказаться тупиковыми хозяевами в сценариях, где дальнейшее смешение исключено, но гораздо более вероятным является повторное появление этих вирусов в любом из циклов. из-за обратного хода. [ 13 ] Очевидно, для поддержания городского цикла арбовирусов между людьми требуется редкое или недостаточно изученное сочетание факторов. Возникает одна из следующих ситуаций:
- Инфицированный человек в городской среде кормит лесного комара (обычно расположенного на удалении), такого как Haemogogus (который имеет относительно большую продолжительность жизни по сравнению с другими комарами и может передавать вирус в течение длительного периода времени), который заражает другого человека или животное, не являющееся человеком, которое будет служить резервуаром.
- Городской Aedes (чаще встречается в городских районах). [ 14 ] питает и передает вирус другому человеку или животному, не являющемуся человеком, которое будет служить резервуаром.
- Достаточное количество лесных комаров-переносчиков и животных-резервуаров населяет одну и ту же экологическую нишу в тесном контакте, что способствует и поддерживает зоонозный цикл вируса.
- Животный резервуар вируса поддерживает подходящий уровень вируса в крови, позволяющий заразиться комару-переносчику.
- Мостовой комар, такой как Aedes albopictus , который может выжить в городских районах и распространиться в сельские, полусельские и лесные районы, может переносить вирус в лесную среду. [ 15 ]
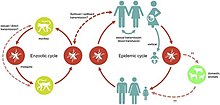
- Лихорадка Зика. Вирус Зика вызывается одноцепочечной РНК- флавивирусом, который использует комара Aedes в качестве вектора для заражения других людей и животных-хозяев. [ 16 ] Штамм вируса Зика 2015 года, выделенный от человека в Бразилии, использовался для заражения беременных макак-резус внутривенно и внутриамниотически . И самки, и плаценты были инфицированы образцами тканей, положительными по вирусу Зика, которые регистрировались в течение 105 дней. Это подтверждает потенциал обратного зоонозного переноса между людьми и приматами. [ 17 ]
- Желтая лихорадка: вирус желтой лихорадки также передается через укус инфицированных комаров вида Aedes или Haemagogus, которые питаются зараженным животным. Исторический ход американской работорговли является ярким примером внедрения возбудителя для создания совершенно нового лесного цикла. Предыдущие гипотезы о « YFV Нового Света » были опровергнуты в исследовании 2007 года, в котором изучались темпы нуклеотидных замен и расхождений, чтобы определить, что желтая лихорадка была завезена в Америку примерно 400 лет назад из Западной Африки . Примерно в 17 веке европейцы, причастные к работорговле, зафиксировали желтую лихорадку. Фактический способ заражения мог иметь место в ряде сценариев, будь то виремированный человек из Старого Света, инфицированный комар Старого Света, яйца, отложенные инфицированным комаром Старого Света, или все трое были перевезены в Америку, поскольку передача желтой лихорадки не произошла. редко встречается на парусных судах. [ 18 ] На фоне недавних вспышек желтой лихорадки на юго-востоке Бразилии потенциал обратного распространения был явно очевиден. [ 19 ] Молекулярные сравнения штаммов приматов, отличных от человека, оказались более тесно связаны с человеческими штаммами, чем штаммы, полученные от других приматов, не являющихся человеком, что позволяет предположить продолжающийся обратный зооноз. [ 20 ]
- Чикунгунья: Вирус Чикунгунья представляет собой альфавирус с одноцепочечной РНК, который обычно передается комарами Aedes другому животному-хозяину. Нет никаких доказательств того, что чикунгунья может препятствовать смене хозяев между людьми и приматами, кроме человека, поскольку у нее нет предпочтений ни к одному из видов приматов. Он имеет высокий потенциал распространения или обратного распространения в лесные циклы, как это было в случае с аналогичным арбовирусом, который был завезен в Америку во время работорговли. [ 21 ] Исследования доказали способность чикунгуньи перорально заражать лесные виды комаров, включая Haemagogus leucocelaenus и Aedes terrens . Более того, в ходе серологического исследования, проведенного на приматах, не являющихся человеком, в городских и пригородных районах штата Баия , у 11 животных были выявлены антитела, нейтрализующие чикунгунья . [ 13 ]
- Лихорадка Денге. Вирус Денге представляет собой флавивирус, который также передается комарами-переносчиками Aedes другим животным-хозяевам. Денге также была завезена в Америку в результате работорговли вместе с Aedes aegypti. [ 22 ] Исследование, проведенное в 2009 году во Французской Гвиане, показало, что инфекции вирусов денге типов с 1 по 4 присутствуют у различных типов неотропических лесных млекопитающих, помимо приматов, таких как грызуны , сумчатые и летучие мыши . После анализа последовательностей было обнаружено, что 4 штамма млекопитающих, не относящихся к человеку, имели индекс сходства от 89% до 99% с человеческими штаммами, циркулирующими в то же время. Это подтверждает, что другие млекопитающие, живущие поблизости, потенциально могут заразиться от человека, и указывает на наличие городского цикла. [ 23 ] [ 24 ] Случай, доказывающий, что членистоногие-переносчики способны заражаться, произошел в Бразилии, где Aedes albopictus (который часто встречается на задних дворах человеческих домов, но легко распространяется в сельской, полусельской и дикой среде) был обнаружен зараженным вирусом денге 3 в Сан-Паулу. Состояние. Тем временем в штате Баия было обнаружено, что лесной переносчик Haemogogus leucocelaenus заражен вирусом денге 1. [ 25 ] В другом исследовании, проведенном в Атлантическом лесу Баии, у приматов ( Leontopithecus chrysomelas и Sapajus xanthosternos ) были обнаружены антитела к вирусам денге 1 и 2, тогда как у ленивцев ( Bradypus torquatus ) были антитела к вирусу денге 3, что позволяет предположить возможное присутствие установленного лесного вируса денге. цикл. [ нужна ссылка ]
Дикие животные
[ редактировать ]
Большое количество диких животных, места обитания которых еще не подверглись вторжению человека, до сих пор подвергаются воздействию сапронотических агентов через загрязненную воду. [ нужна ссылка ]
Лямблии
[ редактировать ]- Бобры : Лямблии были завезены бобрам через сток сточных вод человека выше по течению от колонии бобра. [ 26 ]
Вирус гриппа А подтипа H1N1
[ редактировать ]- Тюлени : В 1999 году дикие тюлени были госпитализированы в реабилитационный центр голландских тюленей с гриппоподобными симптомами , и было обнаружено, что они на самом деле были инфицированы вирусом, подобным человеческому гриппу B , который циркулировал среди людей в 1995 году и претерпел антигенный сдвиг. с момента адаптации к новому хозяину-тюленю. [ 27 ]
Туберкулез
[ редактировать ]- Благородный олень , кабан : На участках интенсивного охотничьего хозяйства, включающих заграждения крупной дичи, места подкормки и выпаса скота, возникли случаи туберкулезного поражения диких благородных оленей и кабанов. У некоторых кабанов и оленей были одни и те же штаммы туберкулеза, которые были аналогичны штаммам, обнаруженным у домашнего скота и людей, что позволяет предположить возможное сапронотическое или сапрозоонозное заражение общих источников воды, дополнительного корма, прямого контакта с людьми или домашним скотом или их выделений. [ 28 ]
Домашние животные-компаньоны
[ редактировать ]кишечная палочка
[ редактировать ]- Собаки , лошади : были обнаружены доказательства заражения человеческими штаммами E. coli у нескольких собак и лошадей по всей Европе, что указывает на возможность зоонозной межвидовой передачи полирезистентных штаммов от человека к животным-компаньонам и наоборот. [ 29 ]
Туберкулез
[ редактировать ]- Собака: был Йоркширский терьер госпитализирован в ветеринарную клинику с хроническим кашлем, плохим удержанием веса и рвотой, о которых сообщалось в течение нескольких месяцев, после чего выяснилось, что владелец выздоровел от туберкулеза, однако первоначально у собаки были отрицательные тесты на туберкулез в 2 различных молекулярных исследованиях. анализы и был выписан. Через 8 дней собаку усыпили из -за обструкции уретры . Была проведена некроскопия, в результате которой образцы печени и трахеобронхиальных лимфатических узлов оказались положительными на тот же штамм туберкулеза, который был у владельца ранее. Это очень яркий случай обратного зооноза. [ 30 ]
Вирус гриппа А подтипа H1N1
[ редактировать ]- Хорьки : Хорьки часто используются в клинических исследованиях на людях , поэтому ранее была подтверждена возможность заражения их человеческим гриппом. Однако подтверждение естественной передачи человеческого штамма H1N1 в результате вспышки 2009 года среди домашних хорьков еще больше указывает на передачу вируса от человека к животному. [ 31 ]
COVID-19
[ редактировать ]В условиях глобальной пандемии COVID -19 2020 года была исследована восприимчивость кошек, хорьков, собак, кур , свиней и уток к SARS-CoV-2 коронавирусу и установлено, что он может воспроизводиться у кошек и хорьков с летальным исходом. .
- Кошки : Вирус может передаваться по воздуху между кошками. Вирусная РНК обнаруживалась в фекалиях в течение 3–5 дней после заражения, а патологоанатомические исследования выявили вирусную РНК в мягком небе , миндалинах и трахее . У котят наблюдались массивные поражения легких, слизистой оболочки эпителия носа и трахеи . Эпиднадзор за SARS-CoV-2 у кошек следует рассматривать как дополнение к ликвидации COVID-19 у людей. [ 32 ]
- Хорьки: хорькам были привиты вирусные штаммы из среды рынка морепродуктов Хуанань в Ухане, Китай, а также человеческие изоляты из Ухани. Было обнаружено, что для обоих изолятов вирус может реплицироваться в верхних дыхательных путях хорьков до 8 дней, не вызывая заболевания или смерти, а вирусная РНК была обнаружена в из прямой кишки мазках . Патологические исследования, проведенные через 13 дней после заражения, выявили легкий перибронхит в легких, тяжелый лимфоплазмоцитарный периваскулит и васкулит среди других заболеваний, при этом антител у всех хорьков была обнаружена выработка против SARS-CoV-2. Тот факт, что SARS-CoV-2 эффективно размножается в верхних дыхательных путях хорьков, делает их потенциальной животной моделью для оценки противовирусных препаратов или вакцин-кандидатов против COVID-19. [ 32 ]
- Собаки: Из протестированных собак породы бигль вирусная РНК была обнаружена в фекалиях, и у 50% привитых биглей наблюдалась сероконверсия через 14 дней, тогда как остальные 50% оставались серонегативными, демонстрируя низкую восприимчивость к SARS-CoV-2 у собак. [ 32 ]
- Курица, утка, свинья: не было никаких доказательств восприимчивости у кур, уток или свиней, при этом все мазки с вирусной РНК давали отрицательные и серонегативные результаты через 14 дней после инокуляции. [ 32 ]
Домашний скот
[ редактировать ]Вирус гриппа А подтипа H1N1
[ редактировать ]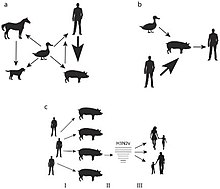
- Индюки : индейки В стаде норвежского наблюдалось снижение яйценоскости без каких-либо других клинических признаков после того, как работник фермы сообщил о наличии вируса H1N1 . Исследование показало, что индейки также были заражены гриппом H1N1 и были серопозитивны к его антигенам. Антитела H1N1, полученные от матери, были обнаружены в яичных желтках, а дальнейший генетический анализ выявил у индеек штамм H1N1, идентичный штамму H1N1, который был у работника фермы, который, вероятно, заразил индеек во время искусственного осеменения . [ 33 ]
- Свиньи: передача вируса H1N1 от человека к свинье была зарегистрирована в Канаде, [ 34 ] Корея, [ 35 ] и в конечном итоге включил в себя все континенты, за исключением Антарктиды во время вспышки 2009 года. [ 36 ] Также известно, что он распространяется во время сезонных эпидемий во Франции между людьми и свиньями. [ 37 ]
Метициллинрезистентный стафилококк золотистый
[ редактировать ]- Лошади: у 11 пациентов- лошадей , поступивших в ветеринарную больницу по разным причинам из разных ферм в течение примерно года, MRSA позже проявились инфекции . Учитывая, что изоляты MRSA встречаются у лошадей крайне редко, было высказано предположение, что вспышка MRSA была вызвана нозокомиальной инфекцией, полученной от человека во время пребывания лошадей в больнице. [ 38 ]
- Коровы, индейки, свиньи: случай обратного зооноза был предложен для объяснения того, как конкретный человеческий штамм Streptococcus Aureus, чувствительный к метициллину , был обнаружен у домашнего скота (свиней, индеек, коров) не только с потерей человеческих генов вирулентности (что могло снизить зоонозный потенциал для колонизации человека), но также добавление устойчивости к метициллину и тетрациклину (что увеличит частоту инфекций MRSA). Обеспокоенность здесь заключается в том, что чрезмерное использование антибиотиков в животноводстве усугубляет создание новых , устойчивых к антибиотикам зоонозных патогенов . [ 39 ]
Дикие животные в неволе
[ редактировать ]Туберкулез
[ редактировать ]- Слоны : В 1996 году Хоторнская цирковая корпорация сообщила, что 4 ее слона и 11 их владельцев являются носителями инфекции M. Tuberculosis . К сожалению, эти слоны были сданы в субаренду различным цирковым представлениям и зоологическим садам по всей Америке. Это спровоцировало общенациональную эпидемию , но поскольку туберкулез не является болезнью, которая обычно передается от животных к человеку, было высказано предположение, что эпидемия возникла из-за передачи заболевания от человека-дрессировщика к слону в неволе. [ 40 ]
Coronavirus
[ редактировать ]- Альпаки : Вспышка коронавируса альпака в 2007 году из-за смешения, произошедшего на национальной выставке альпака, привела к сравнению коронавирусов человека и альпаки в попытке определить источник вспышки. Было обнаружено, что коронавирус альпаки наиболее эволюционно похож на штамм коронавируса человека, который был выделен в 1960-х годах, что позволяет предположить, что коронавирус альпаки вполне мог циркулировать в течение десятилетий, вызывая респираторные заболевания в стадах, оставаясь незамеченными из-за отсутствия диагностических возможностей. Это также предполагает способ передачи вируса от человека к альпаке. [ 41 ]
Корь
[ редактировать ]- Нечеловекообразные приматы: В 1996 году в заповеднике произошла вспышка кори среди 94 нечеловекообразных приматов. Хотя источник вспышки так и не был определен, анализы сыворотки и мочи показали, что вирус определенно был связан с недавними случаями заболевания корью среди людей в США. [ 42 ]
Хеликобактер пилори
[ редактировать ]- Сумчатые : Полосатолицый Даннарт — австралийское сумчатое животное, которое столкнулось с многочисленными вспышками Helicobacter pylori в неволе. Взятие проб желудка сумчатого животного показало, что штамм H. pylori, ответственный за вспышки, на 100% совпадает со штаммом, происходящим из кишечного тракта человека. Таким образом, можно предположить, что вспышка произошла по вине обработчиков. [ 43 ]
Дикие животные в заповедниках
[ редактировать ]Коронавирусы
[ редактировать ]- Шимпанзе : Передача человеческого коронавируса HCoV-OC43 диким шимпанзе ( Pan troglodytes verus ), живущим в национальном парке Тай , Кот-д'Ивуар, была зарегистрирована в 2016–2017 годах. Эти шимпанзе, привыкшие к присутствию человека, изучали этих конкретных животных. сообщества с 1980-х годов [ 44 ] HCoV-OC43, принадлежащий к виду Betacoronavirus 1 (BetaCoV1), обычно вызывает эпизоды простуды у людей (исключая SARS и MERS ), но также обнаруживается у копытных , плотоядных и зайцеобразных . [ 45 ] Таким образом, вполне вероятно, что исследователи или браконьеры могли непреднамеренно передать вирус шимпанзе, тем самым обнаруживая еще один механизм переключения хозяина коронавируса. [ 46 ]
Риновирус С
[ редактировать ]- Шимпанзе: человека ранее считался уникальным патогеном для человека, Хотя риновирус С он был признан причиной вспышки респираторных инфекций у шимпанзе в Уганде в 2013 году . Исследование шимпанзе со всей Африки показало, что они демонстрируют универсальную гомозиготность 3 CDHR3-Y529 по аллели ( члену семейства, связанному с кадгерином ), который является рецептором , который резко увеличивает восприимчивость к инфекции риновируса С и астме у людей. Если респираторные вирусы человеческого происхождения способны поддерживать циркуляцию у приматов, кроме человека, это может оказаться вредным, если инфекция вернется в человеческие сообщества. [ 47 ]
Туберкулез
[ редактировать ]- Слоны: Некроскопия африканского слона, находящегося на свободном выгуле ( Loxodonta africana ) в Национальном парке Крюгера в Южной Африке, выявила значительное повреждение легких из-за человеческого штамма M. Tuberculosis. Слоны исследуют окружающую среду с помощью своих хоботов, поэтому весьма вероятно, что аэрозольные патогены из бытовых отходов, загрязненной воды человеческого сообщества вверх по течению, человеческих экскрементов или зараженной пищи туристов. источником инфекции были [ 48 ]
Пневмовирусы
[ редактировать ]- Шимпанзе: В Уганде сообщения о респираторных вирусах человеческого происхождения заразили две общины шимпанзе (Pan troglodytes schweinfurthii) в одном и том же лесу. Позже было обнаружено, что он вызван метапневмовирусом человека (также известным как MPV, Pneumoviridae , Metapneumovirus ) и респировирусом человека 3 (также известным как HRV3, Paramyxoviridae , Respirovirus или ранее известным как вирус парагриппа 3 ). [ 49 ]
Обратный зооноз у горилл
[ редактировать ]- Гориллы : охраняемые территории, подверженные экотуризму в Уганде, Руанде и Демократической Республике Конго , гориллы, живущие на свободном выгуле, все больше привыкают к присутствию людей, будь то проводники-рейнджеры, туристы, следопыты, ветеринары, браконьеры. или исследователи. Iodamoeba buetschlii , Giardia Lamblia , Chilomastix sp. , Endolimax nana , Entamoeba coli и Entamoeba histolytica были обнаружены в фекалиях горилл и беспорядочных фекалиях, оставленных людьми, вторгающимися в среду обитания. Кроме того, увеличилось количество Cryptosporidium sp. и капилляриозные инфекции были обнаружены у горилл, которые поддерживали более частый контакт с людьми, чем у тех, которые этого не делали. В совокупности эти данные позволяют предположить возникновение обратных зоонозов. [ 50 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Эдвардс С.Дж., Чаттерджи Х.Дж., Сантини Дж.М. (июнь 2021 г.). «Антропоноз и управление рисками: время этической вакцинации дикой природы?» . Ланцетный микроб . 2 (6): е230–е231. дои : 10.1016/S2666-5247(21)00081-1 . ПМК 8016401 . ПМИД 33824953 .
- ^ Перейти обратно: а б с д и ж г час я Хубалек З. (март 2003 г.). «Новые инфекционные болезни человека: антропонозы, зоонозы и сапронозы» . Новые инфекционные заболевания . 9 (3): 403–4. дои : 10.3201/eid0903.020208 . ПМЦ 2958532 . ПМИД 12643844 .
- ^ Зоонозы JF, Организация WH, Nations Fa (1967). Объединенный комитет экспертов ФАО/ВОЗ по зоонозам [заседание состоялось в Женеве с 6 по 12 декабря 1966 г.]: третий отчет . Всемирная организация здравоохранения. hdl : 10665/40679 . ISBN 978-92-4-120378-4 .
- ^ Тузио Х., Эдвардс Д., Элстон Т., Джарбо Л., Кудрак С., Ричардс Дж., Родан I (август 2005 г.). «Руководство по кошачьим зоонозам от Американской ассоциации практикующих кошек». Журнал кошачьей медицины и хирургии . 7 (4): 243–274. дои : 10.1016/j.jfms.2004.11.001 . ПМИД 16130211 . S2CID 8177042 .
- ^ Профилактика CC (28 января 2019 г.). «CDC – Малярия – О малярии – Биология» . www.cdc.gov . Проверено 22 апреля 2020 г.
- ^ Рамасами Р. (18 августа 2014 г.). «Зоонозная малярия – глобальный обзор, потребности в исследованиях и политике» . Границы общественного здравоохранения . 2 : 123. дои : 10.3389/fpubh.2014.00123 . ISSN 2296-2565 . ПМЦ 4135302 . ПМИД 25184118 .
- ^ Лалремруата А., Магрис М., Вивас-Мартинес С., Келер М., Эсен М., Кемпайя П., Джеярадж С., Перкинс Д.Д., Мордмюллер Б., Мецгер В.Г. (сентябрь 2015 г.). «Естественная инфекция Plasmodium brasilianum у людей: человек и обезьяна разделяют четырехкратных малярийных паразитов в венесуэльской Амазонии» . Электронная биомедицина . 2 (9): 1186–1192. дои : 10.1016/j.ebiom.2015.07.033 . ISSN 2352-3964 . ПМЦ 4588399 . ПМИД 26501116 .
- ^ «CDC – Африканский трипаносомоз – Биология» . www.cdc.gov . 12.06.2019 . Проверено 22 апреля 2020 г.
- ^ Фанк С., Нишиура Х., Хистербек Х., Эдмундс В.Дж., Чекки Ф. (17 января 2013 г.). «Идентификация циклов передачи при взаимодействии человека и животного: роль резервуаров животных в поддержании гамбийского африканского трипаносомоза человека» . PLOS Вычислительная биология . 9 (1): e1002855. Бибкод : 2013PLSCB...9E2855F . дои : 10.1371/journal.pcbi.1002855 . ISSN 1553-734X . ПМЦ 3547827 . ПМИД 23341760 .
- ^ Кордон-Обрас К., Кано Дж., Гонсалес-Пакановска Д., Бенито А., Наварро М., Барт Х.М. (23 декабря 2013 г.). «Адаптация Trypanosoma brucei gambiense к сыворотке различных млекопитающих связана с пластичностью сайта экспрессии VSG» . ПЛОС ОДИН . 8 (12): е85072. Бибкод : 2013PLoSO...885072C . дои : 10.1371/journal.pone.0085072 . ISSN 1932-6203 . ПМЦ 3871602 . ПМИД 24376866 .
- ^ Куно Дж., Чанг Г.Дж., Цучия К.Р., Карабатсос Н., Кропп CB (январь 1998 г.). «Филогения рода Flavivirus » Журнал вирусологии . 72 (1): 73–8 doi : 10.1128/JVI.72.1.73-83.1998 . ISSN 0022-538X . ПМК 109351 . ПМИД 9420202 .
- ^ Форрестер Н.Л., Паласиос Г., Теш Р.Б., Савджи Н., Гузман Х., Шерман М., Уивер С.С., Липкин В.И. (март 2012 г.). «Геномная филогения рода альфавирусов предполагает морское происхождение» . Журнал вирусологии . 86 (5): 2729–2738. дои : 10.1128/JVI.05591-11 . ISSN 1098-5514 . ПМК 3302268 . ПМИД 22190718 .
- ^ Перейти обратно: а б Фигейредо LT (2019). «Городские арбовирусы человека могут заражать диких животных и переходить к циклам лесного ухода в Южной Америке» . Границы клеточной и инфекционной микробиологии . 9 : 259. дои : 10.3389/fcimb.2019.00259 . ISSN 2235-2988 . ПМК 6653809 . ПМИД 31380302 .
- ^ Нденга Б.А., Мутуку Ф.М., Нгуги Х.Н., Мбакая Д.О., Асуани П., Мусунзаджи П.С., Вулуле Дж., Мукоко Д., Китрон У., ЛаБо А.Д. (19 декабря 2017 г.). «Характеристики взрослых комаров Aedes aegypti в сельских и городских районах западной и прибрежной Кении» . ПЛОС ОДИН . 12 (12): e0189971. Бибкод : 2017PLoSO..1289971N . дои : 10.1371/journal.pone.0189971 . ISSN 1932-6203 . ПМЦ 5736227 . ПМИД 29261766 .
- ^ Хэнли К.А., Монат Т.П., Уивер СК, Росси С.Л., Ричман Р.Л., Василакис Н. (октябрь 2013 г.). «Лихорадка против лихорадки: роль восприимчивости хозяина и переносчика и межвидовая конкуренция в формировании текущего и будущего распространения лесных циклов вируса денге и вируса желтой лихорадки» . Инфекция, генетика и эволюция . 19 : 292–311. Бибкод : 2013InfGE..19..292H . дои : 10.1016/j.meegid.2013.03.008 . ISSN 1567-7257 . ПМЦ 3749261 . ПМИД 23523817 .
- ^ «Эпидемиология вируса Зика» . www.zikavirusnet.com . Архивировано из оригинала 16 февраля 2020 г. Проверено 22 апреля 2020 г.
- ^ Коффи Л.Л., Ван Ромпей К., Кислер Р., Песавенто П., Сингапурец А., Линнен Дж., Гао К. (22 мая 2017 г.). «HHSF223201610542P Итоговый отчет» (PDF) . Управление по контролю за продуктами и лекарствами . Архивировано (PDF) из оригинала 26 января . Получено 22 . апреля
- ^ Брайант Дж.Э., Холмс Э.К., Барретт А.Д. (май 2007 г.). «Из Африки: молекулярный взгляд на занос вируса желтой лихорадки в Америку» . ПЛОС Патогены . 3 (5): е75. дои : 10.1371/journal.ppat.0030075 . ISSN 1553-7366 . ПМК 1868956 . ПМИД 17511518 .
- ^ Коуто-Лима Д., Мадек И., Берсо М.И., Кампос СС, Мотта М.Д., Сантос Ф.Б., Вазель М., Васконселуш П.Ф., Лоуренсу-де-Оливейра Р., Файу А.Б. (7 июля 2017 г.). «Потенциальный риск повторного возникновения городской передачи вируса желтой лихорадки в Бразилии, чему способствуют компетентные популяции Aedes» . Научные отчеты . 7 (1): 4848. Бибкод : 2017NatSR...7.4848C . дои : 10.1038/s41598-017-05186-3 . ISSN 2045-2322 . ПМК 5501812 . ПМИД 28687779 .
- ^ Морейра-Сото А, Торрес МК, Лима де Мендонса МК, Марес-Гия МА, Дос Сантос Родригес КД, Фабри А.А., Дос Сантос СС, Мачадо Араужу ЭС, Фишер К, Рибейру Ногейра РМ, Дростен К (сентябрь 2018 г.). «Доказательства множественных циклов лесной передачи во время вспышки вируса желтой лихорадки в Бразилии в 2016–2017 годах» . Клиническая микробиология и инфекции . 24 (9): 1019.e1–1019.e4. дои : 10.1016/j.cmi.2018.01.026 . ISSN 1469-0691 . ПМИД 29427798 .
- ^ Цецаркин К.А., Чен Р., Уивер С.С. (февраль 2016 г.). «Межвидовая передача и появление вируса чикунгунья» . Современное мнение в вирусологии . 16 : 143–150. дои : 10.1016/j.coviro.2016.02.007 . ISSN 1879-6257 . ПМЦ 4824623 . ПМИД 26986235 .
- ^ Хэнли К.А., Монат Т.П., Уивер СК, Росси С.Л., Ричман Р.Л., Василакис Н. (октябрь 2013 г.). «Лихорадка против лихорадки: роль восприимчивости хозяина и переносчика и межвидовая конкуренция в формировании текущего и будущего распространения лесных циклов вируса денге и вируса желтой лихорадки» . Инфекция, генетика и эволюция . 19 : 292–311. Бибкод : 2013InfGE..19..292H . дои : 10.1016/j.meegid.2013.03.008 . ISSN 1567-1348 . ПМЦ 3749261 . ПМИД 23523817 .
- ^ де Туази Б., Лакост В., Жермен А., Муньос-Хордан Х., Колон С., Моффри Х.Ф., Делаваль М., Катцефлис Ф., Казанджи М., Матеус С., Дюссар П. (апрель 2009 г.). «Инфекция денге у неотропических лесных млекопитающих» . Трансмиссивные и зоонозные болезни (Ларчмонт, Нью-Йорк) . 9 (2): 157–170. дои : 10.1089/vbz.2007.0280 . ISSN 1557-7759 . ПМИД 18945183 .
- ^ Кальдерон А., Гусман С., Маттар С., Родригес В., Мартинес С., Вайолет Л., Мартинес Х., Фигейредо Л.Т. (октябрь 2019 г.). «Вирус денге у летучих мышей из Кордовы и Сукре, Колумбия» . Трансмиссивные и зоонозные болезни (Ларчмонт, Нью-Йорк) . 19 (10): 747–751. дои : 10.1089/vbz.2018.2324 . ISSN 1557-7759 . ПМК 6765209 . ПМИД 31211661 .
- ^ де Фигейредо М.Л., де К. Гомеш А., Амарилья А.А., де С. Леандро А., де С. Оррико А., де Араужо РФ, до С.М. Кастро Х., Дуригон Э.Л., Акино В.Х., Фигейредо Л.Т. (12 июля 2010 г.). «Комары, зараженные вирусом денге в Бразилии» . Вирусологический журнал . 7 (1): 152. дои : 10.1186/1743-422X-7-152 . ISSN 1743-422X . ПМЦ 2913956 . ПМИД 20624314 .
- ^ Эш А., Лимбери А., Лемон Дж., Виталий С., Томпсон Р.К. (15 декабря 2010 г.). «Молекулярная эпидемиология Giardia duodenalis у находящегося под угрозой исчезновения хищника - африканской раскрашенной собаки» . Ветеринарная паразитология . 174 (3): 206–212. дои : 10.1016/j.vetpar.2010.08.034 . ISSN 0304-4017 . ПМИД 20851525 .
- ^ Остерхаус А.Д., Риммельцваан Г.Ф., Мартина Б.Е., Бестеброер Т.М., Фушье Р.А. (12 мая 2000 г.). «Вирус гриппа B у тюленей». Наука . 288 (5468): 1051–1053. Бибкод : 2000Sci...288.1051O . дои : 10.1126/science.288.5468.1051 . ISSN 0036-8075 . ПМИД 10807575 .
- ^ Барасона Х.А., Висенте Х., Диес-Дельгадо И., Аснар Х., Гортасар К., Торрес М.Дж. (август 2017 г.). «Присутствие комплекса микобактерий туберкулеза в окружающей среде в точках скопления на границе дикой природы и домашнего скота» . Трансграничные и новые болезни . 64 (4): 1148–1158. дои : 10.1111/tbed.12480 . ISSN 1865-1682 . ПМИД 26865411 . S2CID 22483980 .
- ^ Эверс С., Гроббель М., Штамм И., Копп П.А., Диль И., Земмлер Т., Фрут А., Бойтлих Дж., Герра Б., Вилер Л.Х., Гюнтер С. (апрель 2010 г.). «Появление человеческой пандемической Escherichia coli O25:H4-ST131 CTX-M-15, продуцирующей бета-лактамазы расширенного спектра, среди животных-компаньонов» . Журнал антимикробной химиотерапии . 65 (4): 651–660. дои : 10.1093/jac/dkq004 . ISSN 1460-2091 . ПМИД 20118165 .
- ^ Эрвин ПК, Бемис Д.А., МакКомбс С.Б., Шилер Л.Л., Химелрайт И.М., Хэлфорд С.К., Дием Л., Метчок Б., Джонс Т.Ф., Шиллинг М.Г., Томсен Б.В. (декабрь 2004 г.). «Передача микобактерий туберкулеза от человека к собаке» . Новые инфекционные заболевания . 10 (12): 2258–2210. дои : 10.3201/eid1012.040094 . ISSN 1080-6040 . ПМЦ 3323378 . ПМИД 15672533 .
- ^ Свенсон С.Л., Костер Л.Г., Дженкинс-Мур М., Киллиан М.Л., ДеБесс Э.Э., Бейкер Р.Дж., Малруни Д., Вайс Р., Галеота Дж., Бредтауэр А. (сентябрь 2010 г.). «Естественные случаи пандемического вируса гриппа А H1N1 2009 года у домашних хорьков» . Журнал ветеринарных диагностических исследований . 22 (5): 784–788. дои : 10.1177/104063871002200525 . ISSN 1040-6387 . ПМИД 20807944 .
- ^ Перейти обратно: а б с д Ши Дж, Вэнь З, Чжун Г, Ян Х, Ван С, Хуан Б, Лю Р, Хэ Х, Шуай Л, Сунь З, Чжао Ю (08 апреля 2020 г.). «Восприимчивость хорьков, кошек, собак и других домашних животных к SARS-коронавирусу 2» . Наука . 368 (6494): 1016–1020. дои : 10.1126/science.abb7015 . ISSN 0036-8075 . ПМК 7164390 . ПМИД 32269068 .
- ^ Сьюрсет С.К., Гьерсет Б., Брагстад К., Хунгнес О., Вислёфф Х., Эр С., Вальхейм М., Лётведт С.М., Дэвид Б., Ханссен С.А., Хауге Ш.Х. (2017). «Передача гриппа A(H1N1)pdm09 от человека к животному в племенном стаде индеек в Норвегии» . Экология и эпидемиология инфекций . 7 (1): 1416249. Бибкод : 2017InfEE...716249K . дои : 10.1080/20008686.2017.1416249 . ISSN 2000-8686 . ПМЦ 5738641 . ПМИД 29296243 .
- ^ Хауден К.Дж., Брокхофф Э.Дж., Кайя Ф.Д., МакЛеод Л.Дж., Лавуа М., Инг Дж.Д., Быстром Дж.М., Александерсен С., Пасик Дж.М., Берхан Й., Моррисон М.Е. (ноябрь 2009 г.). «Расследование вируса пандемического гриппа человека (H1N1) 2009 года на свиноферме в Альберте» . Канадский ветеринарный журнал . 50 (11): 1153–1161. ISSN 0008-5286 . ПМЦ 2764467 . ПМИД 20119537 .
- ^ Сон М.С., Ли Дж.Х., Паскуа П.Н., Пэк Ю.Х., Квон Хи, Пак К.Дж., Чой Х.В., Шин Ю.К., Сон Дж.И., Ким СиДжей, Чхве Ю.К. (сентябрь 2010 г.). «Доказательства передачи пандемического вируса гриппа (H1N1) 2009 от человека к свинье в Южной Корее» . Журнал клинической микробиологии . 48 (9): 3204–3211. дои : 10.1128/JCM.00053-10 . ISSN 0095-1137 . ПМЦ 2937722 . ПМИД 20610681 .
- ^ Нельсон М.И., Грамер М.Р., Винсент А.Л., Холмс Э.К. (октябрь 2012 г.). «Глобальная передача вирусов гриппа от человека к свиньям» . Журнал общей вирусологии . 93 (Часть 10): 2195–2203. дои : 10.1099/vir.0.044974-0 . ISSN 0022-1317 . ПМЦ 3541789 . ПМИД 22791604 .
- ^ Частагнер А., Энуф В., Пероз Д., Эрве С., Лукас П., Кегинер С., Горен С., Бевен В., Бехиллил С., Леневё П., Гарен Е. (октябрь 2019 г.). «Двунаправленная передача вируса сезонного гриппа A(H1N1)pdm09 от человека к свинье в стаде свиней, Франция, 2018» . Новые инфекционные заболевания . 25 (10): 1940–1943. дои : 10.3201/eid2510.190068 . ISSN 1080-6040 . ПМК 6759248 . ПМИД 31538914 .
- ^ Сеген Дж.К., Уокер Р.Д., Кэрон Дж.П., Клоос В.Е., Джордж К.Г., Холлис Р.Дж., Джонс Р.Н., Пфаллер М.А. (май 1999 г.). «Вспышка метициллин-резистентного золотистого стафилококка в ветеринарной клинической больнице: потенциальная передача от человека к животному» . Журнал клинической микробиологии . 37 (5): 1459–1463. doi : 10.1128/JCM.37.5.1459-1463.1999 . ISSN 0095-1137 . ПМЦ 84801 . ПМИД 10203505 .
- ^ Прайс Л.Б., Стеггер М., Хасман Х., Азиз М., Ларсен Дж., Андерсен П.С., Пирсон Т., Уотерс А.Е., Фостер Дж.Т., Шупп Дж., Джиллис Дж. (21 февраля 2012 г.). «Staphylococcus aureus CC398: адаптация хозяина и возникновение резистентности к метициллину у домашнего скота» . мБио . 3 (1). дои : 10.1128/mBio.00305-11 . ISSN 2150-7511 . ПМК 3280451 . ПМИД 22354957 .
- ^ Холт Н. (24 марта 2015 г.). «Мы находимся в разгаре эпидемии туберкулеза слонов» . Журнал «Сланец» . Проверено 22 апреля 2020 г.
- ^ Кроссли Б.М., Мок Р.Э., Каллисон С.А., Хиетала С.К. (12 декабря 2012 г.). «Идентификация и характеристика нового респираторного коронавируса альпака, наиболее тесно связанного с коронавирусом человека 229E» . Вирусы . 4 (12): 3689–3700. дои : 10.3390/v4123689 . ISSN 1999-4915 . ПМЦ 3528286 . ПМИД 23235471 .
- ^ Вилли М.Е., Вудворд Р.А., Торнтон В.Б., Вольф А.В., Флинн Б.М., Хит Дж.Л., Вилламарзо Ю.С., Смит С., Беллини В.Дж., Рота П.А. (февраль 1999 г.). «Борьба со вспышкой кори среди нечеловекообразных приматов Старого Света». Лабораторное зоотехника . 49 (1): 42–48. ISSN 0023-6764 . ПМИД 10090093 .
- ^ Эвери А.Л., Селвуд Л. , Кастано-Родригес Н., Лу В., Виндзор Х.М., Ви Дж.Л., Сверчак А., Маршалл Б.Дж., Каакуша Н.О., Митчелл Х.М., Саттон П. (07.02.2011). «Вызвала ли передача Helicobacter pylori от человека вспышку заболевания в колонии полосатых даннартов (Sminthopsis macroura)?» . Ветеринарное исследование . 42 (1): 26. дои : 10.1186/1297-9716-42-26 . ISSN 1297-9716 . ПМК 3042409 . ПМИД 21314909 .
- ^ Шимпанзе леса Тай: поведенческая экология и эволюция . Оксфорд, Нью-Йорк: Издательство Оксфордского университета. 15 июня 2000 г. ISBN 978-0-19-850507-5 .
- ^ Корман В.М., Мут Д., Нимейер Д., Дростен С. (2018). «Хозяева и источники эндемичных коронавирусов человека» . Достижения в области исследования вирусов . 100 : 163–188. дои : 10.1016/bs.aivir.2018.01.001 . ISBN 9780128152010 . ISSN 0065-3527 . ПМК 7112090 . ПМИД 29551135 .
- ^ Патроно Л.В., Самуни Л., Корман В.М., Нурифар Л., Рётемайер С., Виттиг Р.М., Дростен С., Кальвиньяк-Спенсер С., Леендерц Ф.Х. (27 июня 2018 г.). «Вспышка человеческого коронавируса OC43 у диких шимпанзе, Кот-д'Ивуар, 2016 г.» . Новые микробы и инфекции . 7 (1): 118. дои : 10.1038/s41426-018-0121-2 . ISSN 2222-1751 . ПМК 6021434 . ПМИД 29950583 .
- ^ Скалли Э.Дж., Баснет С., Рэнгхэм Р.В., Мюллер М.Н., Отали Э., Хероба Д., Гриндл К.А., Паппас Т.Е., Томпсон М.Е., Мачанда З., Уоттерс К.Е. (февраль 2018 г.). «Смертельное респираторное заболевание, связанное с риновирусом человека C, у диких шимпанзе, Уганда, 2013 г.» . Новые инфекционные заболевания . 24 (2): 267–274. дои : 10.3201/eid2402.170778 . ISSN 1080-6040 . ПМК 5782908 . ПМИД 29350142 .
- ^ Миллер М.А., Басс П., Роос Э.О., Хауслер Г., Диппенаар А., Митчелл Э., ван Шалквик Л., Робб-Остерман С., Уотерс В.Р., Сикар-Ганг А., Лященко К.П. (06 февраля 2019 г.). «Смертельный туберкулез у свободно живущего африканского слона и одно из последствий воздействия человеческих патогенов на здоровье в дикой природе» . Границы ветеринарной науки . 6:18 . дои : 10.3389/fvets.2019.00018 . ISSN 2297-1769 . ПМК 6373532 . PMID 30788347 .
- ^ Негри Дж.Д., Редди Р.Б., Скалли Э.Дж., Филлипс-Гарсия С., Оуэнс Л.А., Лангерграбер К.Е., Митани Дж.К., Эмери Томпсон М., Рэнгхэм Р.В., Мюллер М.Н., Отали Е (21 января 2019 г.). «Одновременные вспышки респираторных заболеваний у диких шимпанзе, вызванные отдельными вирусами человеческого происхождения» . Новые микробы и инфекции . 8 (1): 139–149. дои : 10.1080/22221751.2018.1563456 . ISSN 2222-1751 . ПМК 6455141 . PMID 30866768 .
- ^ Низейи Дж.Б., Инносент Р.Б., Эруме Дж., Калема Г.Р., Крэнфилд М.Р., Грачик Т.К. (апрель 2001 г.). «Кампилобактериоз, сальмонеллез и шигеллез у горных горилл Уганды, обитающих на свободном выгуле» . Журнал болезней дикой природы . 37 (2): 239–244. дои : 10.7589/0090-3558-37.2.239 . ISSN 0090-3558 . ПМИД 11310873 .