P16
| CDKN2A | |||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
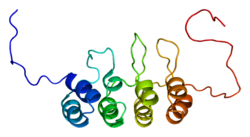 | |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | CDKN2A , CDK4I, CDKN2, CMM2, Ink4, Ink4a, MLM, MTS-1, MTS1, P14, P14ARF, P16, P16-INK4A, P16INK4, P16INK4A, P19, P19ARF, TP16, циклин-зависимая ингибитор KINASE 2A, циклин-зависимая Kinase-kinase Dy-зависимая Kinase Kinase Cinase Dy-зависимая Kinase Kinase-Kinase Dy-зависимая Kinase Kinase-Kinase Dy-зависимая Kinase Kinase-Kinase Dy-зависимая Kinase-Kinase. Ингибитор 2а, гены, p16, arf. | ||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Омим : 600160 ; MGI : 104738 ; Гомологен : 55430 ; GeneCards : CDKN2A ; OMA : CDKN2A - ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| Викидид | |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| Циклин-зависимый ингибитор киназы 2A P19ARF N-конце | |||
|---|---|---|---|
 Структура раствора N-концевой 37 аминокислот белка супрессора опухоли ARF мыши ARF | |||
| Идентификаторы | |||
| Символ | P19ARF_N | ||
| Pfam | PF07392 | ||
| InterPro | IPR010868 | ||
| Краткое содержание | 1hn3 / scope / supfam | ||
| |||
P16 (также известный как P16 Ink4a , циклин-зависимый ингибитор киназы 2A , CDKN2A , множественное опухолевое супрессор 1 и многочисленные другие синонимы), представляет собой белок , который замедляет деление клеток , замедляя прогрессирование клеточного цикла от фазы G1 до фазы S , тем самым действуя как подавляющий опухоль Полем Он кодируется CDKN2A геном . Удаление (упущение части последовательности ДНК во время репликации) в этом гене может привести к недостаточной или нефункциональной P16, ускоряя клеточный цикл и приводя к многим типам рака. [ 5 ] [ 6 ] [ 7 ]
P16 может использоваться в качестве биомаркера для повышения гистологической диагностики точность интраэпителиальной неоплазии шейки матки 3 степени (CIN). P16 также участвует в профилактике меланомы , плоско -клеточной карциномы ротоглотки , рака шейки матки , рака вульвара и рака пищевода .
P16 был обнаружен в 1993 году. Это белок с 148 аминокислотами и молекулярной массой 16 кДа , который включает в себя четыре повторения анкирина . [ 8 ] Название P16 происходит от его молекулярной массы , и альтернативное название p16 Ink4a относится к его роли в ингибировании циклин-зависимой киназы CDK4. [ 8 ]
Номенклатура
[ редактировать ]P16 также известен как:
- P16 Ink4a
- P16 Ink4
- Циклин-зависимый ингибитор киназы 2A (CDKN2A)
- CDKN2
- Ингибитор CDK 4
- Многократный супрессор опухоли 1 (MTS1)
- TP16
- Арф
- MLM
- P14
Ген
[ редактировать ]У людей P16 кодируется геном CDKN2A , расположенным на хромосоме 9 (9P21.3). Этот ген генерирует несколько вариантов транскрипта , которые различаются по их первым экзонами . По меньшей мере три альтернативно сплайсированные кодирующие различные белки, два из которых кодируют структурно связанные изоформы, которые, как известно, функционируют как ингибиторы CDK4 варианты , . Оставшаяся транскрипт включает в себя альтернативный экзон 1, расположенный на 20 кб вверх по течению от оставшейся части гена; Этот транскрипт содержит альтернативную открытую рамку считывания (ARF) , которая указывает белок, который структурно не связан с продуктами других вариантов. [ 9 ] Продукт ARF функционирует как стабилизатор белка -супрессора опухоли p53 , поскольку он может взаимодействовать и секвестра MDM2 , белка, ответственного за деградацию p53. [ 10 ] [ 11 ] Несмотря на их структурные и функциональные различия, изоформы ингибитора CDK и продукт ARF, кодируемые этим геном, посредством регуляторных ролей CDK4 и p53 в прогрессировании клеточного цикла G1 , имеют общую функциональность в контроле фазы G1 клеточного цикла. Этот ген часто мутируется или удаляется в широком спектре опухолей и, как известно, является важным геном -супрессором опухоли. [ 5 ]
Когда организмы возрастают, экспрессия p16 увеличивается, чтобы уменьшить пролиферацию стволовых клеток . [ 12 ] Это снижение деления и производство стволовых клеток защищает от рака , одновременно увеличивая риски, связанные с клеточным старением .
Функция
[ редактировать ]P16 является ингибитором циклина-зависимых киназ (CDK). Он замедляет клеточный цикл, запрещая прогрессирование от фазы G1 до фазы S. В противном случае, CDK4/6 связывает циклин D и образует активный белковый комплекс, который фосфорилирует белок ретинобластомы (PRB). После фосфорилирования PRB диссоциирует от транскрипционного фактора E2F1 . Это освобождает E2F1 из его связанного состояния в цитоплазме и позволяет ему войти в ядро. Оказавшись в ядре, E2F1 способствует транскрипции генов -мишеней, которые необходимы для перехода от фазы G1 к S. [ 13 ] [ 14 ]
Этот путь соединяет процессы онкогенеза опухоли и старения, фиксируя их на противоположных концах спектра. С одной стороны, гиперметилирование, мутация или делеция P16 приводит к подавлению гена и может привести к раку посредством нарушения регуляции прогрессирования клеточного цикла. И наоборот, активация p16 через активные формы кислорода , повреждение ДНК или старение приводит к накоплению p16 в тканях и участвует в старении клеток. [ 13 ]
Регулирование
[ редактировать ]Регуляция p16 является сложной и включает взаимодействие нескольких факторов транскрипции, а также несколько белков, участвующих в эпигенетической модификации посредством метилирования и репрессии промоторной области. [ 13 ]
PRC1 и PRC2 - это два белковых комплекса, которые модифицируют экспрессию p16 посредством взаимодействия различных факторов транскрипции, которые выполняют паттерны метилирования, которые могут подавлять транскрипцию p16. Эти пути активируются в клеточном ответе, чтобы уменьшить старение. [ 15 ] [ 16 ]
Клиническое значение
[ редактировать ]Роль в канцерогенезе
[ редактировать ]Мутации, приводящие к делеции или снижению функции гена CDKN2A, связаны с повышенным риском широкого спектра рака, а изменения гена часто наблюдаются в клеточных линиях раковых клеток . [ 17 ] [ 18 ] Примеры включают:
Аденокарцинома поджелудочной железы часто ассоциируется с мутациями в гене CDKN2A. [ 19 ] [ 20 ] [ 21 ]
Носители мутаций зародышевой линии в CDKN2A имеют, помимо их высоких рисков меланомы, также повышал риск рака поджелудочной железы, легких, гортани и ротоглотки. Курение табака повышает восприимчивость носителей к такому раковому заболеванию. [ 22 ]
Гомозиготные делеции p16 часто обнаруживаются в рака пищевода и рака желудка . клеточных линиях [ 23 ]
Мутации зародышевой линии в CDKN2A связаны с повышенной восприимчивостью к развитию рака кожи . [ 24 ]
Гиперметилирование генов -супрессоров опухолей участвует в различных видах рака. В 2013 году мета-анализ выявил повышенную частоту метилирования ДНК гена p16 при раке пищевода. По мере увеличения степени дифференцировки опухоли и частота метилирования ДНК P16.
Образцы тканей первичной плоскоклеточной карциномы полости рта (OSCC) часто демонстрируют гиперметилирование в промоторных областях P16. Раковые клетки демонстрируют значительное увеличение накопления метилирования на островах CPG в промоторной области P16. Это эпигенетическое изменение приводит к потере функции гена -супрессора опухоли посредством двух возможных механизмов: во -первых, метилирование может физически ингибировать транскрипцию гена, а во -вторых, метилирование может привести к рекрутированию факторов транскрипции, которые подавляют транскрипцию. Оба механизма вызывают один и тот же конечный результат: подавление экспрессии генов, которая приводит к снижению уровня белка p16. Было высказано предположение, что этот процесс отвечает за разработку различных форм рака, служащих альтернативным процессом делеции или мутации генов. [ 25 ] [ 26 ] [ 27 ] [ 28 ] [ 29 ] [ 30 ]
Было показано, что позитивность P16 является благоприятно прогностической при ротоглоточной плоскоклеточной раке. [ 31 ] В ретроспективном анализе пациентов с раком ротоглотки III стадии и IV оценивался статус ВПЧ, и было обнаружено, что 3-летний показатель общей выживаемости составил 82,4% (95% ДИ, 77,2–87,6) в HPV-позитивной подгруппе. и 57,1% (95% ДИ, от 48,1 до 66,1) в подгруппе с негативным ВПЧ, а 3-летняя ставка выживаемости без прогрессирования составила 73,7% (95% ДИ, от 67,7 до 79,8) и 43,4% (95% ДИ, 34,4 до 52,4) соответственно. Статус P16 настолько прогностическим, что система постановки AJCC была пересмотрена, чтобы включить статус P16 в статус группы ротоглоточных сквомочных клеток. [ 32 ] Тем не менее, некоторые люди могут иметь повышенный уровень P16, но испытать отрицательные на ВПЧ и наоборот. Это известно как дискордирующий рак. 5-летняя выживаемость для людей, которые положительно проверяют на ВПЧ и P16 составляет 81%, для дискордантного рака он составляет 53–55%и 40%для тех, кто проверяет отрицательный на P16 и HPV. [ 33 ] [ 34 ]
Клиническое использование
[ редактировать ]Биомаркер для типов рака
[ редактировать ]Экспрессия P16 используется в качестве прогностического биомаркера для определенных типов рака. Причиной этого является различные типы рака, могут оказывать различное влияние на экспрессию P16: раковые заболевания, которые сверхэкспрессируют P16, обычно вызваны папилломой человека (ВПЧ), тогда как рак, при котором p16 понижается, обычно имеют другие причины. Было показано, что для пациентов с пик -карциномой пик -клеток ротоглотости для выявления наличия биомаркера P16 является самым сильным показателем течения заболевания. Наличие биомаркера связано с более благоприятным прогнозом, измеренным с помощью специфической рака выживаемости (CSS), безрезультатной выживаемости (RFS), локализационным контролем (LRC), а также другими измерениями. Появление гиперметилирования p16 также оценивается как потенциальный прогностический биомаркер для рака простаты. [ 35 ] [ 36 ] [ 37 ]
P16 Рыба
[ редактировать ]P16 Удаление , обнаруженная рыбой в эпителиальных мезотелиальных пролиферациях, является прогнозирующей базовой инвазивной мезотелиомы . [ 38 ]
P16 Иммунохимия
[ редактировать ]

По мере того, как растет консенсус в отношении силы P16 в качестве биомаркера для обнаружения и определения прогнозов рака, иммуногистохимия P16 растет в важности. [ 13 ] [ 35 ] [ 40 ]
Гинекологический рак
[ редактировать ]P16 является широко используемым иммуногистохимическим маркером в гинекологической патологии. Сильная и диффузная цитоплазматическая и ядерная экспрессия p16 в плоскоклеточных карциномах (SCC) женского генитального тракта тесно связана с инфекцией вируса папилломы человека с высоким риском (HPV) и новообразований шейного происхождения. Большинство SCCS матки шейки матки Express P16. Однако P16 может экспрессироваться в других новообразованиях и в нескольких нормальных тканях человека. [ 41 ]
Мочевой пузырь SCCS
[ редактировать ]Более трети мочевого пузыря SCCS Express P16. SCCS мочевого пузыря Express P16 независимо от пола. П16 иммуногистохимическая экспрессия не может быть использована для различения SCC, возникающих в результате матки матки и мочевого пузыря. [ 41 ]
Роль в клеточном старении
[ редактировать ]Концентрации p16ink4a резко возрастают по сравнению с возрастом ткани. P16INK4A, наряду с ассоциированной с старением бета-галактозидазы , считается биомаркером клеточного старения . [ 42 ] Следовательно, p16ink4a может потенциально использоваться в качестве анализа крови, который измеряет, насколько быстро ткани организма стареют на молекулярном уровне. [ 43 ] Примечательно, что недавнее обследование клеточного старения, вызванное множественными обработками в нескольких клеточных линиях, не идентифицирует P16 как принадлежащий «основной сигнатуре» маркеров старения. [ 44 ]
Он использовался в качестве цели, чтобы задержать некоторые изменения старения у мышей. [ 45 ]
Роль в нейрогенезе
[ редактировать ]Увеличение экспрессии p16ink4a во время старения связано с пониженными функциями предшественника из субвентрикулярной зоны, которая генерирует на протяжении всей жизни новые нейроны, мигрирующие в обонятельную луковицу, тем самым снижая обонятельный нейрогенез. [ 46 ] Удаление p16ink4a не влияет на нейрогенез в другой нейрогенной нише взрослого взрослого, зубчатой извилине гиппокампа. [ 46 ] Однако в последнее время было продемонстрировано, что P16INK4A защищает от истощения после мощного пронерогенного стимула - ИЕ, работающего - также стволовые и предшественники клетки пожилой зубчатой извилины. [ 47 ] Фактически, после удаления p16ink4a стволовые клетки зубчатой извилины сильно активируются путем бега, в то время как в стволовых клетках Dentate Gyrus дикого типа не влияют. [ 47 ] Следовательно, P16INK4A играет роль в поддержании зубчатых стволовых клеток после стимула, сохраняя резерв их способности к самообновлению во время старения. Поскольку зубчатая извилина играет ключевую роль в формировании пространственной и контекстуальной памяти, P16INK4A участвует в поддержании когнитивных функций во время старения.
Открытие
[ редактировать ]Исследователи Мануэль Серрано, Грегори Дж. Хэннон и Дэвид Бич обнаружили P16 в 1993 году и правильно охарактеризовали белок как циклин-зависимый ингибитор киназы.
Роль в канцерогенезе
[ редактировать ]С момента своего открытия P16 стал значительным в области исследований рака. Предполагалось, что белок участвует в канцерогенезе из -за наблюдения, что мутация или делеция в гене были вовлечены в линии раковых клеток человека. Обнаружение инактивации P16 при семейной меланоме предоставило дополнительные доказательства. Удаление P16, мутация, гиперметилирование или сверхэкспрессия в настоящее время связаны с различными видами рака. Можно ли считать мутации в P16 мутациями драйверов, требует дальнейшего изучения. [ 17 ]
Взаимодействия
[ редактировать ]Было показано, что P16 взаимодействует :
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а беременный в GRCH38: Ensembl Release 89: ENSG00000147889 - ENSEMBL , май 2017 г.
- ^ Jump up to: а беременный в GRCM38: Ensembl Release 89: Ensmusg00000044303 - Ensembl , май 2017 г.
- ^ «Человеческая PubMed ссылка:» . Национальный центр информации о биотехнологии, Национальная медицина США .
- ^ «Мышь Pubmed ссылка:» . Национальный центр информации о биотехнологии, Национальная медицина США .
- ^ Jump up to: а беременный «Ген Entrez: CDKN2A-зависимый ингибитор киназы 2A (меланома, p16, ингибирует CDK4)» .
- ^ Nobori T, Miura K, Wu DJ, Lois A, Takabayashi K, Carson DA (апрель 1994 г.). «Делеции гена ингибитора киназы-4 циклина при множественном раке человека». Природа . 368 (6473): 753–756. Bibcode : 1994natur.368..753n . doi : 10.1038/368753A0 . PMID 8152487 . S2CID 13199401 .
- ^ Stone S, Jiang P, Dayananth P, Tavtigian SV, Katcher H, Parry D, et al. (Июль 1995 г.). «Сложная структура и регуляция локуса P16 (MTS1)» РАНКА 55 (14): 2988–2 7606716PMID
- ^ Jump up to: а беременный в Serrano M, Hannon GJ, Beach D (декабрь 1993 г.). «Новый регуляторный мотив в контроле клеточного цикла, вызывая специфическое ингибирование циклина D/CDK4». Природа . 366 (6456): 704–707. Bibcode : 1993natur.366..704s . doi : 10.1038/366704A0 . PMID 8259215 . S2CID 4368128 .
- ^ Хамош А. «Циклин-зависимый ингибитор киназы 2A; CDKN2A» . Омим Получено 10 декабря 2013 года .
- ^ «Молекулярная биология рака», Oxford University Press, 2005, ISBN 978-0-19-926472-8 , раздел 5.3
- ^ Руссель М.Ф. (сентябрь 1999). «Семейство ингибиторов клеточного цикла Ink4 при раке» . Онкоген . 18 (38): 5311–5317. doi : 10.1038/sj.onc.1202998 . PMID 10498883 .
- ^ Кришнамурти Дж., Рэмси М.Р., Лигон К.Л., Торрис С., Ко А., Боннер-Вайр С. и др. (Сентябрь 2006 г.). «P16INK4A вызывает возрастное снижение регенеративного потенциала островков». Природа . 443 (7110): 453–457. Bibcode : 2006natur.443..453k . doi : 10.1038/nature05092 . PMID 16957737 . S2CID 4402013 .
- ^ Jump up to: а беременный в дюймовый Rayess H, Wang MB, Srivatsan ES (апрель 2012 г.). «Клеточное старение и ген -супрессор опухоли P16» . Международный журнал рака . 130 (8): 1715–1725. doi : 10.1002/ijc.27316 . PMC 3288293 . PMID 22025288 .
- ^ Хара Э., Смит Р., Парри Д., Тахара Х, Стоун С., Петерс Г. (март 1996 г.). «Регуляция экспрессии p16CDKN2 и ее последствия для иммортализации и старения клеток» . Молекулярная и клеточная биология . 16 (3): 859–867. doi : 10.1128/mcb.16.3.859 . PMC 231066 . PMID 8622687 .
- ^ Cao R, Wang L, Wang H, Xia L, Erdjument-Bromage H, Tempst P, et al. (Ноябрь 2002). «Роль гистона H3 лизина 27 Метилирование в молчане поликомб-группа». Наука . 298 (5595): 1039–1043. Bibcode : 2002sci ... 298.1039c . doi : 10.1126/science.1076997 . PMID 12351676 . S2CID 6265267 .
- ^ Bracken AP, Kleine-Kohlbrecher D, Dietrich N, Pasini D, Gargiulo G, Beekman C, et al. (Март 2007 г.). «Поликомбные группы связываются по всему локусу INK4A-Arf и расположены в пожилых клетках» . Гены и развитие . 21 (5): 525–530. doi : 10.1101/gad.415507 . PMC 1820894 . PMID 17344414 .
- ^ Jump up to: а беременный Лиггетт В.Х., Сидранский Д. (март 1998 г.). «Роль гена супрессора опухоли P16 в раке». Журнал клинической онкологии . 16 (3): 1197–1206. doi : 10.1200/jco.1998.16.3.1197 . PMID 9508208 .
- ^ Рокко Дж.В., Сидранский Д. (март 2001 г.). «P16 (MTS-1/CDKN2/Ink4a) в прогрессировании рака». Экспериментальные исследования клеток . 264 (1): 42–55. doi : 10.1006/excr.2000.5149 . PMID 11237522 .
- ^ Caldas C, Hahn SA, Da Costa LT, Redston MS, Schutte M, Seymour AB, et al. (Сентябрь 1994). «Частые соматические мутации и гомозиготные делеции гена P16 (MTS1) при аденокарциноме поджелудочной железы». Природа генетика . 8 (1): 27–32. doi : 10.1038/ng0994-27 . PMID 7726912 . S2CID 23195660 .
- ^ Bartsch D, Shevlin DW, Tung WS, Kisker O, Wells SA, Goodfellow PJ (ноябрь 1995 г.). «Частые мутации CDKN2 в первичных аденокарциномах поджелудочной железы». Гены, хромосомы и рак . 14 (3): 189–195. doi : 10.1002/gcc.2870140306 . PMID 8589035 . S2CID 22823227 .
- ^ Liu L, Lassam NJ, Slingerland JM, Bailey D, Cole D, Jenkins R, et al. (Июль 1995 г.). «Мутация зародышевой линии p16ink4a и дисфункция белка в семействе с наследственной меланомой». Онкоген . 11 (2): 405–412. PMID 7624155 .
- ^ Helgadottir H, Höiom V, Jönsson G, Tuominen R, Ingvar C, Borg A, et al. (Август 2014). «Высокий риск раковых заболеваний, связанных с табаком, в CDKN2A-позитивных семействах меланомы» . Журнал медицинской генетики . 51 (8): 545–552. doi : 10.1136/jmedgenet-2014-102320 . PMC 4112445 . PMID 24935963 .
- ^ Игаки Х, Сасаки Х, Киши Т, Фут Х, Тахимори Ю., Като Х, и т. Д. (Сентябрь 1994). «Высокая частая гомозиготная делеция гена p16 в клеточных линиях раковых пищеводов» Биохимическая и биофизическая исследовательская коммуникация 203 (2): 1090–1 Doi : 10.1006/ brc.1994.2 PMID 8093026
- ^ Tell-Marti G, Fabra To, Martinez-Santamaría L, et al. (Март 2014 г.). есть Биологический Oncotarget 5 (6): 1439–1451. два 10.18632/oncotarget.1444: 4039222PMC 24742402PMID
- ^ Хор Г.Х., Фромминг Г.Р., Зейн Р.Б., Авраам М.Т., Омар Е., Тан С.К. и др. (2013). «Профилирование метилирования ДНК выявило промоторное гиперметилирование, вызванное молчанием p16, ddah2 и dusp1 при первичной плоскоклеточной карциноме полости рта» . Международный журнал медицинских наук . 10 (12): 1727–1739. doi : 10.7150/ijms.6884 . PMC 3805925 . PMID 24155659 .
- ^ Демокан С., Чуан А., Суоглу Ю., Улузан М., Ялньес З., Калифорния Дж.А. и др. (Октябрь 2012 г.). «Метилирование промотора и потеря экспрессии гена p16 (INK4A) при раке головы и шеи». Голова и шея . 34 (10): 1470–1475. doi : 10.1002/hed.21949 . PMID 22106032 . S2CID 11512476 .
- ^ Shaw RJ, Liloglou T, Rogers SN, Brown JS, Vaughan ED, Lowe D, et al. (Февраль 2006 г.). «Метилирование промотора p16, rarbeta, e-cadherin, циклина A1 и цитоглобина при раке полости рта: количественная оценка с использованием пиросеквенирования» . Британский журнал рака . 94 (4): 561–568. doi : 10.1038/sj.bjc.6602972 . PMC 2361183 . PMID 16449996 .
- ^ Sharma G, Mirza S, Prasad CP, Srivastava A, Gupta SD, Ralhan R (апрель 2007 г.). «Промоторное гиперметилирование p16ink4a, p14ARf, cyclind2 и slit2 в сыворотке и опухолевой ДНК у пациентов с раком молочной железы». Жизненные науки . 80 (20): 1873–1881. doi : 10.1016/j.lfs.2007.02.026 . PMID 17383681 .
- ^ Jabloonowski Z, Reszka E, Zładzińska J, Wąsowicz W, Sosnowski M (июнь 2011 г.). «Гиперметилирование областей генов P16 и промотора DAPK у пациентов с неинфазивным раком мочевого пузыря» . Архив медицинской науки . 7 (3): 512–516. Doi : 10.5114/aoms.2011.23421 . PMC 3258754 . PMID 22295037 .
- ^ Xu R, Wang F, Wu L, Wang J, Lu C (январь 2013). «Систематический обзор гиперметилирования гена p16 при раке пищевода». Раковые биомаркеры . 13 (4): 215–226. doi : 10.3233/cbm-130355 . PMID 24240582 .
- ^ Ang KK, Harris J, Wheeler R, Weber R, Rosenthal DI, Nguyen-Tân PF, et al. (Июль 2010). «Человеческий папилломавирус и выживание пациентов с раком ротоглотки» . Новая Англия Журнал медицины . 363 (1): 24–35. doi : 10.1056/nejmoa0912217 . PMC 2943767 . PMID 20530316 .
- ^ Lydiatt WM, Patel SG, O'Sullivan B, Brandwein MS, Ridge JA, Migliacci JC, et al. (Март 2017). «Изменения в раке головы и шеи в Американском совместном комитете по раку восьмого издания Руководство по постановке рака» . Калифорнийский 67 (2): 122–137. doi : 10.3322/caac.21389 . PMID 28128848 .
- ^ Mehanna H, Taberna M, Von Buchwald C, Tous S, Brooks J, Mena M, et al. (Март 2023 г.). «Прогностические последствия распределения P16 и ВПЧ при раке ротоглотки (HNCIG-EPIC-OPC): многоцентровый, многонациональный, отдельный анализ данных пациента». Lancet. Онкология . 24 (3): 239–251. doi : 10.1016/s1470-2045 (23) 00013-х . HDL : 2445/198366 . PMID 36796393 . S2CID 256860640 .
- ^ «Тестирование как на ВПЧ, так и на P16 может дать более точные прогнозы при раке ротоглотки (горла)» . Доказательства NIHR . 2023. doi : 10.3310/nihrevidence_59749 . S2CID 261791439 .
- ^ Jump up to: а беременный OgueJiofor KK, Hall JS, Mani N, Douglas C, Slevin NJ, Homer J, et al. (Ноябрь 2013). «Прогностическая значимость биомаркера P16 при ротоглоточной плоскоклеточной раке». Клиническая онкология . 25 (11): 630–638. doi : 10.1016/j.clon.2013.07.003 . PMID 23916365 .
- ^ Balgkouranidou I, Liloglou T, Lianidou ES (февраль 2013 г.). «Эпигенетика рака легких: новые биомаркеры» . Биомаркеры в медицине . 7 (1): 49–58. doi : 10.2217/bmm.12.111 . PMID 23387484 .
- ^ Синха П., Торстад В.Т., Нуссенбаум Б., Хауги Б.Х., Адкинс Д.Р., Каллогери Д. и др. (Январь 2014). «Отдаленное метастазирование при P16-позитивной пик-карциноме ротоглоточных клеток: критический анализ паттернов и результатов» . Устная онкология . 50 (1): 45–51. doi : 10.1016/j.oraloncology.2013.10.007 . PMC 3942323 . PMID 24211084 .
- ^ Hwang H, TSE C, Rodriguez S, Gown A, Churg A (май 2014). «Удаление рыб P16 при пролиферации поверхностного эпителия мезотелиальных пролиферов является прогнозирующей базовой инвазивной мезотелиомы». Американский журнал хирургической патологии . 38 (5): 681–688. doi : 10.1097/pas.0000000000000176 . PMID 24503757 . S2CID 28068784 .
- ^ Изображение Микаэля Хёггстрем, Md. Ссылка на терминологию: Anjelica Hodgson, MD, MD "P16 " Патология
{{cite web}}: CS1 Maint: Несколько имен: список авторов ссылка ) ( - ^ Dreyer JH, Hauck F, Oliveira-Silva M, Barros MH, Niedobitek G (апрель 2013 г.). «Обнаружение инфекции ВПЧ в плоскоклеточной карциноме головы и шеи: практическое предложение». Virchows Archiv . 462 (4): 381–389. doi : 10.1007/s00428-013-1393-5 . PMID 23503925 . S2CID 7469046 .
- ^ Jump up to: а беременный Cioffi-Lavina M, Chapman-Fredricks J, Gomez-Fernandez C, Ganjei-azar P, Manoharan M, Jorda M (июль 2010 г.). «Экспрессия P16 в плоскоклеточных карциномах шейки матки и мочевого пузыря». Прикладная иммуногистохимия и молекулярная морфология . 18 (4): 344–347. doi : 10.1097/pai.0b013e3181d2bbd7 . PMID 20571342 . S2CID 5065484 .
- ^ Холл Б.М., Балан В., Глейберман А.С., Стру Э., Краснов П., Виртуозо Л.П. и др. (Июль 2016 г.). «Старение мышей связано с P16 (Ink4a)-и β-галактозидазо-позитивным накоплением макрофагов, которое может быть индуцировано у молодых мышей старемными клетками» . Старение . 8 (7): 1294–1315. doi : 10.18632/старение.100991 . PMC 4993332 . PMID 27391570 .
- ^ Liu Y, Sanoff HK, Cho H, Burd CE, Torrice C, Ibrahim JG, et al. (Август 2009 г.). «Экспрессия p16 (ink4a) в Т-клетках периферической крови является биомаркером старения человека» . Старение ячейки . 8 (4): 439–448. doi : 10.1111/j.1474-9726.2009.00489.x . PMC 2752333 . PMID 19485966 .
- ^ Эрнандес-Сегура А., Де Йонг ТВ, Мелов С., Гурив В., Кампизи Дж., Демария М (сентябрь 2017 г.). «Раскрытие транскрипционной гетерогенности в стареющих клетках» . Текущая биология . 27 (17): 2652–2660.e4. Bibcode : 2017cbio ... 27E2652H . doi : 10.1016/j.cub.2017.07.033 . PMC 5788810 . PMID 28844647 .
- ^ Baker DJ, Wijshake T, Tchkonia T, Lebrasseur NK, Childs BG, Van de Sluis B, et al. (Ноябрь 2011). «Очистка p16ink4a-позитивных стареющих клеток задерживает связанные с возрастным расстройствами» . Природа . 479 (7372): 232–236. Bibcode : 2011natur.479..232b . doi : 10.1038/nature10600 . PMC 3468323 . PMID 22048312 .
- ^ Jump up to: а беременный Molofsky AV, Slutsky SG, Joseph NM, He S, Pardal R, Krishnamurthy J, et al. (Сентябрь 2006 г.). «Увеличение экспрессии p16ink4a уменьшает предшественники переднего мозга и нейрогенез во время старения» . Природа . 443 (7110): 448–452. Bibcode : 2006natur.443..448m . doi : 10.1038/nature05091 . PMC 2586960 . PMID 16957738 .
- ^ Jump up to: а беременный Micheli L, D'Andrea G, Ceccarelli M, Ferri A, Scardigli R, Tirone F (2019). «P16INK4A предотвращает активацию старых стволовых клеток с стеблями в возрасте . Границы в клеточной нейробиологии . 13 : 10. doi : 10.3389/fncel.2019.00010 . PMC 6374340 . PMID 30792628 .
- ^ Zhao L, Samuels T, Winckler S, Korgaonkar C, Tompkins V, Horne MC, et al. (Январь 2003). «Циклин G1 обладает ингибирующей активностью роста, связанной с путями супрессора опухолей ARF-MDM2-P53 и PRB». Молекулярное исследование рака . 1 (3): 195–206. PMID 12556559 .
- ^ Jump up to: а беременный Li J, Melvin WS, Tsai MD, Muscarella P (апрель 2004 г.). «Ядерный белок p34sei-1 регулирует киназную активность циклин-зависимой киназы 4 в зависимости от концентрации». Биохимия . 43 (14): 4394–4399. Citeseerx 10.1.1.386.140 . doi : 10.1021/bi035601s . PMID 15065884 .
- ^ Jump up to: а беременный Sugimoto M, Nakamura T, Ohtani N, Hampson L, Hampson In, Shimamoto A, et al. (Ноябрь 1999). «Регуляция активности CDK4 новым CDK4-связывающим белком, p34 (SEI-1)» . Гены и развитие . 13 (22): 3027–3033. doi : 10.1101/gad.13.22.3027 . PMC 317153 . PMID 10580009 .
- ^ Юинг Р.М., Чу П., Элизма Ф., Ли Х, Тейлор П., Клили С. и др. (2007). «Крупномасштабное картирование взаимодействия белка белка человека с помощью масс-спектрометрии» . Биология молекулярных систем . 3 : 89. doi : 10.1038/msb4100134 . PMC 1847948 . PMID 17353931 .
- ^ Jump up to: а беременный Fåhraeus R, Paramio JM, Ball KL, Laín S, Lane DP (январь 1996 г.). «Ингибирование фосфорилирования PRB и прогрессирования клеточного цикла с помощью пептида из 20 остатков, полученного из p16cdkn2/ink4a» . Текущая биология . 6 (1): 84–91. doi : 10.1016/s0960-9822 (02) 00425-6 . HDL : 20.500.11820/9E95B5CC-BE55-4C50-BFD9-04EB51B3E3F9 . PMID 8805225 . S2CID 23024663 .
- ^ Коулман К.Г., Ваутлет Б.С., Моррисси Д., Малгерон Дж., Седман С.А., Бринкли П. и др. (Июль 1997). «Идентификация последовательностей CDK4, участвующих в связывании циклина D1 и P16» . Журнал биологической химии . 272 (30): 18869–18874. doi : 10.1074/jbc.272.30.18869 . PMID 9228064 .
- ^ Руссо А.А., Тонг Л., Ли Джо, Джеффри П.Д., Павлич Н.П. (сентябрь 1998 г.). «Структурная основа для ингибирования циклин-зависимой киназы CDK6 с помощью опухолевого супрессора p16ink4a». Природа . 395 (6699): 237–243. Bibcode : 1998natur.395..237r . doi : 10.1038/26155 . PMID 9751050 . S2CID 204997058 .
- ^ Калдис П., Оджала П.М., Тонг Л., Макеле Т.П., Соломон М.Дж. (декабрь 2001 г.). «CAK-независимая активация CDK6 вирусным циклом» . Молекулярная биология клетки . 12 (12): 3987–3999. doi : 10.1091/mbc.12.12.3987 . PMC 60770 . PMID 11739795 .
- ^ Jump up to: а беременный Ivanchuk SM, Mondal S, Rutka JT (июнь 2008 г.). «P14ARF взаимодействует с DAXX: влияние на HDM2 и P53» . Клеточный цикл . 7 (12): 1836–1850. doi : 10.4161/cc.7.12.6025 . PMID 18583933 .
- ^ Jump up to: а беременный Ризос Х., Дифенбах Е., Бадхвар П., Вудрафф С., Беккер Т.М., Руни Р.Дж. и др. (Февраль 2003 г.). «Ассоциация P14ARF с транскрипционным репрессором P120E4F усиливает ингибирование клеточного цикла» . Журнал биологической химии . 278 (7): 4981–4989. doi : 10.1074/jbc.m210978200 . PMID 12446718 .
- ^ Jump up to: а беременный в Zhang Y, Wolf GW, Bhat K, Jin A, Allio T, Burkhart WA, et al. (Декабрь 2003 г.). «Рибосомный белок L11 отрицательно регулирует онкопротеин MDM2 и опосредует p53-зависимый путь рибосомально-стрессовой контрольной точки» . Молекулярная и клеточная биология . 23 (23): 8902–8912. doi : 10.1128/mcb.23.23.8902-8912.2003 . PMC 262682 . PMID 14612427 .
- ^ Jump up to: а беременный Zhang Y, Xiong Y, Yarbrough WG (март 1998 г.). «ARF способствует деградации MDM2 и стабилизирует делецию локуса P53: ARF-INK4A ухудшает как пути подавления опухоли RB, так и p53» . Клетка . 92 (6): 725–734. doi : 10.1016/s0092-8674 (00) 81401-4 . PMID 9529249 . S2CID 334187 .
- ^ Clark PA, Llanos S, Peters G (июль 2002 г.). «Многочисленные взаимодействующие домены способствуют, что P14ARF -опосредованное ингибирование MDM2» . Онкоген . 21 (29): 4498–4507. doi : 10.1038/sj.onc.1205558 . PMID 12085228 .
- ^ Pomerantz J, Schreiber-Agus N, Liégeois NJ, Silverman A, Alland L, Chin L, et al. (Март 1998 г.). «Продукт гена -супрессора опухоли INK4A, p19ARF, взаимодействует с MDM2 и нейтрализует ингибирование MDM2 P53» . Клетка . 92 (6): 713–723. doi : 10.1016/s0092-8674 (00) 81400-2 . PMID 9529248 . S2CID 17190271 .
- ^ Vivo M, Calogero RA, Sansone F, Calabrò V, Parisi T, Borrelli L, et al. (Апрель 2001 г.). «Арф-супрессор опухоли человека взаимодействует с спинофилином/невробином II, белком-фосфатазом-связывающим белком типа 1» » . Журнал биологической химии . 276 (17): 14161–14169. doi : 10.1074/jbc.m006845200 . PMID 11278317 .
Внешние ссылки
[ редактировать ]- Гены,+P16 в Национальной библиотеке медицины Медицинской библиотеки США (Mesh)
- CDKN2A гена человека в браузере генома UCSC .
- CDKN2A Человеческий ген детали в браузере генома UCSC .