Полный синтез стрихнина
Эту статью может потребовать очистки Википедии , чтобы она соответствовала стандартам качества . Конкретная проблема: MOS (особенно CHEM-MOS и дефисы). ( Март 2020 г. ) |

Полный синтез стрихнина в химии описывает полный синтез сложной биомолекулы стрихнина . Метод, впервые описанный группой Роберта Бернса Вудворда в 1954 году, считается классическим в этой области исследований. [2] [3] [4] [5]
В то время это стало естественным завершением сложного процесса выяснения молекулярной структуры , который начался с выделения стрихнина из бобов Strychnos ignatii Пьером Жозефом Пеллетье и Жозефом Бьенеме Каванту в 1818 году. [6] Основной вклад в эту работу внесли сэр Роберт Робинсон, опубликовавший более 250 публикаций, и Герман Лойхс, написавший еще 125 статей за 40 лет. Робинсон был удостоен Нобелевской премии по химии в 1947 году за исследования алкалоидов, в том числе стрихнина.
Процесс химической идентификации завершился публикациями Робинсона в 1946 году. [7] [8] [9] и позже подтверждено Вудвордом в 1947 году. [10] Рентгеновские структуры, устанавливающие абсолютную конфигурацию, стали доступны между 1947 и 1951 годами благодаря публикациям Йоханнеса Мартина Бийвоета. [11] [12] и Дж. Х. Робертсон [13] [14]
Вудворд опубликовал очень краткий отчет о синтезе стрихнина в 1954 году (всего 3 страницы). [15] и длинный (42 страницы) в 1963 году. [16]

Существует гораздо больше методов, о которых сообщили исследовательские группы Магнуса. [17] Оверман, [18] Кюне, [19] [20] Равал, [21] Босх, [22] [23] Воллхардт, [24] [25] Мори, [26] [27] Сибасаки, [28] Что, [29] Фукуяма [30] Вандервал [31] и Макмиллан. [32] Известен также синтетический (+)-стрихнин. [33] [34] Рацемические синтезы были опубликованы Падвой в 2007 году. [35] и в 2010 году Андраде [36] и Рейссиг. [37] В своей публикации 1963 года Вудворд процитировал сэра Роберта Робинсона, который сказал: [38] по размеру молекул это самое сложное из известных веществ .
Молекула
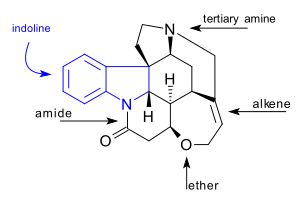
[ редактировать ]Молекула стрихнина C 21 H 22 N 2 O 2 содержит 7 колец, включая индолиновую систему. Он имеет третичную аминогруппу , амидную , алкеновую и эфирную группу. Встречающееся в природе соединение также является хиральным и имеет 6 асимметричных атомов углерода, включая один четвертичный.
Синтез Вудворда
[ редактировать ]Синтез колец II, V
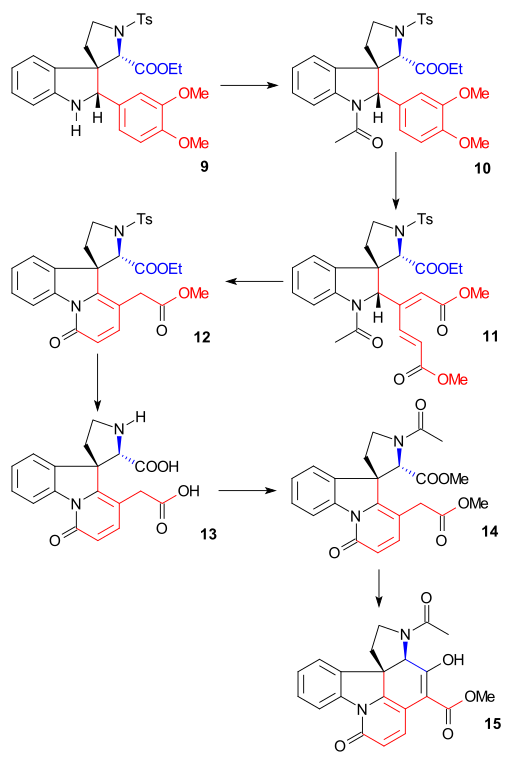
[ редактировать ]Синтез кольца II был осуществлен с помощью индольного синтеза Фишера с использованием фенилгидразина 1 и ацетофенона производного ацетовератрона 2 (катализатор - полифосфорная кислота ) с получением 2-вератрилиндола 3 . Вератриловая группа не только блокирует положение 2 для дальнейшего электрофильного замещения , но и становится частью стрихнинового скелета. Реакция Манниха с формальдегидом и диметиламином дает грамин 4 . Алкилирование иодметаном четвертичной аммониевой привело к образованию промежуточной соли которая прореагировала с цианидом натрия при нуклеофильном замещении до нитрила 5 и затем при восстановлении литийалюминийгидридом , до триптамина 6 . Амин-карбонильная конденсация с этилглиоксилатом дает имин 7 . Реакция этого имина с TsCl в пиридине с замкнутым кольцом N-тозильного соединения 8 была описана Вудвордом как согласованная нуклеофильная енаминная атака и формально реакция Пикте-Шпенглера . Это соединение должно образоваться в виде диастереомерной пары , но обнаружено только одно соединение, хотя какое именно, не исследовали. Наконец вновь образовавшаяся двойная связь сократилась на боргидрид натрия в индолин 9 с атомом водорода C8, приближающимся с наименее затрудненной стороны (этот протон удаляется позже в последовательности и не имеет значения).
Синтез колец III, IV
[ редактировать ]Индолин 9 был ацетилирован до N-ацетильного соединения 10 ( уксусный ангидрид , пиридин ), а затем вератриловая группа затем была раскрыта с помощью озона в водном растворе уксусной кислоты до сложного эфира муконовой кислоты 11 (что стало возможным благодаря двум электронодонорным метоксидным группам). Это пример биоинспирированного синтеза , уже предложенного Вудвордом в 1948 году. [39] Расщепление ацетильной группы и гидролиз эфира HCl в метаноле привели к образованию пиридона эфира 12 с дополнительной изомеризацией экзоциклической . двойной связи в эндоциклическую двойную связь (разрушая один асимметрический центр) Последующая обработка йодоводородом и красным фосфором удалила тозильную группу и гидролизовала обе оставшиеся сложноэфирные группы с образованием двухосновной кислоты 13 . Ацетилирование и этерификация ( диазометан ) давали ацетиловый диэфир 14 , который затем подвергали конденсации Дикмана с метоксидом натрия в метаноле с образованием енола 15 .
Синтез кольца VII
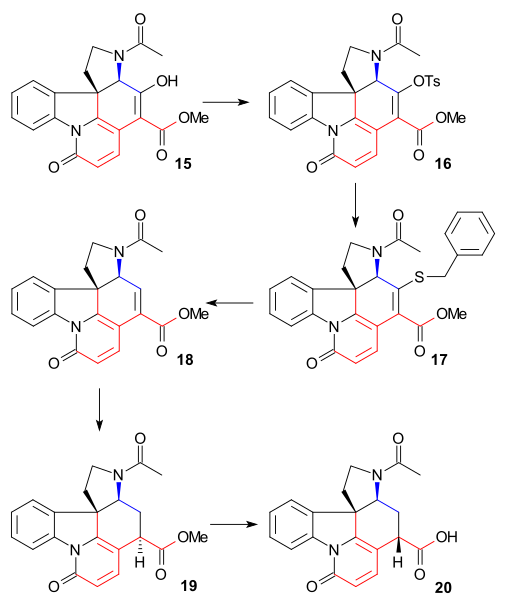
[ редактировать ]Для удаления спиртовой группы C15 енол 15 превращали в тозилат 16 ( TsCl , пиридин ), а затем в меркаптоэфир 17 (бензилмеркаптид натрия), который затем восстанавливали до ненасыщенного эфира 18 Ренея никелем и водородом . Дальнейшее восстановление водородом/ палладием на угле дало насыщенный эфир 19 . Щелочной гидролиз эфира до карбоновой кислоты 20 сопровождался эпимеризацией по С14.
Это конкретное соединение уже было известно из исследований разложения стрихнина. До сих пор все промежуточные соединения были рацемическими , но на этом конкретном этапе хиральность была введена посредством хирального разделения с использованием хинидина .
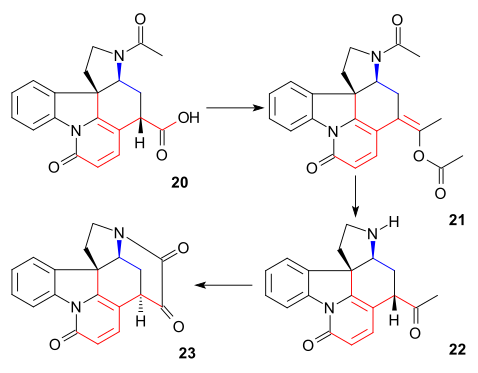
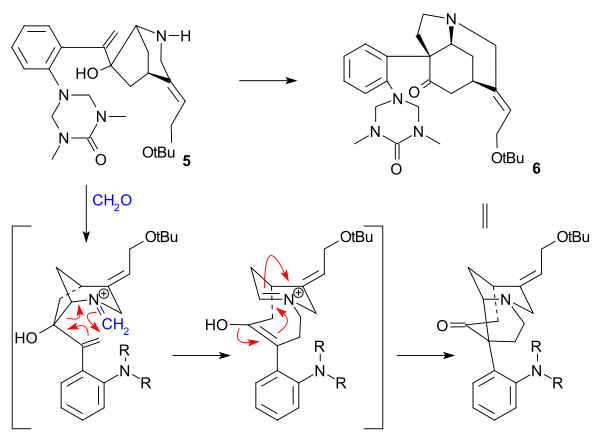
Затем атом углерода C20 был введен уксусным ангидридом с образованием енолацетата 21 , а свободный аминокетон 22 был получен гидролизом соляной кислоты . Кольцо VII в интермедиате 23 замыкается в результате окисления диоксида селена , процесса, сопровождающегося повторной эпимеризацией по C14.
Образование 21 можно представить как последовательность ацилирования, депротонирования, перегруппировки с потерей углекислого газа и снова ацилирования:
Синтез кольца VI
[ редактировать ]К дикетону 23 ( добавляли ацетилид натрия алкинилирование ) (вводя атомы углерода 22 и 23), получая алкин 24 . Это соединение было восстановлено до аллилового спирта 25 с использованием катализатора Линдлара , а алюмогидрид лития удалил оставшуюся амидную группу в 26 . Аллильную перегруппировку в спирт 27 (изострихнин) осуществляли бромистым водородом в уксусной кислоте с последующим гидролизом серной кислотой . На заключительном этапе обработки (-)-стрихнина 28 обработка 27 этанольным гидроксидом калия вызывала перегруппировку двойной связи C12-13 и замыкание кольца при конъюгатном присоединении гидроксильного аниона.
Синтез Магнуса
[ редактировать ]В ходе этой работы первым был синтезирован один из многих продуктов разложения стрихнина (перемежающее соединение), соединение, которое также можно получить в несколько стадий из другого продукта разложения, называемого альдегидом Виланда-Гумлиха . В заключительном этапе из релейного соединения был синтезирован сам стрихнин.
Синтез Овермана
[ редактировать ]В синтезе Овермана (1993) в качестве исходного материала использовалось хиральное соединение циклопентена полученное ферментативным гидролизом цис , -1,4-диацетоксициклопент-2-ена. Это исходное вещество в несколько стадий превращали в триалкилстаннан 2 , который затем связывали с арилйодидом 1 по реакции Стилле в присутствии монооксида углерода ( трис(дибензилиденацетон)дипалладий(0) , трифениларсин ). Внутренний дубль в 3 был преобразован в эпоксид с использованием трет-бутилгидропероксида , карбонильная группа затем была преобразована в алкен в реакции Виттига с использованием Ph 3 P=CH 2 , а группа TIPS была гидролизована ( TBAF ) и заменена трифторацетамидом . группа (NH 2 COCF 3 , NaH ) в 4 . циклизация Затем произошла (NaH), в результате которой эпоксидное кольцо открылось, а трифторацетильная группа была удалена с помощью КОН с получением азабициклооктана 5 .
Ключевой стадией была реакция аза- Коупа - Манниха, инициированная амино-карбонильной конденсацией с использованием формальдегида и образующая 6 с количественным выходом:
В конечной последовательности стрихнин был получен через альдегид Виланда-Гумлиха ( 10 ):
Промежуточное соединение 6 ацилировали с использованием метилцианоформиата и две защитные группы ( трет-бутил и ) удаляли с помощью HCl / MeOH в 7 . Двойную связь C8C13 восстанавливали цинком (MeOH/H + ) до насыщенного эфира 8 (смесь). Эпимеризация по C13 с метоксидом натрия в MeOH привела к образованию бета-эфира 9 , который был восстановлен диизобутилалюминийгидридом до альдегида Виланда-Гумлиха 10 . Превращение этого соединения малоновой кислотой в (-)-стрихнин 11 уже было известно как процедура.
Синтез Кюне
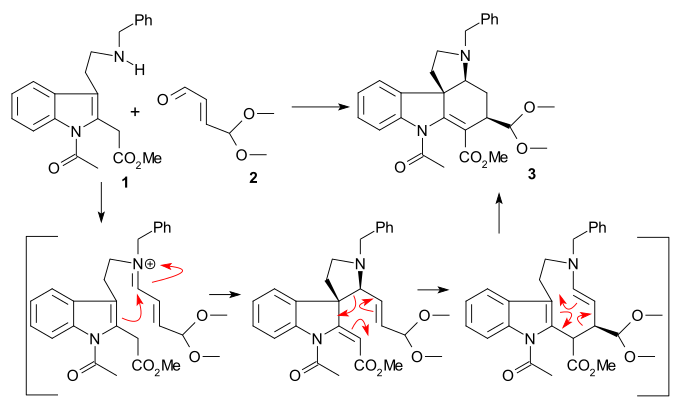
[ редактировать ]Синтез Кене 1993 года касается рацемического стрихнина. Исходные соединения триптамин 1 и 4,4- диметоксиакролеин 2 взаимодействовали с вместе с трифторидом бора образованием ацеталя 3 в виде единственного диастереомера в последовательности амино-карбонильной конденсации / сигматропной перегруппировки .
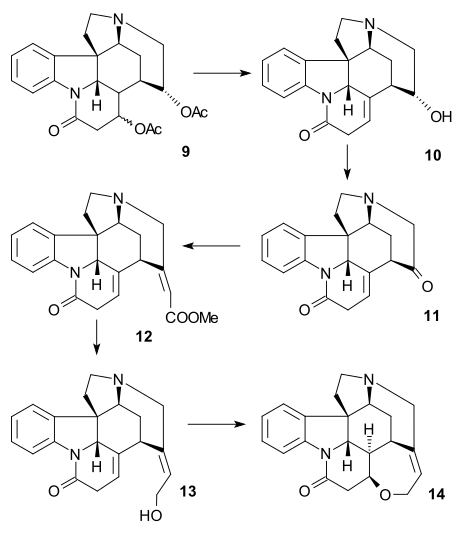
Гидролиз кислотой хлорной дает альдегид 4 . Реакция Джонсона -Кори-Чайковского ( йодид триметилсульфония / н-бутиллитий ) превратила альдегид в эпоксид , который прореагировал in situ с третичным амином с образованием соли аммония 5 (загрязненной другими продуктами циклизации). Восстановление ( палладий на углероде / водороде ) удалило бензильную группу до спирта 6 , дальнейшее восстановление ( цианоборгидрид натрия ) и ацилирование ( уксусный ангидрид / пиридин ) дали 7 в виде смеси эпимеров (по C17). Затем замыкание кольца III- 8 осуществляли с помощью альдольной реакции с использованием бис(триметилсилил)амида лития (используя только эпимер с правильной конфигурацией). Еще большее восстановление ( боргидрид натрия ) и ацилирование привело к образованию эпимерного диацетата 9 .
В результате реакции DBU, опосредованной элиминирования, образуется олефиновый спирт 10 , а последующее окисление Сверна дает нестабильный аминокетон 11 . На заключительных этапах реакция Хорнера-Уодсворта-Эммонса ( метил-2-(диэтилфосфоно)ацетат ) дает акрилата сложный эфир 12 в виде смеси цис- и транс-изомеров , который можно направить в правильном (транс) направлении под действием света в фотохимическом приборе. В результате перегруппировки сложноэфирная группа восстанавливалась ( ДИБАЛ / трифторид бора ) до изострихнина 13 , а рацемический стрихнин 14 образовывался путем катализируемого основанием замыкания кольца, как в синтезе Вудворда.
В синтезе хирального (-)-стрихнина по Кеуне в 1998 году исходный материал был получен из хирального триптофана .
Синтез Равала
[ редактировать ]В синтезе Равала (1994, рацемический) амин 1 и енон 2 были объединены в результате амино-карбонильной конденсации с последующим гашением метилхлорформиатом до триена 3 , который затем подвергся реакции Дильса-Альдера (бензол 185 ° C) до гексена 4 . Три сложноэфирные группы были гидролизованы с использованием иодтриметилсилана с образованием пентациклического лактама 5 после гашения метанолом в комбинации из 7 стадий реакции (одна из них - конденсация Дикмана ). C 6 Сегмент 8 4 был добавлен при алкилировании амина , и реакция Хека 7 образовала изострихнин после снятия защиты с TBS.
Общий выход (10%) на сегодняшний день является самым большим из всех опубликованных методов. [40]
Бош синтез
[ редактировать ]В синтезе Bosch (1999, хиральный) олефиновая группа в дионе 1 была превращена в альдегид путем озонолиза , а хиральный амин 2 образовался в результате двойного восстановительного аминирования с ( S )-1- фенэтиламином . Фенилэтильный заместитель удаляли с помощью ClCO 2 CHClCH 3 и еноновую группу вводили методом отщепления по Грико с использованием TMSI , HMDS, затем PhSeCl, затем озона и затем диизопропиламина с образованием карбамата 3 . С аминогруппы снимали защиту путем кипячения с обратным холодильником в метаноле и затем алкилировали с использованием ( Z )-BrCH 2 CICH=CH 2 OTBDMS до третичного амина 4 . Затем произошла восстановительная реакция Хека с последующим метоксикарбонилированием (LiHMDS, NCCO 2 Me) до трицикла 5 . Реакция с цинковой пылью в 10% серной кислоте удалила TBDMS защитную группу , восстановила нитрогруппу и привела к восстановительной амино-карбонильной циклизации в одну стадию до тетрациклического 6 (эпимерная смесь). На заключительном этапе реакции альдегида Виланда-Гумлиха 7 с NaH в MeOH, приводящей к правильному эпимеру, последовало DIBAH восстановление метилового эфира .
Синтез Фоллхардта
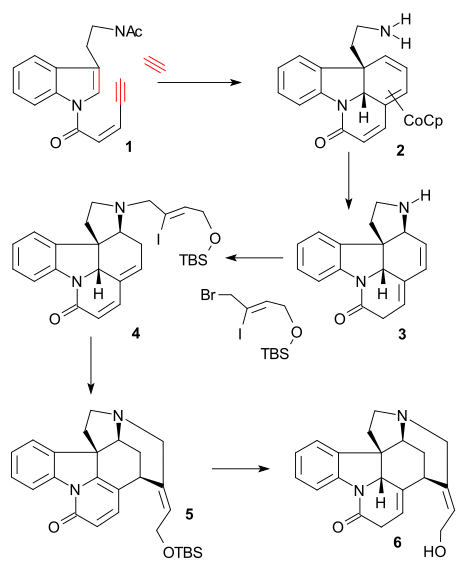
[ редактировать ]Ключевой реакцией синтеза Фоллхардта (2000, рацемический) была алкиновая тримеризация производного триптамина (ТГФ, 0 ° C 1 с ацетиленом и кобальторганическим соединением CpCo(C 2 H 4 ) 2 ) до трицикла 2 после снятия защиты с аминогруппы ( КОН, MeOH/H 2 O, кипячение). Последующая реакция с нитратом железа [1,8] привела к сопряженному присоединению -к тетрациклу 3 , алкилированию амина ( Z )-1-бром-4-[(трет-бутилдиметилсилил)окси]-2-иодбут-2-еном ( Синтез Раваля) и карбоната лития , а изомеризация диеновой см . системы (NaOiPr, iPrOH) образовала енон 4 . Реакция Хека, как и в синтезе Раваля ( ацетат палладия / трифенилфосфин ), сопровождавшаяся ароматизацией, образовывала пиридон 5 , а восстановление литийалюминийгидрида и снятие защитной группы TBS образовывало изострихнин 6 .
Синтез Мори
[ редактировать ]Синтез Мори ((-) хиральный, 2003) был первым, содержащим стадию асимметричной реакции . Он также характеризуется большим количеством реакций, катализируемых Pd. В нем N-тозиламин 1 взаимодействовал с аллилкарбонатом 2 путем аллильного асимметричного замещения с использованием Pd 2 (dba) 3 и асимметрического лиганда (S-BINAPO) с образованием хирального вторичного амина 3 . десилилирование группы TBDMS Затем осуществлялось с помощью HCl до гидроксида , а затем до нитрила 4 ( NaCN ) через бромид ( PBr 3 ). Реакция Хека ( Pd(OAc) 2 / Me 2 PPh ) и дебромирование ( Ag 2 CO 3 ) дали трицикл 5 . LiALH 4 Восстановление нитрила до амина и его защита Boc 2 O до boc амина 6 затем сопровождалось вторым аллильным окислением ( Pd(OAc) 2 / AcOH / бензохинон / MnO 2 ) до тетрацикла 7 . Гидроборирование-окисление ( 9-BBN / H 2 O 2 ) дало спирт 8 и последующее окисление Сверна кетоном 9 . Реакция с LDA / PhNTf 2 давала енолтрифлат 10 , а трифлатная группа удалялась в алкене 11 реакцией с Pd(OAc) 2 и PPh 3 .
Детозилирование 11 ( нафталинид натрия ) и амидирование хлорангидридом , 3-бромакрилоилхлорида дали амид 12 а другая реакция Хека дала пентацикл 13 . изомеризация двойной связи ( натрий / iPrOH ), с Boc-группы снятие защиты ( трифликовая кислота ) и алкилирование амина с помощью (Z)-BrCH 2 CICH=CH 2 OTBDMS (см. Rawal) дали соединение 14 (идентичное одному из промежуточных продуктов Фоллхардта). Заключительная реакция Хека ( 15 ) и снятие защиты с TBDMS образовали (-)-изострихнин 16 .
Синтез Шибасаки
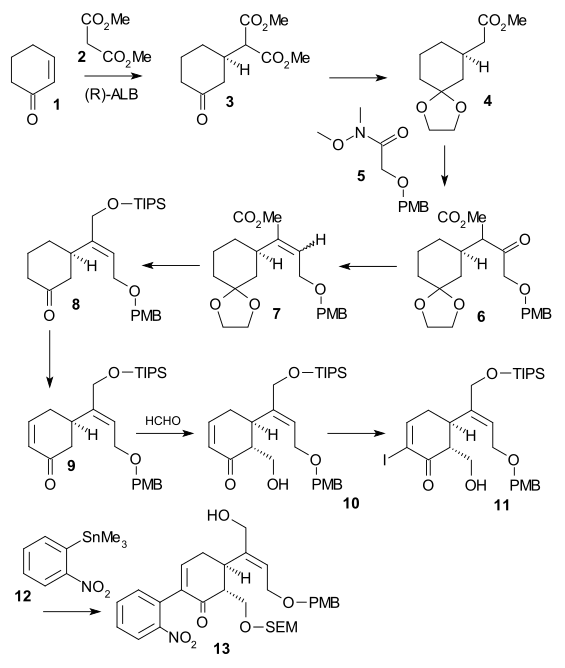
[ редактировать ]Синтез Шибасаки ((-) хиральный, 2002 г.) был вторым опубликованным методом полного синтеза стрихнина с использованием стадии асимметричной реакции . Циклогексенон 1 подвергали взаимодействию с диметилмалонатом 2 по асимметричной реакции Михаэля с использованием AlLibis (бинафоксид) с образованием хирального диэфира 3 . Его кетоновую группу защищали ацеталем ( 2-этил-2-метил-1,3-диоксолан, TsOH ), а карбоксильную группу удаляли ( LiCl , ДМСО 140 °C) в моноэфире 4 . Фрагмент C2 добавляли в виде амида Вейнреба 5 с образованием эфира PMB 6 с использованием LDA . Затем кетон восстанавливали до спирта ( NaBH 3 CN , TiCl 4 воду ), а затем удаляли ( DCC , CuCl ) с образованием алкена 7 . После сложного эфира восстановления ( DIBAL ) до спирта и его TIPS- защиты ( TIPSOTf , триэтиламин ) ацетальную группу удаляли (каталитический CSA ) в кетоне 8 . Энон 9 затем образовался в результате окисления Саэгусы . Превращение в спирт 10 осуществлялось присоединением альдолов Мукаямы с использованием формальдегида , йодирование до 11 ( йод , ДМАП ) с последующим сочетанием Стилле ( Pd 2 dba 3 , Ph 3 As , CuI ), включающий нитробензольное звено 12 . Спирт 13 образовался после защиты SEM (SEMCl,i-Pr2NEt) и удаления TIPS ( HF ).
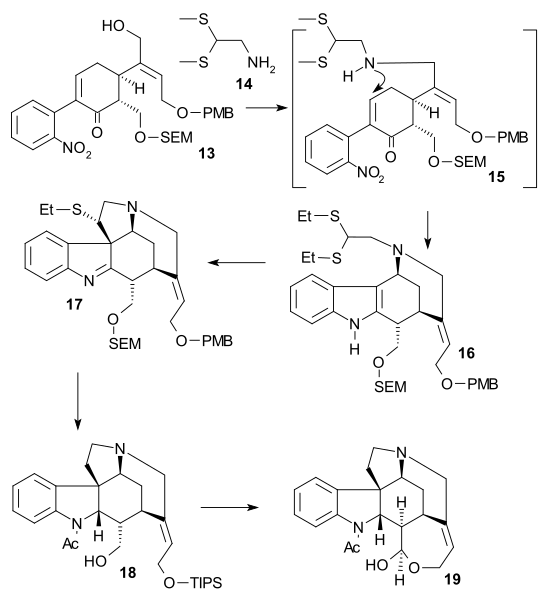
Во второй части последовательности спирт 13 переводили в трифлат ( трифликовый ангидрид , N , N -диизопропилэтиламин ), затем 2,2-бис(этилтио)этиламин 14 добавляли , а затем сразу же цинковый порошок, устанавливая тандемную реакцию с восстановление нитрогруппы до амина, 1,4-присоединение тиоаминной группы и амино-кетоконденсация до индола 16 . Реакция с DMTSF привела к атаке тиония по C7 с образованием 17 , иминная затем группа была восстановлена ( NaBH 3 CN , TiCl 4 ), новая аминогруппа ацилирована ( уксусный ангидрид , пиридин ), обе спиртовые защитные группы удалены ( NaOMe / meOH) и Группа аллилового спирта снова защищена (TIPS). Это позволило удалить этилтиогруппу ( NiCl 2 , NaBH 4 , EtOH/MeOH) до 18 . Спирт окисляли до альдегида с использованием окисления Париха-Деринга , а удаление групп TIPS давало полуацеталь 19, называемый (+)-диаболином, который представляет собой ацилированный альдегид Виланда-Гумлиха .
Синтез лития
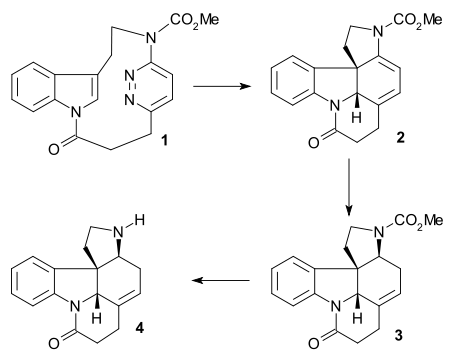
[ редактировать ]Синтез, о котором сообщил Бодвелл/Ли (рацемический, 2002), был формальным синтезом , поскольку он давал соединение, уже полученное Равалем (№ 5 в синтезе Равала). Ключевым этапом была -Альдера циклофана 1 с обратной потребностью электронов при реакция Дильса нагревании в N , N -диэтиланилине (диазот выбрасывается) с последующим восстановлением двойной связи в 2 до 3 боргидридом натрия / трифликовой кислотой и удалением карбамата, защищающего группа ( PDC / целит ) до 4 .
Этот метод оспаривается Рейссигом (см. Синтез Рейссига).
Синтез Фукуямы
[ редактировать ]Синтез Фукуямы (хиральный (-), 2004) начался с циклического амина 1 . В какой-то момент в этот исходный материал была введена хиральность путем ферментативного разделения одного из предшественников. Ацилоин 2 образовался в результате Руботтома окисления и гидролиза . Окислительное расщепление ацетатом свинца образует альдегид 3 , удаление нозильной группы ( тиофенол / карбонат цезия ) запускает амино-карбонильную конденсацию с ионом иминия 4, продолжающим реагировать в трансаннулярной циклизации с образованием диэфира 5 , который может быть преобразован в альдегид Виланда-Гумлиха. по известной химии.
Синтез Рейссига
[ редактировать ]Метод, о котором сообщили Beemelmanns & Reissig (racemic, 2010), представляет собой еще один формальный синтез, ведущий к пентациклу Раваля (см. амин 5 в методе Равала). В этом методе индол 1 превращался в тетрацикл 2 (вместе с побочным продуктом) в ходе однокаскадной реакции с использованием дииодида самария и HMPA . [41] Восстановление никеля Ренея /H 2 дало амин 3 , а реакция в одном котле с использованием метилхлорформиата , DMAP и TEA, затем MsCl , DMAP и TEA , а затем DBU дала предшественник Rawal 4 с ключевыми атомами водорода в желаемой анти-конфигурации.
В прерванном маршруте промежуточное соединение 2 сначала восстанавливалось до имина 5 , затем превращалось в карбамат 6 , затем дегидратировалось до диена 7 ( реагент Берджесса ) и, наконец, восстанавливалось до 8 ( цианоборгидрид натрия ). Атомы водорода в 8 находятся в нежелательном цис-соотношении, что противоречит результатам, полученным в 2002 году Бодвеллом/Ли для той же реакции.
Синтез Вандервала
[ редактировать ]В 2011 году группа Вандервала сообщила о краткой и самой длинной линейной последовательности из 6 этапов полного синтеза стрихнина. [42] Он включал в себя альдегид Цинке с последующей реакцией анионной бициклизации и тандемной перегруппировкой Брука / присоединением конъюгата .
Внешние ссылки
[ редактировать ]Ссылки
[ редактировать ]- ^ рентген; Мессершмидт, М.; Шейнс, С.; Люгер, П. (2005). «Плотность заряда (-)-стрихнина от 100 до 15 К, сравнение четырех наборов данных». Акта Кристаллогр Б. 61 (1): 115–121. дои : 10.1107/S0108768104032781 . ПМИД 15659864 .
- ^ Николау, KC; Соренсен, Э.Дж. (1996). Классика тотального синтеза: цели, стратегии, методы. Уайли. ISBN 978-3-527-29231-8 .
- ^ KC Николау, Дионисиос Вурлумис, Николас Винсингер, Фил С. Баран Искусство и наука полного синтеза на заре двадцать первого века Angewandte Chemie International Edition 2000; Том 39, Выпуск 1, Страницы: 44-122
- ^ Бонжох, Хосеп; Соле, Дэниел (2000). «Синтез стрихнина». хим. Откр. 100 (9): 3455–3482. дои : 10.1021/cr9902547 . ПМИД 11777429 .
- ^ Праудфут, Джон Р. (2013). «Схемы реакций, визуализированные в сетевой форме: синтез стрихнина на примере». Журнал химической информации и моделирования . 53 (5): 1035–1042. дои : 10.1021/ci300556b . ПМИД 23597302 .
- ^ Пеллетье; Кавенту (1818 г.). «Заметка о новой щелочи (Заметка о новой щелочи)» . Анналы химии и физики . 8 : 323–324. См. также: Пеллетье; Кавенту (1819 г.). «Воспоминания о новой растительной щелочи (стрихнине), обнаруженной в бобах святого Игнатия, nux vomica и т. д.» . Анналы химии и физики . 10 : 142–176.
- ^ Робинсон, Р. (1946). «Конституция стрихнина». Эксперименты . 2 (1): 1946. doi : 10.1007/BF02154708 . ПМИД 21012825 .
- ^ Бриггс, Л.Х.; Опеншоу, ХТ; Робинсон, Роберт (1946). «Стрихнин и бруцин. Часть XLII. Состав неоряда оснований и продуктов их окисления». Дж. Хим. Соц. 1946 : 903. doi : 10.1039/JR9460000903 .
- ^ Опеншоу, ХТ; Робинсон, Р. (1946). «Конституция стрихнина и биогенетическая связь стрихнина и хинина» . Природа . 157 (3988): 438. Бибкод : 1946Natur.157..438O . дои : 10.1038/157438a0 . ПМИД 21024272 .
- ^ Вудворд, РБ; Брем, Уоррен Дж.; Нельсон, Ал. (1947). «Структура стрихнина». Дж. Ам. хим. Соц. 69 (9): 2250. doi : 10.1021/ja01201a526 . ПМИД 20262753 .
- ^ Биджвоет, Шун и Боховен, Кон. Голландский Акад. Закон., 50, № 8, 51, № 1. 8, 52, №. 2 ( 1947–49 )
- ^ Боховен, К.; Шун, Дж. К.; Биджвоет, Дж. М. (1951). «Фурье-синтез кристаллической структуры пентагидрата сульфата стрихнина» (PDF) . Акта Кристаллогр . 4 (3): 275–280. дои : 10.1107/S0365110X51000891 .
- ^ Робертсон, Дж. Х.; Биверс, Калифорния (1950). «Кристаллическая структура гидробромида стрихнина». Природа . 165 (4200): 690–691. Бибкод : 1950Natur.165..690R . дои : 10.1038/165690a0 . ПМИД 15416785 .
- ^ Робертсон, Дж. Х.; Биверс, Калифорния (1951). «Кристаллическая структура бромистого водорода стрихнина». Акта Кристаллогр . 4 (3): 270–275. дои : 10.1107/S0365110X5100088X .
- ^ Вудворд, РБ; Кава, Майкл П.; Оллис, штат Вирджиния; Голод, А.; Даеникер, Хьюстон; Шенкер, К. (1954). «Полный синтез стрихнина». Дж. Ам. хим. Соц. 76 (18): 4749–4751. дои : 10.1021/ja01647a088 .
- ^ Вудворд, РБ; Кава, член парламента; Оллис, штат Вирджиния; Голод, А.; Даеникер, Хьюстон; Шенкер, К. (1963). «Полный синтез стрихнина». Тетраэдр . 19 (2): 247–288. дои : 10.1016/s0040-4020(01)98529-1 .
- ^ Магнус, Филип; Джайлз, Мелвин; Боннер, Роджер; Ким, Чунг С.; Маккуайр, Лесли; Мерритт, Эндрю; Викер, Найджел (1992). «Синтез стрихнина через альдегид Виланда-Гумлиха». Дж. Ам. хим. Соц. 114 (11): 4403–4405. дои : 10.1021/ja00037a058 .
- ^ Найт, Стивен Д.; Оверман, Ларри Э.; Пейродо, Гарри (1993). «Применение катионных аза-копе-перегруппировок в синтезе. 26. Энантиоселективный полный синтез (-)-стрихнина». Дж. Ам. хим. Соц. 115 (20): 9293–9294. дои : 10.1021/ja00073a057 .
- ^ Кюне, Мартин Э.; Сюй, Фэн (1993). «Полный синтез алкалоидов стрихнана и аспидосперматана. 3. Полный синтез (+-)-стрихнина». Дж. Орг. хим. 58 (26): 7490–7497. дои : 10.1021/jo00078a030 .
- ^ Кюне, Мартин Э.; Сюй, Фэн (1998). «Синтез алкалоидов типа стрихнан и аспидосперматан. 10. Энантиоселективный синтез (-)-стрихнина через альдегид Виланда-Гумлиха». Дж. Орг. хим. 63 (25): 9427–9433. дои : 10.1021/jo9813989 .
- ^ Равал, Виреш Х.; Иваса, Сейджи (1994). «Краткий стереоконтролируемый синтез стрихнина». Дж. Орг. хим. 59 (10): 2685–2686. дои : 10.1021/jo00089a008 .
- ^ Полный синтез (-)-стрихнина с помощью альдегида Виланда-Гумлиха Angewandte Chemie International Edition , том 38, выпуск 3, 1999 г., страницы: 395-397 Даниэль Соле, Хосеп Бонджох, Сильвина Гарсиа-Рубио, Эмма Пейдро, Джоан Бош
- ^ Соле, Даниэль; Бонжох, Джозеф; Гарсиа-Рубио, Сильвина; Пейдро, Эмма; Босх, Джоан (2000). «Энантиоселективный полный синтез альдегида Виланда-Гумлиха и (-)-стрихнина». Химия: Европейский журнал . 6 (4): 655–665. doi : 10.1002/(SICI)1521-3765(20000218)6:4<655::AID-CHEM655>3.0.CO;2-6 .
- ^ Эйхберг, Майкл Дж.; Дорта, Роза Л.; Ламоттке, Кай; Воллхардт, К. Питер К. (2000). «Формальный полный синтез (±)-стрихнина посредством кобальт-опосредованного [2 + 2 + 2] циклоприсоединения». Орг. Летт. 2 (16): 2479–2481. дои : 10.1021/ol006131m . ПМИД 10956526 .
- ^ Эйхберг, Майкл Дж.; Дорта, Роза Л.; Гротьян, Дуглас Б.; Ламоттке, Кай; Шмидт, Мартин; Воллхардт, К. Питер К. (2001). «Подходы к синтезу (±)-стрихнина посредством кобальт-опосредованного [2 + 2 + 2] циклоприсоединения: быстрая сборка классической структуры». Дж. Ам. хим. Соц. 123 (38): 9324–9337. дои : 10.1021/ja016333t . ПМИД 11562215 .
- ^ Наканиси, Масато; Мори, Мивако (2002). «Тотальный синтез (-)-стрихнина». Angewandte Chemie, международное издание . 41 (11): 1934–1936. doi : 10.1002/1521-3773(20020603)41:11<1934::AID-ANIE1934>3.0.CO;2-F . ПМИД 19750638 .
- ^ Мори, Мивако; Наканиси, Масато; Кадзисима, Дайсуке; Сато, Ёсихиро (2003). «Новый и общий синтетический путь к индольным алкалоидам стрихноса: полный синтез (-)-тубифолина, (-)-дегидротубифолина и (-)-стрихнина с использованием катализируемого палладием асимметричного аллильного замещения». Дж. Ам. хим. Соц. 125 (32): 9801–9807. дои : 10.1021/ja029382u . ПМИД 12904045 .
- ^ Осима, Такаши; Сюй, Юджун; Такита, Ре; Симидзу, Сатоши; Чжун, Дафан; Сибасаки, Масакацу (2002). «Энантиоселективный полный синтез (-)-стрихнина с использованием каталитической асимметричной реакции Михаэля и тандемной циклизации». Дж. Ам. хим. Соц. 124 (49): 14546–14547. дои : 10.1021/ja028457r . ПМИД 12465959 .
- ^ Бодвелл, Грэм Дж.; Ли, Цзян (2002). «Краткий формальный полный синтез (±)-стрихнина с использованием трансаннулярной реакции Дильса – Альдера с обратной потребностью в электронах [3] (1,3) индоло [3] (3,6) пиридазинофана». Angewandte Chemie, международное издание . 41 (17): 3261–3262. doi : 10.1002/1521-3773(20020902)41:17<3261::AID-ANIE3261>3.0.CO;2-K .
- ^ Туман, Y; Токуяма, Х; Фукуяма, Т. (2004). «Тотальный синтез (-)-стрихнина». Дж. Ам. хим. Соц. 126 (33): 10246–10247. дои : 10.1021/ja046407b . ПМИД 15315428 .
- ^ Мартин, Дэвид Британская Колумбия; Вандервал, Кристофер Д. (2011). «Синтез стрихнина с помощью самой длинной линейной последовательности из шести этапов». Химическая наука . 2 (4): 649. дои : 10.1039/C1SC00009H .
- ^ Джонс, Спенсер Б.; Симмонс, Брайон; Мастраккио, Энтони; Макмиллан, Дэвид У.К. (2011). «Коллективный синтез природных продуктов методами органокаскадного катализа» . Природа . 475 (7355): 183–188. дои : 10.1038/nature10232 . ПМЦ 3439143 . ПМИД 21753848 .
- ^ Найт, Стивен Д.; Оверман, Ларри Э.; Пейродо, Гарри (1995). «Асимметричные полные синтезы (-)- и (+)-стрихнина и альдегида Виланда-Гумлиха». Дж. Ам. хим. Соц. 117 (21): 5776–5788. дои : 10.1021/ja00126a017 .
- ^ Не в счет: неопубликованный метод Гилберта Сторка , лекция в Школе органической химии Искья, Искья-Порб, Италия, 21 сентября 1992 г.
- ^ Чжан, Хунцзюнь; Бунсомбат, Джутатип; Падва, Альберт (2007). «Полный синтез (±)-стрихнина посредством каскада [4 + 2]-циклоприсоединения/перегруппировки» . Орг. Летт. 9 (2): 279–282. дои : 10.1021/ol062728b . ПМК 2587098 . ПМИД 17217284 .
- ^ Сирасани, Гопал; Пол, Тапас; Уильям Догерти-младший; Кассель, Скотт; Андраде, Родриго Б. (2010). «Краткий общий синтез (±)-стрихнина и (±)-акуаммицина». Журнал органической химии . 75 (10): 3529–3532. дои : 10.1021/jo100516g . ПМИД 20408591 .
- ^ Бемельманнс, К.; Рейссиг, Х.-У. (2010). «Краткий формальный полный синтез стрихнина с каскадной реакцией, индуцированной дииодидом самария, в качестве ключевого этапа». Angewandte Chemie, международное издание . 49 (43): 8021–8025. дои : 10.1002/anie.201003320 . ПМИД 20848626 .
- ^ Р. Робинсон "Молекулярная структура стрихнина, бруцина и вомицина Prog. Org. Chem. , 1952; 1,2".
- ^ Вудворд, РБ (1948). «Биогенез алкалоидов стрихноса». Природа . 162 (4108): 155–156. Бибкод : 1948Natur.162..155W . дои : 10.1038/162155a0 . ПМИД 18871488 .
- ^ Кэннон, Дж. С.; Оверман, Л.Е. (2012). «Нет ли конца тотальному синтезу стрихнина? Уроки, извлеченные из стратегии и тактики полного синтеза» . Энджью. хим. Межд. Эд . 51 (18): 4288–4311. дои : 10.1002/anie.201107385 . ПМЦ 3804246 . ПМИД 22431197 .
- ^ Шостак, М.; Проктер, диджей (2011). «Краткий синтез стрихнина и энглерина А: сила восстановительных циклизаций, вызванных йодидом самария». Angewandte Chemie, международное издание . 50 (34): 7737–7739. дои : 10.1002/anie.201103128 . ПМИД 21780264 .
- ^ Мартин, Дэвид Британская Колумбия; Вандервал, Кристофер Д. (2011). «Синтез стрихнина с помощью самой длинной линейной последовательности из шести этапов». Химическая наука . 2 (4): 649. дои : 10.1039/C1SC00009H .