Газообразные сигнальные молекулы
Газообразные сигнальные молекулы — это газообразные молекулы , которые либо синтезируются внутри ( эндогенно ) в организме , ткани или клетке , либо поступают в организм, ткань или клетку извне (скажем, из атмосферы или гидросферы , как в случае с кислородом ) и которые используются для передачи химических сигналов, вызывающих определенные физиологические или биохимические изменения в организме, ткани или клетке. Термин применяется, например, к кислороду , диоксиду углерода , диоксиду серы , закиси азота , цианистому водороду , аммиаку , метану , водороду , этилену и т. д.
Некоторые газообразные сигнальные молекулы ведут себя как нейротрансмиттеры и называются газотрансмиттерами . К ним относятся оксид азота , окись углерода и сероводород .
Исторически изучение газов и физиологических эффектов относилось к категории искусственных .
Биологическая роль каждой из газообразных сигнальных молекул описана ниже.
Газотрансмиттеры
[ редактировать ]Газотрансмиттеры представляют собой класс нейромедиаторов . Только три газа принято относить к газотрансмиттерам: оксид азота , окись углерода и сероводород .
Газообразные сигнальные молекулы
[ редактировать ]Кислород
[ редактировать ]Кислород , O 2 , является важной газообразной сигнальной молекулой и биологическим мессенджером, важным во многих физиологических и патологических процессах, действуя через клеточные газорецепторные белки и другие сигнальные пути. [1] [2] Уровни O 2 в клетках или организмах должны строго регулироваться, чтобы обеспечить нормоксические, а не неконтролируемые гипоксические , аноксические или гипероксические состояния. У млекопитающих специализированные ткани, такие как сонные тела, определяют уровни O 2 .
Углекислый газ
[ редактировать ]Углекислый газ СО 2 является одним из медиаторов местной ауторегуляции кровоснабжения. Если его уровень высок, капилляры расширяются, обеспечивая больший приток крови к этой ткани.
Комары привлекают людей, ощущая CO 2 через вкусовые рецепторы, тип газорецепторов. [3]
Хотя организму необходим кислород для метаболизма, низкий уровень кислорода обычно не стимулирует дыхание. Скорее, дыхание стимулируется более высоким уровнем углекислого газа. [4]
Дыхательные центры стараются поддерживать артериальное давление СО 2 на уровне 40 мм рт. ст. При преднамеренной гипервентиляции содержание СО 2 в артериальной крови может быть снижено до 10–20 мм рт. ст. (содержание кислорода в крови изменяется незначительно), а двигательный импульс снижается. Вот почему после гипервентиляции можно задерживать дыхание дольше, чем без гипервентиляции. Это сопряжено с риском потери сознания до того, как потребность в дыхании станет непреодолимой, поэтому гипервентиляция особенно опасна перед фридайвингом.
Оксид азота
[ редактировать ]Оксид азота , NO, является ключевым позвоночных, биологическим мессенджером важным во многих физиологических и патологических процессах, действуя, например, как мощный сосудорасширяющий препарат у человека (см. Биологические функции оксида азота ). Клетки млекопитающих имеют специализированную газорецепторную растворимую гуанилатциклазу , которая связывается с NO и запускает NO-зависимую клеточную передачу сигналов.
Закись азота
[ редактировать ]Закись азота , N 2 O, в биологических системах может образовываться путем ферментативного или неферментативного восстановления оксида азота . [5] Исследования in vitro показали, что эндогенная закись азота может образовываться в результате реакции между оксидом азота и тиолом . [6] Некоторые авторы показали, что этот процесс восстановления NO до N 2 O происходит в гепатоцитах , особенно в их цитоплазме и митохондриях , и предположили, что N 2 O, возможно, может вырабатываться в клетках млекопитающих. [7] Хорошо известно, что N 2 O вырабатывается некоторыми бактериями в ходе процесса, называемого денитрификацией. [8]
В 1981 году на основании клинических исследований закиси азота (N 2 O) было впервые высказано предположение, что газ оказывает прямое действие на фармакологические рецепторы и тем самым действует как нейромедиатор. [9] [10] [11] Эксперименты in vitro подтвердили эти наблюдения. [12] которые позже были воспроизведены в NIDA. [13]
Помимо своего прямого [14] [15] и косвенное действие на опиоидные рецепторы, [16] также было показано, что N 2 O ингибирует опосредованную рецептором NMDA активность и ионные токи и уменьшает опосредованную рецептором NMDA эксайтотоксичность и нейродегенерацию. [17] Закись азота также ингибирует метионинсинтазу и замедляет превращение гомоцистеина в метионин , увеличивает концентрацию гомоцистеина и снижает концентрацию метионина. Этот эффект был показан на лимфоцитов . культурах клеток [18] и в образцах биопсии печени человека. [19]
Закись азота не связывается в качестве лиганда с гемом и не реагирует с тиолсодержащими белками . Тем не менее, исследования показали, что закись азота может обратимо и нековалентно «встраиваться» во внутренние структуры некоторых гемсодержащих белков, таких как гемоглобин , миоглобин , цитохромоксидаза, и изменять их структуру и функцию. [20] Способность закиси азота изменять структуру и функцию этих белков была продемонстрирована сдвигами инфракрасных спектров цистеинтиолов гемоглобина. [21] и путем частичного и обратимого ингибирования цитохромоксидазы. [22]
Эндогенная закись азота, возможно, может играть роль в модуляции эндогенных опиоидов. [23] [24] и NMDA-систеросклероз, тяжелый сепсис, тяжелая малярия или аутоиммунитет. Клинические испытания на людях были проведены, но результаты еще не опубликованы. [25]
Сусид углерода
[ редактировать ]
Суоксид углерода , C 3 O 2 , может быть произведен в небольших количествах в любом биохимическом процессе, который обычно производит оксид углерода , CO, например, во время окисления гема гемоксигеназой-1. Он также может быть образован из малоновой кислоты. Показано, что субоксид углерода в организме способен быстро полимеризоваться в макроциклические полиуглеродные структуры общей формулы (C 3 O 2 ) n (чаще всего (C 3 O 2 ) 6 и (C 3 O 2 ) 8 ), и что эти макроциклические соединения являются мощными ингибиторами Na + /К + -АТФ-аза и Са-зависимая АТФ-аза обладают дигоксиноподобными физиологическими свойствами, а также натрийуретическим и антигипертензивным действием. Считается, что эти макроциклические полимерные соединения субоксида углерода являются эндогенными дигоксиноподобными регуляторами Na. + /К + -АТФ-азы и Са-зависимые АТФ-азы, а также эндогенные натриуретики и антигипертензивные средства. [26] [27] [28] Помимо этого, некоторые авторы также считают, что эти макроциклические соединения субоксида углерода могут уменьшать образование свободных радикалов и окислительный стресс, а также играть роль в эндогенных противораковых защитных механизмах, например, в сетчатке . [29]
Диоксид серы
[ редактировать ]Роль диоксида серы SO 2 в биологии млекопитающих изучена недостаточно. [30] Диоксид серы блокирует нервные сигналы от рецепторов растяжения легких и подавляет инфляционный рефлекс Геринга-Бройера .
Диоксид серы играет роль в уменьшении экспериментального повреждения легких, вызванного олеиновой кислотой . Эндогенный диоксид серы снижает перекисное окисление липидов, образование свободных радикалов, окислительный стресс и воспаление во время экспериментального повреждения легких. И наоборот, успешное повреждение легких приводило к значительному снижению выработки эндогенного диоксида серы и увеличению перекисного окисления липидов, образованию свободных радикалов, окислительному стрессу и воспалению. Более того, блокада фермента , вырабатывающего эндогенный SO 2 , значительно увеличивала объем повреждения легочной ткани в эксперименте. И наоборот, добавление ацетилцистеина или глутатиона в рацион крыс увеличивало количество вырабатываемого эндогенного SO 2 и уменьшало повреждение легких, образование свободных радикалов, окислительный стресс, воспаление и апоптоз. [31]
Эндогенный диоксид серы может играть роль в регуляции функции сердца и кровеносных сосудов , а аберрантный или недостаточный метаболизм диоксида серы может способствовать развитию нескольких различных сердечно-сосудистых заболеваний, таких как артериальная гипертензия , атеросклероз , легочная артериальная гипертензия , стенокардия . [32]
У детей с легочной артериальной гипертензией вследствие врожденных пороков сердца уровень гомоцистеина выше, а уровень эндогенного диоксида серы ниже, чем у нормальных детей контрольной группы. Более того, эти биохимические показатели сильно коррелировали с тяжестью легочной артериальной гипертензии. Авторы считали гомоцистеин одним из полезных биохимических маркеров тяжести заболевания, а метаболизм диоксида серы — одной из потенциальных терапевтических мишеней у этих пациентов. [33]
Эндогенный диоксид серы также снижает скорость пролиферации эндотелиальных гладкомышечных клеток кровеносных сосудов за счет снижения активности МАРК и активации аденилатциклазы и протеинкиназы А. [34] Пролиферация гладкомышечных клеток является одним из важных механизмов гипертонического ремоделирования сосудов и их стеноза , а также важным патогенетическим механизмом при артериальной гипертензии и атеросклерозе.
Эндогенный диоксид серы в низких концентрациях вызывает эндотелийзависимую вазодилатацию . В более высоких концентрациях он вызывает эндотелий-независимую вазодилатацию и оказывает отрицательное инотропное действие на функцию сердечного выброса, тем самым эффективно снижая артериальное давление и потребление кислорода миокардом. Сосудорасширяющее действие диоксида серы опосредуется через АТФ-зависимые кальциевые каналы и кальциевые каналы L-типа («дигидропиридиновые»). Эндогенный диоксид серы также является мощным противовоспалительным, антиоксидантным и цитопротекторным средством. Он снижает артериальное давление и замедляет гипертоническое ремоделирование сосудов, особенно утолщение их интимы. Он также регулирует липидный обмен. [35]
Эндогенный диоксид серы также уменьшает повреждение миокарда, вызванное изопротереноловой адренергической гиперстимуляцией, и усиливает резерв антиоксидантной защиты миокарда. [36]
Цианистый водород
[ редактировать ]Некоторые авторы показали, что нейроны могут вырабатывать цианистый водород (HCN) при активации их опиоидных рецепторов эндогенными или экзогенными опиоидами. Они также показали, что производство HCN в нейронах активирует рецепторы NMDA и играет роль в передаче сигналов между нейрональными клетками ( нейротрансмиссия ). Более того, увеличение выработки эндогенного нейронального HCN под действием опиоидов, по-видимому, было необходимо для адекватной опиоидной анальгезии , поскольку анальгезирующее действие опиоидов ослаблялось поглотителями HCN. Они считали эндогенный HCN нейромодулятором. [37]
Было также показано, что, хотя стимуляция мускариновых холинергических рецепторов в культивируемых феохромоцитомы клетках увеличивает выработку HCN, в живом организме ( in vivo ) мускариновая холинергическая стимуляция фактически снижает выработку HCN. [38]
Лейкоциты генерируют HCN во время фагоцитоза . [37]
, расширение сосудов вызванное нитропруссидом натрия Было показано, что , опосредовано не только образованием NO, но и образованием эндогенных цианидов, что добавляет не только токсичности, но и некоторую дополнительную антигипертензивную эффективность по сравнению с нитроглицерином и другими нецианогенными нитратами, которые не вызывать повышения уровня цианида в крови. [39]
Аммиак
[ редактировать ]Аммиак, NH 3 , также играет роль как в нормальной, так и в аномальной физиологии животных . Он биосинтезируется в ходе нормального метаболизма аминокислот, но токсичен в высоких концентрациях. [40] Печень цикл преобразует аммиак в мочевину посредством серии реакций, известных как мочевины . Дисфункция печени, например, наблюдаемая при циррозе печени , может привести к повышенному количеству аммиака в крови ( гипераммониемии ). Аналогичным образом, дефекты ферментов, ответственных за цикл мочевины, таких как орнитинтранскарбамилаза , приводят к гипераммониемии. Гипераммониемия способствует спутанности сознания и коме при печеночной энцефалопатии , а также неврологических заболеваниях, часто встречающихся у людей с нарушениями цикла мочевины и органической ацидурией . [41]
Аммиак важен для нормального кислотно-щелочного баланса животных. После образования аммония из глутамина может α-кетоглутарат разлагаться с образованием двух молекул бикарбоната , которые затем становятся буферами для пищевых кислот. Аммоний выводится с мочой, что приводит к чистой потере кислоты. Аммиак сам может диффундировать через почечные канальцы, соединяться с ионами водорода и, таким образом, способствовать дальнейшему выведению кислоты. [42]
Метан
[ редактировать ]Некоторые авторы показали, что эндогенный метан СН 4 вырабатывается не только кишечной флорой и затем всасывается в кровь , но также вырабатывается - в небольших количествах - эукариотическими клетками (в процессе перекисного окисления липидов). И они также показали, что эндогенное производство метана увеличивается во время экспериментальной митохондриальной гипоксии , например, интоксикации азидом натрия . Они считали, что метан может быть одним из межклеточных сигналов гипоксии и стресса. [43]
Другие авторы показали, что выработка клеточного метана также увеличивается во время сепсиса или бактериальной эндотоксемии , включая экспериментальную имитацию эндотоксемии введением липополисахаридов (ЛПС). [44]
Некоторые другие исследователи показали, что метан, вырабатываемый кишечной флорой, не является полностью «биологически нейтральным» для кишечника и участвует в нормальной физиологической регуляции перистальтики . А его избыток вызывает не только отрыжку, метеоризм и боли в животе, но и функциональные запоры. [45]
Этилен
[ редактировать ]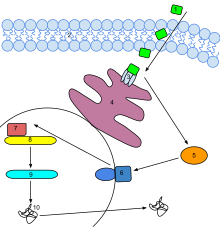
Этилен , H 2 C=CH 2 , служит гормоном в растениях . [46] Он действует на следовых уровнях на протяжении всей жизни растения, стимулируя или регулируя , раскрытие созревание плодов цветов и опадение ( или опадание) листьев .В коммерческих камерах дозревания используются «каталитические генераторы» для производства этиленового газа из жидкого этанола. Обычно уровень газообразования составляет от 500 до 2000 частей на миллион в течение 24–48 часов. Необходимо соблюдать осторожность, чтобы контролировать уровень углекислого газа в камерах дозревания при отравлении газом, поскольку при дозревании при высокой температуре (20 °C; 68 °F) уровень CO 2 составляет 10% за 24 часа. [47]
Этилен использовался со времен древних египтян, которые разрезали инжир, чтобы стимулировать его созревание (ранение стимулирует выработку этилена тканями растения). Древние китайцы сжигали благовония в закрытых помещениях, чтобы ускорить созревание груш. В 1864 году было обнаружено, что утечки газа из уличных фонарей привели к задержке роста, скручиванию растений и аномальному утолщению стеблей. [46] В 1901 году русский учёный Дмитрий Нелюбов показал, что активным компонентом является этилен. [48] Сара Даут обнаружила, что этилен стимулирует отторжение в 1917 году. [49] Лишь в 1934 году Гейн сообщил, что растения синтезируют этилен. [50] В 1935 году Крокер предположил, что этилен является растительным гормоном, ответственным за созревание фруктов, а также за старение вегетативных тканей. [51]
Этилен производится практически из всех частей высших растений, включая листья, стебли, корни, цветы, плоды, клубни и семена.Производство этилена регулируется множеством факторов развития и окружающей среды. В течение жизни растения выработка этилена индуцируется на определенных стадиях роста, таких как прорастание , созревание плодов, опадение листьев и старение цветов. Производство этилена также может быть вызвано различными внешними факторами, такими как механические ранения, стрессы окружающей среды и некоторые химические вещества, включая ауксин и другие регуляторы. [52]
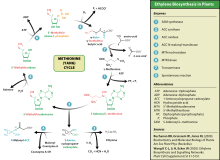
Этилен биосинтезируется из аминокислоты метионина в S -аденозил- L -метионин (SAM, также называемый адомет) с помощью фермента Met-аденозилтрансферазы. Затем SAM преобразуется в 1-аминоциклопропан-1-карбоновую кислоту (АСС) с помощью фермента АСС-синтазы (ACS). Активность АКС определяет скорость продукции этилена, поэтому регуляция этого фермента является ключевой для биосинтеза этилена. Последний этап требует кислорода и включает действие фермента АСС-оксидазы (ACO), ранее известного как этиленобразующий фермент (EFE). Биосинтез этилена может быть вызван эндогенным или экзогенным этиленом. Синтез АСС увеличивается при высоких уровнях ауксинов , особенно индолуксусной кислоты (ИУК) и цитокининов .
Этилен воспринимается семейством из пяти димеров трансмембранных белков, таких как газорецепторный белок ETR 1 у Arabidopsis . Ген , кодирующий рецептор этилена [ который? ] был клонирован в Arabidopsis thaliana , а затем в томате . [ нужна ссылка ] Рецепторы этилена кодируются множеством генов в арабидопсиса и томата геномах . Мутации в любом из семейства генов , которое включает пять рецепторов у арабидопсиса и как минимум шесть у томата, могут привести к нечувствительности к этилену. [53] Последовательности ДНК рецепторов этилена были также идентифицированы у многих других видов растений, а белок, связывающий этилен, даже был идентифицирован у цианобактерий . [46]
Экологические факторы, такие как наводнение, засуха, похолодание, ранения и атака патогенов, могут вызвать образование этилена в растениях. При затоплении корни страдают от недостатка кислорода, или аноксии , что приводит к синтезу 1-аминоциклопропан-1-карбоновой кислоты (АКК). АСС транспортируется вверх по растению и затем окисляется в листьях. Вырабатываемый этилен вызывает резкие движения (эпинастию) листьев, возможно, помогая растению терять воду. [54]
Этилен в растениях вызывает такие реакции:
- У проростка тройная реакция, утолщение и укорочение гипокотиля с выраженным апикальным крючком.
- При опылении , когда пыльца достигает рыльца, предшественник этена, АСС , секретируется в лепесток, АСС выделяет этилен с помощью АСС-оксидазы.
- листьев и цветов Стимулирует старение
- Стимулирует старение зрелых клеток ксилемы при подготовке к использованию в растениях.
- Вызывает опадение листьев
- Стимулирует прорастание семян
- Стимулирует корневых волос рост [55] — повышение эффективности всасывания воды и минералов за счет образования ризооболочки [56] [57]
- Стимулирует рост придаточных корней во время затопления. [58] [59]
- Стимулирует выживание в условиях низкого содержания кислорода ( гипоксии ) в погруженных тканях растений. [60] [61] [62] [63]
- Стимулирует эпинастию — черешок листа отрастает, лист свисает и скручивается сам в себя.
- Стимулирует созревание плодов [64]
- Вызывает климактерическое повышение дыхания у некоторых фруктов, что приводит к выделению дополнительного этилена.
- Влияет на гравитропизм
- Подавляет рост корней в ответ на уплотнение почвы, [65] [66] оттенок [67] [68] и наводнение [63]
- Стимулирует нутационный изгиб
- Подавляет рост стебля и стимулирует расширение стебля и клеток, а также рост боковых ветвей вне стадии рассады (см. Гипонастический ответ ).
- Нарушение транспорта ауксина (при высоких ауксина ) концентрациях
- Подавляет рост побегов и закрытие устьиц, за исключением некоторых водных растений или растений, обычно затопленных, таких как некоторые сорта риса, где происходит обратное (сохранение CO
2 и О
2 ) - Стимулирует цветение ананасов.
- Подавляет зарождение цветков Pharbitus, вызванное коротким днем, ноль. [69] и хризантема морифолиум [70]
Небольшие количества эндогенного этилена также вырабатываются у млекопитающих , включая человека , вследствие перекисного окисления липидов. Некоторая часть эндогенного этилена затем окисляется до этиленоксида , который способен алкилировать ДНК и белки , включая гемоглобин (образуя специфический аддукт с его N-концевым валином , N-гидроксиэтилвалином). [71] Эндогенный оксид этилена, так же как и экологический (экзогенный), может алкилировать гуанин в ДНК, образуя аддукт 7-(2-гидроксиэтил)-гуанин, что представляет собой внутренний канцерогенный риск. [72] Это также мутагенно. [73] [74]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Прабхакар, Нандури Р.; Семенца, Грегг Л. (сентябрь 2015 г.). «Ощущение кислорода и гомеостаз» . Физиология . 30 (5): 340–348. дои : 10.1152/физиол.00022.2015 . ISSN 1548-9213 . ПМЦ 4556828 . ПМИД 26328879 .
- ^ Анбалаган, Савани (17 января 2024 г.). «Гемовые газорецепторы кислорода» . Американский журнал физиологии. Эндокринология и обмен веществ . 326 (2): E178–E181. дои : 10.1152/ajpendo.00004.2024 . ПМИД 38231000 . S2CID 267032865 .
- ^ Сюй, П; Вэнь, Х; Леал, WS (февраль 2020 г.). «CO(2) сам по себе активирует рецепторы углекислого газа» . Биохимия насекомых и молекулярная биология . 117 : 103284. doi : 10.1016/j.ibmb.2019.103284 . ПМЦ 6980743 . ПМИД 31760135 .
- ^ Хогг Н., Сингх Р.Дж., Кальянараман Б. (18 марта 1996 г.). «Роль глутатиона в транспорте и катаболизме оксида азота» . Письма ФЭБС . 382 (3): 223–228. дои : 10.1016/0014-5793(96)00086-5 . ПМИД 8605974 .
- ^ ДеМастер Э.Г., Куаст Б.Дж., Редферн Б., Нагасава Х.Т. (12 сентября 1995 г.). «Реакция оксида азота со свободной сульфгидрильной группой человеческого сывороточного альбумина дает сульфеновую кислоту и закись азота». Биохимия . 34 (36): 11494–11499. дои : 10.1021/bi00036a023 . ПМИД 7547878 .
- ^ Хён Дж., Чаудхури Дж., Фукуто Дж.М. (1 сентября 1999 г.). «Восстановительный метаболизм оксида азота в гепатоцитах: возможное взаимодействие с тиолами» . Метаболизм и распределение лекарств . 27 (9): 1005–1009. ПМИД 10460799 .
- ^ Торрес, MJ; Саймон, Дж.; Роули, Г.; Бедмар, Э.Дж.; Ричардсон, диджей; Гейтс, Эй Джей; Дельгадо, MJ (2016), «Метаболизм закиси азота у нитратредуцирующих бактерий» , «Достижения в микробной физиологии» , 68 , Elsevier: 353–432, doi : 10.1016/bs.ampbs.2016.02.007 , ISBN 978-0-12-804823-8 , PMID 27134026 , получено 14 октября 2021 г.
- ^ Гиллман М.А., Лихтигфельд Ф.Дж. (январь 1981 г.). «Сравнение воздействия сульфата морфина и аналгезии закисью азота на состояния хронической боли у человека». Журнал неврологических наук . 49 (1): 41–45. дои : 10.1016/0022-510X(81)90186-6 . ПМИД 7205318 . S2CID 32640794 .
- ^ Гиллман М.А., Лайтигфельд Ф.Дж. (февраль 1981 г.). «Сходство действия закиси азота и морфия». Боль . 10 (1): 110. дои : 10.1016/0304-3959(81)90054-3 . ПМИД 7232008 . S2CID 53157904 .
- ^ Гиллман М.А., Лихтигфельд Ф.Дж. (май 1983 г.). «Закись азота взаимодействует с опиоидными рецепторами: больше доказательств» . Анестезиология . 58 (5): 483–484. дои : 10.1097/00000542-198305000-00021 . ПМИД 6301312 .
- ^ Дарас С., Кантрилл Р.К., Гиллман М.А. (апрель 1983 г.). «Замещение [3H] налоксона: доказательства использования закиси азота как агониста опиоидных рецепторов». Европейский журнал фармакологии . 89 (1–2): 177–178. дои : 10.1016/0014-2999(83)90626-х . ПМИД 6305684 .
- ^ Ори С., Форд-Райс Ф., Лондонский ED (март 1989 г.). «Влияние закиси азота и галотана на мю- и каппа-опиоидные рецепторы в мозге морских свинок» . Анестезиология . 70 (3): 541–544. дои : 10.1097/00000542-198903000-00027 . ПМИД 2564264 .
- ^ Дарас, К; Кантрилл, Р; Гиллман, Массачусетс (1983). «(3H) Замещение налоксона: доказательства использования закиси азота как агониста опиоидных рецепторов». Эур Дж Фармакол . 89 (1–2): 177–178. дои : 10.1016/0014-2999(83)90626-х . ПМИД 6305684 .
- ^ Ори, К.; Форд-Райс, форвард; Лондон, Эдуард (1989). «Влияние закиси азота и галотана на мю- и каппа-опиоидные рецепторы в мозге морских свинок» . Анестезиология . 70 (3): 541–544. дои : 10.1097/00000542-198903000-00027 . ПМИД 2564264 .
- ^ Финк, А.Д., Саманиего, Э., Нгай, С.Х. [1995]. Закись азота избирательно высвобождает мет5-энкефалин и мет5-энкефалин-arg6-phe7 в спинномозговую жидкость третьего желудочка собаки. Анестезия и анальгезия 80: 664-70.
- ^ Евтович-Тодорович В., Тодорович С.М., Меннерик С., Пауэлл С., Дикранян К., Беншофф Н., Зорумски К.Ф., Олни Дж.В. (апрель 1998 г.). «Закись азота (веселящий газ) является антагонистом NMDA, нейропротектором и нейротоксином». Нат Мед . 4 (4): 460–463. дои : 10.1038/nm0498-460 . ПМИД 9546794 . S2CID 9998244 .
- ^ Кристенсен Б., Рефсум Х., Гаррас А., Уеланд П.М. (июнь 1992 г.). «Реметилирование гомоцистеина при воздействии закиси азота на клетки, культивируемые в средах, содержащих различные концентрации фолатов». J Pharmacol Exp Ther . 261 (3): 1096–1105. ПМИД 1602376 .
- ^ Коблин Д.Д., Васкелл Л., Уотсон Дж.Э., Стокстад Э.Л., Эгер Э.И. 2-е место (февраль 1982 г.). «Закись азота инактивирует метионинсинтетазу в печени человека» . Анест Аналг . 61 (2): 75–78. дои : 10.1213/00000539-198202000-00001 . ПМИД 7198880 . S2CID 31136411 .
- ^ Сампат В., Чжао XJ, Коги В.С. (27 апреля 2001 г.). «Анестетикоподобные взаимодействия оксида азота с альбумином и гемопротеинами. Механизм контроля функции белка» . Журнал биологической химии . 276 (17): 13635–13643. дои : 10.1074/jbc.M006588200 . ПМИД 11278308 . [ постоянная мертвая ссылка ]
- ^ Донг А., Хуан П., Чжао XJ, Сампат В., Коги В.С. (30 сентября 1994 г.). «Характеристика участков, занятых анестетиком закисью азота в белках, с помощью инфракрасной спектроскопии» . Журнал биологической химии . 269 (39): 23911–23917. дои : 10.1016/S0021-9258(19)51025-0 . ПМИД 7929038 .
- ^ Эйнарсдоттир О, Коги В.С. (5 июля 1988 г.). «Взаимодействие анестетика закиси азота с цитохром-с-оксидазой бычьего сердца. Влияние на структуру белка, активность оксидазы и другие свойства» . Журнал биологической химии . 263 (19): 9199–9205. дои : 10.1016/S0021-9258(19)76525-9 . ПМИД 2837481 .
- ^ Гиллман М.А., Лихтигфельд Ф.Дж. (март 1985 г.). «Закись азота действует непосредственно на мю-опиоидный рецептор» . Анестезиология . 62 (3): 375–376. дои : 10.1097/00000542-198503000-00040 . ПМИД 2983587 .
- ^ Гиллман М.А., Лихтигфельд Ф.Дж. (январь 1981 г.). «Сравнение воздействия сульфата морфина и аналгезии закисью азота на состояния хронической боли у человека». Дж. Нейрол. Наука . 49 (1): 41–45. дои : 10.1016/0022-510X(81)90186-6 . ПМИД 7205318 . S2CID 32640794 .
- ^ Джонсон, Кэролайн Ю. (16 октября 2009 г.). «Ядовитый газ может принести медицинскую пользу» . Бостон Глобус . Проверено 16 октября 2009 г.
- ^ Керек Ф (сентябрь 2000 г.). «Структура дигиталисоподобных и натрийуретических факторов, идентифицированных как макроциклические производные неорганического субоксида углерода» . Исследования гипертонии . 23 (Приложение S33): S33–38. doi : 10.1291/hypres.23.Supplement_S33 . ПМИД 11016817 .
- ^ Стимак Р., Керек Ф., Апелл Х.Дж. (апрель 2003 г.). «Макроциклические олигомеры субоксида углерода как мощные ингибиторы Na,K-АТФазы» . Анналы Нью-Йоркской академии наук . 986 (1): 327–329. Бибкод : 2003NYASA.986..327S . дои : 10.1111/j.1749-6632.2003.tb07204.x . ПМИД 12763840 .
- ^ Керек Ф., Стимак Р., Апель Х.Дж., Фройденманн Ф., Мородер Л. (23 декабря 2002 г.). «Характеристика макроциклических факторов субоксида углерода как мощных ингибиторов Na,K-АТФазы и SR Ca-АТФазы» . Biochimica et Biophysical Acta (BBA) – Биомембраны . 1567 (1–2): 213–220. дои : 10.1016/S0005-2736(02)00609-0 . ПМИД 12488055 .
- ^ Тубаро Э. (июнь 1966 г.). «Перекись углерода, вероятный предшественник противоопухолевого клеточного вещества [так в оригинале]: сетчатки». Ферма Болл Чим (на итальянском языке). 105 (6): 415–416. ПМИД 6005012 .
- ^ Лю, Д.; Джин, Х; Тан, К; Ду, Дж (2010). «Диоксид серы: новый газообразный сигнал в регуляции сердечно-сосудистых функций» . Мини-обзоры по медицинской химии . 10 (11): 1039–1045. дои : 10.2174/1389557511009011039 . ПМИД 20540708 . Архивировано из оригинала 26 апреля 2013 г. Проверено 6 марта 2015 г.
- ^ Чэнь С., Чжэн С., Лю З., Тан С., Чжао Б., Ду Дж., Цзинь Х. (февраль 2015 г.). «Эндогенный диоксид серы защищает от острого повреждения легких, вызванного олеиновой кислотой, в сочетании с ингибированием окислительного стресса у крыс» . Лаб. Инвестируйте . 95 (2): 142–156. дои : 10.1038/labinvest.2014.147 . ПМИД 25581610 .
- ^ Тянь Х. (ноябрь 2014 г.). «Достижения в изучении эндогенного диоксида серы в сердечно-сосудистой системе» . Чин Мед Дж . 127 (21): 3803–3807. doi : 10.3760/cma.j.issn.0366-6999.20133031 . ПМИД 25382339 .
- ^ Ян Р., Ян Й, Донг Х, Ву Х, Вэй Й (август 2014 г.). «Корреляция между эндогенным диоксидом серы и гомоцистеином у детей с легочной артериальной гипертензией, связанной с врожденным пороком сердца». Чжунхуа Эр Кэ За Чжи (на китайском языке). 52 (8): 625–629. ПМИД 25224243 .
- ^ Лю Д., Хуан Ю, Бу Д., Лю А.Д., Холмберг Л., Цзя Ю., Тан С., Ду Дж., Цзинь Х. (май 2014 г.). «Диоксид серы ингибирует пролиферацию гладкомышечных клеток сосудов посредством подавления пути киназы Erk/MAP, опосредованного передачей сигналов цАМФ/РКА» . Смерть клетки Дис . 5 (5): e1251. дои : 10.1038/cddis.2014.229 . ПМК 4047873 . ПМИД 24853429 .
- ^ Ван XB, Джин HF, Тан CS, Ду JB (16 ноября 2011 г.). «Биологическое действие эндогенного диоксида серы на сердечно-сосудистую систему». Эур Дж Фармакол . 670 (1): 1–6. дои : 10.1016/j.ejphar.2011.08.031 . ПМИД 21925165 .
- ^ Лян Ю, Лю Д, Окс Т, Тан С, Чен С, Чжан С, Гэн Б, Цзинь Х, Ду Дж (январь 2011 г.). «Эндогенный диоксид серы защищает от повреждения миокарда, вызванного изопротеренолом, и увеличивает антиоксидантную способность миокарда у крыс» . Лаб. Инвестируйте . 91 (1): 12–23. дои : 10.1038/labinvest.2010.156 . ПМИД 20733562 .
- ^ Jump up to: а б Боровиц Дж.Л., Гунасекар П.Г., Исом Г.Е. (12 сентября 1997 г.). «Получение цианида водорода путем активации мю-опиатных рецепторов: возможная нейромодулирующая роль эндогенного цианида». Мозговой Рес . 768 (1–2): 294–300. дои : 10.1016/S0006-8993(97)00659-8 . ПМИД 9369328 . S2CID 12277593 .
- ^ Гунасекар П.Г., Прабхакаран К., Ли Л., Чжан Л., Исом Г.Е., Боровиц Дж.Л. (май 2004 г.). «Рецепторные механизмы, опосредующие образование цианида в клетках PC12 и мозге крыс». Неврологические исследования . 49 (1): 13–18. doi : 10.1016/j.neures.2004.01.006 . ПМИД 15099699 . S2CID 29850349 .
- ^ Смит Р.П., Крушина Х (январь 1976 г.). «Токсикология некоторых неорганических антигипертензивных анионов». Фед. Проц . 35 (1): 69–72. ПМИД 1245233 .
- ^ «Краткая информация о веществах PubChem» . Проверено 7 июля 2009 г.
- ^ Зшоке, Йоханнес; Георг Хоффман (2004). Метаболизм Вадемекума . Фридрихсдорф, Германия: Milupa GmbH.
- ^ Роуз, Бертон; Хельмут Реннке (1994). Почечная патофизиология . Балтимор: Уильямс и Уилкинс. ISBN 978-0-683-07354-6 .
- ^ Эстер Туболи; Андреа Сабо; Денес Гараб; Габор Барта; Агнес Яновски; Габор Эрос; Анна Сабо; Арпад Мохачи; Сабо Габор; Йожеф Кашаки; Миклош Гичи; Михай Борос (15 января 2013 г.). «Биогенез метана при химической гипоксии, вызванной азидом натрия, у крыс». Американский журнал физиологии. Клеточная физиология . 304 (2): 207–214. doi : 10.1152/ajpcell.00300.2012 . ПМИД 23174561 .
- ^ Туболи Э, Сабо А, Эрёш Г, Мохачи А, Сабо Г, Тенголичс Р, Ракхели Г, Борос М (декабрь 2013 г.). «Определение образования эндогенного метана методом фотоакустической спектроскопии» (PDF) . Журнал исследований дыхания . 7 (4): 046004. Бибкод : 2013JBR.....7d6004T . дои : 10.1088/1752-7155/7/4/046004 . ПМИД 24185326 . S2CID 206107686 .
- ^ Саакян А.Б., Джи С.Р., Пиментел М. (август 2010 г.). «Метан и желудочно-кишечный тракт». Dig Dis Sci . 55 (8): 2135–2143. дои : 10.1007/s10620-009-1012-0 . ПМИД 19830557 . S2CID 5493946 .
- ^ Jump up to: а б с Лин, З.; Чжун, С.; Грирсон, Д. (2009). «Последние достижения в исследованиях этилена» . Дж. Эксп. Бот . 60 (12): 3311–36. дои : 10.1093/jxb/erp204 . ПМИД 19567479 .
- ^ Внешняя ссылка на дополнительную информацию об отравлении этиленом газом и контроле над углекислым газом . Архивировано 14 сентября 2010 г. в Wayback Machine . ne-postharvest.com
- ^ Нелюбов Д. (1901). «О горизонтальной нутации стеблей Pisum sativum и некоторых других растений». Бейх Бот Централбл . 10 :128-139.
- ^ Сомнение, Сара Л. (1917). «Реакция растений на осветительный газ» . Ботанический вестник . 63 (3): 209–224. дои : 10.1086/332006 . hdl : 2027/mdp.39015068299380 . JSTOR 2469142 . S2CID 86383905 .
- ^ Гейн Р. (1934). «Производство этилена некоторыми фруктами» . Природа . 134 (3400): 1008. Бибкод : 1934Natur.134.1008G . дои : 10.1038/1341008a0 . S2CID 4090009 .
- ^ Крокер В., Хичкок А.Э., Циммерман П.В. (1935) «Сходство действия этлиена и растительных ауксинов». Вклад. Институт Бойса Томпсона. 7. 231-48. Ауксины Цитокинины ИУК Ростовые вещества, Этилен
- ^ Ян, Сан-Франциско; Хоффман Н.Е. (1984). «Биосинтез этилена и его регуляция у высших растений». Анну. Преподобный Плант Физиол . 35 : 155–89. дои : 10.1146/annurev.pp.35.060184.001103 .
- ^ Бликер, AB; Эш, Джей Джей; Холл, А.Е.; Родригес, Финляндия; Биндер, Б.М. (1998). «Семейство этиленовых рецепторов Arabidopsis: структура и функции» . Философские труды Королевского общества B: Биологические науки . 353 (1374): 1405–12. дои : 10.1098/rstb.1998.0295 . ПМЦ 1692356 . ПМИД 9800203 .
- ^ Объяснение Эпинастии . planthormones.inf
- ^ Танимото, Мими; Робертс, Кейт; Долан, Лиам (декабрь 1995 г.). «Этилен является положительным регулятором развития корневых волосков Arabidopsis thaliana» . Заводской журнал . 8 (6): 943–948. дои : 10.1046/j.1365-313X.1995.8060943.x . ПМИД 8580964 .
- ^ Чжан, Инцзяо; Ду, Хуан; Сюй, Фэйюнь; Дин, Есинь; Гуй, Яо; Чжан, Цзяньхуа; Сюй, Вэйфэн (июнь 2020 г.). «Ассоциации корневых бактерий ускоряют образование ризооболочек в умеренно сухой почве за счет реакции на этилен» . Физиология растений . 183 (2): 780–792. дои : 10.1104/стр.19.01020 . ПМЦ 7271771 . ПМИД 32220965 .
- ^ Хартман, Сьон (3 июня 2020 г.). «В ловушке в ризооболочке: корнево-бактериальные взаимодействия модулируют передачу сигналов этилена» . Физиология растений . 183 (2): 443–444. дои : 10.1104/стр.20.00379 . ПМЦ 7271798 . ПМИД 32493810 .
- ^ Давуд, Тикра; Ян, Синьпин; Виссер, Эрик Дж.В.; те Бик, Тим АХ; Кенше, Филип Р.; Кристеску, Симона М.; Ли, Сансок; Флокова, Кристина; Нгуен, Дуй; Мариани, Селестина; Рье, Иво (апрель 2016 г.). «Совместный гормональный каскад активирует спящие адвентивные корневые зачатки при затоплении дулькамары» . Физиология растений . 170 (4): 2351–2364. дои : 10.1104/стр.15.00773 . ПМЦ 4825138 . ПМИД 26850278 .
- ^ Неги, Сангита; Сукумар, Пурнима; Лю, Син; Коэн, Джерри Д.; Мудай, Глория К. (январь 2010 г.). «Генетическое исследование роли этилена в регуляции ауксин-зависимого образования боковых и придаточных корней у томатов». Заводской журнал . 61 (1): 3–15. дои : 10.1111/j.1365-313X.2009.04027.x . hdl : 10339/30054 . ПМИД 19793078 .
- ^ Хартман, С; Лю, З; ван Вин, Х; Висенте, Дж; Рейнен, Э; Мартопавиро, С; Чжан, Х; ван Донген, Н.; Босман, Ф; Бассель, Джорджия; Виссер, EJW; Бейли-Серрес, Дж; Теодулу, Флорида; Хебельструп, К.Х.; Гиббс, диджей; Холдсворт, MJ; Сасидхаран, Р; Воесенек, LACJ (5 сентября 2019 г.). «Опосредованное этиленом истощение оксида азота предварительно адаптирует растения к гипоксическому стрессу» . Природные коммуникации . 10 (1): 4020. Бибкод : 2019NatCo..10.4020H . дои : 10.1038/s41467-019-12045-4 . ПМК 6728379 . ПМИД 31488841 .
- ^ ван Вин и др., [1] , Plant Cell, 2013.
- ^ Хартман, Сьон; Сасидхаран, Рашми; Воесенек, Лаврентий ACJ (18 января 2020 г.). «Роль этилена в метаболической адаптации к низкому содержанию кислорода» . Новый фитолог . 229 (1): 64–70. дои : 10.1111/nph.16378 . ПМЦ 7754284 . ПМИД 31856295 .
- ^ Jump up to: а б Лю, Цзегуан; Хартман, Сьон; ван Вин, Ганс; Чжан, Хунтао; Лиггангерс, Хендрика АКФ; Мартопавиро, Шенис; Босман, Фемке; де Деуг, Флориан; Су, Пэн; Хаммел, Морин; Ранкенберг, Том; Хассалл, Кирсти Л; Бейли-Серрес, Джулия; Теодулу, Фредерика Л; Воесенек, Лаврентий ACJ; Сасидхаран, Рашми (30 мая 2022 г.). «Этилен повышает устойчивость корней к гипоксии за счет прекращения роста и улучшения активности активных форм кислорода» . Физиология растений . 190 (2): 1365–1383. дои : 10.1093/plphys/kiac245 . ПМЦ 9516759 . ПМИД 35640551 .
- ^ Барри, Корнелиус С.; Джованнони, Джеймс Дж. (6 июня 2007 г.). «Этилен и созревание фруктов». Журнал регулирования роста растений . 26 (2): 143–159. дои : 10.1007/s00344-007-9002-y . S2CID 29519988 .
- ^ Панди, Бипин К.; Хуан, Гоцян; Бхосале, Рахул; Хартман, Сьон; Старрок, Крейг Дж.; Хосе, Лотти; Мартин, Оливье К.; Каради, Михал; Воесенек, Лаврентий ACJ; Люнг, Карин; Линч, Джонатан П.; Браун, Кэтлин М.; Уолли, Уильям Р.; Муни, Саша Дж.; Чжан, Дабин; Беннетт, Малкольм Дж. (15 января 2021 г.). «Корни растений ощущают уплотнение почвы за счет ограниченной диффузии этилена» . Наука . 371 (6526): 276–280. Бибкод : 2021Sci...371..276P . дои : 10.1126/science.abf3013 . PMID 33446554 . S2CID 231606782 .
- ^ Хуан, Гоцян; Килич, Азад; Каради, Михал; Чжан, Цзяо; Мехра, Пунам; Сун, Сяоюнь; Старрок, Крейг Дж.; Чжу, Ваньвань; Цинь, Хуа; Хартман, Сьон; Шнайдер, Ханна М.; Бхосале, Рахул; Додд, Ян К.; Шарп, Роберт Э.; Хуан, Жунфэн; Муни, Саша Дж.; Лян, Ваньци; Беннетт, Малкольм Дж.; Чжан, Дабин; Панди, Бипин К. (26 июля 2022 г.). «Этилен ингибирует удлинение корней риса в уплотненной почве посредством механизмов, опосредованных АБК и ауксином» . Труды Национальной академии наук . 119 (30): e2201072119. Бибкод : 2022PNAS..11901072H . дои : 10.1073/pnas.2201072119 . ПМЦ 9335218 . PMID 35858424 .
- ^ Росадо, Даниэле; Акерманн, Аманда; Спасибойко, Оля; Росси, Магдалена; Педмале, Уллас V (4 февраля 2022 г.). «Факторы транскрипции WRKY и передача сигналов этилена изменяют рост корней во время реакции избегания тени» . Физиология растений . 188 (2): 1294–1311. дои : 10.1093/plphys/kiab493 . ПМЦ 8825332 . ПМИД 34718759 .
- ^ Курбье, Сара; Хартман, Сьон (4 февраля 2022 г.). «WRKY ограничивают рост корней в ответ на тень» . Физиология растений . 188 (2): 937–938. дои : 10.1093/plphys/kiab525 . ПМЦ 8825341 . ПМИД 34791438 .
- ^ Вильмович Э., Кеси Дж., Копцевич Дж. (декабрь 2008 г.). «Взаимодействие этилена и АБК в регуляции индукции цветения при нулевом Pharbitis ». Дж. Физиол растений . 165 (18): 1917–28. дои : 10.1016/j.jplph.2008.04.009 . ПМИД 18565620 .
- ^ Кокшалл К.Е., Хорридж Дж.С. (1978). «2-хлорэтилфосфоновая кислота и зарождение цветка Chrysanthemum morifolium Ramat. В короткие и длинные дни». Журнал садоводческих наук и биотехнологий . 53 (2): 85–90. дои : 10.1080/00221589.1978.11514799 .
- ^ Фильсер Дж.Г., Денк Б., Торнквист М., Кесслер В., Эренберг Л. (1992). «Фармакокинетика этилена у человека; нагрузка на организм оксидом этилена и гидроксиэтилирование гемоглобина за счет эндогенного и экологического этилена». Арх. Токсикол . 66 (3): 157–163. дои : 10.1007/bf01974008 . ПМИД 1303633 . S2CID 39354680 .
- ^ Болт Х.М., Лейтбехер М., Голка К. (1997). «Заметка о физиологической основе аддукта этиленоксида 7-(2-гидроксиэтил)гуанина в ДНК крови человека». Арх. Токсикол . 71 (11): 719–721. дои : 10.1007/s002040050451 . ПМИД 9363847 . S2CID 46278715 .
- ^ Чанади Г.А., Денк Б., Пютц С., Кройцер П.Е., Кесслер В., Баур С., Гаргас М.Л., Филсер Дж.Г. (15 мая 2000 г.). «Физиологическая токсикокинетическая модель экзогенного и эндогенного этилена и оксида этилена у крыс, мышей и человека: образование 2-гидроксиэтильных аддуктов с гемоглобином и ДНК». Токсикол Appl Pharmacol . 165 (1): 1–26. дои : 10.1006/taap.2000.8918 . ПМИД 10814549 .
- ^ Тьер Р., Болт Х.М. (сентябрь 2000 г.). «Канцерогенность и генотоксичность оксида этилена: новые аспекты и последние достижения». Крит Рев Токсикол . 30 (5): 595–608. дои : 10.1080/10408440008951121 . ПМИД 11055837 . S2CID 21154564 .
Внешние ссылки
[ редактировать ] СМИ, связанные с газообразными сигнальными молекулами, на Викискладе?
СМИ, связанные с газообразными сигнальными молекулами, на Викискладе?