Полимиксин
В этой статье отсутствует информация об истории Полимиксина. ( август 2019 г. ) |


Полимиксины являются антибиотиками . Полимиксины B и E (также известные как колистин ) используются при лечении грамотрицательных бактериальных инфекций. Они действуют в основном за счет разрушения мембраны бактериальных клеток . Они являются частью более широкого класса молекул, называемых нерибосомальными пептидами .
В природе они производятся грамположительными бактериями, такими как Paenibacillus Polymyxa .
Медицинское использование
[ редактировать ]Полимиксиновые антибиотики относительно нейротоксичны и нефротоксичны , поэтому обычно используются только в крайнем случае, если современные антибиотики неэффективны или противопоказаны. Типичным применением являются инфекции, вызванные штаммами множественной лекарственно-устойчивой Pseudomonas aeruginosa или карбапенемазы продуцирующими Enterobacteriaceae, . [ 1 ] [ 2 ] Полимиксины оказывают меньшее влияние на грамположительные микроорганизмы и иногда комбинируются с другими агентами (например, с триметопримом/полимиксином ) для расширения спектра действия. [ 3 ]
Полимиксины B не всасываются из желудочно-кишечного тракта, поэтому их назначают перорально только в том случае, если целью является дезинфекция желудочно-кишечного тракта. [ 3 ] Для системного лечения выбирают другой путь введения , например парентеральный (часто внутривенный) или ингаляционный. [ 1 ] [ 3 ] Их также используют наружно в виде крема или капель для лечения наружного отита (уха пловца), а также в качестве компонента мази с тройным антибиотиком для лечения и профилактики кожных инфекций. [ 3 ] [ 4 ]
Механизм действия
[ редактировать ]После связывания с липополисахаридом (ЛПС) на внешней мембране грамотрицательных бактерий полимиксины разрушают как внешнюю, так и внутреннюю мембраны. Гидрофобный хвост играет важную роль в повреждении мембраны, что предполагает детергенту . механизм действия, подобный [ 1 ]
Удаление гидрофобного хвоста полимиксина B дает нонапептид полимиксина, который все еще связывается с ЛПС, но больше не убивает бактериальную клетку. Тем не менее, он по-прежнему заметно увеличивает проницаемость бактериальной клеточной стенки для других антибиотиков, что указывает на то, что он все еще вызывает некоторую степень дезорганизации мембраны. [ 5 ]
Грамотрицательные бактерии могут развивать устойчивость к полимиксинам за счет различных модификаций структуры ЛПС, которые ингибируют связывание полимиксинов с ЛПС. [ 6 ]
Устойчивость к антибиотикам к этому препарату растет, особенно на юге Китая. Недавно ген mcr-1 , отвечающий за устойчивость к антибиотикам, был выделен из бактериальных плазмид Enterobacteriaceae . [ 7 ] [ 8 ]
Химия
[ редактировать ]
Полимиксины представляют собой группу циклических нерибосомальных полипептидов (NRP), которые биосинтезируются бактериями, принадлежащими к роду Paenibacillus . Полимиксины состоят из 10 аминокислотных остатков, шесть из которых представляют собой L-α,γ- диаминомасляную кислоту (L-DAB). Остатки DAB приводят к тому, что полимиксины имеют несколько положительно заряженных групп при физиологическом pH. Семь аминокислотных остатков образуют основной циклический компонент, тогда как остальные три отходят от одного из циклических остатков в виде линейной цепи, оканчивающейся либо 6-метилоктановой кислотой, либо 6-метилгептановой кислотой на N-конце . Во время циклизации остаток 10 связывается с мостиковым остатком 4. [ 9 ] Аминокислотные остатки и мономеры DAB обычно находятся в L (лево)-конфигурации, однако было обнаружено, что некоторые штаммы, такие как P. Polymyxa PKB1, включают DAB с D-(декстро)-конфигурацией в положении 3, производя вариации полимиксина B. [ 10 ]
Полимиксин М также известен как «маттацин». [ 11 ]
Биосинтез
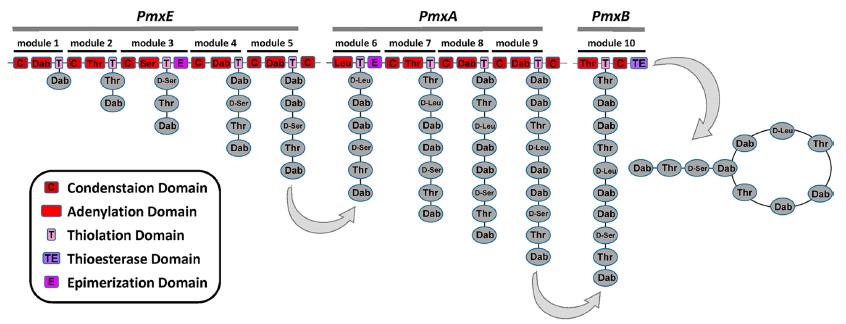
[ редактировать ]Полимиксины продуцируются нерибосомальными пептидсинтетазными системами грамположительных бактерий, таких как Paenibacilluspolymyxa . Как и другие NRP, полимиксины собираются синтетазами с несколькими модулями, каждый из которых содержит набор ферментных доменов, которые последовательно воздействуют на растущую цепь, добавляя следующий остаток и удлиняя цепь посредством образования пептидной связи и реакций конденсации. Заключительные шаги включают тиоэстеразный домен на С-конце последнего модуля для циклизации молекулы и высвобождения цепи из фермента. [ 12 ]
Исследовать
[ редактировать ]Полимиксины используются для нейтрализации или поглощения примесей ЛПС в образцах, например, в иммунологических экспериментах. Минимизация загрязнения ЛПС может иметь важное значение, поскольку ЛПС может вызывать сильную реакцию иммунных клеток, искажая результаты экспериментов.
Повышая проницаемость бактериальной мембранной системы, полимиксин также используется в клинической работе для увеличения высвобождения секретируемых токсинов, таких как шига- токсин, из Escherichia coli . [ 13 ]
Глобальная проблема развития устойчивости к противомикробным препаратам привела к возобновлению интереса к их использованию. [ 14 ]
Смеси соединений в препарате Полимиксин B
[ редактировать ]В составах коммерческого фармацевтического препарата «Полимиксин» основными полимиксинами являются В1 и В2, составляющие 75% и 15% конечной смеси соответственно. [ 15 ] Полимиксин В1, в свою очередь, состоит из нескольких изомеров, таких как изолейцин-полимиксин В1 и В1-1. [ 15 ] Основное препятствие в очистке и выделении одного изомера связано с минимальными структурными различиями между полимиксином B1 и B2, отличающимися только одним углеродом в 6-м положении жирной ацильной боковой цепи, связанной с D-фенилаланином структуры. Полимиксин В1 содержит 6-метилоктановую кислоту, а Полимиксин В2 — 6-метилгептановую кислоту. [ 16 ] Аналогичным образом, полимиксины B3 и B4 также различаются в этом положении: B3 содержит октановую кислоту, а B4 - гептановую кислоту. [ 17 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с Велков Т., Робертс К.Д., Нэйшн Р.Л., Томпсон П.Е., Ли Дж. (июнь 2013 г.). «Фармакология полимиксинов: новый взгляд на «старый» класс антибиотиков» . Будущая микробиология . 8 (6): 711–724. дои : 10.2217/fmb.13.39 . ПМЦ 3852176 . ПМИД 23701329 .
- ^ Фалагас М.Э., Касиаку С.К. (февраль 2006 г.). «Токсичность полимиксинов: систематический обзор данных старых и недавних исследований» . Критическая помощь . 10 (1): Р27. дои : 10.1186/cc3995 . ПМК 1550802 . ПМИД 16507149 .
- ^ Jump up to: а б с д Пуарель Л., Джайол А., Нордманн П. (апрель 2017 г.). «Полимиксины: антибактериальная активность, тестирование чувствительности и механизмы устойчивости, кодируемые плазмидами или хромосомами» . Обзоры клинической микробиологии . 30 (2): 557–596. дои : 10.1128/CMR.00064-16 . ПМЦ 5355641 . ПМИД 28275006 .
- ^ Огбру О. «Неомицина сульфат (кортиспорин): побочные эффекты препарата и дозировка» . МедицинаНет . Проверено 11 июня 2017 г.
- ^ Цубери Х, Офек И, Коэн С, Фридкин М (01 января 2000 г.). «Исследование взаимосвязи структура-активность нонапептида полимиксина B». Биология и патология механизмов врожденного иммунитета . Достижения экспериментальной медицины и биологии. Том. 479. стр. 219–222. дои : 10.1007/0-306-46831-X_18 . ISBN 978-0-306-46409-6 . ПМИД 10897422 .
- ^ Тран А.С., Лестер М.Е., Стед К.М., Раец С.Р., Маскелл Д.Д., МакГрат С.К. и др. (август 2005 г.). «Устойчивость к противомикробному пептиду полимиксину требует миристоилирования липида А Escherichia coli и Salmonella typhimurium» . Журнал биологической химии . 280 (31): 28186–28194. дои : 10.1074/jbc.M505020200 . ПМИД 15951433 .
- ^ Вольф Дж. (декабрь 2015 г.). «Устойчивость к антибиотикам угрожает эффективности профилактики». «Ланцет». Инфекционные болезни . 15 (12): 1368–1369. дои : 10.1016/S1473-3099(15)00317-5 . ПМИД 26482598 .
- ^ Лю Ю., Ван Ю., Уолш Т.Р., Йи Л.С., Чжан Р., Спенсер Дж. и др. (февраль 2016 г.). «Появление плазмидно-опосредованного механизма устойчивости к колистину MCR-1 у животных и людей в Китае: микробиологическое и молекулярно-биологическое исследование». «Ланцет». Инфекционные болезни . 16 (2): 161–168. дои : 10.1016/S1473-3099(15)00424-7 . ПМИД 26603172 .
- ^ Дьюик П.М. (3 января 2002 г.). Лекарственные натуральные продукты: биосинтетический подход . Джон Уайли и сыновья. ISBN 9780471496410 .
- ^ Шахин М., Ли Дж., Росс А.С., Ведерас Дж.К., Дженсен С.Е. (декабрь 2011 г.). «Paenibacillus Polymyxa PKB1 производит варианты антибиотиков полимиксина B-типа». Химия и биология . 18 (12): 1640–8. doi : 10.1016/j.chembiol.2011.09.017 . ПМИД 22195566 .
- ^ Мартин Н.И., Ху Х., Моак М.М., Чури Дж.Дж., Уиттал Р., Воробо Р.В. и др. (апрель 2003 г.). «Выделение, структурная характеристика и свойства маттацина (полимиксин М), циклического пептидного антибиотика, продуцируемого Paenibacillus kobensis M» . Журнал биологической химии . 278 (15): 13124–13132. дои : 10.1074/jbc.M212364200 . ПМИД 12569104 .
- ^ Копп Ф., Марахил М.А. (август 2007 г.). «Стратегии макроциклизации в биосинтезе поликетидов и нерибосомальных пептидов». Отчеты о натуральных продуктах . 24 (4): 735–749. дои : 10.1039/b613652b . ПМИД 17653357 .
- ^ Ёкояма К., Хории Т., Ямасино Т., Хашикава С., Баруа С., Хасегава Т. и др. (ноябрь 2000 г.). «Продукция шига-токсина Escherichia coli, измеренная по отношению к токсинам, связанным с мембранными везикулами» . Письма FEMS по микробиологии . 192 (1): 139–144. doi : 10.1111/j.1574–6968.2000.tb09372.x . ПМИД 11040442 .
- ^ Фалагас М.Э., Грамматикос А.П., Михалопулос А. (октябрь 2008 г.). «Потенциал антибиотиков старого поколения для удовлетворения текущей потребности в новых антибиотиках». Экспертный обзор противоинфекционной терапии . 6 (5): 593–600. дои : 10.1586/14787210.6.5.593 . ПМИД 18847400 . S2CID 13158593 .
- ^ Jump up to: а б Мэн М., Ван Л., Лю С., Джабер О.М., Гао Л., Шевретт Л. и др. (февраль 2016 г.). «Одновременное количественное определение полимиксина B1, полимиксина B2 и полимиксина B1-1 в плазме человека и обработанной моче человека с использованием твердофазной экстракции и тандемной жидкостной хроматографии и масс-спектрометрии». Журнал хроматографии. Б. Аналитические технологии в биомедицине и науках о жизни . 1012–1013: 23–36. дои : 10.1016/j.jchromb.2016.01.013 . ПМИД 26803416 .
- ^ Велков Т., Томпсон П.Е., Nation RL, Ли Дж. (март 2010 г.). «Соотношение структура-активность полимиксиновых антибиотиков» . Журнал медицинской химии . 53 (5): 1898–1916. дои : 10.1021/jm900999h . ПМЦ 2907661 . ПМИД 19874036 .
- ^ Орва Дж.А., Говертс С., Бюссон Р., Роетс Э., Ван Шепдал А., Хоогмартенс Дж. (апрель 2001 г.). «Выделение и структурная характеристика компонентов полимиксина B». Журнал хроматографии А. 912 (2): 369–373. дои : 10.1016/s0021-9673(01)00585-4 . ПМИД 11330807 .