Тикарциллин
 | |
| Клинические данные | |
|---|---|
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а685037 |
| Беременность категория |
|
| Маршруты администрация | внутривенный |
| код АТС | |
| Юридический статус | |
| Юридический статус |
|
| Фармакокинетические данные | |
| Связывание с белками | 45% |
| Период полувыведения | 1,1 часа |
| Экскреция | Реналь |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.047.451 |
| Химические и физические данные | |
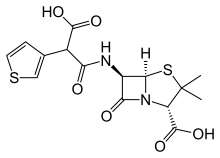
| Формула | С 15 Ч 16 Н 2 О 6 С 2 |
| Молярная масса | 384.42 g·mol −1 |
| 3D model ( JSmol ) | |
| (проверять) | |
Тикарциллин представляет собой карбоксипенициллин . Его можно продавать и использовать в сочетании с клавуланатом как тикарциллин/клавулановая кислота . Поскольку это пенициллин, он также относится к более широкому классу β-лактамных антибиотиков. Его основное клиническое применение — инъекционный антибиотик для лечения грамотрицательных бактерий, особенно Pseudomonas aeruginosa и Proteus vulgaris . Это также один из немногих антибиотиков, способных лечить Stenotropomonasmaltophilia инфекции .
Выпускается в виде белого или бледно-желтого порошка. Он хорошо растворим в воде, но его следует растворять только непосредственно перед использованием, чтобы предотвратить разложение.
Он был запатентован в 1963 году. [1]
Механизм действия
[ редактировать ]Антибиотические свойства тикарциллина обусловлены его способностью предотвращать образование поперечных связей пептидогликана во время синтеза клеточной стенки , когда бактерии пытаются делиться , вызывая гибель клеток. [ нужна ссылка ]
Тикарциллин, как и пенициллин , содержит β-лактамное кольцо, которое может расщепляться β-лактамазами , что приводит к инактивации антибиотика. Таким образом, бактерии, которые могут экспрессировать β-лактамазы, устойчивы к β-лактамным антибиотикам. По крайней мере частично, благодаря общему β-лактамному кольцу, тикарциллин может вызывать реакции у пациентов с аллергией на пенициллин. Тикарциллин также часто сочетают с ингибитором β-лактамаз , таким как клавулановая кислота ( ко-тикарклав ). [ нужна ссылка ]
Другое использование
[ редактировать ]В молекулярной биологии тикарциллин используется в качестве альтернативы ампициллину для проверки поглощения маркерных генов бактериями. Предотвращает появление колоний-сателлитов, возникающих при расщеплении ампициллина в среде. Он также используется в молекулярной биологии растений для уничтожения Agrobacterium , который используется для доставки генов в растительные клетки.
Дозирование и применение
[ редактировать ]Тикарциллин не всасывается при пероральном приеме, поэтому его следует вводить внутривенно или внутримышечно.
Торговые названия и препараты
[ редактировать ]- Тикарциллин: Тикар ранее продавался компанией Beecham , затем SmithKline Beecham до 1999 года, когда она объединилась с Glaxo и образовала GlaxoSmithKline ; он больше не доступен в Великобритании. Распространение в США прекратилось в 2004 году. Тикар был заменен Тиментином.
Однако в отличие от Тикара Тиментин содержит клавуланат.
- Тикарциллин/клавуланат : Тиментин в Австралии, Великобритании и США продавался компанией Beecham, а затем GlaxoSmithKline.
- Доступен в Индии как ТИКАНТРОЛ (ТИКАРИЛЛИН/клавуланат), продается компанией SCUTONIX LIFESCIENCES, Бомбей.
Синтез
[ редактировать ]Карбенициллин используется в клинике прежде всего из-за его низкой токсичности и возможности лечения инфекций мочевыводящих путей, вызванных чувствительными видами Pseudomonas . Его низкая эффективность, низкая пероральная активность и чувствительность к бактериальным бета-лактамазам делают его уязвимым для замены агентами без этих недостатков. Одним из претендентов в этой гонке является тикарициллин. Его происхождение зависело от известного факта, что двухвалентная сера примерно эквивалентна винильной группе (ср. метиопропамин , суфентанил , пизотилин и т. д.).

Один синтез начался с получения монобензилового эфира 3-тиенилмалоновой кислоты, превращения его в хлорангидрид с помощью SOCl2 и конденсации его с 6-аминопенициллановой кислотой ( 6-APA ). Гидрогенолиз (Pd/C) завершил синтез тикарциллина.
Ссылки
[ редактировать ]- ^ Фишер Дж., Ганеллин С.Р. (2006). Открытие аналоговых лекарств . Джон Уайли и сыновья. п. 491. ИСБН 9783527607495 .