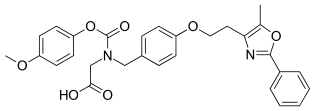
Мураглитазар
 | |
| Клинические данные | |
|---|---|
| Другие имена | 2-[(4-Метоксифенокси)карбонил-[[4-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)этокси]фенил]метил]амино]уксусная кислота |
| код АТС |
|
| Юридический статус | |
| Юридический статус |
|
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ХЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Химические и физические данные | |
| Формула | С 29 Н 28 Н 2 О 7 |
| Молярная масса | 516.550 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
Мураглитазар (предлагаемое торговое название Парглува ) представляет собой двойной агонист рецепторов, активирующих пролифератор пероксисом, обладающий сродством к PPARα и PPARγ . [ 1 ]
Препарат завершил III фазу клинических испытаний . [ 2 ] однако в мае 2006 года Bristol-Myers Squibb объявила о прекращении дальнейшей разработки. [ 3 ]
Данные о мураглитазаре относительно скудны из-за кратковременного введения этого препарата и последующего отказа от него. Одно двойное слепое рандомизированное клиническое исследование. [ 2 ] Сравнивая мураглитазар и пиоглитазон, было обнаружено, что эффекты первого были благоприятными с точки зрения повышения уровня холестерина ЛПВП , снижения общего холестерина , аполипопротеина B , триглицеридов и большего снижения HbA 1c ( p <0,0001 для всех сравнений). Однако в группе мураглитазара наблюдалась более высокая смертность от всех причин, более высокая частота отеков и сердечной недостаточности , а также больший прирост веса по сравнению с группой пиоглитазона. Метаанализ миокарда клинических исследований фазы II и III мураглитазара показал, что он был связан с большей частотой инфаркта , инсульта , транзиторных ишемических атак и застойной сердечной недостаточности (ЗСН) по сравнению с плацебо или пиоглитазоном. [ 4 ]
Привлекая внимание к нежелательным явлениям, о которых стало известно в ходе работы консультативного комитета FDA, д-р Ниссен разработал механизм управления FDA извне. [ нужна ссылка ] Этот механизм реализовался с росиглитазоном (Авандия) и привел к тому, что FDA потребовало продемонстрировать кардиобезопасность новых препаратов для лечения диабета 2 типа. [ нужна ссылка ] Этот процесс описан доктором Робертом Мисбином в «Истории инсулина» от инсайдера FDA, опубликованной 1 июня 2020 года на Amazon. [ повышение? ]
Ссылки
[ редактировать ]- ^ Уэйтс Ч.Р., Доминик М.А., Сандерсон Т.П., Шиллинг Б.Е. (ноябрь 2007 г.). «Доклиническая оценка безопасности мураглитазара, нового агониста PPARальфа/гамма» . Токсикологические науки . 100 (1): 248–58. дои : 10.1093/toxsci/kfm193 . ПМИД 17675651 .
- ^ Jump up to: а б Кендалл Д.М., Рубин С.Дж., Мохидин П., Ледейн Дж.М., Белдер Р., Гросс Дж. и др. (май 2006 г.). «Улучшение гликемического контроля, уровня триглицеридов и холестерина ЛПВП с помощью мураглитара, двойного (альфа/гамма) активатора рецепторов, активирующих пролифератор пероксисом, у пациентов с диабетом 2 типа, неадекватно контролируемым монотерапией метформином: двойное слепое рандомизированное исследование пиоглитазон- сравнительное исследование» (PDF) . Уход при диабете . 29 (5): 1016–23. дои : 10.2337/diacare.2951016 . ПМИД 16644631 .
- ^ «Bristol-Myers Squibb объявляет о прекращении разработки мураглитара, исследуемого перорального препарата для лечения диабета 2 типа» . PR Newswire от Bristol-Myers Squibb. 18 мая 2006 года . Проверено 9 ноября 2016 г.
- ^ Ниссен С.Е., Вольски К., Тополь Э.Ю. (ноябрь 2005 г.). «Влияние мураглитазара на смертность и основные неблагоприятные сердечно-сосудистые события у пациентов с сахарным диабетом 2 типа». ДЖАМА . 294 (20): 2581–6. дои : 10.1001/jama.294.20.joc50147 . ПМИД 16239637 .