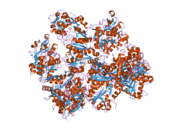Трансферрин
| ТФ | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | TF , PRO1557, PRO2086, TFQTL1, HEL-S-71p, трансферрин | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Опустить : 190000 ; МГИ : 98821 ; Гомологен : 68153 ; Генные карты : TF ; ОМА : TF – ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Трансферрин | |||
|---|---|---|---|
| Идентификаторы | |||
| Символ | Трансферрин | ||
| Пфам | PF00405 | ||
| ИнтерПро | IPR001156 | ||
| PROSITE | PDOC00182 | ||
| ОБЛАСТЬ ПРИМЕНЕНИЯ 2 | 1 куб. футов / ОБЛАСТЬ ПРИМЕНЕНИЯ / СУПФАМ | ||
| |||
Трансферрины — это гликопротеины, обнаруженные у позвоночных , которые связывают и, следовательно, опосредуют транспорт железа (Fe) через плазму крови . [ 5 ] Они вырабатываются в печени и содержат места связывания двух Fe. 3+ ионы. [ 6 ] Трансферрин человека кодируется TF геном и вырабатывается в виде гликопротеина массой 76 кДа . [ 7 ] [ 8 ]
трансферрина Гликопротеины прочно, но обратимо связывают железо. Хотя железо, связанное с трансферрином, составляет менее 0,1% (4 мг) от общего количества железа в организме, оно образует наиболее жизненно важный пул железа с самой высокой скоростью обмена (25 мг/24 ч). Трансферрин имеет молекулярную массу около 80 кДа с высоким сродством и содержит два специфических сайта связывания Fe(III) . Сродство трансферрина к Fe(III) чрезвычайно велико ( константа ассоциации 10 20 М −1 при pH 7,4) [ 9 ] но постепенно уменьшается с уменьшением pH ниже нейтрального. Трансферрины связываются не только с железом, но и с ионами различных металлов. [ 10 ] Эти гликопротеины расположены в различных жидкостях организма позвоночных. [ 11 ] [ 12 ] У некоторых беспозвоночных есть белки, действующие как трансферрин, обнаруженный в гемолимфе . [ 11 ] [ 13 ]
Когда трансферрин не связан с железом, он известен как «апотрансферрин» (см. также апопротеин ).
Возникновение и функция
[ редактировать ]Трансферрины – гликопротеины, часто встречающиеся в биологических жидкостях позвоночных. Когда белок трансферрин, нагруженный железом, встречает рецептор трансферрина на поверхности клетки , например, предшественников эритроида в костном мозге, он связывается с ним и транспортируется в клетку в пузырьке посредством рецептор-опосредованного эндоцитоза . [ 14 ] pH везикулы снижается с помощью водородных ионных насосов ( H +
АТФазы ) примерно до 5,5, заставляя трансферрин высвобождать ионы железа. [ 11 ] Скорость высвобождения железа зависит от нескольких факторов, включая уровень pH, взаимодействие между долями, температуру, соль и хелатор. [ 14 ] Рецептор с его лиганд- связанным трансферрином затем транспортируется через эндоцитарный цикл обратно на поверхность клетки, готовый к следующему раунду поглощения железа.
Каждая молекула трансферрина обладает способностью переносить два иона железа в трехвалентной форме ( Fe 3+
). [ 13 ]
Люди и другие млекопитающие
[ редактировать ]Печень . является основным местом синтеза трансферрина, но другие ткани и органы, включая мозг, также производят трансферрин Основным источником секреции трансферрина в головном мозге является сосудистое сплетение желудочковой системы . [ 15 ] Основная роль трансферрина заключается в доставке железа из центров абсорбции в двенадцатиперстной лейкоцитов кишке и макрофагов ко всем тканям. Трансферрин играет ключевую роль в областях, где происходит эритропоэз и активное деление клеток. [ 16 ] Рецептор помогает поддерживать гомеостаз железа в клетках, контролируя концентрацию железа. [ 16 ]
Ген , кодирующий трансферрин у человека, расположен в участке хромосомы 3q21. [ 7 ]
Медицинские работники могут проверить уровень трансферрина в сыворотке крови при дефиците железа и при заболеваниях, связанных с перегрузкой железом, таких как гемохроматоз .
Другие виды
[ редактировать ]Drosophila melanogaster имеет три гена трансферрина и сильно отличается от всех других модельных клад, у Ciona интестиналиса — один, у Danio rerio — три, сильно отличающихся друг от друга, как и у Takifugu Rubripes , Xenopus тропических и Gallus Gallus , в то время как у Monodelphis Domestica есть два расходящихся ортолога , и Mus musculus имеет два относительно близких и один более отдаленный ортолог. Данные о родстве и ортологии/ паралогии также доступны для Dictyostelium discoideum , Arabidopsis thaliana и Pseudomonas aeruginosa . [ 17 ]
Структура
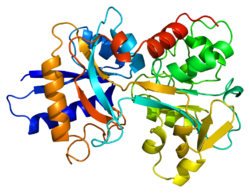
[ редактировать ]У человека трансферрин состоит из полипептидной цепи, содержащей 679 аминокислот , и двух углеводных цепей. Белок состоит из альфа-спиралей и бета-листов , которые образуют два домена . [ 18 ] N- и C-концевые последовательности представлены глобулярными долями, а между двумя долями находится сайт связывания железа. [ 12 ]
Аминокислоты , связывающие ион железа с трансферрином, идентичны для обеих долей; два тирозина , один гистидин и одна аспарагиновая кислота . Для связывания иона железа анион необходим , предпочтительно карбонат ( CO 2−
3 ). [ 18 ] [ 13 ]
Трансферрин также имеет железосвязанный рецептор трансферрина ; это гомодимер с дисульфидной связью . [ 16 ] У человека каждый мономер состоит из 760 аминокислот. Это обеспечивает связывание лиганда с трансферрином, поскольку каждый мономер может связываться с одним или двумя атомами железа. Каждый мономер состоит из трех доменов: протеазного, спирального и апикального. Форма рецептора трансферрина напоминает бабочку за счет пересечения трех четко очерченных доменов. [ 18 ] Два основных рецептора трансферрина, обнаруженные у человека, обозначаются как рецептор трансферрина 1 (TfR1) и рецептор трансферрина 2 (TfR2). Хотя оба они схожи по структуре, TfR1 может специфически связываться только с ТФ человека, тогда как TfR2 также обладает способностью взаимодействовать с ТФ крупного рогатого скота . [ 8 ]
Иммунная система
[ редактировать ]Трансферрин также связан с врожденной иммунной системой . Он содержится в слизистой оболочке и связывает железо, создавая таким образом среду с низким содержанием свободного железа, что препятствует выживанию бактерий в процессе, называемом удержанием железа. Уровень трансферрина снижается при воспалении. [ 21 ]
Роль в болезни
[ редактировать ]Повышенный уровень трансферрина в плазме часто наблюдается у пациентов с железодефицитной анемией , во время беременности и при использовании пероральных контрацептивов, что отражает увеличение экспрессии белка трансферрина. Когда уровни трансферрина в плазме повышаются, происходит взаимное снижение процента насыщения трансферрина железом и соответствующее увеличение общей железосвязывающей способности в состояниях с дефицитом железа. [ 22 ]
Снижение уровня трансферрина в плазме может наблюдаться при заболеваниях, связанных с перегрузкой железом и белковой недостаточностью. Отсутствие трансферрина является результатом редкого генетического заболевания, известного как атрансферринемия , состояния, характеризующегося анемией и гемосидерозом сердца и печени, которое приводит к сердечной недостаточности и многим другим осложнениям, а также к синдрому H63D .
Исследования показывают, что насыщение трансферрина (концентрация железа в сыворотке ÷ общая железосвязывающая способность) более 60 процентов у мужчин и более 50 процентов у женщин указывает на наличие нарушения метаболизма железа (наследственный гемохроматоз, гетерозиготы и гомозиготы) с точностью примерно 95 процентов. Это открытие помогает в ранней диагностике наследственного гемохроматоза, особенно в то время, когда ферритин сыворотки все еще остается низким. Сохраненное железо при наследственном гемохроматозе преимущественно откладывается в паренхиматозных клетках, причем накопление ретикулоэндотелиальных клеток происходит на очень поздних стадиях заболевания. Это контрастирует с трансфузионной перегрузкой железом, при которой отложение железа происходит сначала в ретикулоэндотелиальных клетках, а затем в паренхиматозных клетках. Это объясняет, почему уровень ферритина остается относительно низким при наследственном гемохроматозе, в то время как насыщение трансферрина является высоким. [ 23 ] [ 24 ]
Было показано, что трансферрин и его рецептор уменьшают опухолевые клетки , когда рецептор используется для привлечения антител . [ 16 ]
Трансферрин и наномедицина
[ редактировать ]Многие лекарства затрудняются при оказании лечения при пересечении гематоэнцефалического барьера, что приводит к плохому поступлению в области мозга. Гликопротеины трансферрина способны обходить гематоэнцефалический барьер посредством рецептор-опосредованного транспорта для специфических рецепторов трансферрина, обнаруженных в эндотелиальных клетках капилляров головного мозга. [ 25 ] Предполагается, что благодаря этой функциональности наночастицы , действующие как переносчики лекарств, связанные с гликопротеинами трансферрина, могут проникать через гематоэнцефалический барьер, позволяя этим веществам достигать больных клеток головного мозга. [ 26 ] Достижения в области наночастиц, конъюгированных с трансферрином, могут привести к неинвазивному распределению лекарств в мозге с потенциальными терапевтическими последствиями при заболеваниях центральной нервной системы (ЦНС) (например, болезни Альцгеймера или Паркинсона ). [ 27 ]
Другие эффекты
[ редактировать ]Уровень дефицита углеводов в трансферрине увеличивается в крови при чрезмерном употреблении этанола , и его можно контролировать с помощью лабораторных исследований. [ 28 ]
Трансферрин является белком острой фазы, и его активность снижается при воспалении, раке и некоторых заболеваниях (в отличие от других белков острой фазы, например, С-реактивного белка, уровень которого увеличивается в случае острого воспаления). [ 29 ]
Патология
[ редактировать ]Атрансферринемия связана с дефицитом трансферрина.
При нефротическом синдроме потеря трансферрина с мочой, а также других белков сыворотки, таких как тироксинсвязывающий глобулин, гаммаглобулин и антитромбин III, может проявляться в виде железорезистентной микроцитарной анемии .
Эталонные диапазоны
[ редактировать ]Примерный референтный диапазон трансферрина составляет 204–360 мг/дл. [ 30 ] Результаты лабораторных исследований всегда следует интерпретировать с использованием референтного диапазона, предоставленного лабораторией, проводившей тест. [ нужна ссылка ] .

Высокий уровень трансферрина может указывать на железодефицитную анемию . Уровни сывороточного железа и общая железосвязывающая способность (ОЖЖС) используются в сочетании с трансферрином для выявления каких-либо отклонений. См. интерпретацию TIBC . Низкий уровень трансферрина, вероятно, указывает на недостаточное питание .
Взаимодействия
[ редактировать ]Было показано, что трансферрин взаимодействует с инсулиноподобным фактором роста 2. [ 31 ] и IGFBP3 . [ 32 ] Регуляция транскрипции трансферрина усиливается ретиноевой кислотой . [ 33 ]
Родственные белки
[ редактировать ]Члены этого семейства включают серотрансферрин крови (или сидерофилин, обычно называемый просто трансферрином); лактотрансферрин (лактоферрин); молочный трансферрин; яичного белка овотрансферрин (кональбумин); и мембраносвязанный меланотрансферрин . [ 34 ]
См. также
[ редактировать ]- Бета-2 трансферрин
- Рецептор трансферрина
- Общая железосвязывающая способность
- Насыщение трансферрина
- Ферритин
- Оптиферрин рекомбинантный человеческий трансферрин
- Атрансферринемия
- Гипотрансферринемия
- Мутация гена HFE H63D
Ссылки
[ редактировать ]- ^ Jump up to: а б с GRCh38: Версия Ensembl 89: ENSG00000091513 – Ensembl , май 2017 г.
- ^ Jump up to: а б с GRCm38: выпуск Ensembl 89: ENSMUSG00000032554 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ Крайтон Р.Р., Шарлото-Вотерс М. (май 1987 г.). «Транспортировка и хранение железа» . Европейский журнал биохимии . 164 (3): 485–506. дои : 10.1111/j.1432-1033.1987.tb11155.x . ПМИД 3032619 .
- ^ Холл Д.Р., Хадден Дж.М., Леонард Г.А., Бэйли С., Ной М., Винн М., Линдли П.Ф. (январь 2002 г.). «Кристаллическая и молекулярная структура двухжелезных трансферринов сыворотки свиньи и кролика при разрешении 2,15 и 2,60 А соответственно». Акта Кристаллографика. Раздел D. Биологическая кристаллография . 58 (Часть 1): 70–80. Бибкод : 2002AcCrD..58...70H . дои : 10.1107/s0907444901017309 . ПМИД 11752780 .
- ^ Jump up to: а б Ян Ф., Лам Дж.Б., МакГилл Дж.Р., Мур К.М., Нейлор С.Л., ван Брагт П.Х. и др. (май 1984 г.). «Человеческий трансферрин: характеристика кДНК и хромосомная локализация» . Труды Национальной академии наук Соединенных Штатов Америки . 81 (9): 2752–6. Бибкод : 1984PNAS...81.2752Y . дои : 10.1073/pnas.81.9.2752 . ПМК 345148 . ПМИД 6585826 .
- ^ Jump up to: а б Кавабата Х (март 2019 г.). «Обновление трансферрина и трансферриновых рецепторов». Свободно-радикальная биология и медицина . 133 : 46–54. doi : 10.1016/j.freeradbiomed.2018.06.037 . ПМИД 29969719 . S2CID 49674402 .
- ^ Айсен П., Лейбман А., Цвайер Дж. (март 1978 г.). «Стехиометрические и сайт-характеристики связывания железа с трансферрином человека» . Журнал биологической химии . 253 (6): 1930–7. дои : 10.1016/S0021-9258(19)62337-9 . ПМИД 204636 .
- ^ Никотра С., Сорио Д., Филиппи Г., Де Джоя Л., Патерлини В., Де Пало Э.Ф. и др. (ноябрь 2017 г.). «Хелирование тербия, специфическое флуоресцентное мечение трансферрина человека. Оптимизация условий с учетом его применения для ВЭЖХ-анализа трансферрина с дефицитом углеводов (CDT)». Аналитическая и биоаналитическая химия . 409 (28): 6605–6612. дои : 10.1007/s00216-017-0616-z . ПМИД 28971232 . S2CID 13929228 .
- ^ Jump up to: а б с МакГилливрей Р.Т., Мур С.А., Чен Дж., Андерсон Б.Ф., Бейкер Х., Луо Ю. и др. (июнь 1998 г.). «Две кристаллические структуры рекомбинантной N-доли трансферрина человека с высоким разрешением обнаруживают структурные изменения, связанные с высвобождением железа». Биохимия . 37 (22): 7919–28. дои : 10.1021/bi980355j . ПМИД 9609685 .
- ^ Jump up to: а б Деван Дж.С., Миками Б., Хиросе М., Саккеттини Дж.К. (ноябрь 1993 г.). «Структурные доказательства pH-чувствительного дилизина в N-доле овотрансферрина: последствия для высвобождения железа трансферрина». Биохимия . 32 (45): 11963–8. дои : 10.1021/bi00096a004 . ПМИД 8218271 .
- ^ Jump up to: а б с Бейкер Э.Н., Линдли П.Ф. (август 1992 г.). «Новые взгляды на структуру и функцию трансферринов». Журнал неорганической биохимии . 47 (3–4): 147–60. дои : 10.1016/0162-0134(92)84061-q . ПМИД 1431877 .
- ^ Jump up to: а б Хэлбрукс П.Дж., Хе Кью, Бриггс С.К., Иверс С.Дж., Смит В.К., МакГилливрей Р.Т., Мейсон А.Б. (апрель 2003 г.). «Исследование механизма высвобождения железа из C-доли трансферрина сыворотки человека: мутационный анализ роли рН-чувствительной триады». Биохимия . 42 (13): 3701–7. дои : 10.1021/bi027071q . ПМИД 12667060 .
- ^ Моос Т. (ноябрь 2002 г.). «Гомеостаз железа мозга». Датский медицинский бюллетень . 49 (4): 279–301. ПМИД 12553165 .
- ^ Jump up to: а б с д Маседо М.Ф., де Соуза М. (март 2008 г.). «Трансферрин и рецептор трансферрина: волшебные пули и другие проблемы». Воспаление и аллергия — мишени для лекарств . 7 (1): 41–52. дои : 10.2174/187152808784165162 . ПМИД 18473900 .
- ^ Габальдон Т., Кунин Е.В. (май 2013 г.). «Функциональные и эволюционные последствия ортологии генов» . Обзоры природы. Генетика . 14 (5). Природный портфель : 360–6. дои : 10.1038/nrg3456 . ПМЦ 5877793 . ПМИД 23552219 .
- ^ Jump up to: а б с «Структура трансферрина» . Университет Святого Эдварда. 18 июля 2005 г. Архивировано из оригинала 11 декабря 2012 г. Проверено 24 апреля 2009 г.
- ^ PDB : 1сув ; Ченг Ю, Зак О, Айсен П., Харрисон С.С., Уолц Т. (февраль 2004 г.). «Структура комплекса трансферриновый рецептор-трансферрин человека». Клетка . 116 (4): 565–76. дои : 10.1016/S0092-8674(04)00130-8 . ПМИД 14980223 . S2CID 2981917 .
- ^ ВВП : 2нсу ; Хафенштейн С., Палермо Л.М., Костюченко В.А., Сяо С., Мораис М.К., Нельсон К.Д., Боуман В.Д., Баттисти А.Дж., Чипман П.Р., Пэрриш Ч.Р., Россманн М.Г. (апрель 2007 г.). «Асимметричное связывание рецептора трансферрина с капсидами парвовируса» . Труды Национальной академии наук Соединенных Штатов Америки . 104 (16): 6585–9. Бибкод : 2007PNAS..104.6585H . дои : 10.1073/pnas.0701574104 . ЧВК 1871829 . ПМИД 17420467 .
- ^ Ричи Р.Ф., Паломаки Г.Е., Неве Л.М., Наволоцкая О., Ледью Т.Б., Крейг В.И. (1999). «Эталонные распределения отрицательных сывороточных белков острой фазы, альбумина, трансферрина и транстиретина: практичный, простой и клинически значимый подход в большой когорте» . Журнал клинического лабораторного анализа . 13 (6): 273–9. doi : 10.1002/(SICI)1098-2825(1999)13:6<273::AID-JCLA4>3.0.CO;2-X . ПМК 6808097 . ПМИД 10633294 .
- ^ Миллер Дж.Л. (июль 2013 г.). «Железодефицитная анемия: распространенное и излечимое заболевание» . Перспективы Колд-Спринг-Харбора в медицине . 3 (7): а011866. doi : 10.1101/cshperspect.a011866 . ПМЦ 3685880 . ПМИД 23613366 .
- ^ Бэкон Б.Р., Адамс ПК, Каудли К.В., Пауэлл Л.В., Тавилл А.С. (июль 2011 г.). «Диагностика и лечение гемохроматоза: практическое руководство Американской ассоциации по изучению заболеваний печени, 2011 г.» . Гепатология . 54 (1). Балтимор, Мэриленд: 328–43. дои : 10.1002/hep.24330 . ПМК 3149125 . ПМИД 21452290 .
- ^ «Гемохроматоз» . Guidelinecentral.com .
- ^ Гадири М., Вашигани-Фарахани Э., Атьяби Ф., Кобарфард Ф., Мохамадьяр-Тупканлу Ф., Хоссейнхани Х. (октябрь 2017 г.). «Конъюгированные с трансферрином магнитные наночастицы декстрана и спермина для направленного транспорта лекарств через гематоэнцефалический барьер». Журнал исследований биомедицинских материалов, часть A. 105 (10): 2851–2864. дои : 10.1002/jbm.a.36145 . ПМИД 28639394 .
- ^ Гаспар Р. (февраль 2013 г.). «Наночастицы: отталкиваются от цели белками». Природные нанотехнологии . 8 (2): 79–80. Бибкод : 2013НатНа...8...79Г . дои : 10.1038/nnano.2013.11 . ПМИД 23380930 .
- ^ Ли С., Пэн З., Даллман Дж., Бейкер Дж., Отман А.М., Блэквелдер П.Л., Леблан Р.М. (сентябрь 2016 г.). «Пересечение гематоэнцефалического барьера с помощью углеродных точек, конъюгированных с трансферрином: исследование на модели рыбки данио» . Коллоиды и поверхности. Б. Биоинтерфейсы . 145 : 251–256. дои : 10.1016/j.colsurfb.2016.05.007 . ПМИД 27187189 .
- ^ ПК Шарп (ноябрь 2001 г.). «Биохимическое выявление и мониторинг злоупотребления алкоголем и воздержания». Анналы клинической биохимии . 38 (Часть 6): 652–64. дои : 10.1258/0004563011901064 . ПМИД 11732647 . S2CID 12203099 .
- ^ Джайн С., Гаутам В., Насим С. (январь 2011 г.). «Белки острой фазы: как диагностический инструмент» . Журнал фармации и биологических наук . 3 (1): 118–27. дои : 10.4103/0975-7406.76489 . ПМК 3053509 . ПМИД 21430962 .
- ^ «Таблица нормальных эталонных диапазонов» . Интерактивное тематическое исследование, дополняющее патологические основы заболеваний . Юго-западный медицинский центр Техасского университета в Далласе. Архивировано из оригинала 25 декабря 2011 г. Проверено 25 октября 2008 г.
Кумар В., Хаглер Х.К. (1999). Интерактивное тематическое исследование к книге «Патологические основы болезней Роббинса» (6-е издание (компакт-диск для Windows и Macintosh, индивидуальное) под ред.). WB Saunders Co. ISBN 0-7216-8462-9 . - ^ Шторх С., Кюблер Б., Хёнинг С., Акманн М., Цапф Дж., Блюм В., Браулке Т. (декабрь 2001 г.). «Трансферрин связывает инсулиноподобные факторы роста и влияет на связывающие свойства белка-3, связывающего инсулиноподобный фактор роста» . Письма ФЭБС . 509 (3): 395–8. дои : 10.1016/S0014-5793(01)03204-5 . ПМИД 11749962 . S2CID 22895295 .
- ^ Вайнцимер С.А., Гибсон Т.Б., Коллетт-Сольберг П.Ф., Харе А., Лю Б., Коэн П. (апрель 2001 г.). «Трансферрин представляет собой белок-3, связывающий инсулиноподобный фактор роста» . Журнал клинической эндокринологии и метаболизма . 86 (4): 1806–13. дои : 10.1210/jcem.86.4.7380 . ПМИД 11297622 .
- ^ Сюй С.Л., Линь Ю.Ф., Чжоу К.К. (апрель 1992 г.). «Регуляция транскрипции генов трансферрина и альбумина с помощью ретиноевой кислоты в клеточной линии гепатомы человека Hep3B» . Биохимический журнал . 283 (Часть 2) (2): 611–5. дои : 10.1042/bj2830611 . ПМК 1131079 . ПМИД 1315521 .
- ^ Чунг MC (октябрь 1984 г.). «Структура и функции трансферрина». Биохимическое образование . 12 (4): 146–154. дои : 10.1016/0307-4412(84)90118-3 .
Дальнейшее чтение
[ редактировать ]- Хершбергер К.Л., Ларсон Дж.Л., Арнольд Б., Ростек П.Р., Уильямс П., ДеХофф Б. и др. (декабрь 1991 г.). «Клонированный ген трансферрина человека». Анналы Нью-Йоркской академии наук . 646 (1): 140–54. Бибкод : 1991NYASA.646..140H . дои : 10.1111/j.1749-6632.1991.tb18573.x . ПМИД 1809186 . S2CID 19519911 .
- Боуман Б.Х., Ян Ф.М., Адриан Г.С. (1989). Трансферрин: эволюция и генетическая регуляция экспрессии . Достижения генетики. Том. 25. стр. 1–38. дои : 10.1016/S0065-2660(08)60457-5 . ISBN 9780120176250 . ПМИД 3057819 .
- Парккинен Дж., фон Бонсдорф Л., Эбелинг Ф., Сальстедт Л. (август 2002 г.). «Функция и терапевтическое развитие апотрансферрина». Вокс Сангвинис . 83 (Приложение 1): 321–6. дои : 10.1111/j.1423-0410.2002.tb05327.x . ПМИД 12617162 . S2CID 5876134 .
Внешние ссылки
[ редактировать ]- Трансферрин в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- Обзор всей структурной информации, доступной в PDB для UniProt : P02787 (Серотрансферрин) в PDBe-KB .




![Трансферрин связан со своим рецептором.[19]](http://upload.wikimedia.org/wikipedia/commons/thumb/b/b2/PDB_1suv_EBI.jpg/120px-PDB_1suv_EBI.jpg)
![Комплекс рецепторов трансферрина.[20]](http://upload.wikimedia.org/wikipedia/commons/thumb/b/b1/PDB_2nsu_EBI.jpg/120px-PDB_2nsu_EBI.jpg)