Тромбофилия
| Тромбофилия | |
|---|---|
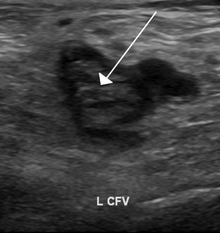 | |
| Ультразвуковое изображение, демонстрирующее тромб в левой общей бедренной вене. | |
| Специальность | Гематология |
Тромбофилия (иногда называемая гиперкоагуляцией или протромботическим состоянием ) — нарушение свертываемости крови , повышающее риск тромбообразования (сгустков крови в кровеносных сосудах). [1] [2] Подобные отклонения можно выявить у 50% людей, у которых возник эпизод тромбоза (например, тромбоз глубоких вен ноги), не спровоцированный другими причинами. [3] У значительной части населения имеются обнаруживаемые тромбофилические нарушения, но у большинства из них тромбоз развивается только при наличии дополнительного фактора риска. [2]
Специфического лечения большинства тромбофилий не существует, но рецидивирующие эпизоды тромбоза могут быть показанием для длительной профилактической антикоагулянтной терапии . [2] Первая серьезная форма тромбофилии, выявленная медицинской наукой, дефицит антитромбина , была выявлена в 1965 году, тогда как наиболее распространенные нарушения (включая фактор V Лейдена ) были описаны в 1990-х годах. [4] [5]
Признаки и симптомы
[ редактировать ]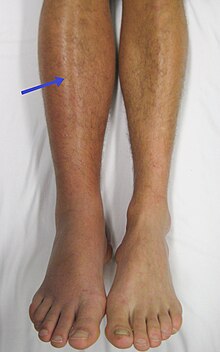
Наиболее распространенными состояниями, связанными с тромбофилией, являются тромбоз глубоких вен (ТГВ) и легочная эмболия (ЛЭ), которые вместе называются венозной тромбоэмболией (ВТЭ). ТГВ обычно возникает в ногах и характеризуется болью, отеком и покраснением конечности. Это может привести к длительному отеку и тяжести из -за повреждения клапанов вен. [6] Сгусток также может оторваться и мигрировать ( эмболизировать ) в артерии легких. В зависимости от размера и местоположения тромба это может привести к внезапно возникшей одышке , боли в груди , сердцебиению и может осложниться коллапсом , шоком и остановкой сердца . [2] [7]
Венозный тромбоз может возникать и в более необычных местах: в венах головного мозга , печени ( тромбоз воротной вены и тромбоз печеночной вены ), брыжеечной вене , почках ( тромбоз почечной вены ) и венах рук . [2] Увеличивает ли тромбофилия риск артериального тромбоза (который является основной причиной сердечных приступов и инсультов ), менее точно установлено. [2] [8] [9] Однако более поздние данные позволяют предположить, что некоторые формы наследственной тромбофилии связаны с повышенным риском артериального ишемического инсульта . [10]
Тромбофилия связана с привычным выкидышем . [11] и, возможно, различные осложнения беременности, такие как задержка внутриутробного развития , мертворождение , тяжелая преэклампсия и отслойка плаценты . [2]
Дефицит белка С может вызвать молниеносную пурпуру — тяжелое нарушение свертываемости крови у новорожденного, которое приводит как к отмиранию тканей, так и к кровотечениям в кожу и другие органы. Состояние также было описано у взрослых. протеина C и Дефицит протеина S также связан с повышенным риском некроза кожи в начале лечения антикоагулянтами варфарином или родственными препаратами. [2] [12]
Причины
[ редактировать ]Тромбофилия может быть врожденной или приобретенной. Врожденная тромбофилия относится к врожденным состояниям (и обычно наследственным, в этом случае можно использовать термин « наследственная тромбофилия »), которые повышают склонность к развитию тромбозов, тогда как, с другой стороны, приобретенная тромбофилия относится к состояниям, возникающим в более позднем возрасте.
Врожденный
[ редактировать ]Наиболее распространенными видами врожденной тромбофилии являются те, которые возникают в результате гиперактивности факторов свертывания крови. Они относительно легкие и поэтому классифицируются как дефекты «типа II». [13] [14] Наиболее распространенными из них являются фактор V Лейдена (мутация гена F5 в положении 1691) и протромбин G20210A , мутация протромбина (в положении 20210 в 3'-нетранслируемой области гена). [1] [15]
Редкие формы врожденной тромбофилии обычно вызваны дефицитом природных антикоагулянтов. Они классифицируются как «тип I» и имеют более серьезную склонность к тромбообразованию. [13] Основными из них являются дефицит антитромбина III , дефицит протеина С и дефицит протеина S. [1] [15] Более легкие и редкие врожденные тромбофилии являются фактора XIII. мутацией [15] и семейная дисфибриногенемия (аномальный фибриноген ). [15] Неясно, являются ли врожденные нарушения фибринолиза (системы, разрушающей тромбы) основным фактором риска тромбоза. [13] Например, врожденный дефицит плазминогена в основном вызывает глазные симптомы, а иногда и проблемы в других органах, но связь с тромбозом более неопределенна. [16]
Группа крови в значительной степени определяет риск тромбообразования. Люди с группами крови, отличными от группы O, подвергаются относительному риску в 2–4 раза. Группа крови O связана со снижением уровня фактора фон Виллебранда (из-за повышенного клиренса) и фактора VIII, который связан с риском тромбообразования. [5]
Приобретенный
[ редактировать ]Ряд приобретенных состояний увеличивают риск тромбоза. Ярким примером является антифосфолипидный синдром . [1] [15] который вызывается антителами против компонентов клеточной мембраны, особенно волчаночного антикоагулянта (впервые обнаруженного у людей с системной красной волчанкой, но часто выявляемого у людей без этого заболевания), антител к кардиолипину и антител к β 2 -гликопротеину 1. ; поэтому оно рассматривается как аутоиммунное заболевание . В некоторых случаях антифосфолипидный синдром может вызвать как артериальный, так и венозный тромбоз. Он также более тесно связан с выкидышем и может вызывать ряд других симптомов (таких как сетчатое ливедо кожи и мигрень ). [17]
Гепарин-индуцированная тромбоцитопения (ГИТ) обусловлена реакцией иммунной системы на антикоагулянт гепарин (или его производные). [1] Хотя ГИТ названа в честь низкого количества тромбоцитов, она тесно связана с риском венозного и артериального тромбоза. [18] Пароксизмальная ночная гемоглобинурия (ПНГ) — редкое заболевание, возникающее в результате приобретенных изменений в гене PIGA , который играет роль в защите клеток крови от системы комплемента . ПНГ увеличивает риск венозного тромбоза, но также связана с гемолитической анемией (анемией, возникающей в результате разрушения эритроцитов). [19] И ГИТ, и ПНГ требуют особого лечения. [18] [19]
Гематологические состояния, связанные с вялым кровотоком, могут увеличить риск тромбоза. Например, серповидно-клеточная анемия (вызванная мутациями гемоглобина ) рассматривается как легкое протромботическое состояние, вызванное нарушением кровотока. [1] Аналогичным образом, миелопролиферативные заболевания , при которых костный мозг производит слишком много клеток крови, предрасполагают к тромбозу, особенно при истинной полицитемии (избыток эритроцитов) и эссенциальном тромбоцитозе (избыток тромбоцитов). Опять же, при выявлении этих состояний обычно требуется специальное лечение. [20]
Рак , особенно метастатический (распространяющийся на другие части тела), является признанным фактором риска тромбоза. [2] [15] Был предложен ряд механизмов, таких как активация системы свертывания крови раковыми клетками или секреция прокоагулянтных веществ. Кроме того, определенные методы лечения рака (например, использование центральных венозных катетеров для химиотерапии ) могут еще больше увеличить риск тромбоза. [21]
Нефротический синдром , при котором белок из кровотока попадает в мочу вследствие заболеваний почек, может предрасполагать к тромбообразованию; [1] это особенно актуально в более тяжелых случаях (на что указывает уровень альбумина в крови ниже 25 г/л) и если синдром вызван состоянием мембранозной нефропатии . [22] Воспалительные заболевания кишечника ( язвенный колит и болезнь Крона ) предрасполагают к тромбозу, особенно когда заболевание активно. Были предложены различные механизмы. [2] [23]
Беременность связана с повышенным риском тромбоза в 2–7 раз. [24] Вероятно, это является результатом физиологической гиперкоагуляции во время беременности , которая защищает от послеродового кровотечения . [25] Эта гиперкоагуляция, в свою очередь, вероятно, связана с высокими уровнями эстрадиола и прогестерона , которые возникают во время беременности. [26]
Эстрогены при использовании в комбинированных гормональных противозачаточных средствах и в менопаузальной гормональной терапии (в сочетании с прогестагенами ) были связаны с увеличением риска венозного тромбоза в 2–6 раз. Риск зависит от типов используемых гормонов, дозы эстрогена и наличия других тромбофилических факторов риска. [27] различные механизмы, такие как дефицит белка S и ингибитора пути тканевого фактора . Считается, что за это ответственны [28]
Ожирение уже давно считается фактором риска венозного тромбоза. Согласно многочисленным исследованиям, это более чем удваивает риск, особенно в сочетании с применением пероральных контрацептивов или в период после операции . У лиц, страдающих ожирением, описаны различные нарушения коагуляции. Ингибитор активатора плазминогена-1 , ингибитор фибринолиза, присутствует в более высоких уровнях у людей с ожирением. У людей с ожирением также имеется большее количество циркулирующих микровезикул (фрагментов поврежденных клеток), несущих тканевой фактор. Агрегация тромбоцитов может быть увеличена, а также наблюдаются более высокие уровни белков свертывания крови, таких как фактор фон Виллебранда, фибриноген, фактор VII и фактор VIII . Ожирение также увеличивает риск рецидива после первоначального эпизода тромбоза. [29]
Неясно
[ редактировать ]Ряд состояний, связанных с венозным тромбозом, возможно, являются генетическими и, возможно, приобретенными. [15] К ним относятся: повышенные уровни фактора VIII, фактора IX , фактора XI , фибриногена и активируемый тромбином ингибитор фибринолиза и снижение уровня ингибитора пути тканевого фактора . Резистентность к активированному протеину С , не связанная с мутациями фактора V, вероятно, вызвана другими факторами и остается фактором риска тромбоза. [15]
Существует связь между уровнем гомоцистеина в крови и тромбозом. [15] хотя об этом не сообщалось последовательно во всех исследованиях. [5] Уровни гомоцистеина определяются мутациями в генах MTHFR и CBS , а также уровнями фолиевой кислоты , витамина B6 и витамина B12 , которые зависят от диеты. [13]
Механизм
[ редактировать ]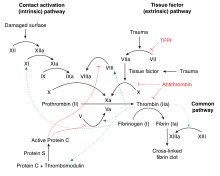
Тромбоз является многофакторной проблемой, поскольку часто существует множество причин, по которым у человека может развиться тромбоз. Эти факторы риска могут включать любое сочетание нарушений стенки кровеносных сосудов, нарушений кровотока (например, при иммобилизации) и нарушений консистенции крови. Тромбофилия вызвана нарушениями консистенции крови, которая определяется уровнями факторов свертывания крови и других циркулирующих белков крови, которые участвуют в «каскаде свертывания крови». [15]
Нормальная коагуляция инициируется высвобождением тканевого фактора из поврежденной ткани. Тканевой фактор связывается с циркулирующим фактором VIIa . Комбинация активирует фактор X в фактор Ха и фактор IX в фактор IXa. Фактор Ха (в присутствии фактора V ) активирует протромбин в тромбин. Тромбин является центральным ферментом в процессе коагуляции: он генерирует фибрин из фибриногена и активирует ряд других ферментов и кофакторов ( фактор XIII , фактор XI , фактор V и фактор VIII , TAFI), которые усиливают сгусток фибрина. [13] Процесс ингибируется TFPI (который инактивирует первую стадию, катализируемую фактором VIIa/тканевым фактором), антитромбином (который инактивирует тромбин, факторы IXa, Xa и XIa), белком C (который ингибирует факторы Va и VIIIa в присутствии белка S). ) и белок Z (который ингибирует фактор Ха). [13]
При тромбофилии нарушается баланс между «прокоагулянтной» и «антикоагулянтной» активностью. Тяжесть дисбаланса определяет вероятность развития тромбоза. Даже небольшие нарушения белков, такие как снижение уровня антитромбина всего до 70–80% от нормального уровня, могут увеличить риск тромбоза; это контрастирует с гемофилией , которая возникает только в том случае, если уровни факторов свертывания крови заметно снижаются. [13]
Помимо воздействия на тромбоз, состояния гиперкоагуляции могут ускорить развитие атеросклероза — заболевания артерий, которое лежит в основе инфаркта миокарда и других форм сердечно-сосудистых заболеваний. [30] [31]
Диагностика
[ редактировать ]
Тесты на тромбофилию включают общий анализ крови (с исследованием мазка крови ), протромбиновое время , частичное тромбопластиновое время , тест тромбодинамики , тромбиновое время и рептилазное время , волчаночный антикоагулянт , антитела к кардиолипину , антитела к гликопротеину 1 β2 , активированный протеин С. резистентность, тесты на фибриноген , фактор V Лейдена и мутация протромбина , а также базальный гомоцистеина . уровень [2] Тестирование может быть более или менее обширным в зависимости от клинического заключения и отклонений, обнаруженных при первоначальной оценке. [2]
В наследственных случаях у пациента должно быть как минимум два отклонения от нормы в тесте плюс семейный анамнез.
Скрининг
[ редактировать ]Существуют разные мнения относительно того, следует ли обследовать на предмет тромбофилии каждого пациента с неспровоцированным эпизодом тромбоза. Даже те, у кого есть форма тромбофилии, не обязательно подвергаются риску дальнейшего тромбоза, тогда как рецидив тромбоза более вероятен у тех, у кого ранее был тромбоз, даже у тех, у кого нет обнаруживаемых тромбофильных нарушений. [8] [12] [32] Рецидивирующая тромбоэмболия или тромбоз необычных участков (например, печеночной вены при синдроме Бадда-Киари ) является общепринятым показанием для скрининга. Это, скорее всего, будет экономически эффективным у людей с сильным личным или семейным анамнезом тромбозов. [33] Напротив, сочетание тромбофилии с другими факторами риска может служить показанием для профилактического лечения, поэтому тестирование на тромбофилию может проводиться даже у тех, кто не соответствует строгим критериям для этих тестов. [32] Поиск нарушений коагуляции обычно не проводится у пациентов, у которых тромбоз имеет очевидный триггер. Например, если тромбоз вызван иммобилизацией после недавней ортопедической операции , он считается «спровоцированным» иммобилизацией и операцией, и маловероятно, что исследования дадут клинически значимые результаты. [12] [32]
Когда венозная тромбоэмболия возникает, когда у пациента наблюдаются преходящие основные факторы риска, такие как длительная неподвижность, хирургическое вмешательство или травма, тестирование на тромбофилию нецелесообразно, поскольку результат теста не повлияет на назначенное пациенту лечение. [34] [35] В 2013 году Американское общество гематологов в рамках рекомендаций кампании «Выбирая мудро» предостерегло от чрезмерного использования скрининга на тромбофилию; ложноположительные результаты тестирования могут привести к тому, что людей ошибочно пометят как больных тромбофилией и начнут лечить антикоагулянтами без клинической необходимости. [34]
В Соединенном Королевстве профессиональные рекомендации содержат конкретные показания для тестирования на тромбофилию. Рекомендуется проводить тестирование только после соответствующего консультирования, поэтому исследования обычно проводятся не во время диагностики тромбоза, а в более позднее время. [12] В определенных ситуациях, таких как тромбоз вен сетчатки , тестирование вообще не рекомендуется, поскольку тромбофилия не считается основным фактором риска. При других редких состояниях, обычно связанных с гиперкоагуляцией, таких как тромбоз церебральных вен и тромбоз воротной вены, данных недостаточно, чтобы с уверенностью утверждать, полезен ли скрининг тромбофилии, и поэтому решения о скрининге тромбофилии при этих состояниях не считаются научно обоснованными . [12] Если в качестве ориентира принять экономическую эффективность ( количество лет жизни с поправкой на качество в обмен на затраты), то, как правило, неясно, оправдывают ли исследования тромбофилии зачастую высокие затраты. [36] если только тестирование не ограничивается избранными ситуациями. [37]
Привычный выкидыш является показанием для скрининга тромбофилии, особенно антифосфолипидных антител (антикардиолипин IgG и IgM, а также волчаночного антикоагулянта), фактора V Лейдена и мутации протромбина, активированной резистентности протеина С и общей оценки коагуляции с помощью исследования, известного как тромбоэластография. . [11]
Женщинам, которые планируют использовать пероральные контрацептивы, не рекомендуется проходить рутинный скрининг на тромбофилии, поскольку абсолютный риск тромботических событий низок. Если у женщины или родственника первой степени родства был тромбоз, риск развития тромбоза увеличивается. Скрининг этой выбранной группы может быть полезным, [28] но даже в случае отрицательного результата все равно может указывать на остаточный риск. [12] Поэтому профессиональные рекомендации предлагают использовать альтернативные формы контрацепции, а не полагаться на скрининг. [12]
Скрининг на тромбофилию у людей с артериальным тромбозом обычно считается бесполезным и не рекомендуется. [12] за исключением, возможно, необычно молодых пациентов (особенно в случае курения или использования эстрогенсодержащих гормональных контрацептивов ) и тех, у кого реваскуляризация, такая как аортокоронарное шунтирование , не удалась из-за быстрой окклюзии трансплантата. [9]
Уход
[ редактировать ]
Специфического лечения тромбофилии не существует, за исключением случаев, когда она вызвана каким-либо заболеванием (например, нефротическим синдромом), когда необходимо лечение основного заболевания. У пациентов с неспровоцированным и/или рецидивирующим тромбозом или у пациентов с формой тромбофилии высокого риска наиболее важным решением является использование антикоагулянтных препаратов, таких как варфарин , на долгосрочной основе, чтобы снизить риск дальнейших эпизодов. [3] Этот риск необходимо сопоставить с риском того, что лечение вызовет значительное кровотечение, поскольку зарегистрированный риск сильного кровотечения составляет более 3% в год, и в результате 11% пациентов с сильным кровотечением могут умереть. [3]
Помимо вышеупомянутых форм тромбофилии, риск рецидива после эпизода тромбоза определяется такими факторами, как степень и тяжесть исходного тромбоза, был ли он спровоцирован (например, иммобилизацией или беременностью), количеством предшествующих тромботических осложнений. события, мужской пол, наличие фильтра нижней полой вены , наличие рака, симптомы посттромботического синдрома и ожирение . [3] Эти факторы, как правило, имеют большее значение для принятия решения, чем наличие или отсутствие выявляемой тромбофилии. [12] [38]
Пациентам с антифосфолипидным синдромом можно предложить долгосрочную антикоагулянтную терапию после первого неспровоцированного эпизода тромбоза. Риск определяется подтипом обнаруженных антител, титром антител (количеством антител), наличием нескольких антител, а также тем, обнаруживается ли оно повторно или только в одном случае. [17]
Женщинам с тромбофилией, планирующим беременность или беременным, обычно требуются альтернативы варфарину во время беременности, особенно в первые 13 недель, когда он может вызвать отклонения от нормы у будущего ребенка. низкомолекулярный гепарин (НМГ, например эноксапарин ). В качестве альтернативы обычно используется [39] Варфарин и НМГ можно безопасно использовать при грудном вскармливании. [39]
Некоторые исследования показали, что низкомолекулярный гепарин снижает риск выкидыша, когда у женщин возникает привычное невынашивание беременности вследствие тромбофилии. При совместном анализе результатов всех исследований не удалось продемонстрировать статистически значимую пользу. [40]
Прогноз
[ редактировать ]У людей без выявляемой тромбофилии кумулятивный риск развития тромбоза к 60 годам составляет около 12%. Около 60% людей с дефицитом антитромбина хотя бы раз пережили тромбоз к 60 годам, равно как и около 50% людей с дефицитом протеина С и около трети людей с дефицитом протеина S. Люди с резистентностью к активированному протеину С (обычно вызванной фактором V Лейдена), напротив, имеют несколько повышенный абсолютный риск тромбоза: у 15% к шестидесяти годам произошло хотя бы одно тромботическое событие. [13] В целом мужчины чаще, чем женщины, испытывают повторные эпизоды венозного тромбоза. [5]
Люди с фактором V Лейдена имеют относительно низкий риск тромбоза, но тромбоз может развиться при наличии дополнительного фактора риска, такого как иммобилизация. У большинства людей с мутацией протромбина (G20210A) тромбоз никогда не развивается. [13]
Эпидемиология
[ редактировать ]Основные тромбофилии («тип 1») встречаются редко. Дефицит антитромбина присутствует у 0,2% населения в целом и у 0,5–7,5% людей с венозным тромбозом. Дефицит протеина С также присутствует у 0,2% населения и обнаруживается у 2,5–6% людей с тромбозом. Точная распространенность дефицита белка S в популяции неизвестна; его обнаруживают у 1,3–5% людей с тромбозами. [13]
Гораздо чаще встречаются малые тромбофилии («тип 2»). Фактор V Лейдена присутствует у 5% населения североевропейского происхождения, но гораздо реже у лиц азиатского или африканского происхождения. У людей с тромбозом 10% имеют фактор V Лейдена. Среди тех, кого направляют на тестирование на тромбофилию, этот дефект имеется у 30–50%. Мутация протромбина встречается у 1–4% населения в целом, у 5–10% людей с тромбозом и у 15% людей, направленных на тестирование на тромбофилию. Как и фактор V Лейдена, эта аномалия редко встречается у африканцев и азиатов. [13]
Точная распространенность антифосфолипидного синдрома неизвестна, поскольку в разных исследованиях используются разные определения этого состояния. Антифосфолипидные антитела выявляются у 24% обследованных на тромбофилию. [17]
История
[ редактировать ]
Немецкий врач Рудольф Вирхов в 1856 году отнес нарушения консистенции крови к фактору развития тромбоза. Точная природа этих нарушений оставалась неясной до тех пор, пока первая форма тромбофилии — дефицит антитромбина — не была признана в 1965 году норвежским гематологом Олавом. Эгеберг. [41] Дефицит протеина С последовал в 1981 году, когда его описали исследователи из Научно-исследовательского института Скриппса США и Центров контроля заболеваний . [42] Дефицит белка S , возникший в 1984 году, был описан исследователями из Университета Оклахомы . [4] [5] [43]
Антифосфолипидный синдром был полностью описан в 1980-х годах, после различных предыдущих сообщений о специфических антителах у людей с системной красной волчанкой и тромбозом. [17] [44] его часто называют синдромом Хьюза . Синдром часто приписывают британскому ревматологу Грэму Р.В. Хьюзу, и по этой причине [45]
Наиболее распространенные генетические тромбофилии были описаны в 1990-х годах. Многие исследования ранее показали, что у многих людей с тромбозом наблюдается резистентность активированного белка С. В 1994 году группа из Лейдена , Нидерланды, выявила наиболее распространенный основной дефект — мутацию фактора V, которая сделала его устойчивым к действию активированного белка С. Дефект получил название фактора V Лейдена , поскольку генетические аномалии обычно называют по месту, где они обнаружены. [46] Два года спустя та же группа описала распространенную мутацию в гене протромбина, которая вызвала повышение уровня протромбина и незначительное увеличение риска тромбоза. [4] [5] [47]
Предполагается, что другие генетические аномалии, лежащие в основе семейных тромбозов, будут обнаружены в будущем путем изучения всего генетического кода в поисках небольших изменений в генах . [4] [5]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г Митчелл Р.С., Кумар В., Аббас А.К., Фаусто Н. (2007). «Глава 4». Основная патология Роббинса (Восьмое изд.). Филадельфия: Сондерс. ISBN 978-1-4160-2973-1 .
- ^ Jump up to: а б с д и ж г час я дж к л Хейт Дж.А. (2007). «Тромбофилия: общие вопросы по лабораторной оценке и лечению» . Гематология Ам. Соц. Гематол. Образование. Программа . 2007 (1): 127–35. дои : 10.1182/asheducation-2007.1.127 . ПМИД 18024620 .
- ^ Jump up to: а б с д Кирл П.А., Розендал Ф.Р., Эйхингер С. (декабрь 2010 г.). «Оценка риска рецидивирующего венозного тромбоза». Ланцет . 376 (9757): 2032–9. дои : 10.1016/S0140-6736(10)60962-2 . ПМИД 21131039 . S2CID 31610364 .
- ^ Jump up to: а б с д Дальбек Б. (июль 2008 г.). «Достижения в понимании патогенетических механизмов тромбофилических нарушений» . Кровь . 112 (1): 19–27. дои : 10.1182/кровь-2008-01-077909 . ПМИД 18574041 .
- ^ Jump up to: а б с д и ж г Rosendaal FR, Reitsma PH (июль 2009 г.). «Генетика венозных тромбозов» . Дж. Тромб. Гемост . 7 (Приложение 1): 301–4. дои : 10.1111/j.1538-7836.2009.03394.x . ПМИД 19630821 .
- ^ Скарвелис Д., Уэллс П.С. (октябрь 2006 г.). «Диагностика и лечение тромбоза глубоких вен» . CMAJ . 175 (9): 1087–92. дои : 10.1503/cmaj.060366 . ПМК 1609160 . ПМИД 17060659 .
- ^ Аньелли Дж., Бекаттини С. (июль 2010 г.). «Острая легочная эмболия». Н. англ. Дж. Мед . 363 (3): 266–74. дои : 10.1056/NEJMra0907731 . ПМИД 20592294 .
- ^ Jump up to: а б Мидделдорп С., ван Хилкама Влиг А (август 2008 г.). «Помогает ли тестирование на тромбофилию в клиническом ведении пациентов?» . Бр. Дж. Гематол . 143 (3): 321–35. дои : 10.1111/j.1365-2141.2008.07339.x . ПМИД 18710381 .
- ^ Jump up to: а б де Мурлуз П., Болен Ф. (апрель 2007 г.). «Наследственная тромбофилия при артериальных заболеваниях: выборочный обзор». Семин. Гематол . 44 (2): 106–13. doi : 10.1053/j.seminhematol.2007.01.008 . ПМИД 17433903 .
- ^ Чиасакул Т., Де Хесус Э., Тонг Дж., Чен Ю., Кроутер М., Гарсия Д., Чай-Адисаксофа К., Мессе С.Р., Кукер А. (октябрь 2019 г.). «Наследственная тромбофилия и риск артериального ишемического инсульта: систематический обзор и метаанализ» . Журнал Американской кардиологической ассоциации . 8 (19): e012877. дои : 10.1161/JAHA.119.012877 . ISSN 2047-9980 . ПМК 6806047 . ПМИД 31549567 .
- ^ Jump up to: а б Рай Р., Риган Л. (август 2006 г.). «Привычный выкидыш». Ланцет . 368 (9535): 601–11. дои : 10.1016/S0140-6736(06)69204-0 . ПМИД 16905025 . S2CID 42968924 .
- ^ Jump up to: а б с д и ж г час я Бэглин Т., Грей Э., Гривс М. и др. (апрель 2010 г.). «Клинические рекомендации по тестированию на наследственную тромбофилию» . Бр. Дж. Гематол . 149 (2): 209–20. дои : 10.1111/j.1365-2141.2009.08022.x . ПМИД 20128794 .
- ^ Jump up to: а б с д и ж г час я дж к Кроутер М.А., Келтон Дж.Г. (2003). «Врожденные тромбофилические состояния, связанные с венозным тромбозом: качественный обзор и предлагаемая система классификации». Энн. Стажер. Мед . 138 (2): 128–34. дои : 10.7326/0003-4819-138-2-200301210-00014 . ПМИД 12529095 . S2CID 43161448 .
- ^ «Врожденные причины венозного тромбоза — система классификации» . Анналы внутренней медицины . 138 (2). Американский колледж врачей: I. 21 января 2003 г. doi : 10.7326/0003-4819-138-2-200301210-00005 . S2CID 53089216 .
- ^ Jump up to: а б с д и ж г час я дж Розендаль, Франция (2005). «Венозный тромбоз: роль генов, окружающей среды и поведения» . Гематология Ам. Соц. Гематол. Образование. Программа . 2005 (1): 1–12. дои : 10.1182/asheducation-2005.1.1 . ПМИД 16304352 .
- ^ Мехта Р., Шапиро А.Д. (ноябрь 2008 г.). «Дефицит плазминогена» . Гемофилия . 14 (6): 1261–8. дои : 10.1111/j.1365-2516.2008.01825.x . ПМИД 19141167 .
- ^ Jump up to: а б с д Руис-Ирасторза Г., Кроутер М., Бранч W, Хамашта М.А. (октябрь 2010 г.). «Антифосфолипидный синдром». Ланцет . 376 (9751): 1498–509. дои : 10.1016/S0140-6736(10)60709-X . hdl : 2318/1609788 . ПМИД 20822807 . S2CID 25554663 .
- ^ Jump up to: а б Килинг Д., Дэвидсон С., Уотсон Х. (май 2006 г.). «Лечение гепарин-индуцированной тромбоцитопении» . Бр. Дж. Гематол . 133 (3): 259–69. дои : 10.1111/j.1365-2141.2006.06018.x . ПМИД 16643427 .
- ^ Jump up to: а б Бродский РА (апрель 2008 г.). «Повествовательный обзор: пароксизмальная ночная гемоглобинурия: физиология гемолитической анемии, связанной с комплементом». Энн. Стажер. Мед . 148 (8): 587–95. CiteSeerX 10.1.1.668.4942 . дои : 10.7326/0003-4819-148-8-200804150-00003 . ПМИД 18413620 . S2CID 19715590 .
- ^ Пападакис Э., Хоффман Р., Бреннер Б. (ноябрь 2010 г.). «Тромбогеморрагические осложнения миелопролиферативных заболеваний». Кровавый преподобный . 24 (6): 227–32. дои : 10.1016/j.blre.2010.08.002 . ПМИД 20817333 .
- ^ Прандони П., Фаланга А., Пиччоли А. (июнь 2005 г.). «Рак и венозная тромбоэмболия». Ланцет Онкол . 6 (6): 401–10. дои : 10.1016/S1470-2045(05)70207-2 . ПМИД 15925818 .
- ^ Халл Р.П., Goldsmith DJ (май 2008 г.). «Нефротический синдром у взрослых» . БМЖ . 336 (7654): 1185–9. дои : 10.1136/bmj.39576.709711.80 . ПМК 2394708 . ПМИД 18497417 .
- ^ Кера Р., Шанахан Ф (октябрь 2004 г.). «Тромбоэмболия - важное проявление воспалительного заболевания кишечника». Являюсь. Дж. Гастроэнтерол . 99 (10): 1971–3. дои : 10.1111/j.1572-0241.2004.40923.x . ПМИД 15447758 . S2CID 11391129 .
- ^ Абдул Султан А, Вест Дж, Стефанссон О, Грейндж М.Дж., Тата Л.Дж., Флеминг К.М., Хьюмс Д., Людвигссон Дж.Ф. (ноябрь 2015 г.). «Определение венозной тромбоэмболии и измерение ее заболеваемости с использованием шведских реестров здравоохранения: общенациональное когортное исследование беременных» . БМЖ Опен . 5 (11): e008864. doi : 10.1136/bmjopen-2015-008864 . ПМЦ 4654387 . ПМИД 26560059 .
- ^ Буржейли Дж., Пайдас М., Халил Х., Розен-Монтелла К., Роджер М. (февраль 2010 г.). «Легочная эмболия при беременности». Ланцет . 375 (9713): 500–12. дои : 10.1016/S0140-6736(09)60996-X . ПМИД 19889451 . S2CID 8633455 .
- ^ Догети ММ, Самуэльсон Банноу БТ (2019). «Гемостаз и тромбозы при беременности». Гемостаз и тромбоз . стр. 197–206. дои : 10.1007/978-3-030-19330-0_30 . ISBN 978-3-030-19329-4 . S2CID 201995636 .
- ^ Депутат Гомеса, Дейчер С.Р. (октябрь 2004 г.). «Риск венозной тромбоэмболии, связанный с гормональными контрацептивами и заместительной гормональной терапией: клинический обзор». Арх. Стажер. Мед . 164 (18): 1965–76. дои : 10.1001/archinte.164.18.1965 . ПМИД 15477430 .
- ^ Jump up to: а б Чайковский С.Н., Розинг Дж. (июль 2010 г.). «Механизмы эстроген-индуцированной венозной тромбоэмболии». Тромб. Рез . 126 (1): 5–11. doi : 10.1016/j.thromres.2010.01.045 . ПМИД 20163835 .
- ^ Штейн П.Д., Голдман Дж. (сентябрь 2009 г.). «Ожирение и тромбоэмболические заболевания». Клин. Грудь Мед . 30 (3): 489–93, viii. дои : 10.1016/j.ccm.2009.05.006 . ПМИД 19700047 .
- ^ Борисофф Дж.И., Спронк Х.М., Хинеман С., тен Кейт Х (2009). «Является ли тромбин ключевым игроком в лабиринте «коагуляции-атерогенеза»?» . Кардиоваск. Рез . 82 (3): 392–403. дои : 10.1093/cvr/cvp066 . ПМИД 19228706 .
- ^ Борисов Дж.И., Спронк Х.М., Тен Кейт Х. (2011). «Система гемостаза как модулятор атеросклероза». Н. англ. Дж. Мед . 364 (18): 1746–1760. дои : 10.1056/NEJMra1011670 . ПМИД 21542745 .
- ^ Jump up to: а б с Дален Дж. Э. (июнь 2008 г.). «Должны ли пациенты с венозной тромбоэмболией проходить обследование на тромбофилию?» . Являюсь. Дж. Мед . 121 (6): 458–63. doi : 10.1016/j.amjmed.2007.10.042 . ПМИД 18501222 .
- ^ Ву О, Робертсон Л., Тваддл С. и др. (октябрь 2005 г.). «Скрининг тромбофилии в ситуациях высокого риска: метаанализ и анализ экономической эффективности» . Бр. Дж. Гематол . 131 (1): 80–90. дои : 10.1111/j.1365-2141.2005.05715.x . ПМИД 16173967 .
- ^ Jump up to: а б Американское общество гематологов (сентябрь 2013 г.), «Пять вопросов, которые должны задавать врачи и пациенты» , «Выбирая мудро »: инициатива Фонда ABIM , Американское общество гематологии , получено 10 декабря 2013 г. , в котором цитируется
- Чонг Л.И., Фену Э., Стэнсби Г., Ходжкинсон С., Разработка рекомендаций G (2012). «Лечение венозных тромбоэмболических заболеваний и роль тестирования на тромбофилию: Краткое изложение рекомендаций NICE». БМЖ . 344 : е3979. дои : 10.1136/bmj.e3979 . ПМИД 22740565 . S2CID 42342532 .
- Бэглин Т., Грей Э., Гривс М., Хант Б.Дж., Килинг Д., Мачин С., Макки И., Макрис М., Нокс Т., Перри Д., Тейт Р.К., Уокер И., Уотсон Х., Британский комитет по стандартам в гематологии (2010). «Клинические рекомендации по тестированию на наследственную тромбофилию» . Британский журнал гематологии . 149 (2): 209–220. дои : 10.1111/j.1365-2141.2009.08022.x . ПМИД 20128794 .
- ^ Хикс Л.К., Беринг Х., Карсон К.Р. и др. (2013). «Кампания ASH Choose Wisely(R): пять гематологических тестов и методов лечения, вызывающих сомнения» . Кровь . 122 (24): 3879–83. дои : 10.1182/blood-2013-07-518423 . ПМИД 24307720 .
- ^ Симпсон Э.Л., Стивенсон MD, Родин А., Папайоанну Д. (январь 2009 г.). «Тестирование тромбофилии у людей с венозной тромбоэмболией: систематический обзор и анализ экономической эффективности» . Технол здоровья. Оценивать . 13 (2): iii, ix – x, 1–91. дои : 10.3310/hta13020 . ПМИД 19080721 .
- ^ Ву О, Грир И.А. (сентябрь 2007 г.). «Является ли скрининг на тромбофилию экономически эффективным?». Курс. Мнение. Гематол . 14 (5): 500–3. дои : 10.1097/MOH.0b013e32825f5318 . ПМИД 17934357 . S2CID 22896788 .
- ^ Кирон С., Кан С.Р., Аньелли Г., Гольдхабер С., Раскоб Г.Е., Комерота А.Дж. (июнь 2008 г.). «Антитромботическая терапия венозных тромбоэмболических заболеваний: Доказательные клинические рекомендации Американского колледжа врачей-торудистов (8-е издание)» . Грудь . 133 (6 доп.): 454S–545S. дои : 10.1378/сундук.08-0658 . ПМИД 18574272 . Архивировано из оригинала 12 января 2013 г.
- ^ Jump up to: а б Бейтс С.М., Грир И.А., Пабингер И., Софаер С., Хирш Дж. (июнь 2008 г.). «Венозная тромбоэмболия, тромбофилия, антитромботическая терапия и беременность: Доказательные клинические рекомендации Американского колледжа врачей-торудистов (8-е издание)» . Грудь . 133 (6 Доп.): 844S–886S. дои : 10.1378/сундук.08-0761 . ПМИД 18574280 . Архивировано из оригинала 12 января 2013 г.
- ^ Скейт Л., Кэрриер М., Каая Р., Мартинелли И., Петрофф Д., Шлейснер Э., Ласкин К.А., Роджер М.А. (2016). «Метаанализ низкомолекулярного гепарина для предотвращения потери беременности у женщин с наследственной тромбофилией» . Кровь . 127 (13): 1650–55. дои : 10.1182/blood-2015-12-626739 . ПМИД 26837697 .
- ^ Эгеберг О. (июнь 1965 г.). «Наследственный дефицит антитромбина, вызывающий тромбофилию». Тромб. Диат. Геморр . 13 (2): 516–30. дои : 10.1055/s-0038-1656297 . ПМИД 14347873 . S2CID 42594050 .
- ^ Гриффин Дж. Х., Эватт Б., Циммерман Т. С., Клейсс А. Дж., Уайдман С. (ноябрь 1981 г.). «Дефицит протеина С при врожденной тромботической болезни» . Дж. Клин. Инвестируйте . 68 (5): 1370–3. дои : 10.1172/JCI110385 . ПМК 370934 . ПМИД 6895379 .
- ^ Компьютерный компьютер, Esmon CT (декабрь 1984 г.). «Рецидивирующая венозная тромбоэмболия у больных с частичным дефицитом белка S». Н. англ. Дж. Мед . 311 (24): 1525–8. дои : 10.1056/NEJM198412133112401 . ПМИД 6239102 .
- ^ Хьюз Г.Р. (октябрь 1983 г.). «Тромбоз, аборт, церебральные заболевания и волчаночный антикоагулянт» . Бр. Мед. Дж. (Клин. Рес. Ред.) . 287 (6399): 1088–89. дои : 10.1136/bmj.287.6399.1088 . ПМЦ 1549319 . ПМИД 6414579 .
- ^ Санна Дж., Д'Круз Д., Куадрадо М.Дж. (август 2006 г.). «Церебральные проявления при антифосфолипидном (Хьюзе) синдроме». Реум. Дис. Клин. Северный Ам . 32 (3): 465–90. дои : 10.1016/j.rdc.2006.05.010 . ПМИД 16880079 .
- ^ Бертина Р.М., Кулеман Б.П., Костер Т. и др. (май 1994 г.). «Мутация фактора свертывания крови V, связанная с устойчивостью к активированному белку С». Природа . 369 (6475): 64–7. Бибкод : 1994Natur.369...64B . дои : 10.1038/369064a0 . ПМИД 8164741 . S2CID 4314040 .
- ^ Поорт С.Р., Розендал Ф.Р., Рейтсма П.Х., Бертина Р.М. (ноябрь 1996 г.). «Общая генетическая вариация в 3'-нетранслируемой области гена протромбина связана с повышенным уровнем протромбина в плазме и увеличением венозного тромбоза» (PDF) . Кровь . 88 (10): 3698–703. doi : 10.1182/blood.V88.10.3698.bloodjournal88103698 . ПМИД 8916933 .
Внешние ссылки
[ редактировать ]- «Тромбофилия» . Пациент Великобритания .