Валентный электрон
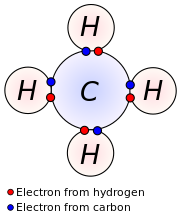
В химии и физике , валентные электроны — это электроны во внешней оболочке атома , которые могут участвовать в образовании химической связи если внешняя оболочка не закрыта. В одинарной ковалентной связи образуется общая пара, в которой оба атома в связи вносят вклад в один валентный электрон.
Наличие валентных электронов может определять свойства элемента валентность химические , например, его — может ли он связываться с другими элементами, и если да, то насколько легко и с каким количеством. данного элемента Таким образом, реакционная способность сильно зависит от его электронной конфигурации . Для элемента основной группы валентный электрон может существовать только во внешней электронной оболочке ; для переходного металла валентный электрон также может находиться во внутренней оболочке.
Атом с замкнутой оболочкой валентных электронов (соответствующей конфигурации благородного газа ) имеет тенденцию быть химически инертным . Атомы с одним или двумя валентными электронами больше, чем закрытая оболочка, обладают высокой реакционной способностью из-за относительно низкой энергии , необходимой для удаления дополнительных валентных электронов с образованием положительного иона . Атом, у которого на один или два электрона меньше, чем в замкнутой оболочке, является реакционноспособным из-за его тенденции либо получить недостающие валентные электроны и образовать отрицательный ион, либо разделить валентные электроны и образовать ковалентную связь.
Подобно остовному электрону , валентный электрон обладает способностью поглощать или выделять энергию в форме фотона . Прирост энергии может заставить электрон переместиться (прыгнуть) на внешнюю оболочку; это известно как атомное возбуждение . Или электрон может даже вырваться из оболочки связанного с ним атома; это ионизация с образованием положительного иона. Когда электрон теряет энергию (тем самым вызывая испускание фотона), он может переместиться на внутреннюю оболочку, которая не полностью занята.
Обзор [ править ]
Электронная конфигурация [ править ]
Электроны, которые определяют валентность – то, как атом реагирует химически – имеют самую высокую энергию .
Для элемента основной группы валентные электроны определяются как электроны, находящиеся в электронной оболочке с наибольшим главным квантовым числом n . [1] Таким образом, количество валентных электронов, которые он может иметь, зависит от электронной конфигурации простым образом . Например, электронная конфигурация фосфора (P) равна 1s. 2 2 с 2 2р 6 3 с 2 3р 3 так что имеется 5 валентных электронов (3s 2 3р 3 ), соответствующий максимальной валентности для P 5 , как в молекуле PF 5 ; эта конфигурация обычно сокращается до [Ne] 3s. 2 3р 3 , где [Ne] означает основные электроны, конфигурация которых идентична конфигурации благородного газа неона .
Однако переходные элементы имеют ( n −1)d энергетические уровни, очень близкие по энергии к уровню n s . [2] Таким образом, в отличие от элементов основной группы, валентный электрон переходного металла определяется как электрон, который находится вне ядра благородного газа. [3] Таким образом, обычно d-электроны в переходных металлах ведут себя как валентные электроны, хотя они и не находятся на внешней оболочке. Например, марганец (Mn) имеет конфигурацию 1с. 2 2 с 2 2р 6 3 с 2 3р 6 4 с 2 3d 5 ; это сокращенно [Ar] 4s 2 3d 5 , где [Ar] обозначает конфигурацию ядра, идентичную конфигурации благородного газа аргона . В этом атоме 3d-электрон имеет энергию, подобную энергии 4s-электрона, и значительно выше, чем у 3s- или 3p-электрона. Фактически возможно семь валентных электронов (4s 2 3d 5 ) вне аргоноподобного ядра; это согласуется с химическим фактом, что марганец может иметь степень окисления до +7 (в перманганат- ионе: MnO −
4 ). (Но обратите внимание, что просто наличие такого количества валентных электронов не означает, что соответствующая степень окисления будет существовать. Например, фтор не известен в степени окисления +7; и хотя максимальное известное количество валентных электронов составляет 16 в иттербии и нобелии ни для одного элемента не известна степень окисления выше +9.)
Чем правее в каждом ряду переходных металлов, тем ниже энергия электрона в подоболочке и тем меньше у такого электрона валентных свойств. Таким образом, хотя атом никеля в принципе имеет десять валентных электронов (4s 2 3d 8 ), его степень окисления никогда не превышает четырех. Для цинка подоболочка 3d является полной во всех известных соединениях, хотя в некоторых соединениях она вносит вклад в валентную зону. [4] Аналогичная закономерность сохраняется и для энергетических уровней ( n −2)f внутренних переходных металлов.
Подсчет d-электронов — альтернативный инструмент для понимания химии переходного металла.
Количество валентных электронов [ править ]
Количество валентных электронов элемента можно определить по группе таблицы Менделеева (вертикальный столбец), к которой относится элемент. В группах 1–12 номер группы соответствует числу валентных электронов; в группах 13–18 цифра единиц номера группы соответствует числу валентных электронов. (Гелий является единственным исключением.) [5]
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | ЧАС 1 | Он 2 | ||||||||||||||||||||||||||||||
| 2 | Что 1 | Быть 2 | Б 3 | С 4 | Н 5 | ТО 6 | Ф 7 | Ne 8 | ||||||||||||||||||||||||
| 3 | Уже 1 | мг 2 | Ал 3 | И 4 | П 5 | С 6 | кл. 7 | С 8 | ||||||||||||||||||||||||
| 4 | К 1 | Что 2 | наук 3 | Из 4 | V 5 | Кр 6 | Мин. 7 | Фе 8 | Ко 9 | В 10 | С 11 | Зн 12 | Здесь 3 | Ге 4 | Как 5 | Се 6 | Бр 7 | НОК 8 | ||||||||||||||
| 5 | руб. 1 | старший 2 | И 3 | Зр 4 | Нб 5 | Мо 6 | Тс 7 | Ру 8 | резус 9 | ПД 10 | В 11 | компакт-диск 12 | В 3 | Сн 4 | Сб 5 | Te 6 | я 7 | Машина 8 | ||||||||||||||
| 6 | Cs 1 | Нет 2 | La 3 | Этот 4 | Пр 5 | Нд 6 | вечера 7 | см 8 | Евросоюз 9 | Б-г 10 | Тб 11 | Те 12 | К 13 | Является 14 | Тм 15 | Ыб 16 | Лу 3 | хф 4 | Облицовка 5 | В 6 | Ре 7 | Ты 8 | И 9 | Пт 10 | В 11 | ртуть 12 | Тл 3 | Pb 4 | С 5 | Po 6 | В 7 | Рн 8 |
| 7 | Пт 1 | Солнце 2 | И 3 | че 4 | Хорошо 5 | В 6 | Например 7 | Мог 8 | Являюсь 9 | См 10 | Бк 11 | См. 12 | Является 13 | Фм 14 | Мэриленд 15 | Нет 16 | лр 3 | РФ 4 | ДБ 5 | Сг 6 | Бх 7 | Хс 8 | гора 9 | Дс 10 | Рг 11 | Сп 12 | Нх 3 | В 4 | Мак 5 | Лев 6 | Ц 7 | И 8 |
Гелий является исключением: несмотря на наличие 1с. 2 имеет некоторое сходство с щелочноземельными металлами с их ns конфигурация с двумя валентными электронами и, таким образом , 2 В валентных конфигурациях его оболочка полностью заполнена и, следовательно, химически очень инертна и обычно помещается в группу 18 вместе с другими благородными газами.
Валентная оболочка [ править ]
Валентная оболочка — это совокупность орбиталей , энергетически доступных для принятия электронов для образования химических связей .
Для элементов основной группы валентная оболочка состоит из ns- и np -орбиталей на внешней электронной оболочке . Для переходных металлов орбитали неполной ( n включены -1)d подоболочки, а для лантаноидов и актиноидов неполные ( n -2)f и ( n -1)d подоболочки. Используемые орбитали могут находиться во внутренней электронной оболочке и не все соответствуют одной и той же электронной оболочке или главному квантовому числу n в данном элементе, но все они имеют одинаковые энергии. [5]
| Тип элемента | Водород и гелий | s- и p-блоки ( элементы основной группы ) | d-блок ( Переходные металлы ) | f-блок ( Лантаноиды и актиниды ) |
|---|---|---|---|---|
| Валентные орбитали [6] |
|
|
|
|
| счета электронов Правила | Правило дуэта/дуплета | Правило октета | правило 18 электронов | Правило 32 электронов |
Как правило, элемент основной группы (за исключением водорода или гелия) имеет тенденцию реагировать с образованием 2 п 6 электронная конфигурация . Эта тенденция называется правилом октета , поскольку каждый связанный атом имеет 8 валентных электронов, включая общие электроны. Точно так же переходный металл имеет тенденцию реагировать с образованием 10 с 2 п 6 электронная конфигурация. Эта тенденция называется правилом 18 электронов , поскольку каждый связанный атом имеет 18 валентных электронов, включая общие электроны.
Тяжелые элементы 2-й группы кальций, стронций и барий ( n -1)d, что придает им некоторое сходство с переходными металлами. также могут использовать подоболочку [7] [8] [9]
Химические реакции [ править ]
Количество валентных электронов в атоме определяет его связывающее поведение. Поэтому элементы, атомы которых имеют одинаковое количество валентных электронов, часто группируются в периодической таблице элементов, особенно если они также имеют одинаковые типы валентных орбиталей. [10]
Наиболее реакционноспособным металлическим элементом является щелочной металл 1-й группы (например, натрий или калий ); это потому, что такой атом имеет только один валентный электрон. При образовании ионной связи , обеспечивающей необходимую энергию ионизации , этот один валентный электрон легко теряется с образованием положительного иона (катиона) с замкнутой оболочкой (например, Na + или К + ). Щелочноземельный металл 2-й группы (например, магний ) несколько менее реакционноспособен, поскольку каждый атом должен потерять два валентных электрона, чтобы образовать положительный ион с замкнутой оболочкой (например, Mg 2+ ). [ нужна ссылка ]
Внутри каждой группы (каждого столбца таблицы Менделеева) металлов реакционная способность увеличивается с каждой нижней строкой таблицы (от легкого элемента к более тяжелому), поскольку более тяжелый элемент имеет больше электронных оболочек, чем более легкий; валентные электроны более тяжелого элемента существуют с более высокими главными квантовыми числами (они находятся дальше от ядра атома и, следовательно, имеют более высокие потенциальные энергии, что означает, что они менее прочно связаны). [ нужна ссылка ]
Атом неметалла имеет тенденцию притягивать дополнительные валентные электроны, чтобы достичь полной валентной оболочки; Этого можно достичь одним из двух способов: атом может либо делиться электронами с соседним атомом ( ковалентная связь ), либо отбирать электроны у другого атома ( ионная связь ). Наиболее реакционноспособным видом неметаллического элемента является галоген (например, фтор (F) или хлор (Cl)). Такой атом имеет следующую электронную конфигурацию: s 2 п 5 ; для образования замкнутой оболочки требуется только один дополнительный валентный электрон. Чтобы образовать ионную связь, атом галогена может отобрать электрон у другого атома, чтобы образовать анион (например, F − , кл − , и т. д.). Для образования ковалентной связи один электрон галогена и один электрон другого атома образуют общую пару (например, в молекуле H–F линия представляет собой общую пару валентных электронов, одного от H и одного от F). [ нужна ссылка ]
Внутри каждой группы неметаллов реакционная способность уменьшается с каждой нижней строкой таблицы (от легкого элемента к тяжелому элементу) периодической таблицы, поскольку валентные электроны имеют все более высокие энергии и, следовательно, все менее прочно связаны. Фактически кислород (самый легкий элемент в группе 16) является наиболее реакционноспособным неметаллом после фтора, хотя он и не является галогеном, поскольку валентные оболочки более тяжелых галогенов имеют более высокие главные квантовые числа.
В этих простых случаях, когда соблюдается правило октета, валентность атома равна числу электронов, полученных, потерянных или разделенных для формирования стабильного октета. Однако есть также много молекул, которые являются исключениями и для которых валентность определена менее четко.
Электропроводность [ править ]
Валентные электроны также отвечают за связь в чистых химических элементах и за то, их электропроводность характерна ли для металлов, полупроводников или изоляторов.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Группа → | ||||||||||||||||||||||||||||||||
| ↓ Период | ||||||||||||||||||||||||||||||||
| 1 | ЧАС | Он | ||||||||||||||||||||||||||||||
| 2 | Что | Быть | Б | С | Н | ТО | Ф | Ne | ||||||||||||||||||||||||
| 3 | Уже | мг | Ал | И | П | С | кл. | С | ||||||||||||||||||||||||
| 4 | К | Что | наук | Из | V | Кр | Мин. | Фе | Ко | В | С | Зн | Здесь | Ге | Как | Се | Бр | НОК | ||||||||||||||
| 5 | руб. | старший | И | Зр | Нб | Мо | Тс | Ру | резус | ПД | В | компакт-диск | В | Сн | Сб | Te | я | Машина | ||||||||||||||
| 6 | Cs | Нет | La | Этот | Пр | Нд | вечера | см | Евросоюз | Б-г | Тб | Те | К | Является | Тм | Ыб | Лу | хф | Облицовка | В | Ре | Ты | И | Пт | В | ртуть | Тл | Pb | С | Po | В | Рн |
| 7 | Пт | Солнце | И | че | Хорошо | В | Например | Мог | Являюсь | См | Бк | См. | Является | Фм | Мэриленд | Нет | лр | РФ | ДБ | Сг | Бх | Хс | гора | Дс | Рг | Сп | Нх | В | Мак | Лев | Ц | И |
Ковалентная металлическая сеть Молекулярная ковалентная связь Одиночные атомы Неизвестно Цвет фона показывает связь простых веществ в периодической таблице . Если их несколько, считается наиболее стабильный аллотроп.
Металлические элементы обычно обладают высокой электропроводностью в твердом состоянии. В каждой строке таблицы Менделеева металлы располагаются слева от неметаллов, поэтому металл имеет меньше возможных валентных электронов, чем неметалл. Однако валентный электрон атома металла имеет небольшую энергию ионизации , и в твердом состоянии этот валентный электрон относительно свободно покидает один атом, чтобы соединиться с другим, находящимся поблизости. Такая ситуация характеризует металлическую связь . Такой «свободный» электрон может перемещаться под действием электрического поля , и его движение представляет собой электрический ток ; он отвечает за электропроводность металла. Медь , алюминий , серебро и золото являются примерами хороших проводников.
Неметаллический элемент имеет низкую электропроводность; он действует как изолятор . Такой элемент находится в правой части таблицы Менделеева и имеет валентную оболочку, заполненную как минимум наполовину (исключение составляет бор ). Его энергия ионизации велика; электрон не может легко покинуть атом при приложении электрического поля, и поэтому такой элемент может проводить только очень малые электрические токи. Примерами твердых элементарных изоляторов являются алмаз ( аллотроп углерода ) и сера . Они образуют ковалентно связанные структуры либо с ковалентными связями, простирающимися по всей структуре (как в алмазе), либо с отдельными ковалентными молекулами, слабо притягивающимися друг к другу межмолекулярными силами (как в сере). ( Благородные газы остаются в виде отдельных атомов, но они также испытывают межмолекулярные силы притяжения, которые становятся сильнее по мере спуска группы: гелий кипит при -269 ° C, а радон кипит при -61,7 ° C.)
Твердые соединения, содержащие металлы, также могут быть изоляторами, если валентные электроны атомов металлов используются для образования ионных связей . Например, хотя элементарный натрий является металлом, твердый хлорид натрия является изолятором, поскольку валентный электрон натрия передается хлору с образованием ионной связи, и, следовательно, этот электрон не может быть легко перемещен.
Полупроводник ; имеет промежуточную электропроводность между металлом и неметаллом Полупроводник также отличается от металла тем, что проводимость полупроводника увеличивается с температурой . Типичными элементарными полупроводниками являются кремний и германий , каждый атом которых имеет четыре валентных электрона. Свойства полупроводников лучше всего объясняются с помощью зонной теории вследствие небольшой энергетической щели между валентной зоной (которая содержит валентные электроны при абсолютном нуле) и зоной проводимости (в которую валентные электроны возбуждаются за счет тепловой энергии).
Ссылки [ править ]
- ^ Петруччи, Ральф Х.; Харвуд, Уильям С.; Херринг, Ф. Джеффри (2002). Общая химия: принципы и современные приложения (8-е изд.). Река Аппер-Седл, Нью-Джерси: Прентис-Холл. п. 339 . ISBN 978-0-13-014329-7 . LCCN 2001032331 . OCLC 46872308 .
- ^ Порядок заполнения 3d и 4s орбиталей . chemguide.co.uk
- ^ Мисслер Г.Л. и Тарр, Д.А., Неорганическая химия (2-е изд. Прентис-Холл, 1999). стр.48.
- ^ Тосселл, Дж. А. (1 ноября 1977 г.). «Теоретические исследования энергий связи валентных орбиталей в твердом сульфиде цинка, оксиде цинка и фториде цинка». Неорганическая химия . 16 (11): 2944–2949. дои : 10.1021/ic50177a056 .
- ↑ Перейти обратно: Перейти обратно: а б Киллер, Джеймс; Уотерс, Питер (2014). Химическая структура и реакционная способность (2-е изд.). Издательство Оксфордского университета. стр. 257–260. ISBN 978-0-19-9604135 .
- ^ Чи, Чаосянь; Пан, Судип; Джин, Джиай; Мэн, Луян; Ло, Минбяо; Чжао, Лили; Чжоу, Минфэй; Френкинг, Гернот (2019). «Октакарбонильные ионные комплексы актинидов [An(CO)8]+/- (An=Th, U) и роль f-орбиталей в связи металл-лиганд» . хим. Евро. Дж. 25 (50): 11772–11784. дои : 10.1002/chem.201902625 . ПМК 6772027 . ПМИД 31276242 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 117. ИСБН 978-0-08-037941-8 .
- ^ Чжоу, Минфэй; Френкинг, Гернот (2021). «Химия переходных металлов более тяжелых щелочноземельных атомов Ca, Sr и Ba». Отчеты о химических исследованиях . 54 (15): 3071–3082. doi : 10.1021/acs.accounts.1c00277 . ПМИД 34264062 . S2CID 235908113 .
- ^ Фернандес, Израиль; Хольцманн, Николь; Френкинг, Гернот (2020). «Валентные орбитали щелочноземельных атомов» . Химия: Европейский журнал . 26 (62): 14194–14210. дои : 10.1002/chem.202002986 . ПМК 7702052 . ПМИД 32666598 .
- ^ Дженсен, Уильям Б. (2000). «Периодический закон и таблица» (PDF) . Архивировано из оригинала (PDF) 10 ноября 2020 г. Проверено 10 декабря 2022 г.
Внешние ссылки [ править ]
- Фрэнсис, Иден. Валентные электроны .