T Helper Cell

Клетки Т -хелпер ( Т -клетки ) , также известные как CD4 + Клетки или CD4-позитивные клетки являются типом Т-клеток , которые играют важную роль в адаптивной иммунной системе . Они помогают активности других иммунных клеток, высвобождая цитокины . Они считаются необходимыми при к клеткам переключении класса антител , разрыву перекрестной толерантности в дендритных клетках, в активации и росте цитотоксических Т-клеток и при максимизации бактерицидной активности фагоцитов, таких как макрофаги и нейтрофилы . CD4 + Клетки представляют собой зрелые ТН -клетки, которые экспрессируют поверхностный белок CD4. Генетические различия в регуляторных элементах, экспрессируемых CD4 + Клетки определяют восприимчивость к широкому классу аутоиммунных заболеваний . [ 1 ]
Структура и функция
[ редактировать ]Клетки T H содержат и высвобождают цитокины, чтобы помочь другим иммунным клеткам. Цитокины являются небольшими белковыми медиаторами, которые изменяют поведение клеток -мишеней, которые экспрессируют рецепторы для этих цитокинов. Эти клетки помогают поляризовать иммунный ответ в зависимости от природы иммунологического оскорбления (например; вирус против внеклеточной бактерии против внутриклеточной бактерии по сравнению с Гельминтом против гриба против Протеста). [ Цитация необходима ]
Зрелые ТН -клетки экспрессируют поверхностный белок CD4 и называются CD4 + Т -клетки . CD4 + Т-клетки, как правило, рассматриваются как имеющие предварительно определенную роль в качестве вспомогательных Т-клеток в иммунной системе . Например, когда антиген-презентативная клетка демонстрирует пептидный антиген на белках класса II MHC , CD4 + Клетка поможет этим клеткам через комбинацию клеточных взаимодействий (например, CD40 (белок) и CD40L ) и через цитокины .
Клетки Т Н не являются монолитным иммунологическим сущностью, потому что они разнообразны с точки зрения функции и их взаимодействия с клетками партнеров. В целом, зрелые наивные Т -клетки стимулируются профессиональным антигеном, представляющими клетки для получения эффекторного модуля. Они определяются наличием фактора транскрипции, определяющего линии (или определяющего линии) (также называемого основным регулятором , хотя этот термин подвергся критике за то, что он был слишком восстановительным). [ 2 ] Потеря функции в линии, с указанием фактора транскрипции, приводит к отсутствию соответствующего класса Helper T -клетки, что может быть разрушительным для здоровья хозяина.
Активация наивных вспомогательных Т -клеток
[ редактировать ]
После развития в тимусе эти клетки (называемые недавними эмигрантами тимуса (RTE)) по сравнению с тимусом и дома ко вторичным лимфоидным органам (SLO; селезенка и лимфатические узлы ). Следует отметить, что лишь очень небольшое меньшинство по выходам Т -клеток из тимуса (оценки обычно варьируются от 1 до 5%, но некоторые эксперты считают даже это щедро). [ 3 ] Созревание RTE в SLO приводит к генерации зрелых наивных Т -клеток (наивное значение, что они никогда не подвергались воздействию антигена , на который они запрограммированы на реагирование), но на наивных Т -клетках сейчас отсутствуют или понижали (пониженную) экспрессию RTE -рецепт, такие как CD31 , PTK7 , комплемент рецептор 1 и 2 ( CR1 , CR2 ) и производство интерлейкина 8 (IL-8) . [ 4 ] [ 5 ] Как и все Т -клетки, они экспрессируют комплекс рецептора Т -клеток - CD3 . Рецептор Т -клеток (TCR) состоит из постоянных и переменных областей. Пратовая область определяет, на какой антиген может реагировать антиген Т -клетка. CD4 + Т -клетки имеют TCR с аффинностью к MHC класса II , а CD4 участвует в определении аффинности MHC во время созревания в тимусе . Белки MHC класса II, как правило, обнаруживаются только на поверхности профессиональных антиген-презентативных клеток (APC). Профессиональные антиген-презентативные клетки представляют собой в первую очередь дендритные клетки , макрофаги и В-клетки , хотя дендритные клетки являются единственной клеточной группой, которая экспрессирует конститутивно MHC класса II (в любое время). Некоторые APC также связывают нативные (или необработанные) антигены с их поверхностью, такие как фолликулярные дендритные клетки (это не те же типы клеток, что и дендритные клетки иммунной системы, а не гематопоэтическое происхождение, и в целом отсутствует MHC. Класс II, что означает, что они не являются настоящими профессиональными антиген-презривающими клетками; [ 6 ] ) Т -клетки требуют, чтобы антигены обрабатывались в короткие фрагменты, которые образуют линейные эпитопы на классе II MHC (в случае вспомогательных Т -клеток, поскольку они экспрессируют CD4) или MHC класса I (в случае цитотоксических Т -клеток , которые экспрессируют CD8 ). Связывающие карманы MHC класса II являются гибкими по отношению к длине пептидов, которые они удерживают. Как правило, существует 9 основных аминокислотных остатков с несколькими фланкирующими аминокислотами, которые образуют длину около 12–16 аминокислот. [ 7 ] но, как известно, содержит до 25 аминокислот. [ 8 ] Для сравнения, белки MHC класса I обычно имеют длину 9-10 пептидов. [ 9 ] Активация наивных Т-клеток обычно объясняется с точки зрения модели 3-сигнала, разработанной ниже. [ 10 ]
Активация (сигнал 1)
[ редактировать ]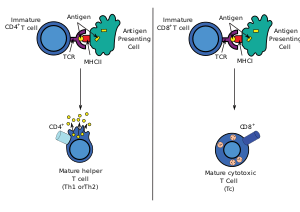
Во время иммунного ответа антигены профессиональных антиген-презентативных клеток (APC) эндоцитозные (обычно бактерии или вирусы), которые подвергаются обработке , затем перемещаются от места инфекции в лимфатические узлы . Как правило, ответственным APC является дендритная ячейка. Если антиген экспрессирует соответствующие молекулярные паттерны (иногда известные как сигнал 0), он может вызвать созревание дендритной клетки, что приводит к усилению экспрессии костимулирующих молекул, необходимых для активации Т -клеток (см. Сигнал 2) [ 11 ] и MHC Class II. [ 12 ] Оказавшись в лимфатических узлах, APC начинают представлять антиген -пептиды, которые связаны с MHC класса II, позволяя CD4 + Т -клетки, которые экспрессируют специфические TCR против комплекса пептида/MHC для активации. [ Цитация необходима ]
Когда T H -клетка встречается и распознает антиген на APC, комплекс TCR - CD3 сильно связывается с комплексом пептид -MHC, присутствующего на поверхности профессиональных APC. CD4 , совместный рецептор комплекса TCR, также связывается с другим разделом молекулы MHC. Подсчитано, что приблизительно 50 из этих взаимодействий необходимы для активации вспомогательных Т-клеток и сборки, известных как микрокластеры, образуя образование между комплексами TCR-CD3-CD4 Т-клетки и белками класса II MHC дендритной клетки в зоне контакта. Когда все они объединяются, CD4 способен рекрутировать киназу, называемую LCK , которая фосфорилирует иммунорецепторные мотивы активации на основе тирозина (ITAM), присутствующие на гамма CD3, дельте, эпсилоне и Zeta. Белок ZAP-70 может связывать эти фосфорилированные ITAM через свой домен SH2 , а затем сама сама становится фосфорилируемым, в котором он организует передачу сигналов нижней части, необходимой для активации Т-клеток. Активация LCK контролируется противоположными действиями CD45 и CSK . [ 13 ] CD45 активирует LCK, дефосфорилируя тирозин в его C-концевом хвосте, в то время как CSK фосфорилирует LCK на этом сайте. Потеря CD45 производит форму SCID, поскольку неспособность активировать LCK предотвращает соответствующую передачу сигналов Т -клеток. Т -клетки памяти также используют этот путь и имеют более высокие уровни экспрессируемых LCK, и в этих клетках ингибируется функция CSK. [ 14 ]
Связывание антиген-MHC с комплексом TCR и CD4 может также помочь APC и T - клеткам прицеливаться во время активации Т - клеток, но белок интегрина LFA-1 на Т-клетках и ICAM на APC являются первичными молекулами адгезии в этом клеточном взаимодействии. [ Цитация необходима ]
Неизвестно, какую роль играет относительно громоздкая внеклеточная область CD45 во время клеточных взаимодействий, но CD45 имеет различные изоформы, которые изменяются в размере в зависимости от активации и состояния созревания Т -клеток . Например, CD45 сокращается в длине после активации T H (CD45RA + к CD45RO + ), но, неизвестно ли это изменение в длине активация. Было предложено, чтобы более крупный CD45RA может уменьшить доступность рецептора Т-клеток для молекулы антигена-MHC, что требует увеличения аффинности (и специфичности) Т-клеток для активации. Однако после того, как активация произошла, CD45 сокращается, позволяя легче взаимодействовать и активацию в качестве эффекторной вспомогательной клетки. [ Цитация необходима ]
Выживание (сигнал 2)
[ редактировать ]Получив первый сигнал TCR/CD3, наивная Т -клетка должна активировать второй независимый биохимический путь, известный как сигнал 2. Этот этап проверки является защитной мерой для обеспечения того, чтобы Т -клетка реагировала на иностранный антиген. Если этот второй сигнал не присутствует во время начального воздействия антигена, Т-клетка предполагает, что он является автореактивной. Это приводит к тому, что клетка стала анергической (анергера генерируется из незащищенных биохимических изменений сигнала 1). Анергические клетки не будут реагировать на какой -либо антиген в будущем, даже если оба сигнала присутствуют позже. Считается, что эти клетки циркулируют по всему организму без значения, пока не подвергаются апоптозу . [ 15 ]
Второй сигнал включает взаимодействие между CD28 на CD4 + Т -клетки и белки CD80 (B7.1) или CD86 (B7.2) на профессиональных APC. И CD80, и CD86 активируют рецептор CD28. Эти белки также известны как костимуляторные молекулы . [ Цитация необходима ]
Хотя этап проверки необходима для активации наивных вспомогательных Т -клеток, важность этой стадии лучше всего демонстрируется во время аналогичного механизма активации CD8 + цитотоксические Т -клетки . Как наивный CD8 + Т -клетки не имеют истинного смещения в отношении иностранных источников, эти Т -клетки должны полагаться на активацию CD28 для подтверждения того, что они распознают иностранный антиген (так как CD80/CD86 экспрессируется только активными APC). CD28 играет важную роль в снижении риска аутоиммунитета Т-клеток против антигенов-хозяев. [ Цитация необходима ]
После того, как наивная Т -клетка имеет оба пути, активированные, биохимические изменения, индуцированные сигналом 1, изменяются, что позволяет клетке активировать, а не переноситься. Второй сигнал затем устарел; Только первый сигнал необходим для будущей активации. Это также верно для Т -клеток памяти, что является одним из примеров изученного иммунитета . Более быстрые ответы возникают при реинфекции, потому что Т -клетки памяти уже подверглись подтверждению и могут вызывать эффекторные клетки гораздо раньше. [ Цитация необходима ]
Дифференциация (сигнал 3)
[ редактировать ]Как только активация двух сигналов завершена, T-Helper Cell (T H ) позволяет себе пролиферировать . Это достигает этого, выпустив мощный фактор роста Т-клеток, называемый интерлейкином 2 (IL-2), который действует на себя аутокринным образом. Активированные Т-клетки также продуцируют альфа-подразделение рецептора IL-2 ( CD25 или IL-2R), что позволяет полностью функциональному рецептору, который может связываться с IL-2, что, в свою очередь, активирует пути пролиферации Т-клеток. [ Цитация необходима ]
Аутокринная H или паракринная секреция IL-2 может связываться с той же Т - клетками или соседними T через IL-2R, тем самым стимулируя пролиферацию и клональную экспансию. TH - клетки, получающие оба сигнала активации, и пролиферацию, затем станут клетками T H 0 (T HELPER 0), которые выделяют IL-2, IL-4 и гамма интерферона (IFN-γ). Затем клетки T H 0 будут дифференцироваться в T H 1 или T H клетки 2 в зависимости от цитокиновой среды. IFN-γ приводит к T H выработке клеток 1, в то время как IL-10 и IL-4 ингибируют T H выработку клеток 1. И наоборот, IL-4 приводит к выработке клеток T H 2, а IFN-γ ингибирует T H клетки 2. Эти цитокины являются плейотропными и выполняют много других функций иммунного ответа. [ Цитация необходима ]
Эффекторная функция
[ редактировать ]В 1991 году три группы сообщили о обнаружении CD154, которая является молекулярной основой функции вспомогательных турниров. Сет Ледерман из Колумбийского университета генерировал мышиное моноклональное антитело, 5C8, которое ингибировало контакт-зависимую функцию Т-клеток в клетках человека, которые характеризовали поверхностный белок 32 кДа, временно экспрессируемая на CD4 + Т -клетки. [ 16 ] Ричард Армитидж в Immunex клонировал кДНК, кодирующую CD154 путем скрининга библиотеки экспрессии с CD40-IG. [ 17 ] Рэндольф Ноэль из Медицинской школы Дартмута генерировал антитело, которое связывало белок 39 кДа на мышиных Т -клетках и ингибировал вспомогательную функцию. [ 18 ]
Определение эффекторного ответа Т -клеток
[ редактировать ]Помощные Т -клетки способны влиять на различные иммунные клетки, и генерируемый ответ Т -клеток (включая внеклеточные сигналы, такие как цитокины ), может иметь важное значение для успешного исхода от инфекции. Чтобы быть эффективными, вспомогательные Т -клетки должны определить, какие цитокины позволят иммунной системе быть наиболее полезной или полезной для хозяина. Понимание того, как именно помощники Т -клетки реагируют на иммунные проблемы, в настоящее время представляет большой интерес к иммунологии , потому что такие знания могут быть очень полезны для лечения заболеваний и повышения эффективности вакцинации . [ Цитация необходима ]
T H 1/T H 2 модель
[ редактировать ]Пролиферирующие вспомогательные Т -клетки, которые развиваются в эффекторные Т -клетки, дифференцируются в два основных подтипа клеток, известных как клетки T H 1 и T H 2 (также известные как Helper T -клетки типа 1 и типа 2 соответственно).
Th 1 Helper Clts приводят к увеличению клеточно-опосредованного ответа (в первую очередь макрофагами и цитотоксическими Т-клетками ), [ 19 ] обычно против внутриклеточных бактерий и простейших. Они запускаются поляризующим цитокином IL-12, а их эффекторные цитокины-IFN-γ и IL-2. Основными эффекторными клетками иммунитета T H 1 являются макрофаги, а также CD8 T-клетки, B-клетки IgG и IFN-γ CD4 T-клетки. Ключевыми факторами транскрипции являются STAT4 и T-BET. IFN-γ, секретируемые CD4 T-клетками, могут активировать макрофаги в фагоцитозу и переваривать внутриклеточные бактерии и простейшие. Кроме того, IFN-γ может активировать INOS (индуцибельный оксид-синтазу оксида азота) для получения свободных радикалов оксида азота, чтобы непосредственно убивать внутриклеточные бактерии и простейшие. Печальная активация в отношении аутоантигенов будет вызывать реакцию гиперчувствительности типа IV или задержки типа. Реакция туберкулина и диабет 1 типа принадлежат к этой категории аутоиммунитета. [ 20 ]
Th 2 Helper Clts приводят к гуморальному иммунному ответу , [ 19 ] обычно против внеклеточных паразитов, таких как гельминт . Они запускаются поляризующими цитокинами IL-4 и IL-2, а их эффекторные цитокины являются IL-4, IL-5, IL-9, IL-10, IL-13 и IL-25. Основными эффекторными клетками являются эозинофилы, базофилы и тучные клетки, а также B-клетки, а также CD4 IL-4 CD4 IL-4. Ключевыми факторами транскрипции являются STAT6 и GATA3 . [ 21 ] IL-4 является цитокином положительной обратной связи для дифференцировки клеток T H 2. Кроме того, IL-4 стимулирует B-клетки для продуцирования антител IgE, которые, в свою очередь, стимулируют тучные клетки для высвобождения гистамина , серотонина и лейкотриена, чтобы вызвать брончо-конструкцию, кишечную перистангу, подкисление желудочной жидкости, чтобы изгнать гелестины. IL-5 из CD4 T-клеток будет активировать эозинофилы для атаки гельминтов. IL-10 подавляет дифференцировку клеток T H 1 и функцию дендритных клеток. T H 2 Перевертка против антигена вызовет гиперчувствительность I типа , которая является аллергической реакцией, опосредованной IGE. Аллергический ринит, атопический дерматит и астма принадлежат к этой категории переоцененной. [ 20 ] В дополнение к экспрессии различных цитокинов, клетки T H 2 также отличаются от клеток T H 1 в их гликанах клеточной поверхности (олигосахариды), что делает их менее восприимчивыми к некоторым индукторам гибели клеток. [ 22 ] [ 23 ]

| Тип 1/ T H 1 | Тип 2/ T H 2 [ 20 ] | |
|---|---|---|
| Основной тип ячейки партнера | Макрофаг , CD8 + Т -клетка | B-Cell , Eosinophil , MAST-клетка |
| Цитокины продуцируются | Интерферон гамма (IFNγ) и TNF-β . Производство интерлейкина 2 и интерлейкина 10 сообщалось в активированной клетке T H 1. [ 25 ] | Интерлейкин 4 , интерлейкин 5 , интерлейкин 6 , интерлейкин 9 , интерлейкин 10 , интерлейкин 13 |
| Иммунная стимуляция продвигается | Клеточная иммунная система . Максимизирует эффективность убийства макрофагов и пролиферацию цитотоксического CD8 + Т -клетки. Также способствует производству IgG, опсонизирующего антитела. | Гуморальная иммунная система . Стимулирует В-клеток в пролиферацию, индуцировать переключение класса антител B-клеток и увеличение нейтрализующих антител (IgG, IGM и IgA, а также антитела IgE). |
| Другие функции | Цитокин типа 1 IFNγ увеличивает выработку интерлейкина 12 дендритными клетками и макрофагами, и посредством положительной обратной связи IL-12 стимулирует выработку IFNγ в вспомогательных T-клетках, тем самым способствуя профилю T H 1. IFNγ также ингибирует продукцию цитокинов, таких как интерлейкин 4 , важный цитокин, связанный с ответом типа 2, и, таким образом, он также действует для сохранения своего собственного ответа. | Ответ типа 2 способствует своему собственному профилю с использованием двух разных цитокинов. Интерлейкин 4 действует на вспомогательные Т-клетки для стимулирования производства цитокинов T H 2 (включая себя; он является авторегуляторным), в то время как интерлейкин 10 (IL-10) ингибирует различные цитокины, включая интерлейкин 2 и IFNγ в Helper T-клетках и IL-12 в дендритных клетках и макрофагах. Комбинированное действие этих двух цитокинов предполагает, что после того, как Т -клетка решила произвести эти цитокины, это решение сохраняется (а также поощряет другие Т -клетки делать то же самое). |
В то время как мы знаем о типах цитокиновых паттернов, которые имеют тенденцию производить Т -клетки. Различные данные свидетельствуют о том, что тип APC, представляющего антиген, Т -клеток, оказывает большое влияние на его профиль. Другие данные свидетельствуют о том, что концентрация антигена, представленная на Т -клетку во время первичной активации, влияет на его выбор. Наличие некоторых цитокинов (например, упомянутых выше) также повлияет на реакцию, который в конечном итоге будет генерироваться, но наше понимание далеко не завершено.
T H 17 Helper Cells
[ редактировать ]Th 17 Helper Cells представляют собой подмножество T -Helper Cells, которые развиваются, отличающиеся от линий T H 1 и T H 2. Клетки T H 17 продуцируют интерлейкин 17 (IL-17), провоспалительное вещество, а также интерлейкины 21 и 22 . [ 26 ] Это означает, что клетки T H 17 особенно хороши в борьбе с внеклеточными патогенами [ 26 ] и грибы, особенно во время слизистого иммунитета против Candida SPP. [ 27 ]
THαβ Helper Cells
[ редактировать ]Клетки THαβ обеспечивают иммунитет хозяина против вирусов. Их дифференциация запускается IFN α/β или IL-10 . Их ключевой эффекторный цитокин-IL-10. Их основными эффекторными клетками являются NK-клетки , а также CD8 T-клетки, B-клетки IgG и CD4 IL-10. Ключевыми факторами транскрипции THα является STAT1 и STAT3, а также IRFS. NK-клеток IL-10 из CD4 T-клеток активируют ADCC к клеткам, инфицированным вирусом апоптозы, и для индукции как хозяина, а также фрагментации вирусной ДНК. IFN Alpha/Beta может подавлять транскрипцию, чтобы избежать репликации вируса и передачи. Перевернители THαβ в отношении аутоантигена вызовет антитело-зависимую цитотоксическую гиперчувствительность типа 2. Myastenia Gravis или болезнь Грейвса принадлежат этой категории. [ 28 ]
Ограничения на модель T H 1/T H 2
[ редактировать ]Взаимодействие между цитокинами из модели T H 1/T H 2 может быть более сложным у некоторых животных. Например, T H 2 цитокин IL-10 ингибирует выработку цитокинов обоих подмножества у людей. Человеческий IL-10 (HIL-10) подавляет пролиферацию и выработку цитокинов всех Т-клеток и активность макрофагов, но продолжает стимулировать плазматические клетки , гарантируя, что выработка антител все еще происходит. Таким образом, HIL-10 не считается по-настоящему способствовать реакции T H 2 у людей, но действует для предотвращения чрезмерной стимуляции вспомогательных Т-клеток, в то же время максимизируя выработку антител . [ Цитация необходима ]
Существуют также другие типы Т -клеток, которые могут влиять на экспрессию и активацию TPER T -клеток, таких как природные регуляторные Т -клетки , наряду с менее распространенными профилями цитокинов, такими как подмножество T H 3 Helper T -клеток. Такие термины, как «регулирующий» и «подавление», стали неоднозначными после открытия, который помощник CD4 + Т -клетки также способны регулировать (и подавлять) свои собственные ответы за пределами выделенных регуляторных Т -клеток. [ Цитация необходима ]
Одно из основных различий между регуляторными Т-клетками и эффекторными Т-клетками заключается в том, что регуляторные Т-клетки обычно служат для модуляции и деактивации иммунного ответа, в то время как эффекторные группы Т-клеток обычно начинаются с иммунопроводящих цитокинов, а затем переключаются на ингибирующие цитокины позже в их жизненном цикле. Последнее является особенностью клеток T H 3, которые превращаются в регуляторное подмножество после его начальной активации и выработки цитокинов. [ Цитация необходима ]
Как регуляторные Т-клетки , так и клетки T H 3 продуцируют цитокиновый трансформирующий фактор роста бета (TGF-β) и IL-10. Оба цитокина ингибируют вспомогательные Т -клетки; TGF-β подавляет активность большей части иммунной системы. Существуют доказательства того, что TGF-β может не подавлять активированные клетки Th2 так же эффективно, как это может подавлять наивные клетки, но обычно не считается цитокином Th2. [ Цитация необходима ]
Новая характеристика другого подтипа T Helper, T Helper 17 Cells (T H 17) [ 29 ] выдвинул дополнительные сомнения в модели базовой T H 1/T H 2. Эти продуцирующие IL-17 клетки были первоначально описаны как патогенная популяция, вовлеченная в аутоиммунитет, но в настоящее время считается своими собственными различными эффекторными и регуляторными функциями. Следует отметить, что некоторые данные свидетельствуют о том, что функциональная пластичность является внутренней способностью T -Helper Cells. Действительно, исследование мышей показало, что клетки T H 17 превращаются в T H клетки 1 in vivo . [ 30 ] Последующее исследование, кроме того, показало, что обширная пластичность T -Helper Cell также является заметной у людей. [ 31 ]
Многие из цитокинов в этой статье также экспрессируются другими иммунными клетками (подробности см. В отдельных цитокинах), и становится ясно, что, хотя оригинальная модель T H 1/T H 2 просветляет и дает представление о функциях помощника T Клетки, слишком просто определить всю его роль или действия. Некоторые иммунологи ставят под сомнение модель полностью, так как некоторые исследования in vivo предполагают, что отдельные туалетные Т -клетки обычно не соответствуют специфическим профилям цитокинов модели Т -Т , и многие клетки экспрессируют цитокины из обоих профилей. [ 32 ] Тем не менее, модель T H все еще сыграла важную роль в развитии нашего понимания ролей и поведения помощников Т -клеток и цитокинов, которые они производят во время иммунного ответа.
Исследования Stockinger et al. показал, что может существовать еще одна подмножество T Helper. Утверждается, что клетки Th9 являются IL9 ( интерлейкин 9 ), продуцирующая подмножество Т -клеток, сфокусированное на защите гельминтовых инфекций. [ 33 ]
Память Т -ячейка
[ редактировать ]Исторически считалось, что Т -клетки памяти принадлежат либо подтипам эффекторной, либо центральной памяти, каждый из которых имеет свой собственный отличительный набор маркеров клеточной поверхности. [ 34 ] Т-клетки центральной памяти находятся в лимфатических узлах, в то время как в Т-клетках с эффекторной памятью отсутствуют рецепторы хемокинового рецептора CC типа 7 (CCR7) и L-селектин (CD62L), что мешает им переносить лимфатические узлы.
В настоящее время известно, что дополнительные популяции памяти Т -клеток существуют. К ним относятся клетки с тканевой памятью T (TRM) и виртуальную память Т-клетки. [ 35 ] Единственная объединяющая тема для всех подтипов Т-клеток памяти заключается в том, что они долгоживущие и могут быстро расширяться до большого количества эффекторных Т-клеток при встрече с их родственным антигеном. По этому механизму они предоставляют иммунную систему «память» против ранее встречающихся патогенов.
Роль в болезнях
[ редактировать ]Принимая во внимание разнообразные и важные ролевые T -клетки в иммунной системе, неудивительно, что эти клетки часто влияют на иммунный ответ на заболевание. Они также время от времени генерируют незвуковые ответы. Очень редко ответный ответ Т -клеток может привести к смерти хозяина. [ Цитация необходима ]
Противоопухолевый иммунитет
[ редактировать ]Гиперчувствительность
[ редактировать ]Иммунная система должна достичь баланса чувствительности, чтобы реагировать на иностранные антигены, не отвечая на антигены самого хозяина. Когда иммунная система реагирует на очень низкие уровни антигена, на который она обычно не должна реагировать, возникает реакция гиперчувствительности . Считается, что гиперчувствительность является причиной аллергии и некоторых аутоиммунных заболеваний .
Реакции гиперчувствительности могут быть разделены на четыре типа:
- Гиперчувствительность типа 1 включает в себя общие иммунные расстройства, такие как астма , аллергический ринит (сенская лихорадка), экзема , крапивница (ульи) и анафилаксия . Все эти реакции включают IgE антитела , которые требуют ответа T H 2 во время развития помощников Т -клеток. Профилактические обработки, такие как кортикостероиды и монтелукаст , сосредоточены на подавлении тучных клеток или других аллергических клеток; Т -клетки не играют первичной роли во время фактического воспалительного ответа. Важно отметить, что чистельное распределение гиперчувствительности «типов» не коррелирует (и совершенно не связано) с «ответом» в T H. модели
- типа 2 и Гиперчувствительность типа 3 связана с осложнениями из аутоиммунных или низких аффинных антител. В обеих этих реакциях Т-клетки могут играть роль соучастника в создании этих автоспецифичных антител, хотя некоторые из этих реакций при гиперчувствительности 2 типа будут считаться нормальными в здоровой иммунной системе (например, реакции фактора-резуса во время ребенка-родов является нормальным иммунным ответом против детских антигенов). Понимание роли вспомогательных Т -клеток в этих ответах ограничено, но обычно считается, что цитокины t h 2 будут способствовать таким расстройствам. Например, исследования показали, что волчанка (SLE) и другие аутоиммунные заболевания сходной природы могут быть связаны с производством цитокинов T H 2.
- Гиперчувствительность типа 4 , также известная как гиперчувствительность с задержкой типа , вызвана чрезмерной стимуляцией иммунных клеток, обычно лимфоцитов и макрофагов , что приводит к хроническому воспалению и высвобождению цитокинов. Антитела не играют прямой роли в этом типе аллергии. Т -клетки играют важную роль в этой гиперчувствительности, поскольку они активируются против самого стимула и способствуют активации других клеток; Особенно макрофаги с помощью цитокинов T H 1.
Другие клеточные гиперчувствительность включают цитотоксические Т-клеточные, опосредованные Т-клетками аутоиммунные заболевания , и сходное явление; отказ от пересадки . Помощные Т -клетки необходимы для создания развития этих заболеваний. Чтобы создать достаточный авто-реактивный убийственный Т-клетки, необходимо продуцировать интерлейкин-2 , и это поставляется CD4 + Т -клетки. CD4 + Т-клетки также могут стимулировать клетки, такие как природные клетки-киллеры и макрофаги, через цитокины, такие как интерферон-гамма , поощряя эти цитотоксические клетки к убийству клеток-хозяев при определенных обстоятельствах.
Механизм, который используют T-клетки-убийцы во время аутоиммунитета, практически идентичен их ответу против вирусов , и некоторые вирусы были обвинены в вызывании аутоиммунных заболеваний, таких как сахарный диабет 1 типа . Клеточное аутоиммунное заболевание происходит потому, что системы распознавания антигена-хозяина терпят неудачу, и иммунная система , по ошибке, что антиген-хозяин является иностранным. В результате CD8 + Т -клетки обрабатывают клетку -хозяина, представляя этот антиген как инфицированный, и продолжают уничтожать все клетки -хозяина (или в случае отторжения трансплантации, органа по пересадке), которые экспрессируют этот антиген.
Некоторые из этого раздела - упрощение. Многие аутоиммунные заболевания более сложны. Хорошо известным примером является ревматоидный артрит , где, как известно, как антитела, так и иммунные клетки играют роль в патологии. Как правило, иммунология большинства аутоиммунных заболеваний не совсем понятна.
ВИЧ -инфекция
[ редактировать ]Возможно, лучший пример важности CD4 + Т -клетки демонстрируются инфекцией вируса иммунодефицита человека (ВИЧ). ВИЧ в основном нацелены на лимфоидный CD4 + Т -клетки, но могут инфицировать другие клетки, которые экспрессируют CD4, такие как макрофаги и дендритные клетки (обе группы экспрессируют CD4 на низких уровнях). [ Цитация необходима ]
Было предложено, что во время нестимптомной фазы ВИЧ-инфекции вирус имеет относительно низкое сродство к Т-клеткам (и имеет более высокое сродство к макрофагам), что приводит к медленной скорости убийства CD4 + Т -клетки иммунной системой. [ Цитация необходима ] Первоначально это компенсируется через производство новых вспомогательных Т -клеток из тимуса (родом из костного мозга ). Однако как только вирус становится лимфотропным (или Т-тропическим), он начинает заражать CD4 + Т-клетки гораздо более эффективно (вероятно, из-за изменения в корецепторах , с которыми он связывается во время инфекции), и иммунная система перегружена. Исследования показывают, что только ~ 5% лимфоидных CD4 T-клеток, нацеленных на ВИЧ, являются добывающими и становятся продуктивно инфицированными вирусом. Более 95% T -клеток CD4, которые умирают, отдыхают и не могут поддерживать продуктивную инфекцию. Эти клетки подвергаются абортивной инфекции с ВИЧ. [ 36 ] Гибель клеток запускается, когда клетка-хозяин обнаруживает промежуточные продукты ВИЧ-иностранных ДНК и инициирует суицидальный путь смерти в попытке защитить хозяина, что приводит к активации каспазы-1 в воспалении , что вызывает пироптоз (высоко воспаливающая форма программированной гибели клеток). [ 37 ] [ 38 ] [ 39 ]
На этом этапе заступает хроническое воспаление и функциональный CD4 + Уровни Т -клеток начинают уменьшаться, в конечном итоге до такой степени, что CD4 + Т -клеточная популяция слишком мала, чтобы распознать весь спектр антигенов , которые могут быть обнаружены. Истощение CD4 T -клеток и развитие хронического воспаления являются процессами подписи в патогенезе ВИЧ, которые продвигают прогрессирование к синдрому приобретенного иммунного дефицита (СПИД). CD4 T -клетка, истощенные до количества клеток менее чем в 200 -м, в крови во время СПИДа, позволяет различным патогенам избежать распознавания Т -клеток, что позволяет оппортунистическим инфекциям , которые обычно вызывают ответный ответ Т -клеток для обхода иммунной системы. [ 40 ] В то время как эти полные ситуации обхода возникают только тогда, когда ответный ответ Т -клеток абсолютно необходим для клиренса инфекции, большинство инфекций увеличиваются в тяжесть и/или продолжительность, поскольку вспомогательные Т -клетки иммунной системы обеспечивают менее эффективный иммунный ответ.
Два компонента иммунной системы особенно затронуты в СПИДе из -за его CD4 + Зависимость Т -клеток:
- CD8 + Т -клетки не стимулируются так же эффективно во время стадии ВИЧ -инфекции СПИДа, что делает пациентов с СПИДом очень восприимчивыми к большинству вирусов, включая сам ВИЧ. Это снижение убийства CD4 + Т -клетки приводят к тому, что вирус продуцируется в течение более длительного периода (инфицированный CD4 + Т -клетки не убивают так быстро), увеличивая пролиферацию вируса и ускоряя развитие заболевания.
- Антител к классу значительно снижается после сбоя функции вспомогательной Т -клеток. Иммунная система теряет свою способность улучшать сродство своих антител и не может генерировать В -клетки, которые могут продуцировать антитела, такие как IgG и IGA . Эти эффекты в первую очередь связаны с потерей любой вспомогательной Т -клеток, которая может правильно взаимодействовать с B -лимфоцитами. Другим симптомом СПИДа является снижение уровней антител из -за снижения цитокинов T H 2 (и меньше взаимодействий с помощью Helper T -клеток). Все эти осложнения приводят к повышению восприимчивости к агрессивным бактериальным инфекциям, особенно в областях организма, недоступных антителами IgM .
Если пациент не отвечает (или не получает) лечение ВИЧ, он обычно поддается либо раковым заболеваниям, либо с инфекциями; Иммунная система, наконец, достигает точки, когда она больше не координируется и не стимулируется, чтобы справиться с заболеванием.
Ингибирование расширения CD4 Т-клеток во время ВИЧ-инфекции может возникнуть из-за микробной транслокации в зависимости от IL-10. Зарабатывание PD-1, экспрессируемое на активированных моноцитах с помощью его лиганда PD-L1, индуцирует продукцию IL-10, которая ингибирует функцию CD4 T-клеток. [ 41 ]
COVID-19
[ редактировать ]При заболевании коронавируса 2019 (Covid-19) B-клеток , природные клетки-киллеры и общее количество лимфоцитов снижается, но оба CD4 + и CD8 + Клетки снижаются в гораздо большей степени. [ 42 ] Указывая, что SARS-COV-2 атакует CD4 + клетки во время инфекции. Низкий CD4 + прогнозировал большую вероятность поступления подразделения интенсивной терапии и CD4 + Количество клеток было единственным параметром, который предсказал продолжительность времени для вирусной РНК . [ 42 ] Несмотря на снижение уровня CD4 + , Пациенты с Covid-19 с тяжелым заболеванием имели более высокие уровни T H 1 CD4 + клетки, чем пациенты с умеренным заболеванием. [ 43 ]
Смотрите также
[ редактировать ]- CD4 + /CD8 + соотношение
- CD4 + Т -клетки и противоопухолевый иммунитет
- CD8 + Т -клетки
- Нацеливание на вакцину против рака CD4 + Т -клетки
- Список отдельных типов клеток в теле человека человека
Ссылки
[ редактировать ]- ^ Burren OS, Rubio García A, Javierre BM, Rainbow DB, Cairns J, Cooper NJ, et al. (Сентябрь 2017). «Контакты хромосом в активированных Т -клетках идентифицируют гены кандидатов на аутоиммунные заболевания» . Биология генома . 18 (1): 165. doi : 10.1186/s13059-017-1285-0 . PMC 5584004 . PMID 28870212 .
- ^ Oestreich KJ, Weinmann As (ноябрь 2012 г.). «Мастер-регуляторы или уклонные к линии? Изменение взглядов на факторы транскрипции CD4+ T-клеток» . Природные обзоры. Иммунология . 12 (11): 799–804. doi : 10.1038/nri3321 . PMC 3584691 . PMID 23059426 .
- ^ FINK PJ (2013-03-21). «Биология недавних эмигрантов тимуса». Ежегодный обзор иммунологии . 31 (1): 31–50. doi : 10.1146/Annurev-Immunol-032712-100010 . PMID 23121398 .
- ^ Ван Ден Брок Т., Борганс Дж.А., Ван Вийк Ф. (июнь 2018 г.). «Полный спектр человеческих наивных Т -клеток». Природные обзоры. Иммунология . 18 (6): 363–373. doi : 10.1038/s41577-018-0001-y . PMID 29520044 . S2CID 3736563 .
- ^ Ван Ден Брок Т., Делемер Э.М., Янссен В.Дж., Нивельштейн Р.А., Броен Дж.С., Тесселаар К. и др. (Март 2016 г.). «Неонатальная тимэктомия выявляет дифференцировку и пластичность в наивных Т -клетках человека» . Журнал клинических исследований . 126 (3): 1126–1136. doi : 10.1172/jci84997 . PMC 4767338 . PMID 26901814 .
- ^ Roche PA, Furuta K (апрель 2015 г.). «Вин и выходы MHC-опосредованной обработки и презентации антигена» . Природные обзоры. Иммунология . 15 (4): 203–216. doi : 10.1038/nri3818 . PMC 6314495 . PMID 25720354 .
- ^ Unanue ER, Turk V, Neefjes J (май 2016 г.). «Изменения в обработке и презентации антигена MHC класса II в отношении здоровья и заболеваний». Ежегодный обзор иммунологии . 34 (1): 265–297. doi : 10.1146/Annurev-Immunol-041015-055420 . PMID 26907214 .
- ^ Wieczorek M, Abualrous ET, Sticht J, Alvaro-Benito M, Stolzenberg S, Noé F, Freund C (2017-03-17). «Основной гистосовместимость комплекса (MHC) класса I и MHC класса II: конформационная пластичность в презентации антигена» . Границы в иммунологии . 8 : 292. DOI : 10.3389/fimmu.2017.00292 . PMC 5355494 . PMID 28367149 .
- ^ Trolle T, McMurtrey CP, Sidney J, Bardet W, Osborn SC, Kaever T, et al. (Февраль 2016 г.). «Распределение длины эпитопов Т-клеток, ограниченных I, определяется как пептидным питанием, так и предпочтением аллеля MHC-специфического связывания» . Журнал иммунологии . 196 (4): 1480–1487. doi : 10.4049/jimmunol.1501721 . PMC 4744552 . PMID 26783342 .
- ^ Мерфи К (2017). Иммунобиология Джейнвея . Гарлендская наука. ISBN 978-0-8153-4551-0 Полем OCLC 1020120603 .
- ^ Парень Б (июль 2007 г.). «Идеальное микс: недавний прогресс в адъювантных исследованиях». Природные обзоры. Микробиология . 5 (7): 505–517. doi : 10.1038/nrmicro1681 . PMID 17558426 . S2CID 25647540 .
- ^ Hammer GE, MA A (2013-03-21). «Молекулярный контроль устойчивого созревания дендритных клеток и иммунного гомеостаза» . Ежегодный обзор иммунологии . 31 (1): 743–791. doi : 10.1146/Annurev-Immunol-020711-074929 . PMC 4091962 . PMID 23330953 .
- ^ Zamoyska R (сентябрь 2007 г.). "Почему на Т -клетках так много CD45?" Полем Иммунитет . 27 (3): 421–423. doi : 10.1016/j.immuni.2007.08.009 . PMID 17892852 .
- ^ Кортни А.Х., Шветс А.А., Лу В., Гриффанте Г., Молленуэр М., Хоркова В. и др. (Октябрь 2019). «CD45 функционирует как сигнальный привратник в Т -клетках» . Наука сигнализация . 12 (604): EAAW8151. doi : 10.1126/scisignal.aaw8151 . PMC 6948007 . PMID 31641081 .
- ^ Elmore S (июнь 2007 г.). «Апоптоз: обзор запрограммированной гибели клеток» . Токсикологическая патология . 35 (4): 495–516. doi : 10.1080/01926230701320337 . PMC 2117903 . PMID 17562483 .
- ^ Ледерман С., Йеллин М.Дж., Кричевский А., Белко Дж., Ли Дж.Дж., Шахматы Л (апрель 1992). «Идентификация нового поверхностного белка на активированных CD4+ T-клетках, которые индуцируют контактную дифференцировку В-клеток, вызывают контакт (справка)» . Журнал экспериментальной медицины . 175 (4): 1091–1101. doi : 10.1084/jem.175.4.1091 . PMC 2119166 . PMID 1348081 .
- ^ Armitage RJ, Fanslow WC, Strockbine L, Sato TA, Clifford KN, Macduff BM, et al. (Май 1992). «Молекулярная и биологическая характеристика мышиного лиганда для CD40». Природа . 357 (6373): 80–82. Bibcode : 1992natur.357 ... 80a . doi : 10.1038/357080a0 . PMID 1374165 . S2CID 4336943 .
- ^ Ноэль Р.Дж., Рой М., Шепард Д.М., Стаменкович И., Ледбеттер Дж.А., Аруффо А (июль 1992 г.). «Белок 39 кДа на активированных вспомогательных Т-клетках связывает CD40 и преобразует сигнал для родственной активации B-клеток» . Труды Национальной академии наук Соединенных Штатов Америки . 89 (14): 6550–6554. Bibcode : 1992pnas ... 89.6550n . doi : 10.1073/pnas.89.14.6550 . PMC 49539 . PMID 1378631 .
- ^ Jump up to: а беременный Belizário JE, Brandão W, Rossato C, Peron JP (2016). «Тимусная и посттимическая регуляция наивных судов линии Т-клеток CD4 (+) на моделях людей и мышей» . Посредники воспаления . 2016 : 9523628. DOI : 10.1155/2016/9523628 . PMC 4904118 . PMID 27313405 .
- ^ Jump up to: а беременный в Чжу Дж, Пол мы (сентябрь 2008 г.). «CD4 T -клетки: судьбы, функции и разломы» . Кровь . 112 (5): 1557–1569. doi : 10.1182/blood-2008-05-078154 . PMC 2518872 . PMID 18725574 .
- ^ Wan Yy (июнь 2014 г.). «Gata3: мастер многих сделок в иммунном регулировании» . Тенденции в иммунологии . 35 (6): 233–242. doi : 10.1016/j.it.2014.04.002 . PMC 4045638 . PMID 24786134 .
- ^ Maverakis E, Kim K, Shimoda M, Gersshwin ME, Patel F, Wilken R, et al. (Февраль 2015 г.). «Гликаны в иммунной системе и измененная теория аутоиммунитета гликана: критический обзор» . Журнал аутоиммунитета . 57 (6): 1–13. doi : 10.1016/j.jaut.2014.12.002 . PMC 4340844 . PMID 25578468 .
- ^ Toscano MA, Bianco GA, Ilarregui JM, Croci Do, Correale J, Hernandez JD, et al. (Август 2007 г.). «Дифференциальное гликозилирование эффекторных клеток Th1, Th2 и Th-17 избирательно регулирует восприимчивость к гибели клеток». Природа иммунология . 8 (8): 825–834. doi : 10.1038/ni1482 . PMID 17589510 . S2CID 41286571 .
- ^ Rang HP, Dale MM, Riter JM, Moore PK (2003). Фармакология . Эдинбург: Черчилль Ливингстон. ISBN 978-0-443-07145-4 Полем Страница 223
- ^ Сарайва М., Кристенсен младший, Вельдхоен М., Мерфи Т.Л., Мерфи К.М., О'Гарра А (август 2009 г.). «Производство интерлейкина-10 с помощью клеток Th1 требует индуцированного интерлейкина-12 транскрипционного фактора STAT4 и активации киназы ERK с высокой дозой антигена» . Иммунитет . 31 (2): 209–219. doi : 10.1016/j.immuni.2009.05.012 . PMC 2791889 . PMID 19646904 .
- ^ Jump up to: а беременный Гуглани Л., Хадер С.А. (2010). «Цитокины Th17 в иммунитете слизистой оболочки и воспалении» . Текущее мнение в ВИЧ и СПИДе . 5 (2): 120–127. doi : 10.1097/coh.0b013e328335c2f6 . PMC 2892849 . PMID 20543588 .
- ^ Tangye SG, Puel A (2023). «Ось TH17/IL-17 и защита хозяина от грибковых инфекций». Журнал аллергии и клинической иммунологии: на практике . 11 (6): 1624–1634. doi : 10.1016/j.jaip.2023.04.015 . PMID 37116791 . S2CID 258380150 .
- ^ Hu W (2007). Анализ микрочипов профилей экспрессии генов PBMC после малярийной инфекции Plasmodium falciparum (кандидатская диссертация). Университет Джона Хопкинса.
- ^ Харрингтон Л.Е., Хаттон Р.Д., Манган П.Р., Тернер Х., Мерфи Т.Л., Мерфи К.М., Уивер КТ (ноябрь 2005 г.). «Интерлейкин 17-продуцирующих CD4+ эффекторные Т-клетки развиваются через линию, отличную от линий T-Helper Type 1 и 2». Природа иммунология . 6 (11): 1123–1132. doi : 10.1038/ni1254 . PMID 16200070 . S2CID 11717696 .
- ^ Хирота К., Дуарте Дж.Х., Вельдхоен М., Хорнсби Э., Ли Й., Куа Д.Дж. и др. (Март 2011 г.). «Картирование судьбы Т-клеток, продуцирующих IL-17 в воспалительных реакциях» . Природа иммунология . 12 (3): 255–263. doi : 10.1038/ni.1993 . PMC 3040235 . PMID 21278737 .
- ^ Ларсен М., Арно Л., Хие М., Паризот С., Доргам К., Шукри М. и др. (Сентябрь 2011). «Многоараметр группировки определяет гетерогенные популяции человеческих производителей IL-17 и/или IL-22 Т-клеток, которые разделяют специфичность антигена с другими подмножествами Т-клеток» . Европейский журнал иммунологии . 41 (9). UPMC Paris 06 Национальный институт здравоохранения и медицинских исследований (Inserm) UMR-S 945: 2596–2605. Doi : 10.1002/eji.201041131 . PMID 21688259 . S2CID 24092508 .
- ^ Nakayamada S, Takahashi H, Kanno Y, O'Shea JJ (июнь 2012 г.). «Помощное Т -клеточное разнообразие и пластичность» . Текущее мнение в иммунологии . 24 (3): 297–302. doi : 10.1016/j.coi.2012.01.014 . PMC 3383341 . PMID 22341735 .
- ^ TATO CM, CUA DJ (декабрь 2008 г.). «Альтернативный образ жизни Т -клеток». Nat Immunol . 9 (12): 1323–5. doi : 10.1038/ni1208-1323 . PMID 19008928 . S2CID 6691974 .
- ^ Саллусто Ф., Лениг Д., Фёрстер Р., Липп М., Ланзавеккия А (октябрь 1999 г.). «Два подмножества Т -лимфоцитов памяти с различными потенциалами самонинга и эффекторными функциями». Природа . 401 (6754): 708–712. Bibcode : 1999natur.401..708s . doi : 10.1038/44385 . PMID 10537110 . S2CID 4378970 .
- ^ Marusina Ai, Ono Y, Merleev AA, Shimoda M, Ogawa H, Wang Ea, et al. (Февраль 2017 г.). "CD4 + Виртуальная память: Т-клетки с антиген-энксперизированием находятся в наивных, регуляторных и памяти Т-клеточных компартментов на аналогичных частотах, последствия для аутоиммунитета » . Журнал аутоиммунитета . 77 (2): 76–88. DOI : 10.1016/j.jaut. 2016.11.001 .
- ^ Doitsh G, Cavrois M, Lassen KG, Zepeda O, Yang Z, Santiago ML, et al. (Ноябрь 2010). «Абортная ВИЧ -инфекция опосредует истощение CD4 T -клеток и воспаление в лимфоидной ткани человека» . Клетка . 143 (5): 789–801. doi : 10.1016/j.cell.2010.11.001 . PMC 3026834 . PMID 21111238 .
- ^ Doitsh G, Galloway NL, Geng X, Yang Z, Monroe KM, Zepeda O, et al. (Январь 2014). «Клеточная гибель путем пироптоза приводит к истощению CD4 Т-клеток при ВИЧ-1 инфекции» . Природа . 505 (7484): 509–514. Bibcode : 2014natur.505..509d . doi : 10.1038/nature12940 . PMC 4047036 . PMID 24356306 .
- ^ Monroe KM, Yang Z, Johnson Jr, Geng X, Doitsh G, Krogan NJ, Greene WC (январь 2014 г.). «ДНК -датчик IFI16 необходим для смерти лимфоидных CD4 T -клеток, абортно инфицированных ВИЧ» . Наука . 343 (6169): 428–432. Bibcode : 2014sci ... 343..428m . doi : 10.1126/science.1243640 . PMC 3976200 . PMID 24356113 .
- ^ Zhang C, Song JW, Huang HH, Fan X, Huang L, Deng JN, et al. (Март 2021 г.). «Воспалена NLRP3 индуцирует потерю CD4+ Т-клеток у пациентов с ВИЧ-1, инфицированными ВИЧ-1» . Журнал клинических исследований . 131 (6). doi : 10.1172/jci1388861 . PMC 7954596 . PMID 33720048 .
- ^ "CD4 Count" . www.aids.gov . Архивировано с оригинала 2015-04-15 . Получено 2015-04-30 .
- ^ Сказал EA, Dupuy FP, Trautmann L, Zhang Y, Shi Y, El-Far M, et al. (Апрель 2010). «Программированная производство интерлейкина-10, индуцированное DEATH-1 с помощью моноцитов, нарушает активацию CD4+ Т-клеток во время ВИЧ-инфекции» . Природная медицина . 16 (4): 452–459. doi : 10.1038/nm.2106 . PMC 4229134 . PMID 20208540 .
- ^ Jump up to: а беременный Huang W, Berube J, McNamara M, Saksena S, Hartman M, Arshad T, et al. (Август 2020). «Подмножество лимфоцитов у пациентов с Covid-19: метаанализ» . Цитометрия. Часть а . 97 (8): 772–776. doi : 10.1002/cyto.a.24172 . PMC 7323417 . PMID 32542842 .
- ^ Перлман С (август 2020 г.). «Covid-19 создает загадку для иммунной системы» . Природа . 584 (7821): 345–346. doi : 10.1038/d41586-020-02379-1 . PMID 32807916 .
Дальнейшее чтение
[ редактировать ]- Doitsh G, Greene WC (март 2016 г.). «Рассыновить, как CD4 T -клетки теряются во время ВИЧ -инфекции» . Ячейка и микроб . 19 (3): 280–291. doi : 10.1016/j.chom.2016.02.012 . PMC 4835240 . PMID 26962940 .
- Канно Y, Вахеди Г., Хирахара К., Синглтон К., О'Ши Дж.Дж. (2012). «Транскрипционное и эпигенетическое контроль спецификации T -Helper Cell: молекулярные механизмы, лежащие в основе приверженности и пластичности» . Ежегодный обзор иммунологии . 30 : 707–731. doi : 10.1146/Annurev-Immunol-020711-075058 . PMC 3314163 . PMID 22224760 .
Внешние ссылки
[ редактировать ]- "T-Cell Group" . Т-клетки . Кардиффский университет .