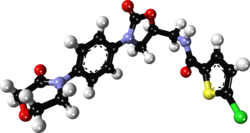
Ривароксабан
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Ксарелто, другие |
| Другие имена | ЗАЛИВ 59-7939 |
| AHFS / Drugs.com | Монография |
| МедлайнПлюс | а611049 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Биодоступность | 80–100%; Cmax = 2–4 часа (10 мг перорально) [ 4 ] |
| Метаболизм | CYP3A4 , CYP2J2 и CYP-независимые механизмы [ 4 ] |
| Период полувыведения | 5–9 часов у здоровых людей в возрасте от 20 до 45 лет. [ 4 ] [ 7 ] |
| Экскреция | 2/3 метаболизируется в печени и 1 / 3 исключено без изменений [ 4 ] |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| КЭБ | |
| ХЭМБЛ | |
| PDB-лиганд | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.210.589 |
| Химические и физические данные | |
| Формула | С 19 Н 18 Cl Н 3 О 5 С |
| Молярная масса | 435.88 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
Ривароксабан под торговой маркой Ксарелто , продаваемый, среди прочего, , представляет собой антикоагулянт (разжижитель крови), используемый для лечения и предотвращения образования тромбов . [ 8 ] В частности, он используется для лечения тромбоза глубоких вен и легочной эмболии , а также для предотвращения образования тромбов при фибрилляции предсердий и после операций на бедре или колене. [ 8 ] Его принимают внутрь . [ 8 ]
Общие побочные эффекты включают кровотечение. [ 8 ] Другие серьезные побочные эффекты могут включать гематому позвоночника и анафилаксию . [ 8 ] Неясно, ли использование во время беременности и грудного вскармливания . безопасно [ 1 ] По сравнению с варфарином он меньше взаимодействует с другими лекарствами . [ 9 ] Он действует путем блокирования активности фактора белка свертывания крови Ха . [ 8 ]
Ривароксабан был запатентован в 2007 году и одобрен для медицинского применения в США в 2011 году. [ 10 ] В Соединенных Штатах он не будет доступен в качестве непатентованного препарата до 2024 года. [ 11 ] [ 12 ] Он входит в Список основных лекарственных средств Всемирной организации здравоохранения . [ 13 ] В 2021 году это было 86-е место среди наиболее часто назначаемых лекарств в США: на него было выписано более 8 миллионов рецептов. [ 14 ] [ 15 ]
Медицинское использование
[ редактировать ]У пациентов с неклапанной фибрилляцией предсердий ривароксабан, по-видимому, так же эффективен, как и варфарин, в предотвращении инсультов и эмболических событий у пациентов, которые классифицируются как группы риска от умеренного до высокого, что определяется по шкале ряда конкретных заболеваний . [ 16 ] [ 17 ]
Великобритании В июле 2012 года Национальный институт здравоохранения и клинического мастерства рекомендовал ривароксабан для профилактики и лечения венозной тромбоэмболии . [ 18 ]
Противопоказания
[ редактировать ]При хирургических операциях из-за опасений по поводу остановки кровотечения прием ривароксабана можно отменить за 24 часа до операции с низким риском кровотечения и за 48–72 часа до операции с высоким риском кровотечения. [ 19 ] [ 20 ] После окончания операции ее можно возобновить через 1–3 дня после консультации врача. [ 19 ] [ 20 ]
Рекомендации по дозированию не рекомендуют назначать ривароксабан с препаратами, которые считаются сильными комбинированными ингибиторами CYP3A4 / P-гликопротеина , поскольку это приводит к значительно более высоким концентрациям ривароксабана в плазме. [ 5 ] [ 21 ] В небольшом ретроспективном когортном исследовании сообщалось, что использование умеренных ингибиторов CYP3A4 и P-гликопротеина, таких как амиодарон или верапамил, увеличивает риск кровотечения при применении с ривароксабаном. [ 22 ] Хотя это увеличение не было статистически значимым, наблюдалась тенденция увеличения кровотечения в группе ривароксабана с умеренными ингибиторами CYP3A4 и P-гликопротеина. [ 22 ] Поэтому важно следить за кровотечением при одновременном применении ривароксабана и умеренных ингибиторов CYP3A4 и P-гликопротеина. [ 22 ]
Побочные эффекты
[ редактировать ]Наиболее серьезным побочным эффектом является кровотечение , в том числе сильное внутреннее кровотечение . [ 23 ] [ 24 ] [ 25 ]
По состоянию на 2015 год [update], постмаркетинговые оценки показали токсичность для печени, и необходимы дальнейшие исследования для количественной оценки этого риска. [ 26 ] [ 27 ] В 2015 году на ривароксабан приходилось наибольшее количество зарегистрированных случаев серьезных повреждений среди лекарств, регулярно отслеживаемых в Системе сообщения о нежелательных явлениях (AERS) FDA. [ 28 ]
Реверсивный агент
[ редактировать ]В октябре 2014 года компания Portola Pharmaceuticals завершила фазы I и II клинических испытаний андексанета альфа в качестве антидота для ингибиторов фактора Ха с небольшим количеством побочных эффектов и начала исследования фазы III. [ 29 ] [ 30 ] Andexanet alfa был одобрен Управлением по контролю за продуктами и лекарствами США в мае 2018 года под торговым названием AndexXa . [ 31 ] [ 32 ]
Механизм действия
[ редактировать ]Ривароксабан ингибирует как свободный, так и связанный фактор Ха в протромбиназном комплексе . [ 33 ] Это селективный прямой ингибитор фактора Ха с началом действия от 2,5 до 4 часов. [ 34 ] Ингибирование фактора Ха прерывает внутренний и внешний путь каскада свертывания крови , подавляя как образование тромбина , так и развитие тромбов. Ривароксабан не ингибирует тромбин (активированный фактор II), и не никакого воздействия на тромбоциты . выявлено [ 4 ] Это позволяет прогнозировать антикоагулянты и корректировать дозу, а также осуществлять регулярный мониторинг коагуляции; [ 4 ] диетические ограничения не нужны. [ 35 ]
Нефракционированный гепарин (НФГ), низкомолекулярный гепарин (НМГ) и фондапаринукс также ингибируют активность фактора Ха косвенно, связываясь с циркулирующим антитромбином (АТ III), и их необходимо вводить инъекционно, тогда как перорально активные варфарин , фенпрокумон и аценокумарол являются антагонистами витамина К (АВК), снижающими ряд факторов свертывания крови, в том числе фактор Х. [ 36 ]
Ривароксабан имеет предсказуемую фармакокинетику у широкого спектра пациентов (возраст, пол, вес, раса) и имеет равномерный ответ на дозу в восьмикратном диапазоне доз (5–40 мг). [ 37 ] Пероральная биодоступность зависит от дозы. [ 5 ] Дозы ривароксабана менее 10 мг можно принимать независимо от приема пищи, поскольку он обладает высокой биодоступностью независимо от того, употреблялась пища или нет. [ 38 ] Если ривароксабан назначается перорально в дозе 15 мг или 20 мг, его необходимо принимать во время еды, чтобы улучшить всасывание препарата и достичь соответствующей биодоступности (≥ 80%). [ 38 ]
Химия
[ редактировать ]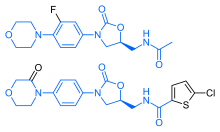
Ривароксабан имеет поразительное структурное сходство с антибиотиком линезолидом : оба препарата имеют одинаковую базовую структуру, производную оксазолидинона . [ 39 ] Соответственно, ривароксабан изучался на предмет возможных антимикробных эффектов и возможности митохондриальной токсичности , которая является известным осложнением длительного применения линезолида. [ 40 ] Исследования показали, что ни ривароксабан, ни его метаболиты не оказывают антибиотического действия в отношении грамположительных бактерий . [ нужна ссылка ] Что касается митохондриальной токсичности, исследования in vitro , опубликованные до 2008 года, показали, что риск низкий. [ 39 ]
История
[ редактировать ]Ривароксабан изначально был разработан компанией Bayer . [ 41 ] В США его продает компания Janssen Pharmaceuticals (часть Johnson & Johnson ). [ 41 ] Это был первый доступный прямой ингибитор фактора Ха , который принимают внутрь. [ 42 ]
Общество и культура
[ редактировать ]
Экономика
[ редактировать ]использование ривароксабана вместо варфарина обходится в 70 раз дороже. По данным Express Scripts Holding Co, крупнейшего менеджера по льготам в аптеках США, [ 35 ] По состоянию на 2016 год компания Bayer утверждала, что препарат лицензирован в 130 странах и что лечение прошли более 23 миллионов пациентов. [ 43 ]
Юридический статус
[ редактировать ]В сентябре 2008 года Министерство здравоохранения Канады выдало разрешение на продажу ривароксабана для предотвращения венозной тромбоэмболии (ВТЭ) у людей, перенесших плановую операцию по полной замене тазобедренного сустава или полной замене коленного сустава . [ 44 ]
В том же месяце Европейская комиссия также выдала регистрационное удостоверение на ривароксабан для предотвращения венозной тромбоэмболии у взрослых, перенесших плановую замену тазобедренного и коленного суставов. [ 45 ] [ 6 ]
США В июле 2011 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило ривароксабан для профилактики тромбоза глубоких вен (ТГВ), который может привести к тромбоэмболии легочной артерии (ЛЭ), у взрослых, перенесших операцию по замене тазобедренного и коленного суставов. [ 46 ]
США В ноябре 2011 года FDA одобрило ривароксабан для профилактики инсульта у людей с неклапанной фибрилляцией предсердий . [ 47 ]
Судебный иск
[ редактировать ]25 марта 2019 года более 25 000 исков по поводу ривароксабана в США были урегулированы на сумму 775 миллионов долларов для выплаты пострадавшим. Истцы обвинили производителей лекарств в том, что они не предупредили о риске кровотечения, утверждая, что их травм можно было бы предотвратить, если бы врачам и пациентам была предоставлена адекватная информация. [ 48 ]
Исследовать
[ редактировать ]Исследователей из Института клинических исследований Дьюка обвинили в сокрытии клинических данных, используемых для оценки ривароксабана. [ 49 ] Дюк протестировал ривароксабан в клиническом исследовании, известном как исследование ROCKET AF. [ 50 ] Клиническое исследование, опубликованное в 2011 году в Медицинском журнале Новой Англии. [ 51 ] и возглавляемый Робертом Калифом , тогдашним комиссаром FDA, [ 52 ] обнаружили, что ривароксабан более эффективен, чем варфарин, в снижении вероятности ишемических инсультов у пациентов с фибрилляцией предсердий. [ 51 ] Достоверность исследования была поставлена под сомнение в 2014 году, когда фармацевтические спонсоры Bayer и Johnson & Johnson обнаружили, что используемые устройства для мониторинга крови INRatio не функционировали должным образом. [ 49 ] [ 50 ] Последующий анализ, проведенный командой Duke, опубликованный в феврале 2016 года, показал, что это не оказало существенного влияния на эффективность и безопасность исследования. [ 53 ]
Отмечается недостаточная представленность расовых меньшинств в клинических исследованиях. [ нужна ссылка ]
Ссылки
[ редактировать ]- ^ Jump up to: а б «Использование ривароксабана во время беременности» . Наркотики.com . Проверено 3 марта 2019 г.
- ^ «Список всех лекарств с предупреждениями о черном ящике, полученный FDA (используйте ссылки «Загрузить полные результаты» и «Просмотреть запрос»).» . nctr-crs.fda.gov . FDA . Проверено 22 октября 2023 г.
- ^ Ксарелто (Bayer Australia Ltd)
- ^ Jump up to: а б с д и ж г «Ксарелто 2,5 мг таблетки, покрытые пленочной оболочкой. Краткое описание характеристик продукта (SmPC)» . (эмс) . 9 августа 2022 г. . Проверено 9 ноября 2022 г.
- ^ Jump up to: а б с «Таблетка Ксарелто-ривароксабана, покрытая пленочной оболочкой Таблетка Ксарелто-ривароксабана, набор Ксарелто-ривароксабана, покрытый пленочной оболочкой» . ДейлиМед . Проверено 13 ноября 2020 г.
- ^ Jump up to: а б «Ксарелто ЭПАР» . Европейское агентство лекарственных средств (EMA) . 17 сентября 2018 года . Проверено 13 ноября 2020 г.
- ^ Абдулсаттар Ю., Бхамбри Р., Ногид А. (май 2009 г.). «Ривароксабан (ксарелто) для профилактики тромбоэмболических заболеваний: взгляд изнутри на пероральный прямой ингибитор фактора Ха» . П& Т 34 (5): 238–44. ПМК 2697099 . ПМИД 19561868 .
- ^ Jump up to: а б с д и ж «Ривароксабан Монография для профессионалов» . Наркотики.com . Американское общество фармацевтов систем здравоохранения . Проверено 3 марта 2019 г.
- ^ Кисер К. (2017). Пероральная антикоагулянтная терапия: случаи и клиническая корреляция . Спрингер. п. 11. ISBN 9783319546438 .
- ^ «Доступность генерика Ксарелто» . Наркотики.com . Проверено 9 мая 2017 г.
- ^ «Оранжевая книга: одобренные лекарственные препараты, прошедшие оценку терапевтической эквивалентности» . www.accessdata.fda.gov . Проверено 24 апреля 2019 г.
- ^ «Bayer, J&J выиграли решение, подтверждающее патент на препарат Ксарелто» . 22 апреля 2019 г. Проверено 24 апреля 2019 г.
- ^ Всемирная организация здравоохранения (2021 г.). Примерный список основных лекарственных средств Всемирной организации здравоохранения: 22-й список (2021 г.) . Женева: Всемирная организация здравоохранения. hdl : 10665/345533 . ВОЗ/MHP/HPS/EML/2021.02.
- ^ «Топ-300 2021 года» . КлинКальк . Архивировано из оригинала 15 января 2024 года . Проверено 14 января 2024 г.
- ^ «Ривароксабан – Статистика применения препарата» . КлинКальк . Проверено 14 января 2024 г.
- ^ Ловенстерн А., Аль-Хатиб С.М., Шаран Л., Чаттерджи Р., Аллен ЛаПойнт Н.М., Шах Б. и др. (декабрь 2018 г.). «Вмешательства по предотвращению тромбоэмболических осложнений у пациентов с фибрилляцией предсердий: систематический обзор» . Анналы внутренней медицины . 169 (11): 774–787. дои : 10.7326/M18-1523 . ПМЦ 6825839 . ПМИД 30383133 .
- ^ Гомес-Оутес А., Терлейра-Фернандес А.И., Кальво-Рохас Г., Суарес-Хеа М.Л., Варгас-Кастрильон Э. (2013). «Дабигатран, ривароксабан или апиксабан по сравнению с варфарином у пациентов с неклапанной фибрилляцией предсердий: систематический обзор и метаанализ подгрупп» . Тромбоз . 2013 : 640723. doi : 10.1155/2013/640723 . ПМЦ 3885278 . ПМИД 24455237 .
- ^ «Ривароксабан для лечения тромбоза глубоких вен и профилактики рецидивов тромбоза глубоких вен и тромбоэмболии легочной артерии» . Национальный институт здравоохранения и передового опыта (NICE) . 25 июля 2012 года . Проверено 1 января 2020 г.
- ^ Jump up to: а б Шейх М.А., Конг X, Хеймарт Б, Каатц С, Крол Г, Козловски Дж и др. (июль 2021 г.). «Сравнение временного перерыва с продолжением приема прямых пероральных антикоагулянтов при процедурах с низким риском кровотечения» . Исследование тромбоза . 203 : 27–32. doi : 10.1016/j.thromres.2021.04.006 . ПМЦ 8225570 . ПМИД 33906063 .
- ^ Jump up to: а б Дукетис Дж.Д., Спиропулос А.С., Дункан Дж., Кэрриер М., Ле Гал Г., Тафур А.Дж. и др. (ноябрь 2019 г.). «Периоперационное ведение пациентов с фибрилляцией предсердий, получающих прямой пероральный антикоагулянт» . JAMA Внутренняя медицина . 179 (11): 1469–1478. doi : 10.1001/jamainternmed.2019.2431 . ПМК 6686768 . ПМИД 31380891 .
- ^ Муек В., Кубица Д., Бека М. (сентябрь 2013 г.). «Совместное применение ривароксабана с препаратами, которые имеют одинаковые пути выведения: фармакокинетические эффекты у здоровых людей» . Британский журнал клинической фармакологии . 76 (3): 455–466. дои : 10.1111/bcp.12075 . ПМЦ 3769672 . ПМИД 23305158 .
- ^ Jump up to: а б с Ханиган С., Дас Дж., Пог К., Барнс Г.Д., член парламента Дорша (май 2020 г.). «Реальное применение комбинации P-гликопротеина и умеренных ингибиторов CYP3A4 с ривароксабаном или апиксабаном увеличивает кровотечение». Журнал тромбозов и тромболизиса . 49 (4): 636–643. дои : 10.1007/s11239-020-02037-3 . ПМИД 31925665 .
- ^ «Справочник по лекарствам – Ксарелто» (PDF) . Управление по контролю за продуктами и лекарствами США . Проверено 1 сентября 2014 г.
- ^ «Побочные эффекты Ксарелто» . ВебМД . Проверено 1 сентября 2014 г.
- ^ «Центр побочных эффектов Ксарелто» . RxList . Проверено 1 сентября 2014 г.
- ^ Раши Э., Полуцци Э., Кочи А., Сальво Ф., Париенте А., Биселли М. и др. (август 2015 г.). «Повреждение печени новыми пероральными антикоагулянтами: оценка постмаркетинговых отчетов в системе отчетности о нежелательных явлениях Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США» . Британский журнал клинической фармакологии . 80 (2): 285–93. дои : 10.1111/bcp.12611 . ПМК 4541976 . ПМИД 25689417 .
- ^ Руссман С., Нидриг Д.Ф., Будмигер М., Шмидт С., Штигер Б., Хюрлиманн С. и др. (август 2014 г.). «Постмаркетинговый риск повреждения печени ривароксабаном» (PDF) . Журнал гепатологии . 61 (2): 293–300. дои : 10.1016/j.jhep.2014.03.026 . ПМИД 24681117 .
- ^ Шредер К. «ISMP считает Ксарелто самым опасным препаратом в Соединенных Штатах» . Новости о наркотиках . Проверено 10 августа 2016 г.
- ^ Шредер К. «Возможное противоядие может помочь пациентам с разжижением крови при кровотечениях» . Новости о наркотиках . Проверено 20 августа 2015 г.
- ^ Мо Ю, Ям ФК (февраль 2015 г.). «Последние достижения в разработке специфических антидотов для пероральных антикоагулянтов целевого действия». Фармакотерапия . 35 (2): 198–207. дои : 10.1002/фар.1532 . ПМИД 25644580 . S2CID 22593448 .
- ^ «Ускоренное одобрение AndexXa» (PDF) . FDA . Проверено 1 августа 2018 г.
- ^ «FDA США одобрило Andexxa компании Portola Pharmaceuticals, первое и единственное противоядие для отмены действия ингибиторов фактора Ха» (пресс-релиз). Portola Pharmaceuticals Inc., 4 мая 2018 г. Получено 1 августа 2018 г. - через GlobeNewswire.
- ^ Рериг С., Штрауб А., Полманн Дж., Лампе Т., Пернерсторфер Дж., Шлеммер К.Х. и др. (сентябрь 2005 г.). «Открытие нового антитромботического агента 5-хлор-N-({(5S)-2-оксо-3-[4-(3-оксоморфолин-4-ил)фенил]-1,3-оксазолидин-5-ил} метил)тиофен-2-карбоксамид (BAY 59-7939): пероральный прямой ингибитор фактора Ха». Журнал медицинской химии . 48 (19): 5900–8. дои : 10.1021/jm050101d . ПМИД 16161994 .
- ^ Анселл Дж. (январь 2019 г.). «Амбулаторная пероральная антикоагулянтная терапия». Консультативный гемостаз и тромбоз (Четвертое изд.). Эльзевир. стр. 747–777. дои : 10.1016/B978-0-323-46202-0.00037-6 . ISBN 978-0-323-46202-0 . S2CID 80951298 .
- ^ Jump up to: а б Беркрот Б (23 декабря 2015 г.). «Новое противоядие, разжижающее кровь, поможет врачам отказаться от варфарина» . Рейтер.
- ^ Turpie AG (январь 2008 г.). «Новые пероральные антикоагулянты при фибрилляции предсердий» . Европейский кардиологический журнал . 29 (2): 155–65. doi : 10.1093/eurheartj/ehm575 . ПМИД 18096568 .
- ^ Эрикссон Б.И., Боррис Л.К., Даль О.Е., Хаас С., Хьюсман М.В., Каккар А.К. и др. (ноябрь 2006 г.). «Пероральный прямой ингибитор фактора Ха ривароксабан (BAY 59-7939) для приема один раз в день для тромбопрофилактики после тотального эндопротезирования тазобедренного сустава» . Тираж . 114 (22): 2374–2381. дои : 10.1161/тираж.106.642074 . ПМИД 17116766 .
- ^ Jump up to: а б Стампфусс Дж., Кубица Д., Бека М., Муек В. (июль 2013 г.). «Влияние еды на всасывание и фармакокинетику ривароксабана». Международный журнал клинической фармакологии и терапии . 51 (7): 549–561. дои : 10.5414/CP201812 . ПМИД 23458226 .
- ^ Jump up to: а б Европейское агентство по лекарственным средствам (2008). «Отчет об оценке ТЭЦ для Xarelto (EMEA/543519/2008)» (PDF) . Проверено 11 июня 2009 г. [ постоянная мертвая ссылка ]
- ^ Сингх А.К., Норонха В., Гупта А., Сингх Д., Сингх П., Сингх А. и др. (2020). «Ривароксабан: Обзор препарата» . Лечение рака Res Stat . 3 (2): 264–269. дои : 10.4103/CRST.CRST_122_19 . S2CID 220129323 .
- ^ Jump up to: а б «История одобрения Ксарелто FDA» . 7 сентября 2020 г.
- ^ Фассиадис Н. (декабрь 2009 г.). «Ривароксабан, первый пероральный прямой ингибитор фактора Ха». Экспертное заключение по фармакотерапии . 10 (18): 2945–2946. дои : 10.1517/14656560903413559 . ПМИД 19925048 . S2CID 23498967 .
- ^ «Комментарий компании Bayer к статье в Британском медицинском журнале (BMJ) о Ксарелто» (PDF) . Bayer AG Коммуникации, отношения с государственными органами и корпоративный бренд. 29 сентября 2016 г. Архивировано из оригинала (PDF) 31 января 2017 г. . Проверено 19 января 2017 г.
- ^ «Ксарелто компании Bayer одобрен в Канаде» (пресс-релиз). Байер . 16 сентября 2008 года . Проверено 31 января 2010 г.
- ^ «Новый антикоагулянт Ксарелто компании Bayer теперь также одобрен в ЕС» (пресс-релиз). Байер . 10 февраля 2008 года. Архивировано из оригинала 22 октября 2008 года . Проверено 31 января 2010 г.
- ^ «FDA одобрило Ксарелто (таблетки ривароксабана) для предотвращения тромбоза глубоких вен у пациентов, перенесших операцию по замене коленного или тазобедренного сустава» (пресс-релиз). Янсен Фармацевтика . 1 июля 2011 года. Архивировано из оригинала 5 ноября 2011 года . Проверено 1 июля 2011 г.
- ^ «FDA одобрило Ксарелто для предотвращения инсульта у людей с распространенным типом нарушения сердечного ритма» . Ассоциация пищевых продуктов и лекарств США . 4 ноября 2011 г. Проверено 27 апреля 2016 г.
- ^ «Bayer, Johnson & Johnson урегулировала более 25 000 исков по поводу препарата для разжижения крови Ксарелто на сумму 775 миллионов долларов» . Вашингтон Пост . Проверено 7 апреля 2019 г.
- ^ Jump up to: а б Томас К. (1 марта 2016 г.). «Документ утверждает, что производители лекарств обманули ведущий медицинский журнал» . Нью-Йорк Таймс . Проверено 3 мая 2016 г.
- ^ Jump up to: а б Патель В. «Клинические испытания Дьюка по делу о наркотиках находятся под пристальным вниманием» . Хроника . Студенческое издательство Duke.
- ^ Jump up to: а б Патель М.Р., Махаффи К.В., Гарг Дж., Пан Дж., Сингер Д.Э., Хак В. и др. (сентябрь 2011 г.). «Ривароксабан по сравнению с варфарином при неклапанной фибрилляции предсердий» . Медицинский журнал Новой Англии . 365 (10): 883–891. дои : 10.1056/NEJMoa1009638 . ПМЦ 3860773 . ПМИД 21830957 .
- ^ «Знакомьтесь, Роберт М. Калифф, доктор медицинских наук, комиссар по контролю за продуктами и лекарствами» . Управление по контролю за продуктами и лекарствами США . Архивировано из оригинала 15 мая 2016 года . Проверено 3 мая 2016 г.
- ^ Патель М.Р., Хеллкамп А.С., Фокс К.А. (февраль 2016 г.). «Мониторинг варфарина в месте оказания медицинской помощи в исследовании ROCKET AF» . Медицинский журнал Новой Англии . 374 (8): 785–8. дои : 10.1056/NEJMc1515842 . hdl : 20.500.11820/69b742f0-5b6d-4f54-93a5-98a1da909653 . ПМИД 26839968 .