Бифторид аммония
| |||
 | |||
 | |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Бифторид аммония | |||
Другие имена
| |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.014.252 | ||
| Номер ЕС |
| ||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
| Число | 1727 | ||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| [NH 4 ][HF 2 ] | |||
| Молярная масса | 57.044 g·mol −1 | ||
| Появление | Бесцветные кристаллы | ||
| Плотность | 1,50 г см −3 | ||
| Температура плавления | 126 ° С (259 ° F, 399 К) | ||
| Точка кипения | 240 ° C (464 ° F, 513 К) (разлагается) | ||
| 63г/(100 мл) (20 °С) | |||
| Растворимость в спирте | слабо растворим | ||
Показатель преломления ( n D ) | 1.390 | ||
| Структура | |||
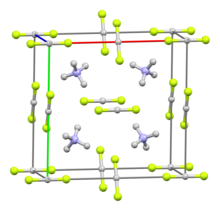
| Кубический, связанный со CsCl. структурой | |||
| [НХ 4 ] + катион: тетраэдрический [ВЧ 2 ] − анион: линейный | |||
| Опасности | |||
| СГС Маркировка : | |||
  [1] [1] | |||
| Х301 , Х314 [1] | |||
| П280 , П301+П310 , П305+П351+П338 , П310 [1] | |||
| NFPA 704 (огненный алмаз) | |||
| Родственные соединения | |||
Другие катионы | бифторид калия | ||
Родственные соединения | фторид аммония | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Бифторид аммония — неорганическое соединение формулы [NH 4 ][HF 2 ] или [NH 4 ]F·HF . Его производят из аммиака и фторида водорода . Эта бесцветная соль является средством для травления стекла и промежуточным продуктом на некогда предполагаемом пути получения плавиковой кислоты .
Структура
[ редактировать ]Бифторид аммония, как следует из названия, содержит аммония катион ( [НХ 4 ] + ) и бифторида или водорода (дифторида) анион ( [ВЧ 2 ] − ). Центросимметричный трехатомный бифторид-анион имеет самую прочную из известных водородных связей с длиной F - H 114 пм. [2] и энергия связи более 155 кДж/моль. [3]
В твердом состоянии [NH 4 ][HF 2 ] , каждый катион аммония окружен четырьмя фторидными центрами в тетраэдре, причем водородно-фтористые водородные связи . между атомами водорода иона аммония и атомами фтора присутствуют [4] [5] Растворы содержат тетраэдрические [НХ 4 ] + катионы и линейные [ВЧ 2 ] − анионы.
Производство и применение
[ редактировать ]Бифторид аммония входит в состав некоторых травителей. Он разъедает кремнеземный компонент стекла:
Бифторид калия является родственным, более часто используемым травителем.
Бифторид аммония рассматривался как промежуточный продукт при производстве плавиковой кислоты из гексафторкремниевой кислоты . Таким образом, гексафторкремниевая кислота гидролизуется с образованием фторида аммония, который термически разлагается с образованием бифторида:
- H 2 [SiF 6 ] + 6 NH 3 + 2 H 2 O → SiO 2 + 6 [NH 4 ]F
- 2 [NH 4 ]F → NH 3 + [NH 4 ][HF 2 ]
Полученный бифторид аммония преобразуется в бифторид натрия , который термически разлагается с выделением HF. [6]
Бифторид аммония также используется в качестве добавки в процессах никелирования оловом, поскольку ион фтора действует как комплексообразователь с оловом, что позволяет лучше контролировать полученный состав и качество отделки.
Токсичность
[ редактировать ]Бифторид аммония токсичен для употребления и вызывает коррозию кожи. промыть ее водой с последующей обработкой глюконатом кальция . При попадании на кожу необходимо [1] В воде бифторид аммония находится в химическом равновесии с плавиковой кислотой , и при нагревании выделяется газообразный фтороводород . [7] Следовательно, существует такой же токсикологический риск, как и при использовании плавиковой кислоты, и применяются те же меры предосторожности. [8] [7]
Бифторид аммония используется в некоторых средствах для чистки автомобильных колес. Многие травмы привели к тому, что пользователи не знали о рисках, связанных с продуктами. [9] Продукты на основе бифторида аммония часто считаются более безопасной альтернативой плавиковой кислоте, однако они по-прежнему представляют явный риск для обслуживающего персонала. [8] как «слишком опасные для любого использования в условиях автомойки» Бифторид аммония, фторид аммония и плавиковая кислота были описаны журналом Professional Car Washing and Detailing . [10] Рекомендации, соответствующие отчету Центров по контролю и профилактике заболеваний США за 2015 год . [11]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д Sigma-Aldrich Co. , Бифторид аммония . Проверено 20 июля 2013 г.
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Эмсли, Дж. (1980) Очень сильные водородные связи , Обзоры химического общества, 9, 91–124. два : 10.1039/CS9800900091
- ^ Макдональд, TRR (1960). «Распределение электронной плотности в бифториде аммония» . Акта Кристаллогр. 13 (2): 113–124. Бибкод : 1960AcCry..13..113M . дои : 10.1107/S0365110X60000261 .
- ^ «Запись ICSD: 14140» . Кембриджская структурная база данных : Структуры доступа . Кембриджский центр кристаллографических данных . Проверено 25 июня 2022 г.
- ^ Эгеперс, Жан; Моллард, Поль; Девильерс, Дидье; Чемла, Мариус; Фарон, Роберт; Романо, Рене; Куэр, Жан Пьер (2000). «Соединения фтора неорганические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley VCH. дои : 10.1002/14356007.a11_307 . ISBN 3527306730 .
- ^ Jump up to: а б Национальная система уведомления и оценки промышленных химикатов (17 апреля 2020 г.). «Бифториды: оценка уровня II здоровья человека» (PDF) . Министерство здравоохранения (Австралия) . Проверено 8 февраля 2023 г.
- ^ Jump up to: а б Дженуино, Гомер К.; Опембе, Нафтали Н.; Ньяги, Эрик С.; Макклейн, Скай; Суиб, Стивен Л. (2012). «Обзор плавиковой кислоты и ее применения в автомойке» . Журнал промышленной и инженерной химии . 18 (5): 1529–1539. дои : 10.1016/j.jiec.2012.03.001 . ISSN 1226-086X .
- ^ Гормли, Джеймс (29 мая 2001 г.). «Правда о бифториде аммония» . Профессиональная мойка и детейлинг автомобилей . Архивировано из оригинала 29 мая 2001 г.
- ^ Кук, Райан (9 октября 2013 г.). «Пять факторов чистоты: химия, часть 1» . Профессиональная мойка и детейлинг автомобилей . Проверено 8 февраля 2023 г.
- ^ Вуди, Мария (1 декабря 2015 г.). «OSHA дает сотрудникам право знать» . Профессиональная мойка и детейлинг автомобилей . Проверено 8 февраля 2023 г.


