Ксилон
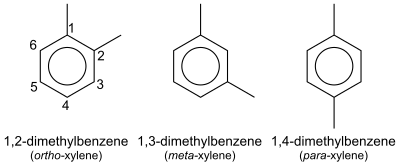
В органической химии , ксилол или ксилол (от греческого ξύλον (Xylon) 'дерево'; [ 1 ] [ 2 ] Имя IUPAC : диметилбензол ) - это любое из трех органических соединений с формулой (Ch 3 ) 2 C 6 H 4 . Они получены из замены двух водорода атомов метильными группами в бензоловое кольцо; которые заменяют гидрогины, определяет, какой из трех структурных изомеров . Это бесцветная, легковоспламеняющаяся, слегка жирная жидкость с большой промышленной ценностью. [ 3 ]
Смесь называют как ксилол, так и, точнее, ксилен. Смешанные ксилены относятся к смесью ксилена плюс этилбензол . Четыре соединения имеют идентичные молекулярные формулы C 8 H 10 . Как правило, четыре соединения производятся различными методами каталитического реформирования и пиролиза . [ 4 ]
Появление и производство
[ редактировать ]Ксильены являются важным нефтехимическим, производимым каталитическим реформированием , а также карбонизацией угля при изготовлении коксового топлива . Они также встречаются в сырой нефти в концентрациях около 0,5–1%, в зависимости от источника. Небольшие количества встречаются в бензине и самолете .
Ксилины производятся в основном в рамках ароматики BTX ( бензол , толуол и ксилен), извлеченного из продукта каталитического реформирования , известного как Reformate .
Ежегодно производится несколько миллионов тонн. [ 3 ] В 2011 году глобальный консорциум начал строительство одного из крупнейших в мире ксиловых заводов в Сингапуре . [ 5 ]
История
[ редактировать ]Ксилол был первым изолирован и назван в 1850 году французским химиком Огюстом Кахуром (1813–1891), который был обнаружен в качестве составляющей деревянной смолы . [ 6 ]
Промышленное производство
[ редактировать ]продуцируются метилированием толуола бензола и . Ксиловые [ 3 ] [ 7 ] Коммерческий или лабораторный ксилол, продуцированный, обычно содержит около 40–65% м -ксилола и до 20% каждый из о ксилол , P -ксилол и этилбензола . [ 8 ] [ 9 ] [ 10 ] Соотношение изомеров может быть сдвинуто, чтобы поддержать высоко оцененный p -ксилол через запатентованный Uop -изомара процесс [ 11 ] или путем трансалкилирования ксилола с собой или триметилбензола. Эти конверсии катализируются цеолитами . [ 3 ]
ZSM-5 используется для облегчения некоторых реакций изомеризации, ведущих к массовому производству современных пластмасс.
Характеристики
[ редактировать ]Физические свойства изомеров ксилола немного отличаются. Точка плавления колеблется от -47,87 ° C (-54,17 ° F) ( м -ксилол) до 13,26 ° C (55,87 ° F) ( P -ксилол) -как обычно, точка плавления Para Isomer намного выше, потому что она больше упаковывает легко в кристаллической структуре. Точка кипения для каждого изомера составляет около 140 ° C (284 ° F). Плотность каждого изомера составляет около 0,87 г/мл (7,3 фунта/США Гал; 8,7 фунта/им. Гал) и, следовательно, менее плотная, чем вода . Запах ксилола обнаруживается в концентрациях от 0,08 до 3,7 ч / млн (части ксилола на миллион частей воздуха) и может быть вкусом в воде при 0,53 до 1,8 ч / млн. [ 9 ]
| Ксиловые изомеры | ||||
|---|---|---|---|---|
| Общий | ||||
| Общее название | Ксилон (смесь) |
o -sylene | м -ксилен | П -силен |
| Систематическое название | Диметилбензол | 1,2-диметилбензол | 1,3-диметилбензол | 1,4-диметилбензол |
| Другие имена | Ксилол | o -sylol? Ортоксилен |
м -силол; Метаксилен |
p -ксилол; Параксилен |
| Молекулярная формула | C 8 H 10 | |||
| Улыбается | CC1C (C) CCCC1 | CC1CC (C) CCC1 | CC1CCC (C) CC1 | |
| Молярная масса | 106.16 g/mol | |||
| Появление | Чистая, бесцветная жидкость | |||
| Номер CAS | [1330-20-7] | [95-47-6] | [108-38-3] | [106-42-3] |
| Характеристики | ||||
| Плотность и фаза | 0,864 г/мл, жидкость | 0,88 г/мл, жидкость | 0,86 г/мл, жидкость | 0,86 г/мл, жидкость |
| Растворимость в воде | Практически нерастворим | |||
| Растворим в неполярных растворителях, таких как ароматические углеводороды | ||||
| Точка плавления | −47,4 ° C (-53,3 ° F; 226 K) | −25 ° C (-13 ° F; 248 K) | −48 ° C (-54 ° F; 225 K) | 13 ° C (55 ° F; 286 K) |
| Точка кипения | 138,5 ° C (281,3 ° F; 412 K) | 144 ° C (291 ° F; 417 K) | 139 ° C (282 ° F; 412 K) | 138 ° C (280 ° F; 411 K) |
| Вязкость | 0,812 C P и 20 ° C (68 ° F) | 0,62 C P и 20 ° C (68 ° F) | 0,34 C P и 30 ° C (86 ° F) | |
| Опасности | ||||
| SDS | Ксилон | o -sylene | м -ксилен | П -силен |
| ЕС пиктограммы |   
| |||
| NFPA 704 | ||||
| точка возгорания | 30 ° C (86 ° F) | 17 ° C (63 ° F) | 25 ° C (77 ° F) | 25 ° C (77 ° F) |
| H & P Фразы | H225 , H226 , H304 , H312 , H315 , H319 , H332 , H335 , H412 P210 , P233 , P240 , P241 , P242 , P243 , P261 , P264 , P271 , P273 , P280 , P301+P310, P302+P352 , P303+P361+P353 , P304+P312, P304+P340, P305+P355, P304, P312, P304+P340, P305+P351+P355 , P353, P304+P312, P304+P340, P361+P353, P304 +P312, P304+P3051+P353 , P304+P312 , P304+P361+P353, P304+P312, P304+P361+P353 , P304 . P312 , P321 , P322 , P331 , P332+P313 , P337+P313 , P362 , P363 , P370+P378 , P403+P233 , P403+P235 , P405 , P501 | |||
| Rtecs номер | ZE2450000 | ZE2275000 | ZE2625000 | |
| Связанные соединения | ||||
| Связанный аромат углеводороды |
Толуол , мезитилен , бензол , этилбензол | |||
| Связанные соединения | Ксилонолы - типы фенолов | |||
| За исключением случаев, если отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C, 100 кПа) Отказ от ответственности Infobox и ссылки | ||||
Ксиловые образуют азеотропы с водой и разнообразными спиртами. Азеотроп с водой состоит из 60% ксилена и кипит при 94,5 ° C. [ 3 ] Как и во многих соединениях алкилбензола , ксиловые образуют комплексы с различными галоглезонами . [ 12 ] Комплексы разных изомеров часто обладают резко различными свойствами друг от друга. [ 13 ]
Приложения
[ редактировать ]Терефталевая кислота и связанные производные
[ редактировать ]P -ксилен является основным предшественником терефталевой кислоты и диметилтерефталата , оба мономеры, используемые при производстве полиэтилентерефталатных (PET) пластиковых бутылок и полиэфирной одежды. 98% производства P -ксилона, и половина всех произведенных ксилен потребляется таким образом. [ 10 ] [ 14 ] O -ксилол является важным предшественником фталического ангидрида . Потребность в изофталевой кислоте относительно скромна, поэтому м -ксилол редко искал (и, следовательно, полезность его преобразования в O -и P -изомеры).
Применение растворителя и промышленные цели
[ редактировать ]Xylenes используются в качестве растворителя в печати , резине и кожаной промышленности. Это общий компонент чернил, резины и клея . [ 15 ] В истончении красок и лаков можно заменить толуол , где требуется более медленная сушка, и, таким образом, используется консерваторами художественных объектов в тестировании растворимости. [ 16 ] Точно так же это чистящий агент , например, для стали , кремниевых пластин и интегрированных цепей . В стоматологии можно использовать ксилол для растворения Gutta Percha , материала, используемого для эндодонтики (обработки корневого канала). В нефтяной промышленности ксилол также является частым компонентом парафиновых растворителей, используемых, когда трубка забивается парафиновым воском.
Лабораторное использование
[ редактировать ]Ксилол используется в лаборатории, чтобы сделать ванны с сухим льдом в прохладные реакционные сосуды, [ 17 ] и в качестве растворителя для удаления синтетического погружного масла микроскопа из объектива в световой микроскопии . [ 18 ] В гистологии ксилол является наиболее широко используемым клирент -агентом. [ 19 ] Ксилол используется для удаления парафина из сушеного микроскопа слайдов перед окрашиванием. После окрашивания слайды микроскопа помещают в ксилол перед установкой с помощью покровного стекла.
Предшественник других соединений
[ редактировать ]В одном крупномасштабном применении парасилен превращается в терефталевую кислоту . Основное применение ортосилола является предшественником фталатных сложных эфиров , используемых в качестве пластификатора . Мета-ксилен превращается в производные изофталевой кислоты , которые являются компонентами алкидных смол . [ 3 ]
Химические свойства
[ редактировать ]Как правило, два вида реакций встречаются с ксиленом: те, которые с участием метильных групп и те, которые связаны с связками C -H кольцо. Будучи бензилическим и, следовательно, ослабленным, связи C-H метильных групп подвержены свободно радикальным реакциям, включая галогенирование с соответствующими ксилололоридами (BIS (хлорметил) бензонов), в то время как монобрейн дает Xylyl бромид , слезоточный газовый агент) Полем Окисление и аммиксидирование также нацелены на метильные группы, обеспечивая дикарбоновые кислоты и динитрилы. Электрофилы атакуют ароматическое кольцо, что приводит к хлор- и нитроксилену. [ 3 ]
Здоровье и безопасность
[ редактировать ]Ксилол воспламеняется, но скромной острой токсичности, с диапазонами 50 от 200 до 5000 мг/кг для животных. Oral LD 50 для крыс составляет 4300 мг/кг. Основным механизмом детоксикации является окисление до метилбензойной кислоты и гидроксилирование до гидроксилена. [ 3 ]
Основным эффектом вдыхания ксилолового пара является депрессия центральной нервной системы (ЦНС), с такими симптомами, как головная боль, головокружение, тошнота и рвота. При воздействии 100 ppm можно испытать тошноту или головную боль. При воздействии от 200 до 500 ч / млн симптомы могут включать ощущение «высокого», головокружения, слабости, раздражительности, рвоты и замедленного времени реакции. [ 20 ] [ 21 ]
Побочные эффекты воздействия низких концентраций ксилола ( <200 ppm ) обратимы и не вызывают постоянного повреждения. Долгосрочное воздействие может привести к головным болям, раздражительности, депрессии, бессоннице, возбуждению, крайней усталости, тремор, потере слуха, нарушению концентрации и краткосрочной потерь памяти. [ 22 ] [ нужно разъяснения ] Состояние, называемое хронической энцефалопатией, индуцированной хроническим растворителем , широко известным как «синдром органического и растворителя», было связано с воздействием ксилола. Доступна очень мало информации, которая изолирует ксилол от других воздействий растворителя при изучении этих эффектов. [ 20 ]
Расстройства слуха также были связаны с воздействием ксилола, как из исследований с экспериментальными животными, [ 23 ] [ 24 ] а также клинические исследования. [ 25 ] [ 26 ] [ 27 ]
Ксилол также является раздражителем кожи и разжигает кожу масла, что делает его более проницаемой для других химических веществ. Использование непроницаемых перчаток и масок, наряду с респираторами, где это необходимо, рекомендуется избежать проблем здоровья профессионального здоровья от воздействия на ксилол. [ 20 ]
Ксильены метаболизируются на метилгиппурические кислоты . [ 28 ] [ 29 ] Присутствие метилгиппариновой кислоты может использоваться в качестве биомаркера для определения воздействия ксилола. [ 29 ] [ 30 ]
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ ξύλον . Лидделл, Генри Джордж ; Скотт, Роберт ; Грек -английский лексикон в проекте Персея .
- ^ Харпер, Дуглас. "Ксилол" . Онлайн этимологический словарь .
- ^ Jump up to: а беременный в дюймовый и фон глин час Фабри, Йорг; Грейзер, Ульрих; Мы, Томас А. (2000). "Xylenes" Энциклопедия doi : 10.1002/ 14366007.a28_4 ISBN 978-3527306732 .
- ^ Cannella, William J. (2000). «Ксильен и этилбензол». Кирк-Отмер Энциклопедия химических технологий . doi : 10.1002/0471238961.2425120503011414.a01 . ISBN 0471238961 .
- ^ Тремблей, Жан-Франсуа (2011). «Создание ароматики в Сингапуре». Архив химических и инженерных новостей . 89 (38): 18–19. doi : 10.1021/cen-v089n038.p018 .
- ^ Cahours, augue (1850) «recherches sur les huiles légéres obtenues dans la distillation du Bois» (исследования светлых масел, полученные путем дистилляции древесины), Compte rendus , 30 : 319-323; Смотрите особенно р. 321. из с. 321: «Je le désignerai sous Le Nomme Xylène ». (Я обозначу его по имени ксилола .) Примечание. Эмпирическая формула Cahours для ксилола неверна, потому что химики в то время использовали неправильную атомную массу для углерода (6 вместо 12).
- ^ Martindale, David C. и Kuchar, Paul J., Производство Xylenes из легких алифатических углеводородов посредством дегидроциклодимеризации и метилирования , патент США № 5,043 502, 1991-8-27. Доступ 2012-4-28.
- ^ «Xylene (смешанные изомеры), резюме с токсичной опасностью воздуха» . Агентство по охране окружающей среды США . Получено 8 февраля 2015 года .
- ^ Jump up to: а беременный Кандила, Рина; Raghavendra, Sumanth Phani C.; Раджасекхаран, Сарасвати Т. (2010). «Xylene: обзор его опасностей для здоровья и профилактических мер» . J Oral Maxillofac Pathol . 14 (1): 1–5. doi : 10.4103/0973-029x.64299 . PMC 2996004 . PMID 21180450 .
- ^ Jump up to: а беременный Ксилон ( архивировано 11 августа 2011 года, в машине Wayback ), шведское агентство химикатов, apps.kemi.se, 2010. Доступ к 2012-4-28.
- ^ «Понимание возможностей для производства пара -ксилола» . UOP, Honeywell Company . Получено 8 февраля 2015 года .
- ^ Кларк Дж. Люти, Р.В. (1955). «Разделение ксилен». Ind. Eng. Химический 47 (2): 250–253. doi : 10.1021/IE50542A028 .
- ^ Стивенсон, Шерил Д.; McElheny, Daniel J.; Кейдж, Дэвид Э.; Ciszewski, James T.; Reiter, Richard C. (1998). «Разделение тесно кипящих изомеров и идентично кипящих изотопомеров посредством экстракции с помощью электронного переноса». Аналитическая химия . 70 (18): 3880. DOI : 10.1021/AC980221B .
- ^ ICIS, Параксилен-Ортоксилен | Цены, анализ новостей и рынка , ICIS.com, 2012. Доступ 2012-04-28.
- ^ Бостик, Лист данных о безопасности Blu-Tack ( архивировано 11 сентября 2011 года, на The Wayback Machine ), № 13135, Bostik Corp., июнь 2007 года. Доступ 2012-04-28.
- ^ Самет, Венди, (Комп.), Приложение I, Каталог по сохранению живописи , Американский институт сохранения исторических и художественных произведений, сохранение wiki.com, сентябрь 1997 года. Доступ 2012-04-28.
- ^ "Охлаждающие ванны" . UC Davis Chem Wiki. 2013-10-02. Архивировано с оригинала 2015-02-08 . Получено 8 февраля 2015 года .
- ^ Cargille, John (1985) [1964], «Иммерсионное масло и микроскоп» , ежегодник Нью-Йоркского микроскопического общества , архивировав с оригинала 2011-09-11 , извлечен 2011-03-10
- ^ Карсон, Фрейда; Хладик, Криста (2009). Гистотехнология: самостоятельный текст (3 изд.). Американское общество клинической патологии пресса. п. 35. ISBN 9780891895817 .
- ^ Jump up to: а беременный в Кандила, Рина; Raghavendra, Sumanth Phani C.; Раджасекхаран, Сарасвати Т. (2010-01-01). «Xylene: обзор его опасностей для здоровья и профилактических мер» . Журнал устной и челюстно -лицевой патологии . 14 (1): 1–5. doi : 10.4103/0973-029x.64299 . ISSN 0973-029X . PMC 2996004 . PMID 21180450 .
- ^ «Островая токсичность Сводка: ксилен» (PDF) . Архивировано из оригинала (PDF) 22 октября 2015 года.
- ^ «Ксиловые (EHC 190, 1997)» .
- ^ Gagnaire, F.; Marignac, B.; Langlais, C.; Bonnet, P. (июль 2001 г.). «Ототоксичность у крыс, подвергшихся воздействию орто-, мета- и парасилоловых паров в течение 13 недель». Фармакология и токсикология . 89 (1): 6–14. doi : 10.1034/j.1600-0773.2001.d01-129.x (неактивный 2024-07-09). ISSN 0901-9928 . PMID 11484912 .
{{cite journal}}: CS1 Maint: doi неактивен по состоянию на июль 2024 г. ( ссылка ) - ^ Gagnaire, F.; Marignac, B.; Blachère, V.; Grossmann, S.; Langlais, C. (2007-03-07). «Роль токсикокинетики в ототоксичности, вызванной ксилолом у крыс и морской свинки». Токсикология . 231 (2–3): 147–158. doi : 10.1016/j.tox.2006.11.075 . ISSN 0300-483X . PMID 17210216 .
- ^ Фуэнте, Адриан; Макферсон, Брэдли; Cardemil, Felipe (сентябрь 2013 г.). «Слуховая дисфункция, вызванная ксилолом у людей». Ухо и слух . 34 (5): 651–660. doi : 10.1097/aud.0b013e31828d27d7 . HDL : 10533/134303 . ISSN 1538-4667 . PMID 23598724 . S2CID 45206975 .
- ^ Дрейпер, THJ; Bamiou, D.-E. (Апрель 2009 г.). «Слуховая невропатия у пациента, подвергшегося воздействию ксилола: отчет о случаях» (PDF) . Журнал ларингологии и отологии . 123 (4): 462–465. doi : 10.1017/s0022215108002399 . ISSN 1748-5460 . PMID 18439334 . Архивировано (PDF) из оригинала 2017-08-09.
- ^ Фуэнте, Адриан; Макферсон, Брэдли; Худ, Линда Дж. (Ноябрь 2012 г.). «Потеря слуха, связанная с воздействием ксилола у лабораторного работника». Журнал Американской академии аудиологии . 23 (10): 824–830. doi : 10.3766/jaaa.23.10.7 . HDL : 10533/137495 . ISSN 1050-0545 . PMID 23169198 .
- ^ «Гиппурская и метил -гиппурная кислота в моче» (PDF) . NIOSH Руководство по аналитическим методам (NMAM) (четвертое изд.).
- ^ Jump up to: а беременный Иноуэ, О.; Сейджи, К.; Kawai, T.; Watanabe, T.; Джин, C.; Cai, SX; Chen, Z.; Q, QS; Zhang, T.; Икеда, М. (1993). «Исключение метилгиппариновых кислот в моче рабочих, подвергшихся воздействию ксилольной смеси: сравнение между тремя изомерами ксилола и толуолом». Международные архивы профессионального и экологического здоровья . 64 (7): 533–539. doi : 10.1007/bf00381104 . PMID 8482596 . S2CID 21534640 .
- ^ Кира С. (1977). «Измерение газовой хроматографией мочевой гиппурной кислоты и метилгиппуриновой кислоты в качестве индексов воздействия толуола и ксилола» . Профессиональная и экологическая медицина . 34 (305–309): 305–309. doi : 10.1136/OEM.34.4.305 . PMC 1008281 . PMID 588486 .
Внешние ссылки
[ редактировать ]- Чисхолм, Хью , изд. (1911). . Encyclopædia Britannica (11 -е изд.). Издательство Кембриджского университета.
- Pocket Guide niosh к химической опасности ( O -ксилол)
- Niosh Pocket Guide по химической опасности ( м -ксилол)
- Pocket Guide niosh к химической опасности ( P -ксилол)
- Ксилол, резюме опасности (EPA) (смешанные изомеры)
- Ушные яды , Синергист , Американская ассоциация промышленной гигиены , ноябрь 2018 г.
