Глюкозо-6-фосфатаза
Борон, Уолтер Ф.; Булпаеп, Эмиль Л., ред. (2017). Медицинская физиология (3-е изд.). Филадельфия, Пенсильвания: Эльзевир. ISBN 978-1-4557-4377-3 .
| Глюкозо-6-фосфатаза. | |||
|---|---|---|---|
| Идентификаторы | |||
| Номер ЕС. | 3.1.3.9 | ||
| Номер CAS. | 9001-39-2 | ||
| Базы данных | |||
| ИнтЭнк | вид IntEnz | ||
| БРЕНДА | БРЕНДА запись | ||
| Экспаси | Просмотр NiceZyme | ||
| КЕГГ | КЕГГ запись | ||
| МетаЦик | метаболический путь | ||
| ПРЯМОЙ | профиль | ||
| PDB Структуры | RCSB PDB PDBe PDBsum | ||
| Генная онтология | АмиГО / QuickGO | ||
| |||

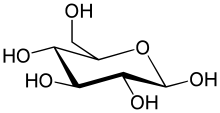
Фермент глюкозо-6-фосфатаза (EC 3.1.3.9, G6Pase ; систематическое название D -глюкозо-6-фосфатфосфогидролаза ) катализирует гидролиз глюкозо-6-фосфата , в результате чего образуется фосфатная группа и свободная глюкоза:
- D -глюкозо-6-фосфат + H 2 O = D -глюкоза + фосфат
Во время голодания адекватный уровень глюкозы в крови обеспечивается за счет глюкозы, высвобождаемой из гликогена запасов печени в результате гликогенолиза, а также глюкозы, образующейся в результате глюконеогенеза в печени, а также - в меньшей степени - в почках. G6P является продуктом обоих этих путей. [ 1 ] и должен быть преобразован в глюкозу, прежде чем ее можно будет экспортировать из клетки в кровь с помощью мембраносвязанных переносчиков глюкозы . [ 2 ] Таким образом, G6Pase в основном экспрессируется в печени и почках. [ 1 ] - хотя скелетные мышцы в совокупности содержат наиболее значительный запас гликогена в организме, глюкоза не может быть мобилизована из него, поскольку в мышцах отсутствует G6Pase. [ 3 ] : 1171
Инсулин ингибирует активность печеночной G6Pase, [ 3 ] : 1046 тогда как глюкагон способствует этому. [ 3 ] : 1052 Экспрессия G6Pase увеличивается во время голодания, диабета и приема глюкокортикостероидов . [ 1 ]
Глюкозо-6-фосфатаза представляет собой комплекс многокомпонентных белков, включая транспортеры G6P, глюкозы и фосфата. Основную функцию фосфатазы выполняет каталитическая субъединица глюкозо-6-фосфатазы. У человека существуют три изозима каталитической субъединицы: глюкозо-6-фосфатаза-α, кодируемая G6PC ; IGRP, закодированный G6PC2 ; и глюкозо-6-фосфатаза-β, кодируемая G6PC3 . [ 4 ]
Глюкозо-6-фосфатаза-α и глюкозо-6-фосфатаза-β являются функциональными фосфогидролазами и имеют сходную структуру активного центра, топологию, механизм действия и кинетические свойства в отношении гидролиза G6P. [ 5 ] Напротив, IGRP практически не обладает гидролазной активностью и может играть иную роль в стимуляции секреции инсулина поджелудочной железой. [ 6 ]



Биохимия
[ редактировать ]Хотя четкого консенсуса достичь не удалось, большое количество ученых придерживаются модели транспорта субстрата, объясняющей каталитические свойства глюкозо-6-фосфатазы. В этой модели глюкозо-6-фосфатаза обладает низкой степенью селективности. Перенос глюкозо-6-фосфата осуществляется белком-транспортером (Т1), а эндоплазматический ретикулум (ЭР) содержит структуры, обеспечивающие выход фосфатной группы (Т2) и глюкозы (Т3). [ 7 ]
Глюкозо-6-фосфатаза состоит из 357 аминокислот и прикреплена к эндоплазматической сети (ЭР) девятью трансмембранными спиралями. Его N -конец и активный сайт находятся на стороне просвета ЭР, а его С -конец выступает в цитоплазму. Из-за тесной связи с ЭР точная структура глюкозо-6-фосфатазы остается неизвестной. Однако выравнивание последовательностей показало, что глюкозо-6-фосфатаза структурно аналогична активному центру ванадийсодержащей хлорпероксидазы, обнаруженной у Curvularia inaequalis. [ 8 ]
На основании исследований рН-кинетики катализа глюкозо-6-фосфатазой-α было высказано предположение, что гидролиз глюкозо-6-фосфата завершается через ковалентное промежуточное соединение фосфогистидин-глюкозо-6-фосфат. Активный центр глюкозо-6-фосфатазы-α первоначально был идентифицирован по наличию консервативного фосфатного сигнатурного мотива, обычно обнаруживаемого в липидных фосфатазах, кислых фосфатазах и галопероксидазах ванадия. [ 5 ]
К основным остаткам в активном центре галопероксидазы ванадия относятся: Lys353, Arg360, Arg490, His404 и His496. Соответствующие остатки в активном центре глюкозо-6-фосфатазы-α включают Arg170 и Arg83, которые отдают ионы водорода фосфату, стабилизируя переходное состояние, His119, который обеспечивает протон дефосфорилированному кислороду, присоединенному к глюкозе, и His176, который завершает нуклеофильная атака фосфата с образованием ковалентно связанного промежуточного фосфорильного фермента. [ 9 ] Было обнаружено, что в составе ванадийсодержащей хлорпероксидазы Lys353 стабилизирует фосфат в переходном состоянии. Однако соответствующий остаток глюкозо-6-фосфатазы-α (Lys76) находится внутри мембраны ЭР, и его функция, если таковая имеется, в настоящее время не определена. За исключением Lys76, все эти остатки расположены на люминальной стороне мембраны ЭР. [ 5 ]
Глюкозо-6-фосфатаза-β представляет собой повсеместно экспрессируемый мембранный белок, состоящий из 346 аминокислот, который на 36% идентичн по последовательности с глюкозо-6-фосфатазой-α. Выравнивание последовательностей фермента глюкозо-6-фосфатазы-β предсказывает, что его активный сайт содержит His167, His114 и Arg79. Как и в активном центре глюкозо-6-фосфатазы-α, His167 представляет собой остаток, обеспечивающий нуклеофильную атаку, а His114 и Arg79 являются донорами водорода. Глюкозо-6-фосфатаза-β также локализована в мембране ЭР, хотя ее ориентация неизвестна. [ 5 ]
Механизм
[ редактировать ]Гидролиз глюкозо-6-фосфата начинается с нуклеофильной атаки His176 на связанный с сахаром фосфат, что приводит к образованию фосфогистидиновой связи и разрушению карбонила. Отрицательно заряженный кислород затем переносит свои электроны, образуя карбонил и разрывая его связь с глюкозой. Отрицательно заряженный кислород, связанный с глюкозой, затем протонируется His119, образуя свободную глюкозу. Фосфо-промежуточный продукт, полученный в результате реакции между His176 и фосфатной группой, затем разрушается гидрофильной атакой; после добавления другого гидроксида и разложения карбонила карбонил преобразуется, отбрасывая электроны, первоначально отданные остатком His176, тем самым создавая свободную фосфатную группу и завершая гидролиз. [ 9 ]
Выражение
[ редактировать ]Гены, кодирующие фермент, экспрессируются преимущественно в печени, коре почек и (в меньшей степени) в β-клетках островков поджелудочной железы и слизистой оболочки кишечника (особенно в период голодания). [ 7 ] Глюкозо-6-фосфатаза присутствует в самых разных мышцах животного мира, хотя и в очень низких концентрациях. [ 10 ] Таким образом, гликоген, запасаемый мышцами, обычно недоступен для остальных клеток организма, поскольку глюкозо-6-фосфат не может проникнуть через сарколемму, если он не дефосфорилирован. Фермент играет важную роль в периоды голодания и при низком уровне глюкозы. Показано, что голодание и диабет вызывают двух-трехкратное увеличение активности глюкозо-6-фосфатазы в печени. [ 7 ] Активность Glc-6-Pase также резко возрастает при рождении, когда организм становится независимым от источника глюкозы матери. Ген Glc-6-Pase человека содержит пять экзонов, охватывающих ДНК размером примерно 125,5 т.п.н., расположенных на хромосоме 17q21. [ 11 ]
Клиническое значение
[ редактировать ]Мутации системы глюкозо-6-фосфатазы, а именно субъединицы глюкозо-6-фосфатазы-α (глюкозо-6-фосфатаза-α), транспортера глюкозы-6 (G6PT) и глюкозо-6-фосфатазы-β (глюкозо-6-фосфатаза-α). Субъединицы β или G6PC3) приводят к нарушениям поддержания межпрандиального гомеостаза глюкозы , а также функции и гомеостаза нейтрофилов . [ 12 ] [ 13 ] Мутации как в глюкозо-6-фосфатазе-α, так и в G6PT приводят к болезни накопления гликогена I типа (GSD 1, болезнь фон Гирке). [ 14 ] Если быть конкретнее, мутации в глюкозо-6-фосфатазе-α приводят к болезни накопления гликогена типа 1а, которая характеризуется накоплением гликогена и жира в печени и почках, что приводит к гепатомегалии и реномегалии. [ 15 ] GSD-1a составляет примерно 80% клинических случаев GSD-1. [ 16 ] Отсутствие G6PT приводит к развитию GSD-1b (GSD-1b), который характеризуется отсутствием G6PT и составляет 20% клинических случаев. [ 16 ] [ 17 ]

Конкретная причина GSD-1a связана с нонсенс-мутациями, инсерциями/делециями со сдвигом рамки считывания или без него или мутациями сайта сплайсинга , которые происходят на генетическом уровне. [ 7 ] Миссенс-мутации затрагивают две большие просветные петли и трансмембранные спирали глюкозо-6-фосфатазы-α, устраняя или значительно снижая активность фермента. [ 7 ] Конкретная причина GSD-1b связана с «серьезными» мутациями, такими как мутации сайта сплайсинга, мутации со сдвигом рамки и замены высококонсервативного остатка, которые полностью разрушили активность G6PT. [ 7 ] Эти мутации приводят к преобладанию GSD-1, предотвращая транспорт глюкозо-6-фосфата (G6P) в просветную часть ЭР , а также ингибируя превращение G6P в глюкозу, которая будет использоваться клеткой.
Третий тип дефицита глюкозо-6-фосфатазы, дефицит глюкозо-6-фосфатазы-β, характеризуется синдромом врожденной нейтропении , при котором у нейтрофилов наблюдается повышенный стресс эндоплазматического ретикулума (ЭР), усиление апоптоза, нарушение энергетического гомеостаза и нарушение функциональности. [ 18 ] Это также может привести к порокам развития сердца и мочеполовой системы. [ 19 ] На этот третий класс дефицита также влияет дефицит G6PT, поскольку глюкозо-6-фосфатаза-β также находится в просвете ЭР и, таким образом, может приводить к симптомам, аналогичным дефициту глюкозо-6-фосфатазы-β, связанным с GSD-1b. [ 17 ] Более того, недавние исследования прояснили эту область сходства между обоими дефицитами и показали, что аберрантное гликозилирование происходит при обоих дефицитах. [ 20 ] Гликозилирование нейтрофилов оказывает глубокое влияние на активность нейтрофилов и, следовательно, также может быть классифицировано как врожденное нарушение гликозилирования. [ 20 ]
Было установлено, что основная функция глюкозо-6-фосфатазы-β заключается в обеспечении рециркулируемой глюкозы в цитоплазму нейтрофилов для поддержания нормальной функции. Нарушение соотношения глюкозы и G6P из-за значительного снижения внутриклеточного уровня глюкозы вызывает значительное нарушение гликолиза и ГМС . [ 13 ] Если этот дефицит не компенсируется поглощением внеклеточной глюкозы, он приводит к дисфункции нейтрофилов. [ 13 ]
соединения ванадия, такие как сульфат ванадил, Было показано, что ингибируют фермент и, таким образом, повышают чувствительность к инсулину in vivo у диабетиков, что оценивается с помощью гиперинсулинемического клэмп-метода , что может иметь потенциальные терапевтические последствия. [ 21 ] [ 22 ]
См. также
[ редактировать ]Примечания
[ редактировать ]Изображения молекулярной графики были получены с использованием UCSF Chimera. [ 23 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с Ван ШАФТИНГЕН, Эмиль; Герин, Изабель (15 марта 2002 г.). «Система глюкозо-6-фосфатазы» . Биохимический журнал . 362 (3): 513–532. дои : 10.1042/0264-6021:3620513 . ПМЦ 1222414 . ПМИД 11879177 .
- ^ Нордли Р. и др. (1985). Ферменты биологических мембран, 2-е издание . Нью-Йорк: Пленум Пресс. стр. 349–398. ISBN 0-306-41453-8 .
- ^ Jump up to: а б с Борон, Уолтер Ф.; Булпаеп, Эмиль Л., ред. (2017). Медицинская физиология (3-е изд.). Филадельфия, Пенсильвания: Эльзевир. ISBN 978-1-4557-4377-3 .
- ^ Хаттон Дж. К., О'Брайен Р. М. (октябрь 2009 г.). «Семейство генов каталитической субъединицы глюкозо-6-фосфатазы» . Журнал биологической химии . 284 (43): 29241–5. дои : 10.1074/jbc.R109.025544 . ПМЦ 2785553 . ПМИД 19700406 .
- ^ Jump up to: а б с д Гош А., Ши Джей Джей, Пан Си Джей, Чоу Джей (март 2004 г.). «Гистидин 167 является акцептором фосфата в глюкозо-6-фосфатазе-β, образуя промежуточный продукт фермента фосфогистидина во время катализа» . Журнал биологической химии . 279 (13): 12479–83. дои : 10.1074/jbc.M313271200 . ПМИД 14718531 .
- ^ Ши Джей-Джей, Пан Си-Джей, Мэнсфилд BC, Чоу JY (сентябрь 2005 г.). «В островково-специфическом белке, родственном глюкозо-6-фосфатазе, антигенная последовательность β-клеток, которая является мишенью при диабете, не несет ответственности за потерю активности фосфогидролазы» . Диабетология . 48 (9): 1851–9. дои : 10.1007/s00125-005-1848-6 . ПМИД 16012821 .
- ^ Jump up to: а б с д и ж ван Шафтинген Э., Герин I (март 2002 г.). «Система глюкозо-6-фосфатазы» . Биохимический журнал . 362 (Часть 3): 513–32. дои : 10.1042/0264-6021:3620513 . ПМЦ 1222414 . ПМИД 11879177 .
- ^ Пан CJ, Лей К.Дж., Аннаби Б., Хемрика В., Чоу Дж.Ю. (март 1998 г.). «Трансмембранная топология глюкозо-6-фосфатазы» . Журнал биологической химии . 273 (11): 6144–8. дои : 10.1074/jbc.273.11.6144 . ПМИД 9497333 .
- ^ Jump up to: а б Гош А., Ши Джей Джей, Пан Си Джей, Сан М. С., Чоу Дж. Ю. (сентябрь 2002 г.). «Каталитический центр глюкозо-6-фосфатазы. HIS176 представляет собой нуклеофил, образующий промежуточный продукт фосфогистидин-фермент во время катализа» . Журнал биологической химии . 277 (36): 32837–42. дои : 10.1074/jbc.M201853200 . ПМИД 12093795 .
- ^ Сурхольт, Б; Ньюсхолм, Э.А. (15 сентября 1981 г.). «Максимальная активность и свойства глюкозо-6-фосфатазы в мышцах позвоночных и беспозвоночных» . Биохимический журнал . 198 (3): 621–9. дои : 10.1042/bj1980621 . ПМЦ 1163310 . ПМИД 6275855 .
- ^ Ангарони С.Дж., де Кремер Р.Д., Белка С.Э., Паскини-Капра А.Э., Гинер-Аяла А.Н., Пецца Р.Дж., Хлеб С.Дж., Чоу Дж.Ю. (ноябрь 2004 г.). «Болезнь накопления гликогена типа Ia в Аргентине: две новые мутации глюкозо-6-фосфатазы, влияющие на стабильность белка». Молекулярная генетика и обмен веществ . 83 (3): 276–9. дои : 10.1016/j.ymgme.2004.06.010 . ПМИД 15542400 .
- ^ Чоу JY, Джун Х.С., Мэнсфилд, Британская Колумбия (декабрь 2010 г.). «Гликогеновая болезнь I типа и дефицит глюкозо-6-фосфатазы-β: этиология и терапия» . Обзоры природы. Эндокринология . 6 (12): 676–88. дои : 10.1038/nrendo.2010.189 . ПМЦ 4178929 . ПМИД 20975743 .
- ^ Jump up to: а б с Джун Х.С., Ли Ю.М., Чунг Ю.И., Макдермотт Д.Х., Мерфи П.М., Де Рэвин С.С., Мэнсфилд BC, Чоу Дж.Ю. (октябрь 2010 г.). «Отсутствие рециркуляции глюкозы между эндоплазматическим ретикулумом и цитоплазмой лежит в основе клеточной дисфункции в нейтрофилах с дефицитом глюкозо-6-фосфатазы-β при синдроме врожденной нейтропении» . Кровь . 116 (15): 2783–92. дои : 10.1182/кровь-2009-12-258491 . ПМЦ 2974586 . ПМИД 20498302 .
- ^ Страйер, Люберт; Берг, Джереми Марк; Тимочко, Джон Л. (2007). Биохимия . Сан-Франциско: WH Freeman. ISBN 978-0-7167-8724-2 .
- ^ Пагон Р.А., Берд Т.Д., Долан Ч.Р. и др. (1993). «Болезнь накопления гликогена типа I». ПМИД 20301489 .
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ Jump up to: а б Чоу JY, Матерн Д., Мэнсфилд BC, Чен Ю.Т. (март 2002 г.). «Болезни накопления гликогена I типа: нарушения комплекса глюкозо-6-фосфатазы». Современная молекулярная медицина . 2 (2): 121–43. дои : 10.2174/1566524024605798 . ПМИД 11949931 .
- ^ Jump up to: а б Фруассар Р., Пиро М., Буджемлин А.М., Виани-Сабан С., Пети Ф., Юбер-Бюрон А., Эбершвайлер П.Т., Гайдос В., Лабрюн П. (2011). «Дефицит глюкозо-6-фосфатазы» . Сиротский журнал редких заболеваний . 6:27 дои 10.1186 / : 1750-1172-6-27 . ПМЦ 3118311 . ПМИД 21599942 .
- ^ Джун Х.С., Ли Ю.М., Сонг К.Д., Мэнсфилд BC, Чоу Дж.Ю. (апрель 2011 г.). «G-CSF улучшает функцию нейтрофилов с дефицитом G6PC3 у мышей путем модуляции апоптоза и энергетического гомеостаза» . Кровь . 117 (14): 3881–92. doi : 10.1182/blood-2010-08-302059 . ПМК 3083300 . ПМИД 21292774 .
- ^ Бозтуг К, Аппасвами Г, Ашиков А, Шеффер А.А., Зальцер Ю, Дистельхорст Дж, Гермесхаузен М, Брандес Г, Ли-Госслер Дж, Ноян Ф, Гацке А.К., Минков М, Грейл Дж, Крац С, Петропулу Т, Пелье И, Белланне-Шантелот С, Резаи Н, Монкемёллер К, Ирани-Хакиме Н, Баккер Х, Жерарди-Шан Р, Зейдлер С, Гримбахер Б, Вельте К, Кляйн С (январь 2009 г.). «Синдром с врожденной нейтропенией и мутациями G6PC3» . Медицинский журнал Новой Англии . 360 (1): 32–43. doi : 10.1056/NEJMoa0805051 . ПМЦ 2778311 . ПМИД 19118303 .
- ^ Jump up to: а б Хэйи Б, Антонопулос А, Мерфи Э.Дж., Рахман ФЗ, Сьюэлл Дж., Смит Б.Н., Маккартни С., Фурман М., Холл Дж., Блум С.Л., Хаслам С.М., Моррис Х.Р., Бозтуг К., Кляйн С., Винчестер Б., Пик Е., Линч Д.С. , Гейл Р.Э., Смит А.М., Делл А., Сигал А.В. (июль 2011 г.). «Мутации G6PC3 связаны с серьезным дефектом гликозилирования: новый механизм дисфункции нейтрофилов» . Гликобиология . 21 (7): 914–24. дои : 10.1093/гликоб/cwr023 . ПМК 3110488 . ПМИД 21385794 .
- ^ «Влияние сульфата ванадила на углеводный и липидный обмен у больных инсулиннезависимым сахарным диабетом. Метаболизм. Клинический и экспериментальный» . www.metabolismjournal.com . Проверено 16 июня 2015 г.
- ^ Шехзад, Сайма (1 января 2013 г.). «Потенциальное влияние соединений ванадия на глюкозо-6-фосфатазу» . Горизонты бионауки . 6 : hzt002. doi : 10.1093/bihorizons/hzt002 . ISSN 1754-7431 .
- ^ Петтерсен Э.Ф., Годдард Т.Д., Хуанг CC, Коуч Г.С., Гринблатт Д.М., Мэн Э.К., Феррин Т.Е. (октябрь 2004 г.). «UCSF Chimera — система визуализации для поисковых исследований и анализа» (PDF) . Журнал вычислительной химии . 25 (13): 1605–12. дои : 10.1002/jcc.20084 . ПМИД 15264254 . S2CID 8747218 .
Внешние ссылки
[ редактировать ]- Глюкозо-6-фосфатаза Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)
- Г6ПК , Г6ПК2 , Г6ПК3 , Г6ПР
- ЭК 3.1.3.9
