Болезнь накопления гликогена I типа.
Эта статья нуждается в дополнительных цитатах для проверки . ( февраль 2009 г. ) |
Эта статья написана как исследовательская статья или научный журнал . ( Апрель 2020 г. ) |
| ГСД Тип I | |
|---|---|
| Другие имена | болезнь фон Гирке |
| Символ болезни накопления гликогена I типа | |
| Произношение | |
| Специальность | Эндокринология , генетика , гематология , иммунология |
| Осложнения | Лактацидоз , гиперлипидемия , неалкогольная жировая болезнь печени , гепатоцеллюлярная аденома , воспалительные заболевания кишечника |
| Продолжительность | Продолжительность жизни |
| Типы | Тип Ia, тип Ib |
| Причины | Аутосомно-рецессивное наследование |
| Метод диагностики | Генетическое тестирование , гипогликемия , гепатомегалия Тип Ib : нейтропения. |
| Уход | Кукурузный крахмал , диета |
| Медикамент | Филграстим |
| Частота | 1 из 100 000 живорождений |
Болезнь накопления гликогена типа I ( БГБ I ) – это наследственное заболевание , которое не позволяет печени правильно расщеплять накопленный гликоген , необходимый для поддержания адекватного уровня сахара в крови . GSD I подразделяется на два основных типа: GSD Ia и GSD Ib, которые различаются по причине, проявлению и лечению. Возможно, существуют также более редкие подтипы: транслоказы неорганического фосфата (GSD Ic) или глюкозы (GSD Id); однако недавнее исследование показывает, что биохимические анализы, используемые для дифференциации GSD Ic и GSD Id от GSD Ib, ненадежны и, следовательно, относятся к GSD Ib. [1]
ГСД Ia вызван дефицитом фермента глюкозо -6-фосфатазы ; GSD Ib – дефицит транспортного белка глюкозо-6-фосфат-транслоказы . Поскольку гликогенолиз является основным метаболическим механизмом, с помощью которого печень поставляет глюкозу в организм во время голодания , оба дефицита вызывают тяжелую гипогликемию и, со временем, избыточное накопление гликогена в печени и (в некоторых случаях) в почках .
Из-за накопления гликогена у пациентов с GSD I обычно наблюдается увеличение печени вследствие неалкогольной жировой болезни печени . [2] Другие функции печени и почек при GSD I изначально сохранены, но подвержены другим проблемам. [ нечеткий ] Без надлежащего лечения GSD I вызывает хронический низкий уровень сахара в крови, что может привести к избытку молочной кислоты , аномально высокому уровню липидов в крови и другим проблемам. Частое кормление кукурузным крахмалом или другими углеводами является основным методом лечения всех форм GSD I.
GSD Ib также характеризуется хронической нейтропенией из-за дисфункции продукции нейтрофилов в костном мозге . Этот иммунодефицит , если его не лечить, делает пациентов с GSD Ib восприимчивыми к инфекции. [3] Основным лечением этого признака GSD Ib является филграстим ; однако пациентам часто по-прежнему требуется лечение от частых инфекций, а хроническое увеличение селезенки . частым побочным эффектом является [4] У пациентов с GSD Ib часто наблюдаются воспалительные заболевания кишечника . [5]
Это наиболее распространенная из болезней накопления гликогена . GSD I составляет Встречаемость примерно 1 на 100 000 рождений среди американского населения и примерно 1 на 20 000 рождений среди евреев-ашкенази . [6] Заболевание было названо в честь немецкого врача Эдгара фон Гирке , впервые описавшего его в 1929 году. [7] [8]
Признаки и симптомы
[ редактировать ]Ранние исследования GSD I выявили многочисленные клинические проявления, которые ошибочно считались основными признаками генетического заболевания. Однако продолжающиеся исследования показали, что эти клинические особенности являются следствием только одного (при GSD Ia) или двух (при GSD Ib) фундаментальных отклонений:
- нарушение способности печени превращать накопленный гликоген в глюкозу посредством гликогенолиза. [9]
- при GSD Ib - нарушение способности нейтрофилов поглощать глюкозу, что приводит к дисфункции нейтрофилов и нейтропении. [10]
Эти фундаментальные отклонения приводят к небольшому количеству первичных клинических проявлений, которые учитываются при диагностике ЖКБ I:
- Низкий уровень сахара в крови (гипогликемия) из-за нарушения распада гликогена (гликогенолиза), что приводит к недостаточному уровню глюкозы в крови натощак. [11]
- гепатомегалия при неалкогольной жировой болезни печени из-за нарушения гликогенолиза, вызывающего накопление гликогена в печени. [2]
- при GSD Ib повышенный риск инфекции из-за нейтропении и дисфункции нейтрофилов. [3]
У больных людей обычно наблюдаются вторичные клинические проявления, связанные с одним или несколькими первичными клиническими проявлениями:
- Высокий уровень мочевой кислоты в крови и сопутствующий риск подагры или повреждения почек, вызванный низким уровнем инсулина в сыворотке крови при длительной гипогликемии.
- Высокий уровень молочной кислоты в крови , в крайних случаях приводящий к лактоацидозу , вызванному длительной гипогликемией. [11]
- аденомы печени, развивающиеся во взрослом возрасте [12] и сопутствующий риск анемии , [13] предположительно вызвано нарушением регуляции уровня глюкозы в крови на фоне неалкогольной жировой болезни печени
- при GSD Ib, воспалительном заболевании кишечника и сопутствующем риске анемии , [13] вызвано дисфункцией нейтрофилов и усугубляется повышенным потреблением углеводов, необходимым для предотвращения гипогликемии. [3]
Кроме того, существует ряд клинических проявлений, которые часто возникают в результате лечения первичных клинических проявлений:
- поджелудочной железы гипертрофия из-за увеличения потребления углеводов, вызывающего частую реакцию инсулина [14]
- при GSD Ib — спленомегалия , обусловленная длительным применением филграстима для лечения нейтропении, вызывающей секвестрацию факторов крови в селезенке [4]
- при GSD Ib может наблюдаться аномально низкое количество тромбоцитов в крови из-за длительного применения филграстима, вызывающего секвестрацию тромбоцитов в селезенке. [15]
- при GSD Ib анемия из-за длительного применения филграстима, вызывающая секвестрацию гемоглобина в селезенке, потенциально усугубляемая неконтролируемым воспалительным заболеванием кишечника. [16]
Гипогликемия
[ редактировать ]Низкий уровень сахара в крови (гипогликемия) является основным клиническим симптомом, общим как для GSD Ia, так и для GSD Ib, и чаще всего требует первоначальной диагностики заболевания. Во время плода развития внутриутробного материнская глюкоза, передаваемая через плаценту, предотвращает гипогликемию . Однако после рождения неспособность поддерживать уровень глюкозы в крови за счет запасов гликогена в печени вызывает измеримую гипогликемию не более чем через 1–2 часа после кормления. Без надлежащего диетического лечения после рождения длительная гипогликемия часто приводит к внезапному лактоацидозу , который может вызвать первичную респираторную недостаточность в период новорожденности, а также кетоацидоз . [ нужна ссылка ]
Неврологические проявления гипогликемии при GSD I менее выражены, чем в других случаях. Вместо острой гипогликемии у пациентов с GSD I наблюдается стойкая легкая гипогликемия. Уменьшение вероятности неврологических проявлений связано с привыканием мозга к легкой гипогликемии. Учитывая снижение уровня глюкозы в крови, мозг адаптируется к использованию альтернативных видов топлива, таких как лактат . Эта постепенная метаболическая адаптация в младенчестве делает тяжелые симптомы, такие как потеря сознания или судороги, редкими до постановки диагноза. [ нужна ссылка ]
В первые недели жизни недиагностированные дети с GSD I переносят стойкую гипогликемию и компенсированный лактоацидоз между кормлениями без каких-либо симптомов. Без постоянного углеводного питания уровень глюкозы в крови младенцев обычно составляет от 25 до 50 мг/дл (от 1,4 до 2,8 ммоль/л). Через несколько недель или месяцев без лечения постоянным пероральным употреблением углеводов у младенцев начнут проявляться явные симптомы гипогликемии и лактоацидоза. У младенцев может проявляться бледность, липкость, раздражительность, расстройство дыхания и неспособность спать всю ночь даже на втором году жизни. Задержка развития не является внутренним следствием GSD I, но встречается часто, если диагноз не установлен в раннем детстве. [ нужна ссылка ]
Генетика
[ редактировать ]
GSD I наследуется по аутосомно-рецессивному типу. Люди с одной копией дефектного гена являются носителями заболевания и не имеют симптомов. Как и в случае с другими аутосомно-рецессивными заболеваниями, каждый ребенок, рожденный от двух носителей заболевания, имеет 25%-ную вероятность унаследовать обе копии дефектного гена и проявить заболевание. Незатронутые родители ребенка с ГБД I могут считаться носителями. Пренатальный диагноз устанавливался с помощью биопсии печени плода на сроке 18–22 недель беременности, но лечение плода не предлагалось. Пренатальная диагностика возможна с помощью ДНК плода , полученной путем отбора проб ворсин хориона, когда известно, что плод находится в группе риска. [ нужна ссылка ]
Наиболее распространенные формы GSD I обозначаются GSD Ia и GSD Ib, причем на первую приходится более 80% диагностированных случаев, а на вторую - менее 20%. Описано несколько более редких форм.
- GSD Ia возникает в результате мутаций G6PC , гена глюкозо-6-фосфатазы. [17] расположен на хромосоме 17q21 . [18]
- GSD Ib возникает в результате мутаций гена SLC37A4 или «G6PT1», транспортера глюкозо-6-фосфата. [18] [19]
- GSD Ic возникает в результате мутаций SLC17A3 или SLC37A4 . [20]
Глюкозо-6-фосфатаза — фермент, расположенный на внутренней мембране эндоплазматической сети . Каталитическая единица связана с кальций- связывающим белком и тремя транспортными белками (Т1, Т2, Т3), которые облегчают перемещение глюкозо-6-фосфата (G6P), фосфата и глюкозы (соответственно) в фермент и из него.
Патофизиология
[ редактировать ]Нормальный углеводный баланс и поддержание уровня глюкозы в крови
[ редактировать ]Гликоген в печени и (в меньшей степени) почках служит формой хранимой, быстродоступной глюкозы, благодаря чему уровень глюкозы в крови может поддерживаться между приемами пищи. В течение примерно 3 часов после приема пищи, содержащей углеводы, высокий уровень инсулина заставляет клетки печени брать глюкозу из крови, превращать ее в глюкозо-6-фосфат (G6P) с помощью фермента глюкокиназы и присоединять молекулы G6P к концам. цепей гликогена (синтез гликогена). Избыток G6P также направляется на производство триглицеридов и экспортируется для хранения в жировой ткани в виде жира .
Когда переваривание еды завершено, уровень инсулина падает, и ферментные системы в клетках печени начинают удалять молекулы глюкозы из нитей гликогена в форме G6P. Этот процесс называется гликогенолизом . G6P остается внутри клетки печени, если фосфат не расщепляется глюкозо-6-фосфатазой. Эта дефосфорилирования реакция приводит к образованию свободной глюкозы и свободного PO.
4 аниона . Свободные молекулы глюкозы могут транспортироваться из клеток печени в кровь для поддержания адекватного снабжения глюкозой мозга и других органов тела. Гликогенолиз может обеспечить потребности взрослого организма в глюкозе на 12–18 часов.
Когда голодание продолжается более нескольких часов, падение уровня инсулина приводит к белка и катаболизму мышечного триглицеридов из жировой ткани. Продуктами этих процессов являются аминокислоты (главным образом аланин ), свободные жирные кислоты и молочная кислота . Свободные жирные кислоты из триглицеридов превращаются в кетоны и в ацетил-КоА . Аминокислоты и молочная кислота используются для синтеза нового G6P в клетках печени в процессе глюконеогенеза . Последним этапом нормального глюконеогенеза, как и последним этапом гликогенолиза, является дефосфорилирование G6P глюкозо-6-фосфатазой с высвобождением глюкозы и ПО.
4 .
Таким образом, глюкозо-6-фосфатаза опосредует заключительный, ключевой этап обоих двух основных процессов производства глюкозы во время голодания. Эффект усиливается, поскольку образующиеся в результате высокие уровни глюкозо-6-фосфата ингибируют более ранние ключевые этапы как гликогенолиза, так и глюконеогенеза.
Патофизиология
[ редактировать ]Основными метаболическими эффектами дефицита глюкозо-6-фосфатазы являются гипогликемия , лактоацидоз , гипертриглицеридемия и гиперурикемия .

Гипогликемия . GSD I называется «постабсорбционной», обычно примерно через 4 часа после полного переваривания пищи Эта неспособность поддерживать адекватный уровень глюкозы в крови во время голодания является результатом комбинированного нарушения как гликогенолиза, так и глюконеогенеза. Гипогликемия натощак часто является наиболее серьезной проблемой при GSD I и обычно является проблемой, которая приводит к постановке диагноза. Хроническая гипогликемия вызывает вторичные метаболические адаптации, включая хронически низкие уровни инсулина и высокие уровни глюкагона и кортизола .
Лактоацидоз возникает вследствие нарушения глюконеогенеза. Молочная кислота образуется как в печени, так и в мышцах и окисляется НАД. + до пировиноградной кислоты , а затем конвертируется глюконеогенным путем в G6P. Накопление G6P ингибирует превращение лактата в пируват. Уровень молочной кислоты повышается во время голодания по мере снижения уровня глюкозы. У людей с GSD I он может не полностью упасть до нормы, даже когда нормальный уровень глюкозы восстанавливается.
Гипертриглицеридемия, возникающая в результате усиленного производства триглицеридов, является еще одним косвенным эффектом нарушения глюконеогенеза, усиливающегося хронически низким уровнем инсулина. Во время голодания нарушается нормальное превращение триглицеридов в свободные жирные кислоты, кетоны и, в конечном итоге, в ацетил-КоА. Уровни триглицеридов при GSD I могут в несколько раз превышать норму и служить клиническим показателем «метаболического контроля».
Гиперурикемия возникает в результате сочетания повышенного образования и снижения экскреции мочевой кислоты , которая образуется, когда повышенное количество G6P метаболизируется по пентозофосфатному пути . Это также побочный продукт распада пуринов . Мочевая кислота конкурирует с молочной кислотой и другими органическими кислотами за почечную экскрецию с мочой. При GSD I повышенная доступность G6P для пентозофосфатного пути, повышенная скорость катаболизма и снижение экскреции с мочой из-за высокого уровня молочной кислоты - все это в совокупности приводит к повышению уровня мочевой кислоты, в несколько раз превышающему нормальный. Хотя гиперурикемия протекает бессимптомно в течение многих лет, постепенно нарастает поражение почек и суставов.
Повышенный лактат и лактоацидоз
[ редактировать ]Высокий уровень молочной кислоты в крови наблюдается у всех людей с ЖКТ I типа вследствие нарушения глюконеогенеза . Исходное повышение обычно составляет от 4 до 10 моль/мл и не оказывает никакого клинического воздействия. Однако во время и после эпизода низкого уровня сахара в крови уровень лактата резко возрастает и превышает 15 моль/мл, порог лактат-ацидоза . Симптомы лактоацидоза включают рвоту и гиперпноэ , оба из которых могут усугубить гипогликемию на фоне GSD I. В случаях острого лактоацидоза пациентам необходима неотложная помощь для стабилизации кислорода в крови и восстановления уровня глюкозы в крови. Правильная идентификация лактоацидоза у недиагностированных детей представляет собой проблему, поскольку первыми симптомами обычно являются рвота и обезвоживание, которые имитируют детские инфекции, такие как гастроэнтерит или пневмония . Более того, обе эти распространенные инфекции могут спровоцировать более тяжелую гипогликемию у невыявленных детей, что затрудняет диагностику основной причины.
Поскольку повышенный уровень лактата сохраняется, мочевая кислота, кетокислоты и свободные жирные кислоты еще больше увеличивают анионный разрыв . У взрослых и детей высокие концентрации лактата вызывают значительный дискомфорт в мышцах. Этот дискомфорт является усиленной формой ощущения жжения, которое бегун может ощущать в четырехглавых мышцах после спринта, и которое вызвано кратковременным накоплением молочной кислоты. Правильный контроль гипогликемии при ГСД I исключает возможность лактоацидоза.
Повышенный уровень уратов и осложнения
[ редактировать ]Высокий уровень мочевой кислоты часто является следствием повышенного уровня молочной кислоты у пациентов с GSD I типа. Когда уровень лактата повышен, переносимая через кровь молочная кислота конкурирует за тот же механизм транспортировки почечных канальцев, что и ураты, ограничивая скорость выведения уратов почками в мочу. Если он присутствует, повышенный катаболизм пуринов является дополнительным фактором, способствующим этому. Уровни мочевой кислоты от 6 до 12 мг/дл (от 530 до 1060 мкмоль/л) часто встречаются у пациентов с GSD I, если заболевание не лечится должным образом. применение препарата аллопуринол Некоторым больным людям необходимо для снижения уровня уратов в крови. Последствия гиперурикемии у пациентов с GSD I включают развитие камней в почках и накопление кристаллов мочевой кислоты в суставах, что приводит к заболеванию почек и подагре соответственно.
Гиперлипидемия и плазменные эффекты
[ редактировать ]Повышенные уровни триглицеридов при GSD I возникают в результате низкого уровня инсулина в сыворотке крови у пациентов с частыми длительными гипогликемиями. Это также может быть вызвано внутриклеточным накоплением глюкозо-6-фосфата с вторичным шунтированием в пируват , который превращается в ацетил-КоА , который транспортируется в цитозоль , где происходит синтез жирных кислот и холестерина . Триглицериды выше 3,4 ммоль/л (300 мг/дл) могут вызывать видимую липемию и даже легкую псевдогипонатриемию из-за снижения водной фракции плазмы крови . При GSD I уровень холестерина обычно незначительно повышен по сравнению с другими липидами .
Гепатомегалия
[ редактировать ]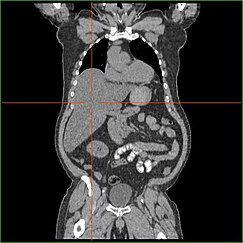
Нарушение способности печени осуществлять глюконеогенез приводит к клинически выраженной гепатомегалии . Без этого процесса организм не может высвободить гликоген из печени и преобразовать его в глюкозу крови, что приводит к накоплению запасов гликогена в печени. Гепатомегалия из-за накопления запасов гликогена в печени считается формой неалкогольной жировой болезни печени . У пациентов с GSD I степень гепатомегалии наблюдается на протяжении всей жизни, но тяжесть часто связана с потреблением избыточного количества углеводов с пищей . Возможно снижение массы печени, поскольку у большинства пациентов сохраняется остаточная функция печени, позволяющая высвобождать накопленный гликоген с ограниченной скоростью.
У пациентов с GSD I часто гепатомегалия возникает с момента рождения. При развитии плода материнская глюкоза, передаваемая плоду, предотвращает гипогликемию, но хранение глюкозы в виде гликогена в печени приводит к гепатомегалии. Нет никаких доказательств того, что эта гепатомегалия представляет какой-либо риск для правильного развития плода.
Гепатомегалия при ЖКТ I типа обычно возникает без симпатического увеличения селезенки. У пациентов с GSD Ib может наблюдаться спленомегалия, но это связано с использованием филграстима для лечения нейтропении этого подтипа, а не сопутствующей гепатомегалии. Гепатомегалия в некоторой степени сохраняется на протяжении всей жизни, часто вызывая выпячивание живота, а в тяжелых случаях может пальпироваться на уровне пупка или ниже него . При неалкогольной жировой болезни печени, связанной с ЖКБ, функция печени обычно сохраняется, при этом ферменты печени и билирубин остаются в пределах нормы. Однако в зрелом возрасте на функцию печени могут влиять и другие печеночные осложнения, включая развитие аденомы печени .
Аденомы печени
[ редактировать ]Конкретная этиология аденом печени при ЖКТ I остается неизвестной, несмотря на продолжающиеся исследования. Типичным пациентом с диагнозом GSD I, по крайней мере, с одной аденомой, является взрослый человек, хотя поражения наблюдались и у пациентов в возрасте четырнадцати лет. Аденомы, состоящие из гетерогенных новообразований, могут возникать по отдельности или в виде множества. Оценки скорости превращения гепатоцеллюлярной аденомы в гепатоцеллюлярную карциному при GSD I варьируются от 0% до 11%, причем последняя цифра представляет собой более поздние исследования. Одной из причин увеличения оценки является растущая популяция пациентов с диагнозом GSD I, доживающих до зрелого возраста, когда развивается большинство аденом.
Стандарты лечения диктуют регулярное наблюдение за печенью с помощью МРТ или КТ для выявления структурных нарушений. аденомы печени могут быть ошибочно приняты за фокальную узловую гиперплазию При диагностической визуализации , хотя это состояние встречается редко. Однако аденомы печени при GSD I исключительно связаны с диффузным отложением гиалина Маллори , что в противном случае обычно наблюдается при фокальной узловой гиперплазии. В отличие от обычных аденом печени, связанных с приемом пероральных контрацептивов, кровотечения у пациенток с диагнозом GSD I встречаются редко.
Хотя причина высокой распространенности аденом при GSD I неясна, исследования, проведенные с 1970-х годов, показали, что сывороточный глюкагон является потенциальным фактором. В исследованиях пациенты, которым была назначена диета для поддержания уровня сахара в крови в нормальном диапазоне от 72 до 108 мг/дл (от 4,0 до 6,0 ммоль/л), показали снижение вероятности развития аденом. Более того, у пациентов с хорошо контролируемым уровнем глюкозы в крови постоянно наблюдается уменьшение размера и количества аденом печени, что позволяет предположить, что аденомы могут быть вызваны дисбалансом гепатотропных агентов, таких как сывороточный инсулин и особенно сывороточный глюкагон в печени. [21]
Остеопения
[ редактировать ]У пациентов с GSD I часто развивается остеопения . Конкретная этиология низкой минеральной плотности костной ткани при ЖКБ неизвестна, хотя она тесно связана с плохим метаболическим контролем. Остеопения может быть непосредственно вызвана гипогликемией или возникающими в результате эндокринными и метаболическими последствиями. Постоянно доказано, что улучшение метаболического контроля предотвращает или обращает вспять клинически значимую остеопению у пациентов с диагнозом GSD I. [22] В случаях, когда остеопения прогрессирует с возрастом, минеральная плотность костей в ребрах обычно более выражена, чем в позвонках. [23] В некоторых случаях Т-показатель минеральной плотности костной ткани упадет ниже -2,5, что указывает на остеопороз. Есть некоторые доказательства того, что остеопения может быть связана с сопутствующими нарушениями почек при GSD I, особенно с глобулярной гиперфильтрацией. [24] Это состояние также, по-видимому, поддается лечению добавками кальция. Во многих случаях минеральная плотность костной ткани может увеличиться и вернуться к нормальному уровню при условии надлежащего метаболического контроля и приема добавок кальция, обращая вспять остеопению.
Эффекты на почки
[ редактировать ]Почки обычно увеличены на 10–20% за счет накопленного гликогена. У взрослых с GSD I хроническое повреждение клубочков , подобное диабетической нефропатии, может привести к почечной недостаточности . GSD I может проявляться различными осложнениями со стороны почек. Нарушения почечных канальцев, связанные с гиперлактатемией, наблюдаются в раннем возрасте, вероятно, потому, что длительный лактоацидоз чаще возникает в детстве. Это часто проявляется как синдром Фанкони с множественными нарушениями почечной канальцевой реабсорбции, включая канальцевый ацидоз с потерей бикарбонатов и фосфатов. Эти канальцевые аномалии при GSD I обычно выявляются и контролируются с помощью кальция в моче. В долгосрочной перспективе эти нарушения могут усугубить нефропатию мочевой кислоты, в противном случае вызываемую гиперлактатемией. В подростковом возрасте и позже заболевание клубочков может развиваться независимо, первоначально проявляясь клубочковой гиперфильтрацией, на что указывает повышение рСКФ в моче.
Спленомегалия
[ редактировать ]Увеличение селезенки (спленомегалия) часто встречается при GSD I и имеет две основные причины. При GSD Ia спленомегалия может быть вызвана соотношением между печенью и селезенкой, которое заставляет либо расти, либо сжиматься, чтобы соответствовать относительному размеру другой печени, в меньшей степени. При GSD Ib это побочный эффект применения филграстима для лечения нейтропении.
Эффекты кишечника
[ редактировать ]Поражение кишечника может вызвать легкую мальабсорбцию с жирным стулом ( стеаторея ), но обычно не требует лечения.
Риск заражения
[ редактировать ]Нейтропения является отличительной особенностью GSD Ib и отсутствует при GSD Ia. Микробиологическая причина нейтропении при GSD Ib недостаточно изучена. В широком смысле проблема возникает из-за нарушения клеточного метаболизма нейтрофилов, что приводит к ускорению апоптоза нейтрофилов. Нейтропения при ЖКБ характеризуется как снижением абсолютного количества нейтрофилов, так и снижением функции нейтрофилов. Нейтрофилы используют специфический метаболический путь G6P, который зависит от присутствия G6Pase-β или G6PT для поддержания энергетического гомеостаза внутри клетки. Отсутствие G6PT в GSD Ib ограничивает этот путь, что приводит к стрессу эндоплазматического ретикулума , окислительному стрессу внутри нейтрофилов и запуску преждевременного апоптоза. [3] Гранулоцитарный колониестимулирующий фактор (G-CSF), доступный в виде филграстима , может снизить риск заражения. В некоторых случаях G-CSF в форме пегфилграстима , продаваемого под торговым названием Neulasta, может использоваться в качестве альтернативы медленного действия, требующей менее частого приема.
Тромбоцитопения и проблемы со свертываемостью крови
[ редактировать ]Нарушение агрегации тромбоцитов является редким последствием хронической гипогликемии, наблюдаемой у пациентов с GSD I типа. Исследования продемонстрировали снижение функции тромбоцитов, характеризующееся снижением потребления протромбина , аномальными реакциями агрегации, увеличением времени кровотечения и низкой адгезией тромбоцитов. Тяжесть дисфункции тромбоцитов обычно коррелирует с клиническим состоянием, при этом наиболее тяжелые случаи коррелируют с лактоацидозом и тяжелой липидемией. [25] Это может вызвать клинически значимое кровотечение, особенно носовое . Кроме того, у пациентов с GSD I может наблюдаться тромбоцитопения вследствие спленомегалии. При спленомегалии различные гематологические факторы могут связываться в тканях селезенки, поскольку кровь фильтруется через этот орган. Это может снизить уровень тромбоцитов в кровотоке, что приводит к тромбоцитопении .
Эффекты развития
[ редактировать ]Задержка развития является потенциальным вторичным эффектом хронической или рецидивирующей гипогликемии, но ее, по крайней мере, теоретически можно предотвратить. Нормальные нейрональные и мышечные клетки не экспрессируют глюкозо-6-фосфатазу и, следовательно, не подвергаются непосредственному воздействию GSD I. Однако без надлежащего лечения гипогликемии задержка роста обычно является результатом хронически низкого уровня инсулина, стойкого ацидоза, хронического повышения уровня катаболических гормонов и недостаточности калорий (или мальабсорбции ). Наиболее резкие задержки развития часто являются причиной тяжелых (а не только стойких) эпизодов гипогликемии.
Диагностика
[ редактировать ]Несколько различных проблем могут привести к диагнозу, обычно к двум годам:
- судороги или другие проявления тяжелой гипогликемии натощак
- гепатомегалия с выпячиванием живота
- гипервентиляция и выраженный респираторный дистресс вследствие метаболического ацидоза
- эпизоды рвоты вследствие метаболического ацидоза, часто провоцируемые легкими заболеваниями и сопровождающиеся гипогликемией.
При подозрении на диагноз множественность клинических и лабораторных признаков обычно является веским косвенным аргументом. Если гепатомегалия, гипогликемия натощак и плохой рост сопровождаются лактоацидозом, гиперурикемией, гипертриглицеридемией и увеличением почек по данным УЗИ, наиболее вероятным диагнозом является GSD I. В список дифференциальной диагностики входят гликогенозы III и VI типов, дефицит фруктозо-1,6-бисфосфатазы и ряд других состояний (стр. 5). [ нужна ссылка ] , но вряд ли ни один из них будет обладать всеми функциями GSD I.
Следующим шагом обычно является тщательно контролируемое голодание. Гипогликемия часто возникает в течение шести часов. Критический образец крови, полученный во время гипогликемии, обычно выявляет легкий метаболический ацидоз, высокое содержание свободных жирных кислот и бета-гидроксибутирата, очень низкие уровни инсулина и высокие уровни глюкагона, кортизола и гормона роста. Введение внутримышечного или внутривенного глюкагона (от 0,25 до 1 мг, в зависимости от возраста) или адреналина приводит к незначительному повышению уровня сахара в крови.
Диагноз окончательно подтверждается биопсией печени с электронной микроскопией и определением активности глюкозо-6-фосфатазы в ткани и/или тестированием специфических генов, доступными в последние годы.
Уход
[ редактировать ]Первичной целью лечения является предотвращение гипогликемии и вторичных метаболических нарушений путем частого употребления продуктов с высоким содержанием глюкозы или крахмала (которые легко перевариваются до глюкозы). Чтобы компенсировать неспособность печени обеспечивать сахар, общее количество пищевых углеводов должно приближаться к 24-часовой скорости производства глюкозы. Диета должна содержать примерно 65–70% углеводов, 10–15% белков и 20–25% жиров. Не менее трети углеводов должно поступать в течение ночи, чтобы ребенок раннего возраста обходился без углеводов не более 3–4 часов.После установления диагноза приоритетом лечения GSD I является поддержание адекватного уровня глюкозы в крови. Пациенты стремятся поддерживать уровень глюкозы в крови выше порогового уровня 72 мг/дл (4,0 ммоль/л) при гипогликемии. Пациенты с GSD Ib имеют дополнительный приоритет лечения, связанный с нейтропенией. Правильное регулирование уровня глюкозы в крови при ГСД I имеет решающее значение для предотвращения более серьезных последствий высокого уровня молочной кислоты и мочевая кислота в крови и развитие аденомы печени .
За последние 30 лет для достижения этой цели у детей раннего возраста использовались два метода: (1) непрерывная ночная желудочная инфузия глюкозы или крахмала; и (2) ночное кормление сырым кукурузным крахмалом. Элементарную смесь, полимер глюкозы и/или кукурузный крахмал можно вводить непрерывно в течение ночи со скоростью, обеспечивающей 0,5–0,6 г/кг/ч глюкозы для младенца или 0,3–0,4 для ребенка старшего возраста. Для этого метода требуется назогастральный или гастростомический зонд и насос. Внезапная смерть от гипогликемии произошла из-за неисправности или отключения, и теперь периодическое кормление кукурузным крахмалом предпочтительнее непрерывной инфузии.
Кукурузный крахмал — недорогой способ обеспечить постепенно усваиваемую глюкозу. Одна столовая ложка содержит около 9 г углеводов (36 калорий). Хотя этот метод безопаснее, дешевле и не требует оборудования, он требует, чтобы родители вставали каждые 3–4 часа, чтобы дать кукурузный крахмал. Типичная потребность маленького ребенка составляет 1,6 г/кг каждые 4 часа.
Длительное лечение должно устранить симптомы гипогликемии и поддерживать нормальный рост. Лечение должно обеспечить нормальный уровень глюкозы, молочной кислоты и электролитов и лишь незначительное повышение уровня мочевой кислоты и триглицеридов.
Избегание других сахаров
[ редактировать ]Потребление углеводов , которые для использования должны быть преобразованы в G6P (например, галактозу и фруктозу ), следует свести к минимуму. Хотя для младенцев доступны элементарные смеси, многие продукты содержат фруктозу или галактозу в форме сахарозы или лактозы . После младенчества приверженность лечению становится спорным вопросом.
Другие терапевтические меры
[ редактировать ]Стойкое повышение уровня мочевой кислоты выше 6,5 мг/дл требует лечения аллопуринолом для предотвращения отложения мочевой кислоты в почках и суставах.
Из-за возможности нарушения функции тромбоцитов перед операцией следует проверить способность коагуляции и нормализовать метаболическое состояние. Время кровотечения можно нормализовать за 1–2 дня нагрузки глюкозой и улучшить с помощью ddavp. Во время операции внутривенные жидкости должны содержать 10% декстрозы и не содержать лактата.
Пациенту с GSD типа 1b в 1993 году в Медицинском центре UCSF была проведена трансплантация печени, что привело к разрешению эпизодов гипогликемии и необходимости держаться подальше от естественных источников сахара. Другие пациенты также прошли эту процедуру с положительными результатами. Хотя трансплантация печени привела к разрешению гипогликемии, она, однако, не устранила хроническую нейтропению и риск инфицирования пациентов.
Лечение эпизодов острого метаболического ацидоза
[ редактировать ]Наиболее серьезной острой проблемой в детстве является предрасположенность к эпизодам метаболического ацидоза, провоцируемого легкими заболеваниями. Если рвота сохраняется более 2–4 часов, ребенка следует осмотреть и оценить на предмет обезвоживания, ацидоза и гипогликемии. Если они развиваются, следует вводить внутривенные жидкости в дозе, превышающей поддерживающую. При легком ацидозе эффективной жидкостью является 10% декстроза в ½ физиологического раствора с 20 мэкв/л KCl, но при тяжелом ацидозе – 75–100 мэкв/л NaHCO.
3 и 20 мэкв/л ацетата калия можно заменить NaCl и KCl.
Метаболический контроль
[ редактировать ]Метаболический контроль часто снижается во время и после полового созревания в результате того, что пациент перерастает свой план диетического лечения. [26]
Прогноз
[ редактировать ]Без адекватного метаболического лечения пациенты с GSD I умирали в младенчестве или детстве от тяжелой гипогликемии и ацидоза. Те, кто выжил, имели задержку физического роста и половое созревание из-за хронически низкого уровня инсулина. Умственную отсталость, возникающую в результате рецидивирующей тяжелой гипогликемии, считается предотвратимой при соответствующем лечении.
У некоторых пациентов осложнения со стороны печени были серьезными. Аденомы печени могут развиться во втором десятилетии или позже с небольшой вероятностью последующей злокачественной трансформации в гепатому или карциному печени (обнаруживается с помощью скрининга альфа-фетопротеина). Состояние нескольких детей с тяжелыми печеночными осложнениями улучшилось после трансплантации печени.
Дополнительные проблемы, о которых сообщалось у подростков и взрослых с GSD I, включали гиперурикемическую подагру , панкреатит и хроническую почечную недостаточность . Несмотря на гиперлипидемию , атеросклеротические осложнения встречаются редко.
При диагностике до возникновения серьезного вреда, быстром купировании ацидотических эпизодов и соответствующем долгосрочном лечении большинство детей будут здоровыми. За некоторыми исключениями и оговорками, здоровье и продолжительность жизни взрослых также могут быть довольно хорошими, хотя отсутствие эффективного лечения до середины 1980-х годов означает, что информация о долгосрочной эффективности ограничена.
Эпидемиология
[ редактировать ]В Соединенных Штатах заболеваемость GSD I составляет примерно 1 на 50 000. [27] до 100 000 [28] рождения. Ни один из гликогенозов в настоящее время не выявляется при стандартном или расширенном скрининге новорожденных .
Заболевание чаще встречается у людей ашкеназского еврейского , мексиканского, китайского и японского происхождения. [29]
Ссылки
[ редактировать ]- ^ Вейга-да-Кунья, М.; Герин, И.; Ван Шафтинген, Э. (май 2000 г.). «Сколько форм болезни накопления гликогена I типа?» . Европейский журнал педиатрии . 159 (5): 314–318. дои : 10.1007/s004310051279 . ISSN 0340-6199 . ПМИД 10834514 .
- ^ Jump up to: а б Ниман, Джейкоб М.; Мисдраджи, Джозеф; Кори, Кэтлин Э. (май 2012 г.). «Вторичные причины неалкогольной жировой болезни печени» . Терапевтические достижения в гастроэнтерологии . 5 (3): 199–207. дои : 10.1177/1756283X11430859 . ISSN 1756-283X . ПМЦ 3342568 . ПМИД 22570680 .
- ^ Jump up to: а б с д Чоу, Дженис Ю.; Джун, Хён Сик; Мэнсфилд, Брайан К. (январь 2010 г.). «Нейтропения при болезни накопления гликогена Ib типа» . Современное мнение в гематологии . 17 (1): 36–42. дои : 10.1097/MOH.0b013e328331df85 . ISSN 1065-6251 . ПМК 3099242 . ПМИД 19741523 .
- ^ Jump up to: а б Дейл, Дэвид С.; Больярд, Одри Анна; Марреро, Трейси М.; Фан, Лан; Боксер, Лоуренс А.; Кишнани, Прия С.; Курцберг, Джоан; Вайнштейн, Дэвид А. (18 ноября 2011 г.). «Нейтропения при болезни накопления гликогена 1b (GSD1b)». Кровь . 118 (21): 4791. doi : 10.1182/blood.V118.21.4791.4791 . ISSN 0006-4971 .
- ^ Виссер, Гепке; Рейк, Ян Питер; Лабрюн, Филипп; Леонард, Джеймс В.; Моисей, Шимон; Ульрих, Курт; Вендель, Удо; Гренье, Клаас Х.; Смит, Г. Питер А. (октябрь 2002 г.). «Гранулоцитарный колониестимулирующий фактор при болезни накопления гликогена типа 1b. Результаты европейского исследования болезни накопления гликогена типа 1». Европейский журнал педиатрии . 161 (Приложение 1): S83–87. дои : 10.1007/s00431-002-1010-0 . ISSN 0340-6199 . ПМИД 12373578 . S2CID 33840498 .
- ^ «Болезнь накопления гликогена I типа» . НОРД (Национальная организация по редким заболеваниям) . Проверено 29 сентября 2019 г.
- ^ Синдром Гирке в журнале Who Named It?
- ^ Гирке, Э. (1929). «Гликогенная гепато-нефромегалия (заболевание накопления гликогена в печени и почках)». Вклад в патологическую анатомию и общую патологию . 82 . Йена: 497–513.
- ^ Парих, Нирзар С.; Ахлават, Раджни (2019), «Болезнь накопления гликогена типа I (болезнь фон Гирке)» , StatPearls , StatPearls Publishing, PMID 30480935 , получено 1 ноября 2019 г.
- ^ Джун, Хён Сик; Вайнштейн, Дэвид А.; Ли, Ён Мок; Мэнсфилд, Брайан С.; Чоу, Дженис Ю. (01 мая 2014 г.). «Молекулярные механизмы дисфункции нейтрофилов при болезни накопления гликогена типа Ib» . Кровь . 123 (18): 2843–2853. doi : 10.1182/blood-2013-05-502435 . ISSN 0006-4971 . ПМК 4007611 . ПМИД 24565827 .
- ^ Jump up to: а б Кишнани, Прия С.; Остин, Стефани Л.; Абденур, Хосе Э.; Арн, Памела; Бали, Дикша С.; Бони, Энн; Чанг, Венди К.; Дагли, Адити И.; Дейл, Дэвид; Кеберл, Дуайт; Сомерс, Майкл Дж. (ноябрь 2014 г.). «Диагностика и лечение болезни накопления гликогена I типа: практическое руководство Американского колледжа медицинской генетики и геномики» . Генетика в медицине . 16 (11): е1. дои : 10.1038/gim.2014.128 . ISSN 1530-0366 . ПМИД 25356975 .
- ^ Лабрюн, П.; Триош, П.; Дювальтье, И.; Шевалье, П.; Одьевр, М. (март 1997 г.). «Гепатоцеллюлярные аденомы при болезни накопления гликогена I и III типа: серия из 43 пациентов и обзор литературы» . Журнал детской гастроэнтерологии и питания . 24 (3): 276–279. дои : 10.1097/00005176-199703000-00008 . ISSN 0277-2116 . ПМИД 9138172 .
- ^ Jump up to: а б Ван, Дэвид К.; Каррерас, Кэролайн Т.; Фиске, Лори М.; Остин, Стефани; Бори, Даниэль; Кишнани, Прия С.; Вайнштейн, Дэвид А. (сентябрь 2012 г.). «Характеристика и патогенез анемии при болезни накопления гликогена типа Ia и Ib» . Генетика в медицине . 14 (9): 795–799. дои : 10.1038/gim.2012.41 . ISSN 1098-3600 . ПМЦ 3808879 . ПМИД 22678084 .
- ^ Дэвид, Вайнштейн (04 сентября 2019 г.). «Конференц-связь по данным Ultragenyx DTX401 фазы 1/2 когорты 2» . Edge.media-server.com . Проверено 30 октября 2019 г.
- ^ Такамацу, Ясуши; Джими, Широ; Сато, Томохито; Хара, Сюдзи; Судзумия, Джунджи; Тамура, Кадзуо (январь 2007 г.). «Тромбоцитопения в сочетании со спленомегалией во время лечения гранулоцитарным колониестимулирующим фактором у мышей не вызвана гиперспленизмом и разрешается спонтанно» . Переливание . 47 (1): 41–49. дои : 10.1111/j.1537-2995.2007.01061.x . ISSN 0041-1132 . ПМИД 17207228 . S2CID 36128181 .
- ^ Чен, Цзы-Линь; Чан, Я-Вэнь; Линь, Гуань-Лин; Чанг, Синь-Хоу; Лянь, Дэ-Шэн; Ше, Минь-Хуа; Сунь, Дер-Шань (2 мая 2018 г.). «Различное влияние гранулоцитарного колониестимулирующего фактора и эритропоэтина на эритропоэз» . Исследования и терапия стволовыми клетками . 9 (1): 119. дои : 10.1186/s13287-018-0877-2 . ISSN 1757-6512 . ПМК 5930863 . ПМИД 29720275 .
- ^ «Гликогенная болезнь I типа» . Домашний справочник по генетике из Национальной медицинской библиотеки США и Национальных институтов здравоохранения . Проверено 6 июля 2013 г.
- ^ Jump up to: а б Бали, Д.С.; Чен, Ю.Т.; Гольдштейн, Дж. Л.; Пагон, РА; Адам, член парламента; Берд, Т.Д.; Долан, ЧР; Фонг, Коннектикут; и др. (1993). «Болезнь накопления гликогена типа I». ПМИД 20301489 .
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ Интернет-менделевское наследование у человека (OMIM): болезнь накопления гликогена Ib - 232220
- ^ Интернет-менделевское наследование у человека (OMIM): болезнь накопления гликогена Ic - 232240
- ^ ПАРКЕР, ПОЛ (1981). «Регрессия аденомы печени при болезни накопления гликогена типа Ia на фоне диетотерапии» . Гастроэнтерология . 81 (3): 534–536. дои : 10.1016/0016-5085(81)90606-5 . ПМИД 6941908 .
- ^ Минарич, Лори А.; Кирпич, Александр; Фиске, Лори М.; Вайнштейн, Дэвид А. (2013). «Минеральная плотность костей при болезни накопления гликогена типа Ia и Ib» . Генетика в медицине . 14 (8): 737–741. дои : 10.1038/gim.2012.36 . ISSN 1098-3600 . ПМК 3884026 . ПМИД 22481133 .
- ^ Соэдзима, К.; Лендинг, Ч.Д.; Роу, ТФ; Суонсон, В.Л. (1985). «Патологические исследования остеопороза при болезни фон Гирке (гликогеноз 1а)». Детская патология . 3 (2–4): 307–319. дои : 10.3109/15513818509078791 . ISSN 0277-0938 . ПМИД 3867867 .
- ^ Пан, Бо-Лин; Локи, Сон-Сен (10 января 2018 г.). «Хроническая болезнь почек, связанная со снижением минеральной плотности костей, мочевой кислоты и метаболическим синдромом» . ПЛОС ОДИН . 13 (1): e0190985. Бибкод : 2018PLoSO..1390985P . дои : 10.1371/journal.pone.0190985 . ISSN 1932-6203 . ПМК 5761949 . ПМИД 29320555 .
- ^ Чапек, Эмили Э.; Дейкин, Дэниел; Зальцман, Эдвин В. (1 февраля 1973 г.). «Дисфункция тромбоцитов при болезни накопления гликогена I типа» . Кровь . 41 (2): 235–247. дои : 10.1182/blood.V41.2.235.235 . ISSN 0006-4971 . ПМИД 4350560 .
- ^ Деркс, Терри Дж.Дж.; ван Рейн, Маргрит (2015). «Липиды при заболеваниях накопления гликогена в печени: патофизиология, мониторинг диетического питания и будущие направления» . Журнал наследственных метаболических заболеваний . 38 (3): 537–543. дои : 10.1007/s10545-015-9811-2 . ISSN 0141-8955 . ПМК 4432100 . ПМИД 25633903 .
- ^ Болезнь накопления гликогена типа I в eMedicine
- ^ https://rarediseases.org/rare-diseases/гликоген-storage-disease-type-i/ Национальная организация по редким заболеваниям
- ^ Гольдман, Ли (2011). Cecil Medicine от Goldman (24-е изд.). Филадельфия: Эльзевир Сондерс. стр. 1356 . ISBN 978-1437727883 .
Дальнейшее чтение
[ редактировать ]Внешние ссылки
[ редактировать ] СМИ, связанные с болезнью накопления гликогена I типа, на Викискладе?
СМИ, связанные с болезнью накопления гликогена I типа, на Викискладе?