Рак печени
| Рак печени | |
|---|---|
| Другие имена | Рак печени, первичное злокачественное новообразование печени, первичный рак печени |
 | |
| КТ печени при холангиокарциноме | |
| Специальность | Гастроэнтерология Гепатология Онкология |
| Симптомы | Припухлость или боль в правом боку под грудной клеткой , вздутие живота , желтоватая кожа , легкие синяки, потеря веса, слабость. [1] |
| Обычное начало | от 55 до 65 лет [2] |
| Причины | гепатит В , гепатит С , алкоголизм , афлатоксин , неалкогольная жировая болезнь печени , печеночные сосальщики [3] [4] |
| Метод диагностики | Анализы крови , медицинская визуализация , биопсия тканей. [1] |
| Профилактика | Иммунизация против гепатита В , лечение инфицированных гепатитом В или С, [3] снижение воздействия афлатоксина, снижение высокого уровня потребления алкоголя |
| Уход | Хирургия , таргетная терапия , лучевая терапия [1] |
| Прогноз | Пятилетняя выживаемость ~ 18% (США); [2] 40% (Япония) [5] |
| Частота | 618 700 (на момент 2015 г.) [6] |
| Летальные исходы | 782,000 (2018) [7] |
Рак печени , также известный как рак печени , первичный рак печени или первичное злокачественное новообразование печени , представляет собой рак , который начинается в печени . [1] Рак печени может быть первичным, при котором рак начинается в печени, или метастазом в печень , или вторичным, при котором рак распространяется из других частей тела в печень. Метастазирование в печень является более распространенным из двух видов рака печени. [3] Случаи рака печени растут во всем мире. [8] [9]
Первичный рак печени является шестым по распространенности раком в мире и четвертой по значимости причиной смертности от рака. [7] [10] В 2018 году это заболевание произошло у 841 000 человек и привело к 782 000 смертям во всем мире. [7] Более высокие показатели заболеваемости раком печени наблюдаются там, где распространены гепатиты B и C, включая Азию и страны Африки к югу от Сахары . [3] Мужчины чаще болеют гепатоцеллюлярной карциномой (ГЦК), чем женщины. [3] Диагноз чаще всего диагностируется среди людей в возрасте от 55 до 65 лет. [2]
Основной причиной рака печени является цирроз печени , вызванный гепатитом В , гепатитом С или алкоголем . [4] Другие причины включают афлатоксин , неалкогольную жировую болезнь печени и печеночные сосальщики . [3] Наиболее распространенными типами являются ГЦК, составляющая 80% случаев, и внутрипеченочная холангиокарцинома . [3] Диагноз может быть подтвержден анализами крови и медицинской визуализацией , а также подтвержден биопсией тканей . [1]
Учитывая, что существует множество различных причин рака печени, существует множество подходов к профилактике рака печени. Эти усилия включают иммунизацию против гепатита В , [3] лечение гепатита В, лечение гепатита С, снижение употребления алкоголя, [8] снижение воздействия афлатоксина в сельском хозяйстве и борьба с ожирением и диабетом . [9] Скрининг рекомендуется лицам с хроническими заболеваниями печени . [3] Например, людям с хроническими заболеваниями печени, подверженным риску гепатоцеллюлярной карциномы, рекомендуется каждые 6 месяцев проходить ультразвуковое обследование. [8]
Поскольку рак печени является общим термином для многих типов рака, признаки и симптомы зависят от того, какой тип рака присутствует. Симптомы могут быть неопределенными и обширными. Холангиокарцинома связана с потливостью , желтухой , болями в животе , потерей веса и увеличением печени . [11] Гепатоцеллюлярная карцинома связана с образованием брюшной полости , болью в животе , рвотой , анемией , болью в спине , желтухой , зудом , потерей веса и лихорадкой . [12]
Варианты лечения могут включать хирургическое вмешательство , таргетную терапию и лучевую терапию . [1] В некоторых случаях абляционная терапия , эмболизирующая терапия или трансплантация печени . может быть использована [1]
Классификация
[ редактировать ]печени, Рак печени может возникать из паренхимы а также из других структур печени, таких как желчные протоки , кровеносные сосуды и иммунные клетки. [13] Существует множество подтипов рака печени, наиболее распространенные из которых описаны ниже.
Гепатоцеллюлярная карцинома
[ редактировать ]
Наиболее частым раком печени, на долю которого приходится примерно 75% всех первичных раков печени, является гепатоцеллюлярная карцинома (ГЦК). [15] ГЦК — это рак, образованный клетками печени, известными как гепатоциты , которые становятся злокачественными. С точки зрения смертности от рака во всем мире ГЦК считается третьей по распространенности причиной смертности от рака. [16]
Что касается диагностики ГЦК, людям с факторами риска (включая известные хронические заболевания печени , цирроз печени и т. д.) рекомендуется проходить скрининговое ультразвуковое исследование. Если ультразвуковое исследование показывает очаговую область размером более 1 сантиметра, пациентам следует пройти трехфазную КТ или МРТ с контрастным усилением . [17] Затем ГЦК можно диагностировать рентгенологически с использованием системы отчетности и данных по визуализации печени (LI-RADS). [18] Существует также вариантный тип ГЦК, который состоит как из ГЦК, так и из холангиокарциномы. [19]
Внутрипеченочная холангиокарцинома
[ редактировать ]Рак желчных протоков ( холангиокарцинома и холангиоцеллюлярная цистаденокарцинома ) составляют примерно 6% первичных раков печени. [20] Внутрипеченочная холангиокарцинома (ОПХ) — эпителиальный рак ветвей внутрипеченочного желчного дерева. [21] Внутрипеченочный ОКА является второй по значимости причиной первичного рака печени. [21] Чаще встречается у мужчин и обычно диагностируется у 60-70 лет. [21] Факторы риска развития внутрипеченочного ОКА включают Opisthorchus viverrini инфекцию Clonorchis sinensis , инфекцию , склерозирующий холангит , кисты холедоха , перенесенные процедуры на желчном дереве, воздействие торотраста и диоксинов и цирроз печени . [21] Этот рак обычно протекает бессимптомно, пока заболевание не прогрессирует. Симптомы включают боль в животе, ночную потливость, потерю веса и усталость. [21] Маркерами печени, уровень которых может повышаться при внутрипеченочном CCA, являются карциноэмбриональный антиген (CEA) , CA19-9 и CA-125 . [21]
Ангиосаркома и гемангиосаркома
[ редактировать ]Это редкие и агрессивные виды рака печени, однако они являются третьим по распространенности первичным раком печени, составляя 0,1–2,0% от первичного рака печени. [22] Ангиосаркома и гемангиосаркома печени происходят из эндотелиального слоя кровеносных сосудов . Эти опухоли имеют плохие результаты, поскольку они быстро растут и легко метастазируют . Их также трудно диагностировать, но их обычно подозревают при КТ или МРТ , на которых видны очаговые поражения с разной интенсивностью сигнала (эти опухоли характеризуются обильным кровотечением или кровоизлиянием и последующим отмиранием ткани ( некрозом )). [23] Биопсия с гистопатологической оценкой позволяет поставить окончательный диагноз. [22] Хотя причина часто никогда не выявляется (75% случаев являются идиопатическими ), они связаны с воздействием таких веществ, как винилхлорид , мышьяк , торотраст (например, профессиональное воздействие). Радиация также является фактором риска. [22] У взрослых эти опухоли чаще встречаются у мужчин; однако у детей они чаще встречаются у женщин. [22]
Даже после операции прогноз плохой: большинство людей не живут дольше шести месяцев после постановки диагноза. Лишь 3% особей живут дольше двух лет. [22]
Гепатобластома
[ редактировать ]Другим типом рака, образованным клетками печени, является гепатобластома , которая образуется из незрелых клеток печени. [20] Это редкая злокачественная опухоль, которая преимущественно развивается у детей и составляет примерно 1% всех случаев рака у детей и 79% всех первичных раков печени в возрасте до 15 лет. [24] [25] Большинство гепатобластом формируются в правой доле. [26]
Метастазирование в печень
[ редактировать ]Многие виды рака, обнаруживаемые в печени, не являются истинным раком печени, а представляют собой раковые заболевания из других участков тела, которые распространились на печень (известные как метастазы ). Часто местом происхождения является желудочно-кишечный тракт , поскольку печень расположена близко ко многим из этих метаболически активных, богатых кровью органов, вблизи кровеносных сосудов и лимфатических узлов (таких как рак поджелудочной железы , рак желудка , рак толстой кишки и карциноидные опухоли, главным образом, приложение , ), но и от рака молочной железы , рака яичников простаты рака легких , рака почек , рака .
Дети
[ редактировать ]Группа детской онкологии (COG) разработала протокол, помогающий диагностировать и лечить опухоли печени у детей. [27]
Причины
[ редактировать ]Вирусная инфекция
[ редактировать ]
Вирусная инфекция вирусом гепатита С (HCV) или вирусом гепатита B (HBV) сегодня является основной причиной рака печени в мире, на ее долю приходится 80% случаев ГЦК. [28] [29] [30] Мужчины с хроническим ВГС или ВГВ более склонны к развитию ГЦК, чем женщины с хроническим ВГС или ВГВ; однако причины этой гендерной разницы неизвестны. Инфекция HBV также связана с холангиокарциномой . [31] Роль других вирусов, кроме HCV или HBV, в развитии рака печени гораздо менее ясна, хотя есть некоторые доказательства того, что совместная инфекция HBV и вируса гепатита D может увеличить риск развития ГЦК. [32]
HBV и HCV могут привести к ГЦК, поскольку эти вирусные инфекции вызывают массивное воспаление , фиброз и, в конечном итоге, возникает цирроз печени. [33] Кроме того, при инфекции HCV и HBV в клетках печени формируется множество генетических и эпигенетических изменений, что является основным фактором образования опухолей печени. Вирусы вызывают злокачественные изменения в клетках, изменяя метилирование генов , влияя на экспрессию генов и стимулируя или подавляя пути передачи клеточного сигнала . Поступая таким образом, вирусы могут предотвратить запрограммированную форму гибели клеток ( апоптоз ) и способствовать репликации и персистенции вируса. [28] [34]
HBV и HCV также вызывают злокачественные изменения, вызывая повреждение ДНК и нестабильность генома . Это включает в себя генерацию активных форм кислорода , экспрессию белков, которые мешают ферментам репарации ДНК, и индуцированную ВГС активацию мутаторного фермента . [35] [36]
цирроз печени
[ редактировать ]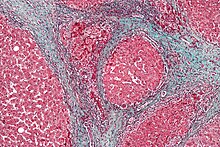
Помимо описанного выше вирусного цирроза , к ГЦК могут привести и другие причины цирроза. Употребление алкоголя коррелирует с риском развития ГЦК, причем риск намного выше у людей с циррозом печени, вызванным алкоголем. [37] Известно несколько заболеваний, которые вызывают цирроз печени и приводят к раку, включая наследственный гемохроматоз и первичный билиарный цирроз печени . [38]
Афлатоксин
[ редактировать ]Воздействие афлатоксина может привести к развитию ГЦК. [39] Афлатоксины представляют собой группу химических веществ, вырабатываемых грибами Aspergillus flavus (название происходит от токсина A. flavus ) и A. parasiticus . Заражение пищевых продуктов грибками приводит к попаданию в организм химических веществ, которые очень токсичны для печени. Обычными продуктами питания, загрязненными токсинами, являются крупы, арахис и другие овощи. Количество (доза) и продолжительность (продолжительность) контакта человека с афлатоксином связаны с ГЦК. [39] Загрязнение пищевых продуктов распространено в Африке, Юго-Восточной Азии и Китае. Механизм, с помощью которого афлатоксины вызывают рак, заключается в мутациях и эпигенетических изменениях . Афлатоксины вызывают целый спектр мутаций, [40] [41] в том числе в p53 гене- супрессоре опухоли , мутация которого наблюдается при многих типах рака. [40] Мутация р53, предположительно в сочетании с другими мутациями, вызванными афлатоксином, и эпигенетическими изменениями. [42] , индуцированного афлатоксином вероятно, является частой причиной канцерогенеза .
Неалкогольный стеатогепатит (НАСГ) и неалкогольная жировая печень (НАФЛ)
[ редактировать ]НАСГ и НАФЛ начинают называть фактором риска рака печени, особенно ГЦК. [43] В последние годы отмечено увеличение количества трансплантаций печени по поводу ГЦК, обусловленного НАСГ. [39] Необходимы дополнительные исследования в этой области и NASH/NAFL. [43]
Другие факторы риска у взрослых
[ редактировать ]- Диспластические узелки высокой степени злокачественности являются предраковыми поражениями печени. В течение двух лет риск развития рака из-за этих узелков составляет 30–40%. [44]
- Ожирение и метаболический синдром стали важными факторами риска, поскольку они могут привести к стеатогепатиту . [30] [45]
- Диабет увеличивает риск развития ГЦК. [45] [39]
- Курение увеличивает риск развития ГЦК по сравнению с некурящими и бывшими курильщиками. [45]
- составляет около 5–10% Риск развития холангиокарциномы в течение жизни у людей с первичным склерозирующим холангитом . [46]
- Инфекция печеночного двуустка увеличивает риск развития холангиокарциномы , и именно по этой причине в Таиланде особенно высок уровень заболеваемости этим раком. [47]
- Кисты холедоха , болезнь Кароли и врожденный фиброз печени связаны с развитием холангиокарциномы. [48]
- Генетические состояния : нелеченный наследственный гемохроматоз , дефицит альфа-1-антитрипсина , болезни накопления гликогена , поздняя кожная порфирия , болезнь Вильсона , тирозинемия - все они связаны с развитием ГЦК. [39] [43]
- Пероральные контрацептивы . Недостаточно доказательств, чтобы считать пероральные контрацептивы фактором риска. Однако недавние исследования показали, что прием пероральных контрацептивов в течение более пяти лет связан с ГЦК. [39]
Дети
[ редактировать ]Рак печени у детей встречается редко. [27] Подтипами рака печени, наиболее часто встречающимися у детей, являются гепатобластома , гепатоцеллюлярная карцинома , эмбриональная саркома печени, инфантильная хориокарцинома печени и билиарная рабдомиосаркома. [27] Повышенный риск рака печени у детей может быть вызван синдромом Беквита-Видемана (связанным с гепатобластомой), [49] [50] семейный аденоматозный полипоз (связанный с гепатобластомой), [50] низкий вес при рождении (связанный с гепатобластомой), [26] Прогрессирующий семейный внутрипеченочный холестаз (связанный с ГЦК) [51] и трисомия 18 (связанная с гепатобластомой). [50]
Диагностика
[ редактировать ]Многие методы визуализации используются для диагностики рака печени. Для ГЦК к ним относятся медицинское УЗИ , компьютерная томография (КТ) и магнитно-резонансная томография (МРТ). При визуализации печени с помощью ультразвука большие поражения, скорее всего, будут ГЦК (например, опухоль размером более 2 см имеет более 95% шансов быть ГЦК). Учитывая приток крови к печени , ГЦК будет наиболее заметен при контрастировании. течет через артерии печени (также называемая артериальной фазой), а не когда контраст течет через вены (также называемая венозной фазой). [17] Иногда врачи назначают биопсию печени , если их беспокоит ГЦК, а визуализирующие исследования (КТ или МРТ) не дают четких результатов. [17] Большинство холангиокарцим возникают в прикорневой области печени и часто проявляются обструкцией желчных протоков. При подозрении на злокачественную причину обструкции эндоскопическую ретроградную холангиопанкреатографию (ЭРХПГ), УЗИ, КТ, МРТ и магнитно-резонансную холангиопанкреатографию (МРХПГ). применяют [52]
Опухолевые маркеры — химические вещества, которые иногда обнаруживаются в крови людей, больных раком, — могут быть полезны в диагностике и мониторинге течения рака печени. Высокие уровни альфа-фетопротеина (АФП) в крови можно обнаружить во многих случаях ГЦК и внутрипеченочной холангиокарциномы. [17] Следует отметить, что АФП наиболее полезен для мониторинга рецидивов рака печени после лечения, а не для первоначальной диагностики. [17] Холангиокарциному можно обнаружить с помощью этих широко используемых опухолевых маркеров: углеводного антигена 19-9 (CA 19-9), карциноэмбрионального антигена (CEA) и ракового антигена 125 ( CA125 ). Эти опухолевые маркеры обнаруживаются при первичном раке печени, а также при других видах рака и некоторых других заболеваниях. [53] [54]
Профилактика
[ редактировать ]Профилактику рака можно разделить на первичную, вторичную и третичную. Первичная профилактика упреждающе снижает воздействие фактора риска рака печени. Одной из наиболее успешных мер первичной профилактики рака печени является вакцинация против гепатита В. [43] Вакцинация против вируса гепатита С в настоящее время недоступна. [55] Другие формы первичной профилактики направлены на ограничение передачи этих вирусов путем пропаганды безопасной практики инъекций, проверки продуктов донорства крови и скрининга бессимптомных лиц из группы высокого риска. [55] Воздействия афлатоксина можно избежать, приняв меры по предотвращению появления плесени после сбора урожая, которые оказались эффективными в Западной Африке . Снижение уровня расстройств, связанных с употреблением алкоголя , ожирения и сахарного диабета также снизит уровень заболеваемости раком печени. Контроль диеты при гемохроматозе может снизить риск перегрузки железом , снижая риск рака. [56]
Вторичная профилактика включает в себя как излечение от возбудителя, участвующего в формировании рака ( канцерогенез ), так и предупреждение канцерогенеза, если это невозможно. Вылечить инфицированных вирусом людей невозможно, но лечение противовирусными препаратами может снизить риск развития рака печени. Хлорофиллин может потенциально снижать воздействие афлатоксина. [56]
Третичная профилактика включает лечение, направленное на предотвращение рецидива рака печени. К ним относятся применение хирургических вмешательств, химиотерапевтических препаратов и противовирусных препаратов. [56]
Уход
[ редактировать ]Общие соображения
[ редактировать ]Как и при многих видах рака, лечение зависит от конкретного типа рака печени, а также от стадии рака. Основной способ определения стадии рака основан на системе стадирования TMN . Существуют также системы стадирования рака печени, каждая из которых имеет варианты лечения, которые могут привести к предотвращению рецидива рака или излечению. [57] [58] [59] Например, при ГЦК обычно используется система стадирования рака печени клиники Барселона. [39]
Лечение включает хирургическое вмешательство, медикаментозное лечение и методы абляции. Существует множество химиотерапевтических препаратов, одобренных для лечения рака печени, в том числе: атезолизумаб , ниволумаб , пембролизумаб , регорафениб . [60] Все чаще иммунотерапевтические агенты (также называемые таргетной терапией рака или точной медициной ) используются для лечения гепатобилиарного рака . [61]
Последние достижения в лечении рака печени заключаются в изучении Т-клеток, созданных с использованием химерных антигенных рецепторов (CAR), нацеленных на глипикан-3 (GPC3), таких как GAP T-клетки, которые демонстрируют потенциал в борьбе с GPC3-положительными опухолями, особенно при раке печени у детей. [62] [63]
Гепатоцеллюлярная карцинома
[ редактировать ] этого раздела Фактическая точность может быть нарушена из-за устаревшей информации . ( июнь 2017 г. ) |

Частичная хирургическая резекция является рекомендуемым методом лечения гепатоцеллюлярной карциномы (ГЦК), когда у пациентов имеется достаточный резерв функции печени. [39] За последние несколько десятилетий 5-летняя выживаемость после резекции значительно улучшилась и теперь может варьироваться от 41 до 74%. [39] Однако частота рецидивов после резекции может превышать 70%, будь то из-за распространения исходной опухоли или образования новых опухолей. [64] Трансплантацию печени также можно рассмотреть в случаях ГЦК, когда эта форма лечения переносится и опухоль соответствует определенным критериям (например, Миланским критериям ). Как правило, пациенты, которым рассматривается возможность трансплантации печени, имеют множественные поражения печени, тяжелую дисфункцию печени или и то, и другое.
Чрескожная абляция — единственный нехирургический метод лечения, который может обеспечить излечение. Существует множество форм чрескожной абляции, которые заключаются либо в инъекциях химических веществ в печень ( этанол или уксусная кислота ), либо в создании экстремальных температур с использованием радиочастотной абляции , микроволн , лазеров или криотерапии . Среди них радиочастотная абляция имеет одну из лучших репутаций при ГЦК, но ограничения включают в себя неспособность лечить опухоли, расположенные вблизи других органов и кровеносных сосудов, из-за выделения тепла и эффекта теплоотвода соответственно. [65] [66] Кроме того, долгосрочные результаты процедур чрескожной абляции при ГЦК недостаточно изучены. В целом, если это возможно, хирургическое вмешательство является предпочтительным методом лечения.
Системные химиотерапевтические средства обычно не используются при ГЦК, хотя местную химиотерапию можно использовать в процедуре, известной как трансартериальная химиоэмболизация (ТАСЕ). При этой процедуре на опухоль вводятся препараты, убивающие раковые клетки и прерывающие кровоснабжение. Поскольку большинство системных препаратов неэффективны при лечении ГЦК, исследования молекулярных путей, участвующих в образовании рака печени, позволили создать сорафениб , препарат таргетной терапии , который предотвращает пролиферацию клеток и рост клеток крови . Сорафениб получил одобрение FDA для лечения распространенной гепатоцеллюлярной карциномы в ноябре 2007 года. [67] Этот препарат обеспечивает преимущество в выживаемости при поздней стадии ГЦК. [66]
Трансартериальная радиоэмболизация (TRACE) является еще одним вариантом лечения ГЦК. [39] В этой процедуре лучевое лечение нацелено на опухоль. TRACE по-прежнему считается дополнением к лечению, а не препаратом первого выбора для лечения ГЦК. [39] поскольку двойное лечение лучевой терапией плюс химиоэмболизация, местная химиотерапия, системная химиотерапия или препараты таргетной терапии могут оказаться более эффективными по сравнению с одной только лучевой терапией. [68]
Методы абляции (например, радиочастотная абляция или микроволновая абляция ) также являются вариантом лечения ГЦК. [39] [69] Этот метод рекомендуется при небольших локализованных опухолях печени, поскольку рекомендуется, чтобы площадь, подвергаемая радиочастотной абляции, составляла 2 сантиметра или меньше. [69]

Внутрипеченочная холангиокарцинома
[ редактировать ]Резекция является вариантом лечения холангиокарциномы, но менее 30% случаев холангиокарциномы операбельны на момент постановки диагноза. Причина, по которой большинство внутрипеченочных холангиокарцином не поддаются хирургическому удалению, заключается в том, что в печени часто наблюдаются множественные очаговые опухоли. [70] После операции частота рецидивов достигает 60%. [71] [72] Трансплантация печени может использоваться там, где частичная резекция невозможна, а адъювантная химиолучевая терапия . в некоторых случаях может помочь [46]
60% холангиокарцином формируются в перихилярной области, и фотодинамическую терапию можно использовать для улучшения качества жизни и увеличения времени выживания. в этих неоперабельных случаях [48] Фотодинамическая терапия — это новый метод лечения опухоли, в котором для лечения опухоли используются активированные светом молекулы. Соединения активируются в области опухоли лазерным светом, который вызывает высвобождение токсичных активных форм кислорода, убивающих опухолевые клетки. [71] [73]
Системная химиотерапия, такая как гемцитабин и цисплатин, иногда используется в неоперабельных случаях холангиокарциномы. [46]
Радиочастотная абляция , трансартериальная химиоэмболизация и внутренняя лучевая терапия ( брахитерапия ) являются перспективными в лечении холангиокарциномы. [72] и иногда может улучшить отток желчи , что может уменьшить симптомы, которые испытывает пациент. [70]
Лучевая терапия может использоваться в качестве адъювантного или паллиативного лечения холангиокарциномы. [74]
Гепатобластома
[ редактировать ]Удаление опухоли путем хирургической резекции или трансплантации печени может быть использовано при лечении гепатобластомы. В некоторых случаях хирургическое вмешательство может помочь излечиться. Химиотерапию можно использовать до и после операции и трансплантации. [75]
Химиотерапия , включая цисплатин , винкристин , циклофосфамид и доксорубицин , используется для системного лечения гепатобластомы. Из этих препаратов цисплатин кажется наиболее эффективным. [76]
Ангиосаркома и гемангиосаркома
[ редактировать ]Многие из этих опухолей в конечном итоге не поддаются хирургическому лечению. [23] Варианты лечения включают хирургическое удаление пораженных частей печени. [22] Трансплантация печени и химиотерапия не эффективны при ангиосаркомах и гемангиосаркомах печени. [22]
Эпидемиология
[ редактировать ]
Во всем мире рак печени распространен и растет. [10] Самые последние эпидемиологические данные показывают, что рак печени входит в десятку наиболее частых причин как по распространенности, так и по смертности (отмечено, что он является шестой по распространенности причиной рака и четвертой по распространенности причиной смерти). [43] Сотрудничество по глобальному бремени заболеваний раком печени обнаружило, что с 1990 по 2015 год количество новых случаев рака печени в год увеличивалось на 75%. [10] По оценкам, основанным на самых последних данных, каждый год во всем мире диагностируется 841 000 новых диагнозов рака печени и 782 000 случаев смерти. [55] Рак печени является наиболее распространенным раком в Египте , Гамбии , Гвинее , Монголии , Камбодже и Вьетнаме . [55] С точки зрения гендерной разбивки, во всем мире рак печени чаще встречается у мужчин, чем у женщин. [43] [55]
Учитывая, что ГЦК является наиболее распространенным типом рака печени, регионами мира с наибольшим количеством новых случаев ГЦК каждый год являются Северная и Западная Африка, а также Восточная и Юго-Восточная Азия. [43] В Китае зарегистрировано 50% случаев ГЦК во всем мире, и более 80% от общего числа случаев приходится на страны Африки к югу от Сахары или в Восточную Азию из-за гепатита В. вируса [47] [77] Фактические данные указывают на то, что в этих регионах с высоким бременем болезней большинство инфекций HBC и HCV происходит перинатально (также называемая передачей от матери ребенку). [43] Однако важно отметить, что факторы риска ГЦК варьируются в зависимости от географического региона. Например, в хроническая Китае инфекция ВГВ и афлатоксин являются крупнейшими факторами риска; тогда как в Монголии является сочетание сочетанной инфекции ВГВ и ВГС , а также высокого уровня употребления алкоголя . причиной высокого уровня ГЦК [55]
Что касается внутрипеченочной холангиокарциномы, то в настоящее время у нас нет достаточных эпидемиологических данных, поскольку это редкий вид рака. По данным Национального института рака США, частота возникновения холангиокарциномы неизвестна. Холангиокарцинома также имеет значительное географическое распространение: в Таиланде наблюдаются самые высокие показатели заболеваемости во всем мире из-за присутствия печеночного двуустка. [47] [78]
В США в 2020 году было зарегистрировано 42 810 новых случаев рака печени и внутрипеченочных желчных протоков, что составляет 2,4% от всех новых случаев рака в США. [79] В Соединенных Штатах около 89 950 человек страдают раком печени и внутрипеченочным раком печени. [79] Что касается смертности, 5-летняя выживаемость при раке печени и внутрипеченочных желчных протоков в США составляет 19,6%. [79] В Соединенных Штатах вероятность заболеть раком печени на протяжении всей жизни оценивается в 1%, что делает этот рак относительно редким. [79] Несмотря на небольшое количество случаев, это одна из основных причин смертности от рака. [43]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г «Первичное лечение рака печени у взрослых (PDQ®) – версия для пациентов» . НЦИ . 6 июля 2016 года. Архивировано из оригинала 2 октября 2016 года . Проверено 29 сентября 2016 г.
- ^ Перейти обратно: а б с «Информационные бюллетени SEER: рак печени и внутрипеченочных желчных протоков» . НЦИ . Архивировано из оригинала 28 июля 2017 г.
- ^ Перейти обратно: а б с д и ж г час я Всемирный доклад о раке, 2014 год . Всемирная организация здравоохранения. 2014. С. Глава 5.6. ISBN 978-9283204299 .
- ^ Перейти обратно: а б Нагави М., Ван Х., Лозано Р., Дэвис А., Лян Х., Чжоу М. и др. (GBD 2013 Смертность, причины смерти сотрудников) (январь 2015 г.). «Глобальная, региональная и национальная смертность от всех причин и по конкретным причинам в разбивке по возрасту и по конкретным причинам по 240 причинам смерти, 1990–2013 гг.: систематический анализ для исследования глобального бремени болезней, 2013 г.» . Ланцет . 385 (9963): 117–171. дои : 10.1016/S0140-6736(14)61682-2 . ПМК 4340604 . ПМИД 25530442 .
- ^ «Сводные данные о внутрибольничных онкологических регистрах, таких как базовые больницы по лечению рака: [Регистр рака / Статистика Национального онкологического центра]» Проверено . 2 февраля 2020 г. .
- ^ Вос Т., Аллен С., Арора М., Барбер Р.М., Бхутта З.А., Браун А. и др. (октябрь 2016 г.). «Глобальная, региональная и национальная заболеваемость, распространенность и продолжительность жизни с инвалидностью по 310 заболеваниям и травмам, 1990-2015 гг.: систематический анализ для исследования глобального бремени болезней 2015 г.» . Ланцет . 388 (10053): 1545–1602. дои : 10.1016/S0140-6736(16)31678-6 . ПМК 5055577 . ПМИД 27733282 .
- ^ Перейти обратно: а б с Брэй Ф., Ферлей Дж., Сурджоматарам И., Сигел Р.Л., Торре Л.А., Джемал А. (ноябрь 2018 г.). «Глобальная статистика рака за 2018 год: оценки GLOBOCAN заболеваемости и смертности во всем мире от 36 видов рака в 185 странах» . КА . 68 (6): 394–424. дои : 10.3322/caac.21492 . ПМИД 30207593 . S2CID 52188256 .
- ^ Перейти обратно: а б с Брюикс Дж., Хан К.Х., Горс Дж., Лловет Дж.М., Маццаферро В. (апрель 2015 г.). «Рак печени: подход к индивидуальному лечению» . Журнал гепатологии . 62 (1 дополнение): S144–S156. дои : 10.1016/j.jhep.2015.02.007 . ПМК 4520430 . ПМИД 25920083 .
- ^ Перейти обратно: а б Мантовани А., Таргер Г. (июль 2017 г.). «Сахарный диабет 2 типа и риск гепатоцеллюлярной карциномы: внимание к неалкогольной жировой болезни печени» . Анналы трансляционной медицины . 5 (13): 270. doi : 10.21037/атм.2017.04.41 . ПМК 5515814 . ПМИД 28758096 .
- ^ Перейти обратно: а б с Акинемию Т., Абера С., Ахмед М., Алам Н., Алемайоху М.А., Аллен С. и др. (декабрь 2017 г.). «Бремя первичного рака печени и его этиологии с 1990 по 2015 год на глобальном, региональном и национальном уровне: результаты исследования глобального бремени болезней, 2015 год» . JAMA Онкология . 3 (12): 1683–1691. дои : 10.1001/jamaoncol.2017.3055 . hdl : 10037/11672 . ПМЦ 5824275 . ПМИД 28983565 .
- ^ Холангиокарцинома в eMedicine
- ^ «Опухоли печени у детей» . Бостонская детская больница. Архивировано из оригинала 4 июня 2011 г.
- ^ «Рак печени – Симптомы и причины» . Клиника Мэйо . Проверено 06 февраля 2023 г.
- ^ Таблица 37.2 в: Штернберг С (2012). Диагностика хирургической патологии Штернберга . Место издания не указано: LWW. ISBN 978-1-4511-5289-0 . OCLC 953861627 .
- ^ Ян Дж.Д., Эно П., Горс Г.Дж., Амаду А., Плимот А., Робертс Л.Р. (октябрь 2019 г.). «Глобальный взгляд на гепатоцеллюлярную карциному: тенденции, риск, профилактика и лечение» . Обзоры природы. Гастроэнтерология и гепатология . 16 (10): 589–604. дои : 10.1038/s41575-019-0186-y . ПМК 6813818 . ПМИД 31439937 .
- ^ Мокдад А.А., Сингал АГ, Йопп АС (22 декабря 2015 г.). «СТРАНИЦА ПАЦИЕНТА JAMA. Рак печени». ДЖАМА . 314 (24): 2701. дои : 10.1001/jama.2015.15425 . ПМИД 26720038 .
- ^ Перейти обратно: а б с д и «Первичное лечение рака печени у взрослых (PDQ®) – версия для медицинских работников – Национальный институт рака» . www.cancer.gov . 15 января 2021 г. Проверено 25 февраля 2021 г.
- ^ Митчелл Д.Г., Брюикс Дж., Шерман М., Сирлин CB (март 2015 г.). «LI-RADS (система отчетов и данных о визуализации печени): резюме, обсуждение и консенсус рабочей группы по управлению LI-RADS и будущие направления» . Гепатология . 61 (3): 1056–1065. дои : 10.1002/hep.27304 . ПМИД 25041904 . S2CID 205894014 .
- ^ Хан С.А., Дэвидсон Б.Р., Голдин Р.Д., Хитон Н., Карани Дж., Перейра С.П. и др. (декабрь 2012 г.). «Руководство по диагностике и лечению холангиокарциномы: обновление» . Гут . 61 (12): 1657–1669. дои : 10.1136/gutjnl-2011-301748 . ПМИД 22895392 .
- ^ Перейти обратно: а б Ахмед I, Лобо Д.Н. (январь 2009 г.). «Злокачественные опухоли печени». Операция . 27 (1). Оксфорд: 30–37. дои : 10.1016/j.mpsur.2008.12.005 .
- ^ Перейти обратно: а б с д и ж Дули Дж.С., Лок А.С., Гарсиа-Цао Дж., Пинцани М. (8 июня 2018 г.). Шерлоковские болезни печени и желчевыводящей системы . Джон Уайли и сыновья. стр. 705–729. ISBN 978-1-119-23764-8 . OCLC 1187411089 .
- ^ Перейти обратно: а б с д и ж г Кумар А., Шарма Б., Самант Х. (2021 г.). «Ангиосаркома печени» . СтатПерлс . Остров сокровищ (Флорида): StatPearls Publishing. ПМИД 30855812 . Проверено 25 февраля 2021 г.
- ^ Перейти обратно: а б Чен Н, Ю А, Юнг Дж (31 мая 2018 г.). «Выбор редакции: Первичная ангиосаркома печени: краткий обзор литературы» . Emj Hepatol Гепатология 6.1 2018 . 6 (1): 64–71. дои : 10.33590/emjhepatol/10314175 . S2CID 53063864 . Проверено 25 февраля 2021 г.
- ^ Редакционная коллегия PDQ по педиатрическому лечению (2002 г.), «Лечение рака печени у детей (PDQ®): версия для медицинских работников» , Сводка информации о раке PDQ , Bethesda (MD): Национальный институт рака (США), PMID 26389232 , получено 25 февраля 2021 г.
- ^ Ханна Р., Верма С.К. (сентябрь 2018 г.). «Детская гепатоцеллюлярная карцинома» . Всемирный журнал гастроэнтерологии . 24 (35): 3980–3999. дои : 10.3748/wjg.v24.i35.3980 . ПМК 6148423 . ПМИД 30254403 .
- ^ Перейти обратно: а б Эмре С., Маккенна Дж.Дж. (декабрь 2004 г.). «Опухоли печени у детей». Детская трансплантация . 8 (6): 632–638. дои : 10.1111/j.1399-3046.2004.00268.x . ПМИД 15598339 . S2CID 35883310 .
- ^ Перейти обратно: а б с «Лечение рака печени у детей (PDQ®) – Версия для медицинских работников – Национальный институт рака» . www.cancer.gov . 27.11.2020 . Проверено 25 февраля 2021 г.
- ^ Перейти обратно: а б Арзуманян А, Рейс Х.М., Фейтельсон М.А. (февраль 2013 г.). «Патогенетические механизмы гепатоцеллюлярной карциномы, ассоциированной с HBV и HCV». Обзоры природы. Рак . 13 (2): 123–135. дои : 10.1038/nrc3449 . ПМИД 23344543 . S2CID 29447705 .
- ^ Розен HR (июнь 2011 г.). «Клиническая практика. Хронический гепатит С». Медицинский журнал Новой Англии . 364 (25): 2429–2438. дои : 10.1056/NEJMcp1006613 . ПМИД 21696309 . S2CID 19755395 .
- ^ Перейти обратно: а б «Общая информация о первичном раке печени у взрослых» . Национальный институт ракаb. 1 января 1980 г. Архивировано из оригинала 2 января 2013 года . Проверено 13 января 2013 г.
- ^ Ральфс С., Хан С.А. (май 2013 г.). «Роль вирусов гепатита в холангиокарциноме». Журнал вирусного гепатита . 20 (5): 297–305. дои : 10.1111/jvh.12093 . ПМИД 23565610 . S2CID 44318080 .
- ^ Кью MC (март 2013 г.). «Вирусы гепатита (кроме вирусов гепатита B и C) как причины гепатоцеллюлярной карциномы: обновленная информация». Журнал вирусного гепатита . 20 (3): 149–157. дои : 10.1111/jvh.12043 . ПМИД 23383653 . S2CID 206164005 .
- ^ Дули Дж.С., Лок А.С., Гарсиа-Цао Дж., Пинцани М. (8 июня 2018 г.). Дули Дж.С., Лок А.С., Гарсия-Цао Дж., Пинцани М. (ред.). Заболевания печени и желчевыводящей системы Шерлока . Джон Уайли и сыновья. ISBN 978-1-119-23756-3 . OCLC 1019837000 .
- ^ Чон С.В., Чан Дж.И., Чунг РТ (декабрь 2012 г.). «Вирус гепатита С и гепатокарциногенез» . Клиническая и молекулярная гепатология . 18 (4): 347–356. дои : 10.3350/cmh.2012.18.4.347 . ПМК 3540370 . ПМИД 23323249 .
- ^ Такеда Х., Такаи А., Инузука Т., Марусава Х. (январь 2017 г.). «Генетическая основа гепатоцеллюлярной карциномы, связанной с вирусом гепатита: связь между инфекцией, воспалением и онкогенезом» . Журнал гастроэнтерологии . 52 (1): 26–38. дои : 10.1007/s00535-016-1273-2 . ПМИД 27714455 .
- ^ Ян С.Ф., Чанг К.В., Вэй Р.Дж., Шиуэ Ю.Л., Ван С.Н., Йе Ю.Т. (2014). «Вовлечение путей ответа на повреждение ДНК при гепатоцеллюлярной карциноме» . БиоМед Исследования Интернэшнл . 2014 : 153867. дои : 10.1155/2014/153867 . ПМК 4022277 . ПМИД 24877058 .
- ^ Ду Х, Хидаят К., Ши Б.М. (июнь 2017 г.). «Абдоминальное ожирение и риск рака пищевода: систематический обзор и метаанализ проспективных исследований» . Отчеты по биологическим наукам . 37 (3): BSR20160474. дои : 10.1042/BSR20160474 . ПМЦ 5426287 . ПМИД 28336766 .
- ^ Фаттович Г., Строффолини Т., Загни И., Донато Ф. (ноябрь 2004 г.). «Гепатоцеллюлярная карцинома при циррозе печени: заболеваемость и факторы риска» . Гастроэнтерология . 127 (5 Приложение 1): С35–С50. дои : 10.1053/j.gastro.2004.09.014 . ПМИД 15508101 .
- ^ Перейти обратно: а б с д и ж г час я дж к л Балог Дж., Виктор Д., Эшам Э.Х., Берроуз С.Г., Боктур М., Сахария А. и др. (октябрь 2016 г.). «Гепатоцеллюлярная карцинома: обзор» . Журнал гепатоцеллюлярной карциномы . 3 : 41–53. дои : 10.2147/JHC.S61146 . ПМК 5063561 . ПМИД 27785449 .
- ^ Перейти обратно: а б Смела М.Э., Карриер С.С., Бейли Э.А., Эссигманн Дж.М. (апрель 2001 г.). «Химия и биология афлатоксина B(1): от мутационной спектрометрии к канцерогенезу» . Канцерогенез . 22 (4): 535–545. дои : 10.1093/carcin/22.4.535 . ПМИД 11285186 .
- ^ Пердука В., Омичессан Х., Бальетто Л., Севери Дж. (январь 2018 г.). «Мутационные и эпигенетические признаки раковой ткани, связанные с воздействием окружающей среды и образом жизни». Современное мнение в онкологии . 30 (1): 61–67. doi : 10.1097/CCO.0000000000000418 . ПМИД 29076965 . S2CID 20842446 .
- ^ Дай Ю, Хуан К., Чжан Б, Чжу Л, Сюй В (ноябрь 2017 г.). «Эпигенетические изменения, вызванные афлатоксином B1: обзор». Пищевая и химическая токсикология . 109 (Часть 1): 683–689. дои : 10.1016/j.fct.2017.06.034 . ПМИД 28645871 .
- ^ Перейти обратно: а б с д и ж г час я «Профилактика (гепатоцеллюлярного) рака печени (PDQ®) – версия для медицинских работников – Национальный институт рака» . www.cancer.gov . 23 мая 2005 г. Проверено 23 февраля 2021 г.
- ^ Ди Томмазо Л., Санджованни А., Борзио М., Парк Ю.Н., Фаринати Ф., Ронкалли М. (апрель 2013 г.). «Распространенные предраковые поражения печени». Лучшие практики и исследования. Клиническая гастроэнтерология . 27 (2): 269–284. дои : 10.1016/j.bpg.2013.03.015 . ПМИД 23809245 .
- ^ Перейти обратно: а б с Чуанг СК, Ла Веккья К, Боффетта П (декабрь 2009 г.). «Рак печени: описательная эпидемиология и факторы риска, кроме инфекции ВГВ и ВГС». Письма о раке . 286 (1): 9–14. дои : 10.1016/j.canlet.2008.10.040 . hdl : 11585/682618 . ПМИД 19091458 .
- ^ Перейти обратно: а б с Разумилава Н., Горес Г.Дж. (январь 2013 г.). «Классификация, диагностика и лечение холангиокарциномы» . Клиническая гастроэнтерология и гепатология . 11 (1): 13–21.e1, викторина e3–4. дои : 10.1016/j.cgh.2012.09.009 . ПМК 3596004 . ПМИД 22982100 .
- ^ Перейти обратно: а б с Джемал А., Брэй Ф., Центр ММ, Ферлей Дж., Уорд Э., Форман Д. (март – апрель 2011 г.). «Глобальная статистика рака» . КА . 61 (2): 69–90. дои : 10.3322/caac.20107 . ПМИД 21296855 . S2CID 30500384 .
- ^ Перейти обратно: а б Патель Т. (апрель 2011 г.). «Холангиокарцинома - противоречия и проблемы» . Обзоры природы. Гастроэнтерология и гепатология . 8 (4): 189–200. дои : 10.1038/nrgastro.2011.20 . ПМЦ 3888819 . ПМИД 21460876 .
- ^ ДеБаун М.Р., Такер М.А. (март 1998 г.). «Риск развития рака в течение первых четырех лет жизни у детей из реестра синдромов Беквита-Видемана» . Журнал педиатрии . 132 (3 ч. 1): 398–400. дои : 10.1016/S0022-3476(98)70008-3 . ПМИД 9544889 .
- ^ Перейти обратно: а б с Спектор Л.Г., Берч Дж. (ноябрь 2012 г.). «Эпидемиология гепатобластомы» . Детская кровь и рак . 59 (5): 776–779. дои : 10.1002/pbc.24215 . ПМИД 22692949 . S2CID 65545 .
- ^ Давит-Спраул А., Гонсалес Э., Боссан С., Жакмен Э. (январь 2009 г.). «Прогрессирующий семейный внутрипеченочный холестаз» . Сиротский журнал редких заболеваний . 4 :1. дои : 10.1186/1750-1172-4-1 . ПМК 2647530 . ПМИД 19133130 .
- ^ Арифф Б., Ллойд Ч.Р., Хан С., Шариф М., Тиллайнаягам А.В., Банси Д.С. и др. (март 2009 г.). «Визуализация рака печени» . Всемирный журнал гастроэнтерологии . 15 (11): 1289–1300. дои : 10.3748/wjg.15.1289 . ПМЦ 2658841 . ПМИД 19294758 .
- ^ Малагуарнера Г, Паладина И, Джордано М, Малагуарнера М, Бертино Дж, Берретта М (2013). «Сывороточные маркеры внутрипеченочной холангиокарциномы» . Маркеры заболеваний . 34 (4): 219–228. дои : 10.1155/2013/196412 . ПМЦ 3809974 . ПМИД 23396291 .
- ^ Чжао Ю.Дж., Цзюй Ц., Ли Г.К. (июль 2013 г.). «Онкомаркеры гепатоцеллюлярной карциномы» . Молекулярная и клиническая онкология . 1 (4): 593–598. дои : 10.3892/mco.2013.119 . ПМЦ 3915636 . ПМИД 24649215 .
- ^ Перейти обратно: а б с д и ж Брэй Ф., Ферлей Дж., Сурджоматарам И., Сигел Р.Л., Торре Л.А., Джемал А. (ноябрь 2018 г.). «Глобальная статистика рака за 2018 год: оценки GLOBOCAN заболеваемости и смертности во всем мире от 36 видов рака в 185 странах» . КА . 68 (6): 394–424. дои : 10.3322/caac.21492 . ПМИД 30207593 .
- ^ Перейти обратно: а б с Хосида Ю., Фукс БК, Танабэ К.К. (ноябрь 2012 г.). «Профилактика гепатоцеллюлярной карциномы: потенциальные мишени, экспериментальные модели и клинические проблемы» . Текущие цели в области лекарств от рака . 12 (9): 1129–1159. дои : 10.2174/156800912803987977 . ПМЦ 3776581 . ПМИД 22873223 .
- ^ Йен Ю., Ченг Ю. Ф., Ван Дж. Х., Линь CC, Чен Ю., Юн CC и др. (12 марта 2020 г.). «Реальная мировая клиническая практика лечения распространенной гепатоцеллюлярной карциномы: когда Восток встречается с Западом» . ПЛОС ОДИН . 15 (3): e0230005. Бибкод : 2020PLoSO..1530005Y . дои : 10.1371/journal.pone.0230005 . ПМК 7067409 . ПМИД 32163475 .
- ^ Брюикс Дж., Шерман М. (март 2011 г.). «Лечение гепатоцеллюлярной карциномы: обновленная информация» . Гепатология . 53 (3): 1020–1022. дои : 10.1002/hep.24199 . ПМК 3084991 . ПМИД 21374666 .
- ^ Чен Ч. (01.12.2016). «Чрескожная радиочастотная абляция при гепатоцеллюлярной карциноме: короткая продолжительность не означает ее эффективности» . Достижения в области пищеварительной медицины . 3 (4): 149–150. дои : 10.1016/j.aidm.2016.10.001 . S2CID 44047011 .
- ^ «Лекарства, одобренные для лечения рака печени - Национальный институт рака» . www.cancer.gov . 04.10.2011 . Проверено 25 февраля 2021 г.
- ^ «Информационный бюллетень по таргетной терапии рака - Национальный институт рака» . www.cancer.gov . 25 января 2021 г. Проверено 25 февраля 2021 г.
- ^ Ли В., Го Л., Рати П., Маринова Э., Гао Х., Ву М.Ф. и др. (май 2017 г.). «Перенаправление Т-клеток на глипикан-3 с помощью химерных антигенных рецепторов 4-1BB приводит к поляризации Th1 и мощной противоопухолевой активности» . Генная терапия человека . 28 (5): 437–448. дои : 10.1089/hum.2016.025 . ПМЦ 5444493 . ПМИД 27530312 .
- ^ Номер клинического исследования NCT02932956 «Глипикан-3-специфичный химерный антигенный рецептор, экспрессируемый в Т-клетках для пациентов с детскими солидными опухолями (GAP)» на сайте ClinicalTrials.gov.
- ^ Брюикс Дж., Шерман М. (март 2011 г.). «Лечение гепатоцеллюлярной карциномы: обновленная информация» . Гепатология . 53 (3): 1020–1022. дои : 10.1002/hep.24199 . ПМК 3084991 . ПМИД 21374666 .
- ^ Ван З, Чжан Г, Ву Дж, Цзя М (август 2013 г.). «Адъювантная терапия гепатоцеллюлярной карциномы: современное состояние и перспективы» . Открытия лекарств и терапия . 7 (4): 137–143. дои : 10.5582/ddt.2013.v7.4.137 . ПМИД 24071575 .
- ^ Перейти обратно: а б де Лопе Ч.Р., Тремозини С., Форнер А., Рейг М., Брюикс Дж. (2012). «Управление ЖЦК». Журнал гепатологии . 56 (Приложение 1): S75–S87. дои : 10.1016/S0168-8278(12)60009-9 . ПМИД 22300468 . S2CID 5349344 .
- ^ Китинг GM, Санторо А (2009). «Сорафениб: обзор его применения при распространенной гепатоцеллюлярной карциноме». Наркотики . 69 (2): 223–240. дои : 10.2165/00003495-200969020-00006 . ПМИД 19228077 .
- ^ Фэн М., Бен-Йозеф Э. (октябрь 2011 г.). «Лучевая терапия гепатоцеллюлярной карциномы». Семинары по радиационной онкологии . 21 (4): 271–277. дои : 10.1016/j.semradonc.2011.05.002 . ПМИД 21939856 .
- ^ Перейти обратно: а б Тарасик А., Ярошевич Ю., Янушкевич М. (март 2017 г.). «Хирургическое лечение опухолей печени – собственный опыт и обзор литературы» . Клиническая и экспериментальная гепатология . 3 (1): 1–8. дои : 10.5114/ceh.2017.65498 . ПМЦ 5497454 . ПМИД 28856283 .
- ^ Перейти обратно: а б «Лечение рака желчных протоков (холангиокарциномы) (PDQ®) – версия для медицинских работников – Национальный институт рака» . www.cancer.gov . 19 февраля 2021 г. Проверено 25 февраля 2021 г.
- ^ Перейти обратно: а б Ульструп Т., Педерсен FM (февраль 2013 г.). «[Фотодинамическая терапия холангиокарцином]». Еженедельный журнал Laeger . 175 (9): 579–582. ПМИД 23608009 .
- ^ Перейти обратно: а б Кульманн Ю.Б., Блюм Х.Э. (май 2013 г.). «Локорегионарная терапия холангиокарциномы». Современное мнение в гастроэнтерологии . 29 (3): 324–328. дои : 10.1097/MOG.0b013e32835d9dea . ПМИД 23337933 . S2CID 37403999 .
- ^ Ортнер М.А. (сентябрь 2011 г.). «Фотодинамическая терапия холангиокарциномы». Лазеры в хирургии и медицине . 43 (7): 776–780. дои : 10.1002/lsm.21106 . ПМИД 22057505 . S2CID 36852386 .
- ^ Валеро В., Косгроув Д., Герман Дж.М., Павлик Т.М. (август 2012 г.). «Лечение перихилярной холангиокарциномы в эпоху мультимодальной терапии» . Экспертный обзор гастроэнтерологии и гепатологии . 6 (4): 481–495. дои : 10.1586/egh.12.20 . ПМЦ 3538366 . ПМИД 22928900 .
- ^ Мейерс Р.Л., Чаудерна П., Отте Дж.Б. (ноябрь 2012 г.). «Хирургическое лечение гепатобластомы». Детская кровь и рак . 59 (5): 800–808. дои : 10.1002/pbc.24220 . ПМИД 22887704 . S2CID 27329163 .
- ^ Перилонго Г., Малоголовкин М., Фойснер Дж. (ноябрь 2012 г.). «Клинические исследования гепатобластомы: извлеченные уроки и будущие проблемы». Детская кровь и рак . 59 (5): 818–821. дои : 10.1002/pbc.24217 . ПМИД 22678761 . S2CID 19059413 .
- ^ Эль-Сераг Х.Б., Рудольф К.Л. (июнь 2007 г.). «Гепатоцеллюлярная карцинома: эпидемиология и молекулярный канцерогенез». Гастроэнтерология . 132 (7): 2557–2576. дои : 10.1053/j.gastro.2007.04.061 . ПМИД 17570226 .
- ^ Хан С.А., Толедано МБ, Тейлор-Робинсон С.Д. (2008). «Эпидемиология, факторы риска и патогенез холангиокарциномы» . Е.П.Б. 10 (2): 77–82. дои : 10.1080/13651820801992641 . ПМК 2504381 . ПМИД 18773060 .
- ^ Перейти обратно: а б с д «Рак печени и внутрипеченочных желчных протоков - факты о раке» . ПРОИДЧИК . Проверено 23 февраля 2021 г.