Десмопластическая мелкокруглоклеточная опухоль
| Десмопластическая мелкокруглоклеточная опухоль | |
|---|---|
| Другие имена | ДСРКТ [ 1 ] |
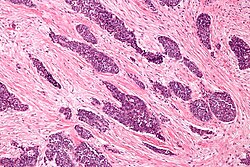 | |
| Микрофотография десмопластической мелкокруглоклеточной опухоли, показывающая характерную десмопластическую строму и угловатые гнезда мелких круглых клеток. Пятно H&E . | |
| Специальность | онкология |
| Прогноз | Пятилетняя выживаемость 15% [ 2 ] |
| Частота | Зарегистрировано около 200 случаев [ 2 ] [ 3 ] |
Десмопластическая мелкокруглоклеточная опухоль (DSRCT) — агрессивный и редкий рак , который преимущественно возникает в виде образований в брюшной полости . [ 4 ] Другие пораженные области могут включать лимфатические узлы , слизистую оболочку брюшной полости , диафрагму , селезенку, печень, грудную стенку, череп, спинной мозг, толстую кишку, тонкую кишку, мочевой пузырь, головной мозг, легкие, яички, яичники и таз . Зарегистрированные места метастатического распространения включают печень , легкие , лимфатические узлы , мозг , череп и кости . Он характеризуется слитым белком EWS-WT1.
Опухоль и классифицируется как саркома мягких тканей небольшая круглая синеклеточная опухоль . Чаще всего встречается у детей мужского пола. Заболевание редко встречается у женщин, но в этом случае опухоли можно принять за рак яичников . [ 5 ]
Признаки и симптомы
[ редактировать ]

Ранних признаков того, что у пациента есть DSRCT, немного. Пациенты часто молодые и здоровые, поскольку опухоли растут и беспрепятственно распространяются в брюшной полости. Это редкие опухоли, и врачи часто неправильно диагностируют симптомы. Абдоминальные образования могут вырасти до огромных размеров, прежде чем пациент их заметит. Опухоли можно ощутить как твердые округлые образования при пальпации живота. [ нужна ссылка ]
Первые симптомы заболевания часто включают вздутие живота, образование опухолей в животе, боль в животе или спине, желудочно-кишечную непроходимость, отсутствие аппетита, асцит , анемию и кахексию . [ нужна ссылка ]
Другие зарегистрированные симптомы включают неизвестные уплотнения, заболевания щитовидной железы, гормональные нарушения, свертывание крови, проблемы с почками и урологические проблемы, образования в яичках, молочной железе, матке, влагалище и яичниках. [ нужна ссылка ]
Генетика
[ редактировать ]Не существует известных факторов риска, специфичных для этого заболевания. Опухоль, по-видимому, возникает из примитивных детских клеток и считается детским раком. [ нужна ссылка ]
Исследования показали, что существует химерная связь между DSRCT и опухолью Вильмса и саркомой Юинга . Вместе с нейробластомой и неходжкинской лимфомой они образуют мелкоклеточные опухоли . [ нужна ссылка ]
DSRCT связан с уникальной хромосомной транслокацией (обозначенной как t(11;22)(p13:q12)) [ 6 ] который объединяет EWSR1 ген семейства FET, обычно расположенный на участке 12 длинного (или «q») плеча хромосомы 22, с частью WT1, гена транскрипционного фактора обычно расположенного на участке 13 короткого плеча хромосомы 11 . [ 7 ] Полученный слитый ген EWSR1-WT1 преобразуется в слитый транскрипт. [ 8 ] который управляет образованием химерного белка EWSR1-WT1 . [ 9 ] Химерный белок EWSR1-WT1 содержит N-концевой трансактивации EWSR1 домен и ДНК-связывающий WT1 домен . Эта транслокация наблюдается практически во всех случаях DSRCT. [ 10 ]
Продукт транслокации EWS/WT1 нацелен на ENT4 . [ 11 ] ENT4 также известен как PMAT.
Патология
[ редактировать ]Существо было впервые описано патологами Уильямом Л. Джеральдом и Хуаном Росай в 1989 году. [ 12 ] Патология выявляет хорошо очерченные солидные опухолевые узелки внутри плотной десмопластической стромы . Часто наблюдаются участки центрального некроза. Опухолевые клетки имеют гиперхромные ядра с повышенным ядерно-цитоплазматическим соотношением. [ нужна ссылка ]
По данным иммуногистохимии, эти клетки имеют трилинейную коэкспрессию, включая эпителиальный маркер цитокератин, мезенхимальные маркеры десмин и виментин, а также нейрональный маркер нейрон-специфической енолазы. Таким образом, хотя первоначально считалось, что он имеет мезотелиальное происхождение из-за мест презентации, в настоящее время предполагается, что он возникает из клетки-предшественника с мультифенотипической дифференцировкой. [ нужна ссылка ]
Диагностика
[ редактировать ]Дифференциальный диагноз
[ редактировать ]Поскольку это редкая опухоль, с этим заболеванием знакомы немногие семейные врачи и онкологи. У молодых пациентов DSRCT можно ошибочно принять за другие опухоли брюшной полости, включая рабдомиосаркому , нейробластому и мезентериальный карциноид . У пожилых пациентов ДСРКТ может напоминать лимфому , мезотелиому брюшины и канцероматоз брюшины. У мужчин DSRCT может быть ошибочно принят за рак половых клеток или яичек, тогда как у женщин DSRCT может быть ошибочно принят за рак яичников. DSRCT имеет общие характеристики с другими мелкокруглыми синеклеточными раками, включая саркому Юинга, острый лейкоз, мелкоклеточную мезотелиому, нейробластому, примитивную нейроэктодермальную опухоль , рабдомиосаркому и опухоль Вильмса. [ нужна ссылка ]
Уход
[ редактировать ]DSRCT часто ставится ошибочный диагноз . Взрослых пациентов всегда следует направлять к специалисту по саркомам. Это агрессивная, редкая, быстро распространяющаяся опухоль, поэтому как детей, так и взрослых пациентов следует лечить в саркомном центре. [ нужна ссылка ]
Стандартного протокола лечения этого заболевания не существует; [ 13 ] однако в недавних журналах и исследованиях сообщалось, что некоторые пациенты реагируют на высокодозную химиотерапию (протокол P6) , поддерживающую химиотерапию , операцию по уменьшению объема , циторедуктивную хирургию и лучевую терапию . Другие варианты лечения включают: трансплантацию гемопоэтических стволовых клеток , лучевую терапию с модулированной интенсивностью, радиочастотную абляцию , стереотаксическую лучевую терапию тела, внутрибрюшинную гипертермическую химиоперфузию и клинические исследования .
Прогноз
[ редактировать ]Прогноз для DSRCT остается плохим. [ 14 ] Прогноз зависит от стадии рака. Поскольку заболевание может быть неправильно диагностировано или оставаться необнаруженным, опухоли часто вырастают до больших размеров в брюшной полости и метастазируют или размножаются в другие части тела.
Не существует известного органа или области происхождения. DSRCT может метастазировать через лимфатические узлы или кровоток. Места метастазирования включают селезенку, диафрагму, печень, толстую и тонкую кишку, легкие, центральную нервную систему, кости, матку, мочевой пузырь, половые органы, брюшную полость и головной мозг.
Мультимодальный подход, включающий высокодозную химиотерапию, агрессивную хирургическую резекцию, [ 15 ] радиация и спасение стволовых клеток улучшают выживаемость некоторых пациентов. Отчеты показали, что пациенты первоначально реагируют на химиотерапию и лечение первой линии, но рецидивы встречаются часто.
Некоторые пациенты в стадии ремиссии или с неоперабельной опухолью, по-видимому, получают пользу от долгосрочной химиотерапии в низких дозах, превращая DSRCT в хроническое заболевание.
Исследовать
[ редактировать ]Примеры и перспективы в этом разделе могут не отражать мировую точку зрения на предмет . ( Июль 2016 г. ) |
Фонд Штелина [ 16 ] в настоящее время предлагает пациентам DSRCT возможность бесплатно отправлять образцы своих опухолей на тестирование. Ученые-исследователи выращивают образцы на голых мышах и тестируют различные химические агенты, чтобы определить, какие из них наиболее эффективны против опухоли человека.
Пациенты с продвинутой стадией DSRCT могут иметь право на участие в клинических исследованиях новых лекарств для лечения этого заболевания.
Фонд Кори Монзинго — это организация 501(c)(3) , которая поддерживает исследования в области лечения и лечения DSRCT. Фонд Кори Монзинго предоставляет финансирование Онкологическому центру доктора медицины Андерсона, а также может предоставлять финансирование другим некоммерческим организациям, занимающимся исследованием рака.
В 2002 году Нисио и др. [ 17 ] создали новую линию опухолевых клеток человека, полученную из плеврального выпота пациента с типичным внутрибрюшным DSRCT, названную JN-DSRCT-1. [ 18 ] которые теперь можно использовать в исследованиях.
В 2018 году Детская исследовательская больница Св. Иуды предоставила ресурсы Сети детских солидных опухолей, которая по запросу предоставляет доступ к ортотопическим ксенотрансплантатам, полученным от пациента. [ 19 ]
Альтернативные названия
[ редактировать ]Это заболевание также известно как: десмопластическая мелкокруглая синеклеточная опухоль; внутрибрюшная десмопластическая мелкокруглая синеклеточная опухоль; десмопластическая мелкоклеточная опухоль; десмопластический рак; десмопластическая саркома; ДСРКТ.
Никакой связи с мезотелиомой брюшины — еще одним заболеванием, которое иногда называют десмопластическим.
См. также
[ редактировать ]- Десмоплазия
- Кейт Грейнджер (1981–2016), английский врач, чей диагноз DSRCT привел к ее кампании по улучшению ухода за пациентами и сбору средств для исследований рака.
Ссылки
[ редактировать ]- ^ ЗАРЕЗЕРВИРОВАНО, ВСТАВИТЬ US14 -- ВСЕ ПРАВА. «Орфанет: Десмопластическая мелкокруглоклеточная опухоль» . www.orpha.net . Проверено 17 ноября 2019 г.
{{cite web}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ Jump up to: а б «Десмопластическая мелкокруглоклеточная опухоль» . Детская исследовательская больница Св. Иуды . Проверено 22 марта 2023 г.
- ^ «Десмопластические мелкокруглоклеточные опухоли (DSRCT)» . Национальный институт рака . Проверено 22 марта 2023 г.
- ^ Ли Ю.С., Сяо Ч.Х.: Десмопластическая мелкокруглоклеточная опухоль: клинико-патологическое, иммуногистохимическое и молекулярное исследование четырех пациентов. J Formos Med Assoc 2007; 106: 854–860.
- ^ Бланд А.Е., Шах А.А., Писцителли Дж.Т., Бентли Р.К., Секорд А.А. (2007). «Десмопластическая мелкокруглоклеточная опухоль, маскирующаяся под распространенный рак яичников». Международный журнал гинекологического рака . 18 (4): 847–50. дои : 10.1111/j.1525-1438.2007.01110.x . ПМИД 18081791 .
- ^ Мерфи А.Дж., Бишоп К., Перейра С. и др. (декабрь 2008 г.). «Новый молекулярный вариант десмопластической мелкоклеточной опухоли: значение иммуноокрашивания WT1 в этом случае». Хм. Патол . 39 (12): 1763–70. дои : 10.1016/j.humpath.2008.04.019 . ПМИД 18703217 .
- ^ Флюк Ю, ван Нозель М.М., Сиозопулу В., Крейтенс Д., Топс Б.Б., ван Горп Дж.М., Химке-Джива Л.С. (июнь 2021 г.). «EWSR1 — наиболее распространенный реаранжированный ген при поражениях мягких тканей, который также встречается при различных поражениях костей: обновленный обзор» . Диагностика (Базель, Швейцария) . 11 (6): 1093. doi : 10.3390/diagnostics11061093 . ПМЦ 8232650 . ПМИД 34203801 .
- ^ Джеральд В.Л., Хабер Д.А. (июнь 2005 г.). «Слияние генов EWS-WT1 в десмопластической мелкокруглоклеточной опухоли». Семин. Рак Биол . 15 (3): 197–205. doi : 10.1016/j.semcancer.2005.01.005 . ПМИД 15826834 .
- ^ Ли Ю.С., Сяо Ч. (2007). «Десмопластическая мелкокруглоклеточная опухоль: клинико-патологическое, иммуногистохимическое и молекулярное исследование четырех пациентов» . Дж. Формос. Мед. доц . 106 (10): 854–60. дои : 10.1016/S0929-6646(08)60051-0 . ПМИД 17964965 .
- ^ Мартинес-Труферо Х, Крус Хурадо Х, Эрнандес-Леон С.Н., Корреа Р., Асенсио Х.М., Бернабеу Д., Альварес Р., Хинди Н., Мата К., Маркина Г., Мартинес В., Редондо А., Флория Л.Дж., Гомес-Матео М.К., Лаверниа Дж., Себио А., Гарсия Дель Муро Х., Мартин-Брото Х., Вальверде-Моралес К. (сентябрь 2021 г.). «Нечастые и своеобразные саркомы мягких тканей: Междисциплинарный обзор и практические рекомендации. Испанская группа по исследованию саркомы (GEIS-GROUP). Часть II». Обзоры лечения рака . 99 : 102260. doi : 10.1016/j.ctrv.2021.102260 . ПМИД 34340159 .
- ^ Ли Х., Смолен Г.А., Бирс Л.Ф. и др. (2008). «Переносчик аденозина ENT4 является прямой мишенью продукта транслокации EWS/WT1 и высоко экспрессируется в десмопластической мелкоклеточной опухоли» . ПЛОС ОДИН . 3 (6): е2353. Бибкод : 2008PLoSO...3.2353L . дои : 10.1371/journal.pone.0002353 . ПМК 2394657 . ПМИД 18523561 .

- ^ Джеральд, WL; Розаи, Дж. (1989). «Случай 2. Десмопластическая мелкоклеточная опухоль с дивергентной дифференцировкой». Педиатр. Патол . 9 (2): 177–83. дои : 10.3109/15513818909022347 . ПМИД 2473463 .
- ^ Таларико Ф., Юско Д., Негри Л., Белинелли Д.: Комбинированная резекция и многоагентная адъювантная химиотерапия при внутрибрюшной десмопластической мелкоклеточной опухоли: отчет о случае и обзор литературы. Г Чир 2007; 28: 367–370.
- ^ Лал Д.Р., Су В.Т., Волден С.Л., Ло К.С., Модак С., член парламента Ла Квалья (январь 2005 г.). «Результаты мультимодального лечения десмопластических мелкокруглоклеточных опухолей». Ж. Педиатр. Сург . 40 (1): 251–5. дои : 10.1016/j.jpedsurg.2004.09.046 . ПМИД 15868593 .
- ^ Таларико Ф, Юско Д, Негри Л, Белинелли Д (октябрь 2007 г.). «Комбинированная резекция и мультиагентная адъювантная химиотерапия интраабдоминальной десмопластической мелкоклеточной опухоли: описание случая и обзор литературы» . Г Чир . 28 (10): 367–70. ПМИД 17915050 .
- ^ «Официальный сайт Фонда Стелина» . Архивировано из оригинала 12 апреля 2021 г. Проверено 8 октября 2006 г.
- ^ Нисио, июнь; Ивасаки, Хироши; Исигуро, Масако; Оджими, Юко; Фудзита, Чикаго; Янаи, Фумио; Нибу, Кейко; Мицудомэ, Он горит; Канеко, Ясухико (сентябрь 2002 г.). «Создание и характеристика новой линии десмопластических клеток мелкокруглых опухолевых клеток человека, JN-DSRCT-1» . Лабораторные исследования; Журнал технических методов и патологии . 82 (9): 1175–1182. дои : 10.1097/01.LAB.0000028059.92642.03 . ISSN 0023-6837 . ПМИД 12218078 .
- ^ «Джн-Дсркт-1» .
- ^ «Детская исследовательская больница Святого Иуды» .