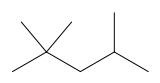
2,2,4-триметилпентан
| |

| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
2,2,4-триметилпентан [ 1 ] | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 1696876 | |
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.007.964 |
| Номер ЕС |
|
| МеШ | 2,2,4-триметилпентан |
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 1262 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 8 Ч 18 | |
| Молярная масса | 114.232 g·mol −1 |
| Появление | Бесцветная жидкость |
| Запах | нефтеподобный |
| Плотность | 0,692 г см −3 |
| Температура плавления | −107,38 °С; −161,28 ° F; 165,77 К |
| Точка кипения | 99,30 °С; 210,74 °Ф; 372,45 К |
| войти P | 4.373 |
| Давление пара | 5,5 кПа (при 21 °C) |
Закон Генри
постоянная ( k H ) |
3,0 нмоль Па −1 кг −1 |
| УФ-видимое излучение (λ макс .) | 210 нм |
| -98.34·10 −6 см 3 /моль | |
Показатель преломления ( n D )
|
1.391 |
| Термохимия | |
Теплоемкость ( С )
|
242,49 Дж.К. −1 моль −1 |
Стандартный моляр
энтропия ( S ⦵ 298 ) |
328.03 ДжК −1 моль −1 |
Стандартная энтальпия
образование (Δ f H ⦵ 298 ) |
от -260,6 до -258,0 кДж моль −1 |
Стандартная энтальпия
горение (Δ c H ⦵ 298 ) |
от −5462,6 до −5460,0 кДж моль −1 |
| Опасности | |
| СГС Маркировка : | |
   
| |
| Опасность | |
| Х225 , Х304 , Х315 , Х336 , Х410 | |
| П210 , П261 , П273 , П301+П310 , П331 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | −12 ° C (10 ° F; 261 К) |
| 396 ° С (745 ° F, 669 К) | |
| Взрывоопасные пределы | 1.1–6.0% |
| Родственные соединения | |
Родственные алканы
|
|
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
2,2,4-Триметилпентан , также известный как изооктан или изооктан , представляет собой органическое соединение формулы (CH 3 ) 3 CCH 2 CH(CH 3 ) 2 . Это один из нескольких изомеров октана ( C 8 H 18 ). Этот конкретный изомер является стандартным 100-м баллом по октановой шкале (нулевая точка — н -гептан ). Это важный компонент бензина , часто используемый в относительно больших количествах (около 10%) для повышения детонационной стойкости топлива. [ 2 ] [ 3 ]
Строго говоря, если следовать стандартному значению слова «изо», название «изооктан» следует зарезервировать для изомера 2-метилгептана . Однако 2,2,4-триметилпентан на сегодняшний день является наиболее важным изомером октана, и исторически ему было присвоено это название. [ 4 ]
Производство
[ редактировать ]масштабах производится в нефтяной промышленности путем алкилирования изобутена изобутаном Изооктан в огромных . Этот процесс проводится в установках алкилирования в присутствии кислотных катализаторов . [ 5 ]

Его также можно получить из изобутилена путем димеризации с использованием Amberlyst катализатора для получения смеси изооктенов. Гидрирование этой смеси дает 2,2,4-триметилпентан. [ 6 ]
История
[ редактировать ]Детонация двигателя — нежелательный процесс, который может возникнуть при высоких степенях сжатия в двигателях внутреннего сгорания . В 1926 году Грэм Эдгар добавил в бензин различные количества н -гептана и 2,2,4-триметилпентана и обнаружил, что детонация прекращается при добавлении 2,2,4-триметилпентана. Эта работа положила начало шкале октанового числа . [ 7 ] Испытательные двигатели, использующие 2,2,4-триметилпентан, показали определенные характеристики, стандартизированные как октановое число 100. Те же самые испытательные двигатели, работавшие таким же образом с использованием гептана, показали производительность, стандартизованную как 0 октановое число. Все остальные соединения и смеси соединений затем классифицировались по этим двум стандартам и им присваивались октановые числа.
Безопасность
[ редактировать ]Как и все углеводороды, 2,2,4-триметилпентан горюч. [ 8 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ «2,2,4-триметилпентан - Краткое описание соединений» . Пабхим соединение . США: Национальный центр биотехнологической информации. 26 марта 2005 г. Идентификация и соответствующие записи . Проверено 11 марта 2012 г.
- ^ Вернер Дабельштейн; Арно Реглицки; Андреа Шютце; Клаус Редерс (2007). «Автомобильное топливо». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a16_719.pub2 . ISBN 978-3527306732 .
- ^ Ричардсон, Калифорния; Уилмер, Дж.Л.; Смит-Симпсон, Д; Скопек, Т.Р. (февраль 1986 г.). «Оценка генотоксического потенциала неэтилированного бензина и 2,2,4-триметилпентана в лимфобластах человека in vitro». Токсикология и прикладная фармакология . 82 (2): 316–22. дои : 10.1016/0041-008x(86)90207-3 . ПМИД 3945956 .
- ^ Клейден, Джонатан (2005). Органическая химия (Переиздается (с исправлениями). Под ред.). Оксфорд [ua]: Oxford Univ. Нажимать. стр. 315 . ISBN 978-0-19-850346-0 .
- ^ Бипин В. Вора; Джозеф А. Кокал; Пол Т. Баргер; Роберт Дж. Шмидт; Джеймс А. Джонсон (2003). «Алкилирование». Энциклопедия химической технологии Кирка-Отмера . дои : 10.1002/0471238961.0112112508011313.a01.pub2 . ISBN 0471238961 .
- ^ Димеризация изобутилена , Amberlyst.com
- ^ Справочник по топливу и смазочным материалам , Том 1, Джордж Э. Тоттен, Стивен Р. Уэстбрук, Раджеш Дж. Шах, стр. 62
- ^ 2,2,4-триметилпентан , Интегрированная система информации о рисках, Агентство по охране окружающей среды США.
