Гистрионикотоксины

Гистрионикотоксины представляют собой группу родственных токсинов, обнаруженных в коже ядовитых лягушек семейства Dendrobatidae , особенно Oophaga histrionica (ранее Dendrobates histrionicus ), которые являются родными для Колумбии. [1] Вполне вероятно, что, как и другие алкалоиды ядовитых лягушек, гистрионикотоксины не производятся амфибиями, а поглощаются из насекомых, находящихся в их рационе, и сохраняются в железах их кожи. [2] [3] Они значительно менее токсичны, чем другие алкалоиды, обнаруженные у ядовитых лягушек, однако их особая структура действует как нейротоксин за счет неконкурентного ингибирования никотиновых рецепторов ацетилхолина . [4]
История
[ редактировать ]Первое упоминание о гистрионикотоксинах датируется 1823 годом капитаном Чарльзом Стюартом Кокрейном. [5] Кокрейн исследовал тропические леса вокруг Колумбии и Панамы. В его отчетах упоминаются племена индейцев, которые использовали стрелы с отравленными наконечниками и дротики для охоты и войны. В ходе дальнейших исследований Кокрейн обнаружил, что эти индейцы извлекали яд из шкур ядовитой лягушки-дрозофилы, известной тогда как Dendrobates histrionicus . Запись из его дневника гласит:
называют rana de veneno «[...] испанцы , длиной около трех дюймов, желтыми на спине, с очень большими черными глазами… те, кто использует яд, ловят лягушек в лесу и заключают их в полый тростник, где они регулярно кормят их до тех пор, пока им не понадобится яд, а затем берут несчастную рептилию и пропускают ей в горло заостренный кусок дерева. Эта пытка заставляет бедную лягушку сильно потеть, особенно на спине, от чего она сильно потеет. покрывается белой пеной; это самый сильный яд, который он выделяет, и в нее они опускают или катают кончики своих стрел, которые сохраняют свою разрушительную силу в течение года. После этого под этим белым веществом появляется желтое вещество. масло, которое тщательно соскребают, и сохраняет свое смертоносное действие в течение четырех-шести месяцев, по доброте (как говорят) лягушки. Этим путем из одной лягушки получается достаточно яда примерно на пятьдесят стрел».
Химические свойства
[ редактировать ]Гистрионикотоксины представляют собой класс, а не конкретный яд, и этот широкий спектр создает синтетические проблемы. Структуры гистрионикотоксинов были охарактеризованы в 1971 году. [6] С тех пор было проведено несколько синтетических исследований и полных синтезов. В таблице 1 описаны некоторые из многих вариаций алкалоидов гистрионикотоксина исходной молекулы (283A). [7]

Синтез
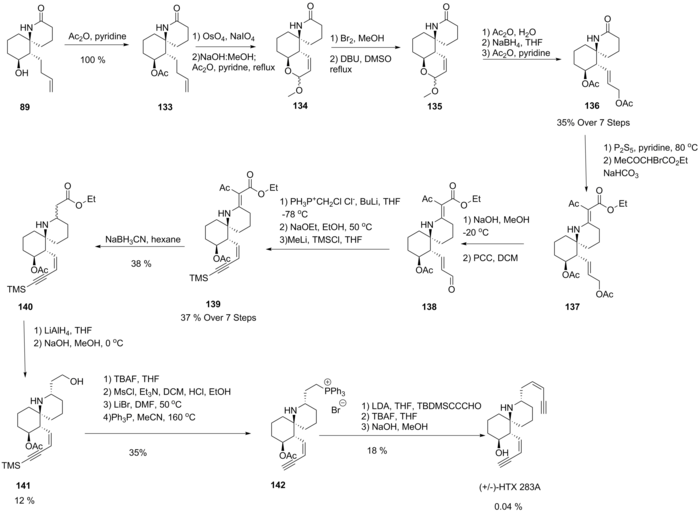
[ редактировать ]С момента описания разработка синтетических путей получения гистрионикотоксина представляла интерес для исследовательских групп из-за его необычной функциональности. Группа Киши предложила первый полный синтез исходного 283А в 1985 году с использованием 89, ранее синтезированного лактама, используемого для синтеза других вариантов. [8] Обработка уксусным ангидридом дала количественный выход 133. Циклический эфир енола 134 образовался в результате окислительного расщепления, способствующего внутримолекулярному присоединению, с последующим снятием основной защиты и дегидратацией. Затем было обнаружено, что бромирование с последующим дегидробромированием в метаноле дает эпимерную смесь ненасыщенного 135. Гидролиз, восстановление и ацетилирование дают 136. Образование тиолактама с последующей конденсацией с этилбромацетатом дает 137. Селективное снятие защиты с аллилового спирта с последующим окислением дает 138. Затем в результате реакции Виттига образовался хлоралкен, который при удалении HCl с помощью основания дал концевой алкин, который впоследствии был защищен с образованием 139. Олефиновая функция 139 была сначала восстановлена с использованием цианборгидрида, а затем дальнейшее восстановление 140 до эпимера. смесь спиртов. Затем было проведено ретро-присоединение по методу Михаэля в основных условиях при низкой температуре, что привело к успешной эпимеризации этого соединения с получением желаемого эпимера 141. Затем реакция с трифенилфосфином привела к образованию фосфониевой соли 142, а затем можно было провести реакцию Виттига для присоединения силил- защищенная цис-ен-иновая функция, с которой затем была снята защита с получением целевого (±)-HTX 283A.
Механизм действия
[ редактировать ]HTX действует как неконкурентный антагонист никотиновых рецепторов ацетилхолина, которые участвуют в передаче нервных сигналов. Будучи неконкурентным антагонистом, HTX связывается с субъединицей никотинового рецептора ацетилхолина. 3 Это фактически увеличивает сродство к агонисту ацетилхолину и стабилизирует десенсибилизированный рецептор. [9] Это блокирует потенциалы действия и замедляет нервную функцию. Было показано, что гистрионикотоксин конкурентно связывается со многими местными анестетиками, такими как тетракаин, а также с другими неконкурентными антагонистами рецепторов ароматических аминов, что указывает на то, что эти соединения, вероятно, имеют общий сайт связывания; этот сайт взаимодействия расположен за пределами трансмембранного домена никотинового рецептора ацетилхолина, хотя точное взаимодействие остается неустановленным. [10] [11] Хотя гистрионикотоксин действительно имеет общее место связывания с другими неконкурентными антагонистами никотиновых рецепторов ацетилхолина, было доказано, что он имеет относительно более высокое сродство к десенсибилизированным рецепторам, чем фенциклидин, что указывает на еще большую, но нехарактерную тонкость природы его связывания. [10] Кроме того, исследования влияния гистрионикотоксина на потенциал концевой пластинки показали, что это соединение препятствует распространению мембранного потенциала, но имеет новые характеристики при гиперполяризации мембраны. [12] Связывание гистрионикотоксина быстро обратимо, поэтому его можно легко удалить из пораженных участков при многократном промывании или, in vivo , путем естественной диффузии в организм. [12] Было продемонстрировано, что высокие концентрации HTX оказывают антагонистическое действие на батрахотоксин. [13]
Токсичность
[ редактировать ]Гистрионикотоксин относительно не так токсичен, как другие алкалоиды ядовитых древолазов. Предварительные испытания показали, что мыши могут пережить дозу гистрионикотоксина 283a в дозе 5 мг/кг и выздороветь в течение 3 часов без каких-либо длительных последствий. [6]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Дейли Дж.В. (1982). «Алкалоиды неотропических ядовитых лягушек (Dendrobatidae)». Прогресс в химии органических природных продуктов . Том 41. С. 205–340. дои : 10.1007/978-3-7091-8656-5_6 . ISBN 978-3-7091-8658-9 . ПМИД 7049875 .
- ^ Дейли Дж. В. (январь 1995 г.). «Химия ядов в коже земноводных» . Труды Национальной академии наук Соединенных Штатов Америки . 92 (1): 9–13. Бибкод : 1995ПНАС...92....9Д . дои : 10.1073/pnas.92.1.9 . ПМК 42808 . ПМИД 7816854 .
- ^ Джонс Т.Х., Адамс Р.М., Спанде Т.Ф., Гарраффо Х.М., Канеко Т., Шульц Т.Р. (ноябрь 2012 г.). «Алкалоиды гистрионикотоксина наконец обнаружены у муравья». Журнал натуральных продуктов . 75 (11): 1930–6. дои : 10.1021/np300485v . ПМИД 23088730 .
- ^ Обертюр В., Мун П., Бауманн Х., Лотспайх Ф., Виттманн-Либольд Б., Хучо Ф. (август 1986 г.). «Место реакции неконкурентного антагониста в дельта-субъединице никотинового рецептора ацетилхолина» . Журнал ЭМБО . 5 (8): 1815–9. дои : 10.1002/j.1460-2075.1986.tb04431.x . ПМК 1167045 . ПМИД 3758027 .
- ^ Эдвардс Н., Рид М. «Гистрионикотоксин южноамериканских лягушек-дротоголовок» . Химические лаборатории . Проверено 3 июня 2017 г.
- ^ Jump up to: а б Дейли Дж.В., Карл И., Майерс К.В., Токуяма Т., Уотерс Дж.А., Виткоп Б. (август 1971 г.). «Гистрионикотоксины: рентгеноструктурный анализ новых алленовых и ацетиленовых спироалкалоидов, выделенных из колумбийской лягушки Dendrobates histrionicus » . Труды Национальной академии наук Соединенных Штатов Америки . 68 (8): 1870–5. Бибкод : 1971PNAS...68.1870D . дои : 10.1073/pnas.68.8.1870 . ПМК 389311 . ПМИД 5288773 .
- ^ Синклер А., Стокман Р.А. (апрель 2007 г.). «Тридцать пять лет синтетических исследований, направленных на семейство алкалоидов гистрионикотоксина» . Отчеты о натуральных продуктах . 24 (2): 298–326. дои : 10.1039/b604203c . ПМИД 17389999 .
- ^ Кэри С.К., Аратани М., Киши Ю. (1985). «Полный синтез d,1-гистрионикотоксина». Буквы тетраэдра . 26 (48): 5887–5890. дои : 10.1016/S0040-4039(00)98253-4 .
- ^ Бургермейстер В., Каттералл В.А., Виткоп Б. (декабрь 1977 г.). «Гистрионикотоксин усиливает вызванную агонистами десенсибилизацию рецептора ацетилхолина» . Труды Национальной академии наук Соединенных Штатов Америки . 74 (12): 5754–8. Бибкод : 1977PNAS...74.5754B . дои : 10.1073/pnas.74.12.5754 . ПМК 431872 . ПМИД 272000 .
- ^ Jump up to: а б Галлахер М.Дж., Кьяра, округ Колумбия, Коэн Дж.Б. (июнь 2001 г.). «Взаимодействия между 3-(трифторметил)-3-(m-[ 125 I] йодфенил)диазирин и тетракаин, фенциклидин или гистрионикотоксин в ионном канале никотинового ацетилхолинового рецептора вида Torpedo ». Молекулярная фармакология . 59 (6): 1514–22. : 10,1124 / моль.59.6.1514 . PMID 11353813. doi S2CID 66377 73 .
- ^ Джонсон Д.А., Насс Дж.М. (август 1994 г.). «Чувствительный к гистрионикотоксину сайт связывания этидия расположен за пределами трансмембранного домена никотинового рецептора ацетилхолина: исследование флуоресценции». Биохимия . 33 (31): 9070–7. дои : 10.1021/bi00197a007 . ПМИД 8049208 .
- ^ Jump up to: а б Масукава Л.М., Альбукерке EX (сентябрь 1978 г.). «Вольт-зависимое и времязависимое действие гистрионикотоксина на ток концевой пластинки мышцы лягушки» . Журнал общей физиологии . 72 (3): 351–67. дои : 10.1085/jgp.72.3.351 . ПМЦ 2228541 . ПМИД 308995 .
- ^ Бартельс-Берналь Э., Диас Э., Кадена Р., Рамос Дж., Дейли Дж.В. (сентябрь 1983 г.). «Действие гистрионикотоксина на ионные каналы в синаптических и проводящих мембранах электроплакса Electrophorus electricus ». Клеточная и молекулярная нейробиология . 3 (3): 203–12. дои : 10.1007/bf00710947 . ПМИД 6322994 . S2CID 30388813 .
Внешние ссылки
[ редактировать ]- Яд лягушки - гистрионикотоксин в Периодической таблице видео (Ноттингемский университет)