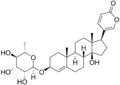
Аренобуфагин
 | |
| Имена | |
|---|---|
| Название ИЮПАК 5-[(3S,5R,10S,11S,13R,14S,17R)-3,11,14-тригидрокси-10,13-диметил-12-оксо-2,3,4,5,6,7,8 ,9,11,15,16,17-додекагидро-1H-циклопента[а]фенантрен-17-ил]пиран-2-он | |
| Другие имена Аренобуфагин | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 24 Н 32 О 6 | |
| Молярная масса | 416.514 g·mol −1 |
| Появление | жидкость |
| Плотность | 1,4±0,1 г/см3 |
| Точка кипения | 637,2±55,0 °С при 760 мм рт. ст. |
| Давление пара | 0,0±4,3 мм рт. ст. при 25 °C |
Показатель преломления ( n D ) | 1.622 |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | Кардиотоксический |
| СГС Маркировка : | |
 | |
| Опасность | |
| точка возгорания | 219,3±25,0 °С |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Аренобуфагин — кардиотоксический буфанолидный стероид , выделяемый аргентинской жабой Bufo arenarum . [1] Он имеет эффекты, аналогичные наперстянке , блокируя насос Na+/K+ в тканях сердца. [2]
Источники
[ редактировать ]Соединение аренофагин является одним из основных компонентов жабьего яда . Его получают из высушенной кожи гигантских жаб, таких как Bufo gargarizans и Bufo melanostictus Suhneider . Аренобуфагин специально секретируется Rhinella arenarum , обитающей в Южной Америке. Яд этих видов жаб содержит около 1,75% аренофагина. [3] Другая основная часть яда состоит в основном из похожих на вид буфагинов , которые являются токсичными стероидами . Жабы производят яд, когда они напуганы, ранены или спровоцированы, в качестве защитного механизма от хищников.
История
[ редактировать ]Аренобуфагин является компонентом яда жабы, известного под названием Чансу. На протяжении веков этот яд использовался в китайской традиционной медицине для лечения печени рака . Также сообщается, что он оказывает стимулирующее воздействие на сердце . Его получают из выделений высушенной кожи гигантских жаб. В исследовании 2013 года было показано, что аренофагин подавляет рост некоторых опухолевых клеток печени. Фактически, это соединение показало самую сильную противоопухолевую активность среди пятнадцати буфадионолидов, выделенных из Чансу. [4]
Функция в медицине
[ редактировать ]Как уже упоминалось, аренофагин широко используется в традиционной китайской медицине (ТКМ) для борьбы с канцерогенезом , поскольку он подавляет рост некоторых раковых клеток. Это один из основных активных ингредиентов жабьего яда для лечения. [5] Это происходит как в очищенном виде, так и в сочетании с другими ингредиентами, преимущественно растительными компонентами. Жабий яд до сих пор используется в клинической практике традиционной китайской медицины для лечения гепатоцеллюлярной карциномы (ГЦК). [6] До сих пор мало что известно об антиангиогенных свойствах аренобуфагина. Одно исследование показывает, что аренобуфагин ингибирует VEGF-индуцированное образование эндотиальных клеточных трубок. [7]
Впуск
[ редактировать ]В нормальных условиях аренофагин представляет собой твердое вещество . В китайской традиционной медицине его принимают внутрь или местно, например, на кожу. известно мало О его токсикокинетике .
Токсикодинамика
[ редактировать ]
Считается, что аренобуфагин играет роль в регуляции транспорта воды и электролитов через клеточные мембраны в физиологических условиях. Результаты экспериментов показывают, что аренобуфагин ингибирует натрий-калий-аденозинтрифосфатазу ( Na+/K+-АТФазу ). Это один из самых мощных блокаторов, известных науке, наряду с уабаином . Высказано предположение, что незаряженные и неполярные аминокислоты могут участвовать в связывании аренофагина с внеклеточной поверхностью АТФазы. Если это так, то стероидное ядро аренобуфагина, вероятно, также способствует связыванию. Более того, наличие сахарной группы в уабаине и отсутствие таковой в аренобуфагине позволяет предположить, что он может быть более липофильным, чем уабаин, и, как таковой, образовывать более стабильный комплекс с Na+-K+-насосом.
Помимо воздействия на насос Na+-K+, аренофагин оказывает и другие эффекты на клетки , которые были обнаружены в экспериментах с линиями раковых клеток .Он вызывает апоптоз путем воздействия на митохондрии . В обработанных им клетках обнаружено снижение митохондриального потенциала (дозозависимым образом), а также высокое соотношение Bax /Bcl-2, что связано с апоптозом – запрограммированной гибелью клеток. транслокации Bax из цитозоля Также было обнаружено увеличение в митохондрии.В дополнение к этим эффектам аренофагин также вызывает морфологические изменения в органеллах , вздутие плазматической мембраны, сморщивание ядерной мембраны и конденсацию хроматина . Эти наблюдения также указывают на возникновение апоптоза. И последнее, но не менее важное: лечение аренобуфагином также индуцировало специфическое расщепление поли( АДФ-рибозы ) полимеразы ( PARP ) и снижение уровня прокаспазы9 и 3. PARP в основном участвует в восстановлении клеток и запрограммированной гибели клеток.После лечения аренофагином некоторые клетки производят больше аутофагосомы и лизосомы , тогда как другие клетки подвергаются апоптозу. Аренобуфагин также приводит к увеличению экспрессии LC3-II, Biclin1 (начальное образование пузырьков), Atg5 (удлинение и завершение), Atg9, Atg16L1 и p62 / SQSTM1 , всех белков , которые индуцируют аутофагию. Блокаторы аутофагии усиливают цитотоксический эффект аренофагина. Добавление 3-МА увеличивает долю клеток, в которых наблюдается увеличенное расщепление PARP и ограниченное расщепление каспазы-9 и каспазы-3 . Это указывает на то, что пути аутофагии защищают клетку от апоптоза аренобуфагином.Была выдвинута гипотеза, что аренофагин может ингибировать путь PI3K / Akt, контролируя гибель и дифференцировку клеток в ответ на внешние стимулы. Установлено, что аренофагин ингибировал белки Akt, PDK1 и PI3K, одновременно стимулируя белок PHEN. Это достигается за счет изменения степени фосфорилирования. Все эти белки участвуют в пути PI3/Akt. В дальнейшем аренофагин косвенно ингибирует mTOR – белок, который участвует в апоптозе, а также в аутофагии. [8]
Детоксикация
[ редактировать ]Биотрансформация аренобуфагина Alternaria alternata приводит к образованию следующих трех метаболитов: 3-оксо-аренобуфагина (1а), ψ-буфареногина (1b), [9] и 3-оксо-ψ-буфареногин (1в). Процессы биотрансформации состоят из основной реакции, при которой происходит дегидрирование 3-гидроксильной группы. За этим процессом следует изомеризация. [10]
Похожие формы
[ редактировать ]Аренобуфагин является производным так называемых буфадиенолидов , где он также имеет стероидную структуру. Характерной особенностью буфадиенолидов является то, что все они содержат две двойные связи в лактонном кольце.
Симптомы
[ редактировать ]Кровеносная система
[ редактировать ]Аренобуфагин действует как сердечные гликозиды. Он ингибирует натриево-калиевый насос , поскольку стабилизирует переходное состояние E2-P, при котором насос неактивен. Второй мембранный транспортер NCX отвечает за транспорт 3Na/Ca. Если Na-K-насос не работает правильно, концентрация Ca внутри клетки повысится, что приведет к сердечной недостаточности.Однако в экспериментах, посвященных противораковому действию аренофагина на мышах, не было обнаружено никаких отрицательных эффектов.
Пищеварительная система
[ редактировать ]Было показано, что аренобуфагин вызывает апоптоз в клетках гепатоцеллюлярной карциномы у мышей, хотя этот метод не используется для лечения гепатоцеллюлярной карциномы в современной медицине человека.
Отношения структура-деятельность
[ редактировать ]существует довольно большая гомология по строению Между аренофагином и сердечными гликозидами . Сердечные гликозиды — это природные соединения, обнаруженные в растениях, которые вызывают инактивацию натриево-калиевого насоса, например аренобуфагин. Специфическая стероидная структура связывается с насосом таким образом, что ингибирует процесс перекачки калия в клетку и выведения натрия из клетки. Точный способ связывания с Na-K-Pump еще не задокументирован.
- Структура аренофагина
- Структура сердечного гликозида просцилларидина
Токсичность
[ редактировать ]Острая токсичность
[ редактировать ]Хотя низкие дозы аренобуфагина можно использовать в качестве лекарства от проблем с сердечным ритмом, высокие дозы могут привести к острым проблемам с сердцем и даже к смерти. Аренобуфагин также токсичен для клеток гепатоцеллюлярной карциномы , что является положительным результатом для организма.
Хроническое воздействие
[ редактировать ]Токсичность вследствие хронического воздействия до сих пор четко не документирована. Однако обсуждается, что хроническое воздействие этого соединения может вызвать развитие опухолей .
См. также
[ редактировать ]- Буфагин
- Буфадиенолид
- Цинофагин
- Гамабуфагин
- Маринобуфагин
- Кверцикобуфагин
- Регуляробуфагин
- Валлиспобуфагин
- Виридифагин
- Дигиталис
Ссылки
[ редактировать ]- ^ Гарраффо Х.М., Грос Э.Г. Биосинтез буфадиенолидов у жаб. VI. Эксперименты с [1,2-3H]холестерином, [21-14C]копростанолом и 5-бета-[21-14 °C]прегнанолоном на жабе Bufo arenarum. Стероиды . Сентябрь-октябрь 1986 г.; 48(3-4): 251-7. PMID 3127947
- ^ Круз Дж. дос С., Мацуда Х. Аренобуфагин, соединение в яде жабы, блокирует ток насоса Na(+)-K+ в сердечных миоцитах. Европейский журнал фармакологии . 3 августа 1993 г.; 239 (1-3): 223-6. ПМИД 8223897
- ^ Ли, Манмей; Ву, Шуай; Лю, Чжун; Чжан, Вэй; Сюй, Цзин; Ван, Ин; Лю, Цзюньшань; Чжан, Дунмей; Тиан, Хайян; Ли, Яолань; Йе, Вэньцай (2012). «Аренофагин, соединение буфадиенолида из яда жабы, ингибирует VEGF-опосредованный ангиогенез посредством подавления сигнального пути VEGFR-2». Биохимическая фармакология . 83 (9): 1251–1260. дои : 10.1016/j.bcp.2012.01.023 . ПМИД 22305746 .
- ^ Чжан, DM и др. (2013). «Аренофагин, природный буфадиенолид из яда жабы, индуцирует апоптоз и аутофагию в клетках гепатоцеллюлярной карциномы человека посредством ингибирования пути PI3K/Akt/mTOR». Канцерогенез 34(6): 1331-1342.
- ^ Ли М, Ву С, Лю З, Чжан В, Сюй Дж, Ван Ю, Лю Дж, Чжан Д, Тянь Х, Ли Ю, Йе В. (2012). «Аренофагин, буфадиенолидное соединение из яда жабы, ингибирует VEGF-опосредованный ангиогенез посредством подавления сигнального пути VEGFR-2». Биохимическая фармакология. 83, 1251–1260 гг.
- ^ Тан, Дж. и др. (2008) «Прогресс исследований по клиническому применению препарата venenum bufonis в качестве противоопухолевого препарата». Китайская фармацевтика, 17, 15-16.
- ^ Ли М, Ву С, Лю З, Чжан В, Сюй Дж, Ван Ю, Лю Дж, Чжан Д, Тянь Х, Ли Ю, Йе В. (2012). «Аренофагин, буфадиенолидное соединение из яда жабы, ингибирует VEGF-опосредованный ангиогенез посредством подавления сигнального пути VEGFR-2». Биохимическая фармакология. 83, 1251–1260 гг.
- ^ Чжан, DM и др. (2013). «Аренофагин, природный буфадиенолид из яда жабы, индуцирует апоптоз и аутофагию в клетках гепатоцеллюлярной карциномы человека посредством ингибирования пути PI3K/Akt/mTOR». Канцерогенез 34(6): 1331-1342.
- ^ Лю, Яньфан; Фэн, Цзятао; Сяо, Юаньшэн; Го, Чжимоу; Чжан, Цзин; Сюэ, Синья; Дин, Джин; Чжан, Сюли; Лян, Синьмяо (2010). «Очистка активных буфадиенолидов из кожи жабы с помощью препаративной обращенно-фазовой жидкостной хроматографии в сочетании с хроматографией гидрофильного взаимодействия». Журнал науки о разделении . 33 (10): 1487–1494. дои : 10.1002/jssc.200900848 . ПМИД 20432230 .
- ^ Чжан, Син; Дун, Инь-Хуэй; Ху, Тао, Си-Цзя; Чен, Инь, Цзюнь; Го, Де-Ань (2011). цинобуфоталин Alternaria alternata». Биокатализ и биотрансформация . 29 (2–3): 96–101. doi : 10.3109/10242422.2011.578248 . S2CID 84624677 .