Онковирус

Онковирус вызвать или онкогенный вирус — это вирус, который может рак . [ 4 ] Этот термин возник в результате исследований остротрансформирующих ретровирусов в 1950–60-х годах. [ 5 ] когда термин онкорнавирусы использовался для обозначения их РНК- вирусного происхождения. [ 6 ] После удаления букв РНК оно теперь относится к любому вирусу с геномом ДНК или РНК, вызывающим рак, и является синонимом опухолевого вируса или вируса рака . Подавляющее большинство вирусов человека и животных не вызывают рак, вероятно, из-за длительной совместной эволюции вируса и его хозяина. Онковирусы сыграли важную роль не только в эпидемиологии , но и в исследованиях механизмов контроля клеточного цикла , таких как белок ретинобластомы .
Всемирной здравоохранения организации По оценкам Международного агентства по исследованию рака , в 2002 году инфекция стала причиной 17,8% случаев рака у человека, причем 11,9% были вызваны одним из семи вирусов. [ 7 ] Исследование 2658 образцов 38 различных типов рака, проведенное в 2020 году, показало, что 16% из них связаны с вирусом. [ 8 ] Эти виды рака можно легко предотвратить с помощью вакцинации (например, вакцины против папилломавируса ), диагностики с помощью простых анализов крови и лечения менее токсичными противовирусными препаратами.
Причинность
[ редактировать ]Как правило, опухолевые вирусы вызывают небольшое заболевание или вообще не вызывают заболевания после заражения у своих хозяев или вызывают неопухолевые заболевания , такие как острый гепатит в случае вируса гепатита В или мононуклеоз в случае вируса Эпштейна-Барр . У меньшинства людей (или животных) после заражения развивается рак. Это усложнило попытки определить, вызывает ли данный вирус рак. Известные постулаты Коха — конструкции XIX века, разработанные Робертом Кохом для установления вероятности того, что Bacillus anthracis вызовет заболевание сибирской язвой , неприменимы к вирусным заболеваниям. Во-первых, это связано с тем, что вирусы невозможно действительно выделить в чистой культуре — даже строгие методы изоляции не могут исключить необнаруженные контаминирующие вирусы с аналогичными характеристиками плотности, и вирусы необходимо выращивать на клетках. Во-вторых, для большинства опухолевых вирусов нормой является бессимптомное заражение и носительство вируса, что нарушает третий принцип Коха. Релман и Фредерикс описали трудности применения постулатов Коха к раку, индуцированному вирусами. [ 9 ] Наконец, ограничение хозяина для вирусов человека делает неэтичным экспериментальную передачу вируса, подозреваемого в раке. Другие меры, такие как критерии А. Б. Хилла , [ 10 ] более актуальны для вирусологии рака, но также имеют некоторые ограничения в определении причинно-следственной связи.
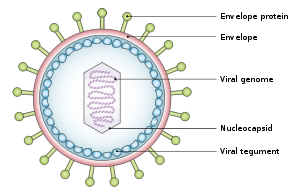
Опухолевые вирусы бывают разных форм: вирусы с ДНК- геномом , такие как аденовирусы , и вирусы с РНК-геномом, такие как вирус гепатита С (ВГС), могут вызывать рак, равно как и ретровирусы, имеющие как ДНК, так и РНК-геномы ( Человеческие вирусы). Т-лимфотропный вирус и вирус гепатита В , который обычно реплицируется как смешанный двухцепочечный и одноцепочечный ДНК-вирус, но также имеет ретровирусный компонент репликации). Во многих случаях опухолевые вирусы не вызывают рак у своих местных хозяев, а только у тупиковых видов. Например, аденовирусы не вызывают рак у людей, а вызывают простуду, конъюнктивит и другие острые заболевания. Они становятся канцерогенными только при заражении определенными видами грызунов, такими как сирийские хомяки. Некоторые вирусы являются онкогенными, когда они заражают клетку и сохраняются в виде кольцевых эписом или плазмид, реплицирующихся отдельно от ДНК клетки-хозяина ( вирус Эпштейна-Барра и герпесвирус, ассоциированный с саркомой Капоши ). Другие вирусы, такие как полиомавирусы и папилломавирусы, являются канцерогенными только тогда, когда они интегрируются в геном клетки-хозяина в результате биологической катастрофы. [ нужна ссылка ]
Онкогенный вирусный механизм
[ редактировать ]
Прямой онкогенный вирусный механизм [ 11 ] включает либо вставку дополнительных вирусных онкогенных генов в клетку-хозяина, либо усиление уже существующих онкогенных генов ( протоонкогенов ) в геноме. Например, было показано, что vFLIP и vCyclin косвенно вмешиваются в сигнальный путь TGF-β, индуцируя онкогенный кластер mir17-92 хозяина. [ 12 ]
Косвенная вирусная онкогенность включает хроническое неспецифическое воспаление, возникающее на протяжении десятилетий после заражения, как в случае рака печени, вызванного ВГС. Эти два механизма различаются по своей биологии и эпидемиологии: вирусы прямой опухоли должны иметь по крайней мере одну копию вируса в каждой опухолевой клетке, экспрессирующую по крайней мере один белок или РНК, вызывающий превращение клетки в раковую. чужеродные вирусные антигены , люди с ослабленным иммунитетом, такие как больные СПИДом или пациенты, перенесшие трансплантацию, подвергаются более высокому риску развития этих типов рака. Поскольку в этих опухолях экспрессируются [ нужна ссылка ]
Вирусы хронических непрямых опухолей, с другой стороны, могут быть потеряны (по крайней мере теоретически) из зрелой опухоли, накопившей достаточно мутаций и условий роста (гиперплазии) в результате хронического воспаления вирусной инфекции. В этом последнем случае спорно, но, по крайней мере, теоретически возможно, что вирус непрямой опухоли может подвергнуться «наезду и бегству», и поэтому вирус будет потерян из клинически диагностированной опухоли. С практической точки зрения, это редкое явление, если оно действительно происходит. [ нужна ссылка ]
ДНК-онковирусы
[ редактировать ]
ДНК-онковирусы обычно повреждают два семейства белков-супрессоров опухолей: опухолевые белки p53 и белки ретинобластомы (Rb). Вирусам эволюционно выгодно инактивировать р53, поскольку р53 может вызвать остановку клеточного цикла или апоптоз в инфицированных клетках, когда вирус пытается реплицировать свою ДНК. [ 13 ] Точно так же белки Rb регулируют многие важные функции клеток, включая, помимо прочего, важнейшую контрольную точку клеточного цикла, что делает их мишенью для вирусов, пытающихся нарушить регулярную функцию клеток. [ 14 ]
Хотя было обнаружено несколько ДНК-онковирусов, три из них тщательно изучены. Аденовирусы могут вызывать опухоли у грызунов, но не вызывают рак у людей; однако их использовали в качестве средств доставки в генной терапии таких заболеваний, как муковисцидоз и рак. [ 15 ] Обезьяний вирус 40 (SV40), полиомавирус , может вызывать опухоли у грызунов, но не является онкогенным для человека. [ 16 ] Это явление стало одним из главных противоречий онкогенеза в 20-м веке, поскольку, по оценкам, 100 миллионов человек случайно подверглись воздействию SV40 через вакцины против полиомиелита. [ 16 ] шеи . Было показано, что вирус папилломы человека-16 (ВПЧ-16) приводит к раку шейки матки и другим видам рака, включая рак головы и [ 17 ] Эти три вируса имеют параллельные механизмы действия, образуя архетип ДНК-онковирусов. Все три ДНК-онковируса способны интегрировать свою ДНК в клетку-хозяина и использовать ее для ее транскрипции и трансформации клеток, минуя контрольную точку G1/S клеточного цикла. [ нужна ссылка ]
Интеграция вирусной ДНК
[ редактировать ]ДНК-онковирусы трансформируют инфицированные клетки, интегрируя свою ДНК в геном клетки-хозяина. [ 18 ] Считается, что ДНК встраивается во время транскрипции или репликации, когда две отожженные цепи разделяются. [ 18 ] Это событие относительно редкое и, как правило, непредсказуемое; кажется, не существует детерминированного предсказателя места интеграции. [ 18 ] После интеграции клеточный цикл хозяина теряет регуляцию со стороны Rb и p53, и клетка начинает клонировать с образованием опухоли. [ 19 ]
Контрольно-пропускной пункт G1/S
[ редактировать ]Rb и p53 регулируют переход между фазами G1 и S , останавливая клеточный цикл перед репликацией ДНК до тех пор, пока не будут завершены соответствующие входные контрольные точки, такие как восстановление повреждений ДНК. [ 20 ] p53 регулирует ген p21, который продуцирует белок, связывающийся с комплексом Cyclin D-Cdk4/6. [ 21 ] Это предотвращает фосфорилирование Rb и предотвращает переход клетки в S-фазу. [ 21 ] У млекопитающих, когда Rb активен (нефосфорилирован), он ингибирует E2F семейство транскрипционных факторов , которые регулируют комплекс Cyclin E - Cdk2 , который ингибирует Rb, образуя петлю положительной обратной связи, удерживая клетку в G1 до тех пор, пока входной сигнал не преодолеет пороговое значение. . [ 20 ] Чтобы преждевременно перевести клетку в S-фазу, вирусы должны инактивировать р53, который играет центральную роль в контрольной точке G1/S, а также Rb, который, хотя и находится ниже нее, обычно поддерживается активным благодаря петле положительной обратной связи. [ нужна ссылка ]
Инактивация р53
[ редактировать ]Вирусы используют различные методы инактивации р53. Белок E1B аденовируса (55K) предотвращает регуляцию генов р53 путем связывания с участком р53, который связывается с геномом. [ 13 ] Аналогом SV40 является большой Т-антиген (LT); LT также связывается с несколькими другими клеточными белками, такими как p107 и p130 , по тем же остаткам. [ 22 ] LT связывается со связывающим доменом p53 на ДНК (а не на белке), снова не позволяя p53 соответствующим образом регулировать гены. [ 13 ] Вместо этого ВПЧ разрушает р53: белок Е6 ВПЧ связывается с клеточным белком, называемым белком, ассоциированным с Е6 (E6-AP, также известным как UBE3A ), образуя комплекс, который вызывает быстрое и специфическое убиквитинирование р53. [ 23 ]
Инактивация Rb
[ редактировать ]Rb инактивируется (тем самым обеспечивая беспрепятственное развитие перехода G1/S) различными, но аналогичными вирусными онкопротеинами. ( Ранняя область 1А аденовируса Е1А) представляет собой онкопротеин, который связывается с Rb и может стимулировать транскрипцию и трансформировать клетки. [ 13 ] SV40 использует тот же белок для инактивации Rb, LT, для инактивации p53. [ 21 ] ВПЧ содержит белок Е7, который может связываться с Rb почти таким же образом. [ 24 ] Rb может быть инактивирован посредством фосфорилирования, связывания с вирусным онкобелком или мутаций — мутации, которые предотвращают связывание онкобелка, также связаны с раком. [ 22 ]
Вариации
[ редактировать ]ДНК-онковирусы обычно вызывают рак, инактивируя р53 и Rb, тем самым обеспечивая нерегулируемое деление клеток и создавая опухоли. Может существовать множество различных механизмов, которые развивались отдельно; Помимо описанных выше, например, вирус папилломы человека инактивирует р53, изолируя его в цитоплазме. [ 13 ]
SV40 хорошо изучен и не вызывает рака у людей, но недавно обнаруженный аналог, называемый полиомавирусом клеток Меркеля , связан с карциномой клеток Меркеля , формой рака кожи. [ 25 ] Считается, что функция связывания Rb у обоих вирусов одинакова. [ 25 ]
РНК-онковирусы
[ редактировать ]В 1960-е годы считалось, что процесс репликации РНК-вируса подобен процессу репликации других одноцепочечных РНК. Репликация одноцепочечной РНК включает РНК-зависимый синтез РНК, а это означает, что ферменты, кодирующие вирус, будут частично создавать двухцепочечную РНК. Было показано, что это мнение неверно, поскольку в ретровирусной клетке не обнаружено двухцепочечной РНК. В 1964 году Говард Темин предложил гипотезу провируса, но вскоре после этого была открыта обратная транскрипция в геноме ретровируса.
Описание вируса
[ редактировать ]Все ретровирусы имеют три основных кодирующих домена; кляп , пол и окр . В gag- области вируса поддерживается синтез внутренних белков вириона, составляющих белки матрикса, капсида и нуклеокапсида. В pol хранится информация для ферментов обратной транскрипции и интеграции. В env он происходит с поверхности и трансмембранно для белка оболочки вируса. Существует четвертый кодирующий домен, который меньше по размеру, но существует во всех ретровирусах. Pol — домен, кодирующий протеазу вириона.
Ретровирус проникает в клетку-хозяина
[ редактировать ]Ретровирус начинает свое путешествие в клетку-хозяина, прикрепляя поверхностный гликопротеин к рецептору плазматической мембраны клетки. Попав внутрь клетки, ретровирус проходит обратную транскрипцию в цитоплазме и генерирует двухцепочечную ДНК-копию генома РНК. Обратная транскрипция также производит идентичные структуры, известные как длинные концевые повторы (LTR). Длинные концевые повторы находятся на концах цепей ДНК и регулируют экспрессию вирусных генов. Затем вирусная ДНК транслоцируется в ядро, где одна цепь ретровирусного генома встраивается в хромосомную ДНК с помощью вирионной интегразы. На этом этапе ретровирус называется провирусом. Попав в хромосомную ДНК, провирус транскрибируется клеточной РНК-полимеразой II. Транскрипция приводит к сплайсингу и полноразмерным мРНК, а также полноразмерной РНК вириона потомства. Белок вириона и дочерняя РНК собираются в цитоплазме и покидают клетку, тогда как другие копии отправляют транслированные вирусные сообщения в цитоплазму.
Классификация
[ редактировать ]
ДНК-вирусы
[ редактировать ]- Вирус папилломы человека (ВПЧ), ДНК-вирус, вызывает трансформацию клеток путем взаимодействия с белками-супрессорами опухолей, такими как р53 . Вмешательство в действие р53 позволяет клетке, инфицированной вирусом, перейти на другую стадию клеточного цикла, позволяя реплицировать геном вируса. Принуждение клетки к S-фазе клеточного цикла может привести к трансформации клетки. [ 26 ] Инфекция, вызванная вирусом папилломы человека, является основной причиной рака шейки матки , рака вульвы , рака влагалища , рака полового члена , анального рака и ВПЧ-положительного рака ротоглотки . [ 7 ] [ 27 ] [ 28 ] [ 29 ] [ 30 ] [ 31 ] [ 32 ] Существует около 200 различных вирусов папилломы человека (ВПЧ). [ 30 ] и многие типы ВПЧ канцерогенны. [ 7 ] [ 27 ]
- Вирус гепатита B (HBV) связан с гепатокарциномой [ 33 ]
- Вирус Эпштейна-Барр (EBV или HHV-4) связан с четырьмя типами рака.
- Цитомегаловирус человека (ЦМВ или ВГЧ-5) связан с мукоэпидермоидной карциномой и, возможно, другими злокачественными новообразованиями. [ 34 ]
- Герпесвирус, ассоциированный с саркомой Капоши (KSHV или HHV-8), связан с саркомой Капоши , типом рака кожи. [ 35 ]
- Полиомавирус клеток Меркеля – вирус полиомы – связан с развитием карциномы клеток Меркеля. [ 25 ]
РНК-вирусы
[ редактировать ]Не все онковирусы являются ДНК-вирусами . некоторые РНК-вирусы, Также были ассоциированы такие как вирус гепатита С , а также некоторые ретровирусы, например, Т-лимфотропный вирус человека (HTLV-1) и вирус саркомы Рауса (RSV).
Обзорная таблица
[ редактировать ]Приблизительный процент новых случаев рака, вызванных этим вирусом, во всем мире в 2002 году. [ 7 ] NA означает, что недоступно. Связь других вирусов с раком человека постоянно исследуется.
Основные вирусы, вызывающие рак человека
[ редактировать ]
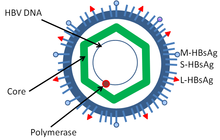
Основными вирусами, вызывающими рак человека, являются вирус папилломы человека , вирусы гепатита В и гепатита С , вирус Эпштейна-Барра , Т-лимфотропный вирус человека , герпесвирус, ассоциированный с саркомой Капоши (KSHV), и полиомавирус клеток Меркеля . Экспериментальные и эпидемиологические данные указывают на причинную роль вирусов, и они, по-видимому, являются вторым по важности фактором риска развития рака у людей, уступая только курению. [ 41 ] Тип вирусно-индуцированных опухолей можно разделить на два: остро трансформирующиеся и медленно трансформирующиеся . В вирусах с острой трансформацией вирусные частицы несут ген, который кодирует сверхактивный онкоген, называемый вирусным онкогеном (v-onc), и инфицированная клетка трансформируется, как только экспрессируется v-onc. Напротив, в медленно трансформирующихся вирусах геном вируса встраивается, тем более что вставка вирусного генома является обязательной частью ретровирусов , рядом с протоонкогеном в геноме хозяина. Вирусный промотор или другие элементы регуляции транскрипции, в свою очередь, вызывают сверхэкспрессию этого протоонкогена, что, в свою очередь, вызывает неконтролируемую клеточную пролиферацию. Поскольку вставка вирусного генома неспецифична для протоонкогенов и вероятность вставки рядом с этим протоонкогеном невелика, медленно трансформирующиеся вирусы имеют очень длительный латентный период в опухоли по сравнению с остро трансформирующими вирусами, которые уже несут вирусный онкоген. [ нужна ссылка ]
Вирусы гепатита, включая гепатит В и гепатит С , могут вызывать хроническую вирусную инфекцию, которая приводит к раку печени у 0,47% пациентов с гепатитом В в год (особенно в Азии, в меньшей степени в Северной Америке) и у 1,4% носителей гепатита С. в год. Цирроз печени, будь то вследствие хронического вирусного гепатита или алкоголизма, связан с развитием рака печени, а сочетание цирроза и вирусного гепатита представляет самый высокий риск развития рака печени. Во всем мире рак печени является одним из наиболее распространенных и самых смертоносных видов рака из-за огромного бремени передачи вирусного гепатита и других заболеваний. [ нужна ссылка ]
Благодаря достижениям в области исследований рака были созданы вакцины, предназначенные для предотвращения рака. Вакцина против гепатита B является первой вакциной, созданной для предотвращения рака ( гепатоцеллюлярной карциномы ) путем предотвращения заражения вызывающим его вирусом. В 2006 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США одобрило вакцину против вируса папилломы человека под названием Гардасил . Вакцина защищает от четырех типов ВПЧ, которые вместе вызывают 70% случаев рака шейки матки и 90% остроконечных кондилом. США (ACIP) Центров по контролю и профилактике заболеваний (CDC В марте 2007 года Консультативный комитет по практике иммунизации ) официально рекомендовал вакцинацию женщинам в возрасте 11–12 лет и указал, что женщины в возрасте от 9 до 26 лет также являются кандидатами на иммунизацию. [ нужна ссылка ]
История
[ редактировать ]История открытия вируса рака переплетается с историей исследований рака и историей вирусологии . Самым старым сохранившимся свидетельством о раке человека является Вавилонский кодекс Хаммурапи (датированный примерно 1754 г. до н.э.), но научная онкология могла возникнуть только в 19 веке, когда опухоли изучались на микроскопическом уровне с помощью составного микроскопа и ахроматических линз . XIX века Микробиология накопила доказательства участия бактерий, дрожжей , грибов и простейших в развитии рака. В 1926 году Нобелевская премия была присуждена за подтверждение того, что червь-нематода может провоцировать рак желудка у крыс. Но то, что рак может иметь инфекционное происхождение, было признано гораздо позже, поскольку вирус был впервые обнаружен Дмитрием Ивановским и Мартинусом Бейеринком в конце XIX века. [ 42 ]
История нечеловеческих онковирусов
[ редактировать ]
Теория о том, что рак может быть вызван вирусом, возникла с экспериментов Олуфа Банга и Вильгельма Эллермана в 1908 году в Копенгагенском университете . Банг и Эллерман продемонстрировали, что вирус птичьего саркомного лейкоза может передаваться между цыплятами после бесклеточной фильтрации и впоследствии вызывать лейкоз. [ 43 ] [ 44 ] Впоследствии это было подтверждено для солидных опухолей у кур в 1910–1911 годах Пейтоном Роусом . [ 45 ] [ 46 ] Раус из Университета Рокфеллера расширил эксперименты Банга и Эллермана, чтобы показать бесклеточную передачу саркомы солидной опухоли цыплятам (теперь известную как саркома Рауса ). Причины, по которым куры настолько восприимчивы к такой передаче, могут заключаться в необычных характеристиках стабильности или нестабильности, связанных с эндогенными ретровирусами . [ 46 ] [ 47 ] Шарлотта Френд подтвердила выводы Банга и Эллермана о жидкой опухоли у мышей. [ 48 ] В 1933 году Ричард Шоп и Эдвард Уэстон Херст показали, что бородавки диких кроликов содержат вирус папилломы Шопе . [ 42 ] В 1936 году Джон Джозеф Биттнер идентифицировал вирус опухоли молочной железы у мышей , «экстрахромосомный фактор» (то есть вирус), который мог передаваться между лабораторными линиями мышей при грудном вскармливании. [ 49 ]
К началу 1950-х годов было известно, что вирусы могут удалять и включать гены и генетический материал в клетки. Было высказано предположение, что такие типы вирусов могут вызывать рак путем внедрения в геном новых генов. Генетический анализ мышей, инфицированных вирусом Френд, подтвердил, что интеграция ретровирусов может нарушать гены-супрессоры опухолей, вызывая рак. [ 50 ] Впоследствии были обнаружены и идентифицированы вирусные онкогены , вызывающие рак. [ нужна ссылка ] Людвик Гросс идентифицировал первый вирус мышиного лейкоза ( вирус мышиного лейкоза ) в 1951 году. [ 42 ] и в 1953 году сообщили о компоненте экстракта мышиного лейкоза , способном вызывать солидные опухоли у мышей. [ 51 ] Это соединение впоследствии было идентифицировано как вирус Сарой Стюарт и Бернис Эдди в Национальном институте рака , в честь которых оно когда-то было названо «SE-полиомой». [ 52 ] [ 53 ] [ 54 ] В 1957 году Шарлотта Френд открыла вирус Френд , штамм вируса мышиного лейкоза, способный вызывать рак у иммунокомпетентных мышей. [ 48 ] Хотя ее выводы вызвали значительную негативную реакцию, в конечном итоге они были приняты в этой области и закрепили достоверность вирусного онкогенеза. [ 55 ]
В 1961 году Эдди открыл обезьяний вакуолирующий вирус 40 ( SV40 ). Лаборатория Merck также подтвердила существование вируса макаки-резус, контаминирующего клетки, используемые для изготовления полиовакцин Солка и Сэбина . Несколько лет спустя было показано, что он вызывает рак у сирийских хомяков , что вызвало обеспокоенность по поводу возможных последствий для здоровья человека. Научный консенсус теперь полностью согласен с тем, что это вряд ли вызовет рак у человека. [ 56 ] [ 57 ]
История онковирусов человека
[ редактировать ]В 1964 году Энтони Эпштейн , Берт Ачонг и Ивонн Барр идентифицировали первый человеческий онковирус из клеток лимфомы Беркитта . Этот вирус герпеса формально известен как вирус герпеса человека 4, но чаще его называют вирусом Эпштейна-Барра или ВЭБ. [ 58 ] В середине 1960-х годов Барух Блумберг впервые физически изолировал и охарактеризовал гепатит B, работая в Национальном институте здравоохранения (NIH), а затем в онкологическом центре Фокса Чейза . [ 59 ] Хотя этот агент был очевидной причиной гепатита и мог способствовать развитию гепатоцеллюлярной карциномы рака печени , эта связь не была твердо установлена до тех пор, пока в 1980-х годах не были проведены эпидемиологические исследования Р. Палмером Бизли и другими. [ 60 ]
первый ретровирус человека, Т-лимфотропный вирус человека 1 (HTLV-I). обнаружили В 1980 году Бернард Поес и Роберт Галло из Национального института здравоохранения США [ 61 ] [ 62 ] и независимо Мицуаки Ёсида и его коллеги в Японии. [ 63 ] Но не было точно установлено, способствует ли HTLV-I лейкемии. В 1981 году Йорио Хинума и его коллеги из Киотского университета сообщили о визуализации ретровирусных частиц, продуцируемых линией лейкозных клеток, полученной от пациентов с Т-клеточным лейкозом/лимфомой взрослых . Этим вирусом оказался HTLV-1, и исследования установили причинную роль вируса HTLV-1 в развитии АТЛ. [ 42 ]

Между 1984 и 1986 годами Харальд цур Хаузен и Лутц Гиссманн обнаружили ВПЧ16 и ВПЧ18. Вместе эти папилломавирусные вирусы (ВПЧ) ответственны примерно за 70% папилломавирусных инфекций человека , вызывающих рак шейки матки . За открытие того, что ВПЧ вызывает рак у человека, в 2008 году была присуждена Нобелевская премия. [ 64 ] В 1987 году вирус гепатита С (ВГС) был обнаружен путем анализа библиотеки кДНК, полученной из больных тканей, на наличие чужеродных антигенов, распознаваемых сывороткой пациентов. Эту работу выполнили Майкл Хоутон из Chiron биотехнологической компании и Дэниел У. Брэдли из Центров по контролю и профилактике заболеваний (CDC). [ 65 ] Впоследствии было показано, что ВГС является основным виновником гепатоцеллюлярной карциномы (рака печени) во всем мире. [ 42 ]
В 1994 году Патрик С. Мур и Юань Чанг в Колумбийском университете ), работая вместе с Этель Сезарман , [ 66 ] [ 67 ] выделили герпесвирус, ассоциированный с саркомой Капоши (KSHV или HHV8), с использованием репрезентативного разностного анализа . Этот поиск был вызван работой Валери Бераль и ее коллег, которые на основании эпидемии саркомы Капоши среди пациентов со СПИДом сделали вывод, что этот рак должен быть вызван другим инфекционным агентом, помимо ВИЧ, и что это, вероятно, был второй вирус. [ 68 ] Последующие исследования показали, что KSHV является «агентом СК» и отвечает за эпидемиологическую картину СК и связанных с ним видов рака. [ 69 ]
В 2008 году Юань Чанг и Патрик С. Мур разработали новый метод идентификации раковых вирусов, основанный на компьютерном вычитании последовательностей человека из транскриптома опухоли , названный вычитанием цифрового транскриптома (DTS). [ 70 ] DTS использовался для выделения фрагментов ДНК полиомавируса клеток Меркеля из карциномы клеток Меркеля, и в настоящее время считается, что этот вирус вызывает 70–80% этих видов рака. [ 25 ]
См. также
[ редактировать ]- Инфекционные причины рака
- Канцероген
- Онкогенный
- Онкоген
- Т-клеточный лейкоз/лимфома взрослых
- Раковые бактерии
- Онколитический вирус — вирус, который заражает и убивает раковые клетки.
- Слитый белок Gag-onc
- Список инфекционных заболеваний
Ссылки
[ редактировать ]- ^ Ферри С., Себастиани М., Джуджиоли Д., Колачи М., Фаллахи П., Пилузо А. и др. (март 2015 г.). «Синдром вируса гепатита С: совокупность органо- и неорганоспецифичных аутоиммунных заболеваний, В-клеточной неходжкинской лимфомы и рака» . Всемирный журнал гепатологии . 7 (3): 327–343. дои : 10.4254/wjh.v7.i3.327 . ПМЦ 4381161 . ПМИД 25848462 .
- ^ Русин I, Лимон С.М. (апрель 2014 г.). «Механизмы рака печени, вызванного ВГС: что мы узнали из исследований in vitro и на животных?» . Письма о раке . 345 (2): 210–215. дои : 10.1016/j.canlet.2013.06.028 . ПМК 3844040 . ПМИД 23871966 .
- ^ Группа медицинского и редакционного контента ACS (30 июля 2020 г.). «Вирусы, которые могут привести к раку» . www.cancer.org . Американское онкологическое общество . Проверено 27 февраля 2021 г.
- ^ Чанг И , Мур П.С. , Вайс Р.А. (октябрь 2017 г.). «Онкогенные вирусы человека: природа и открытие» . Философские труды Лондонского королевского общества. Серия Б, Биологические науки . 372 (1732). Издательство Королевского общества : 1–9. дои : 10.1098/rstb.2016.0264 . JSTOR 44679143 . ПМЦ 5597731 . ПМИД 28893931 .
- ^ Валладарес Ю (1960). «Исследование патогенеза рака. Получение истинной лейкемии и полицитемии с помощью раковых нуклеопротеинов из тканевых культур». Медицина Эксперименталис . 2 : 309–316. дои : 10.1159/000134890 . ПМИД 13779782 .
- ^
Герберман Р.Б. (2012). «12: Иммунология онкорнавирусов». В Нахмиасе А.Дж., О'Рейли Р.Дж. (ред.). Иммунология человеческих инфекций: Часть II: Вирусы и паразиты; Иммунодиагностика и профилактика инфекционных болезней . Комплексная иммунология. Том. 9 (переиздание). Нью-Йорк: Издательская корпорация Plenum. стр. 273, 275. ISBN. 9781468410129 . Проверено 20 октября 2016 г.
Вирусы, известные как онкогенные РНК-вирусы или онкорнавирусы, были описаны у самых разных видов позвоночных [...] было очень мало, если вообще были, полностью убедительных примеров выделения онкорнавирусов человека.
- ^ Перейти обратно: а б с д и ж г час я дж к Паркин Д.М. (июнь 2006 г.). «Глобальное бремя инфекционно-ассоциированных раковых заболеваний в здравоохранении в 2002 году» . Международный журнал рака . 118 (12): 3030–3044. дои : 10.1002/ijc.21731 . ПМИД 16404738 . S2CID 10042384 .
- ^ Запатка М., Борозан И., Брюэр Д.С., Искар М., Грундхофф А., Алави М. и др. (март 2020 г.). «Пейзаж вирусных ассоциаций при раке человека» . Природная генетика . 52 (3): 320–330. дои : 10.1038/s41588-019-0558-9 . ПМК 8076016 . ПМИД 32025001 .
- ^ Фредрикс Д.Н., Релман Д.А. (январь 1996 г.). «Идентификация микробных патогенов на основе последовательностей: пересмотр постулатов Коха» . Обзоры клинической микробиологии . 9 (1): 18–33. дои : 10.1128/CMR.9.1.18 . ПМК 172879 . ПМИД 8665474 .
- ^ Хилл AB (май 1965 г.). «Окружающая среда и болезни: связь или причинная связь?» . Труды Королевского медицинского общества . 58 (5): 295–300. дои : 10.1177/003591576505800503 . ПМК 1898525 . ПМИД 14283879 .
- ^ Парсонне, Джули (1999). Микробы и злокачественные новообразования: инфекция как причина рака человека . Оксфорд: Издательство Оксфордского университета. ISBN 978-0-19-510401-1 . [ нужна страница ]
- ^ Чой Х.С., Джайн В., Крюгер Б., Маршалл В., Ким Ч.Х., Шислер Дж.Л. и др. (2015). «Герпесвирус, ассоциированный с саркомой Капоши (KSHV), индуцирует онкогенный кластер миР-17-92 и подавляет передачу сигналов TGF-β» . ПЛОС Патогены . 11 (11): e1005255. doi : 10.1371/journal.ppat.1005255 . ПМЦ 4636184 . ПМИД 26545119 .
- ^ Перейти обратно: а б с д и Мантовани Ф., Бэнкс Л. (ноябрь 2001 г.). «Белок E6 вируса папилломы человека и его вклад в злокачественное прогрессирование» . Онкоген . 20 (54): 7874–7887. дои : 10.1038/sj.onc.1204869 . ПМИД 11753670 .
- ^ Фельсани А., Милео А.М., Пагги М.Г. (август 2006 г.). «Белки семейства ретинобластомы как ключевые мишени онкопротеинов малых ДНК-вирусов» . Онкоген . 25 (38): 5277–5285. дои : 10.1038/sj.onc.1209621 . ПМИД 16936748 .
- ^ Гастон, К., ред. (2012). Малые ДНК-опухолевые вирусы . Кайстер Академик Пресс . ISBN 978-1-904455-99-8 .
- ^ Перейти обратно: а б Пулен Д.Л., ДеКаприо Дж.А. (сентябрь 2006 г.). «Есть ли роль SV40 в развитии рака у человека?». Журнал клинической онкологии . 24 (26): 4356–4365. дои : 10.1200/JCO.2005.03.7101 . ПМИД 16963733 .
- ^ Вист Т., Шварц Э., Эндерс С., Флехтенмахер С., Bosch FX (февраль 2002 г.). «Участие экспрессии интактного гена E6/E7 HPV16 в раке головы и шеи с неизмененным статусом p53 и нарушенным контролем клеточного цикла pRb» . Онкоген . 21 (10): 1510–1517. дои : 10.1038/sj.onc.1205214 . ПМИД 11896579 .
- ^ Перейти обратно: а б с Сэмбрук Дж., Грин Р., Стрингер Дж., Митчисон Т., Ху С.Л., Ботчан М. (1980). «Анализ сайтов интеграции последовательностей вирусной ДНК в клетках крысы, трансформированных аденовирусом 2 или SV40». Симпозиумы Колд-Спринг-Харбор по количественной биологии . 44 (1): 569–584. дои : 10.1101/sqb.1980.044.01.059 . ПМИД 6253158 .
- ^ Левин, Арнольд Дж. (7 февраля 1997 г.). «p53, клеточный привратник роста и разделения» . Клетка . 88 (3): 323–331. дои : 10.1016/S0092-8674(00)81871-1 . ISSN 0092-8674 . ПМИД 9039259 .
- ^ Перейти обратно: а б Морган, DO (2007). Клеточный цикл: принципы управления . Новая научная пресса. ISBN 978-1-904455-99-8 .
- ^ Перейти обратно: а б с Левин Эй Джей (февраль 2009 г.). «Общие механизмы трансформации небольшими ДНК-опухолевыми вирусами: инактивация продуктов гена-супрессора опухоли: p53» . Вирусология . 384 (2): 285–293. дои : 10.1016/j.virol.2008.09.034 . ПМИД 19081592 .
- ^ Перейти обратно: а б ДеКаприо Дж.А. (февраль 2009 г.). «Как структура и функция опухолевого супрессора Rb были выявлены при исследовании аденовируса и SV40» . Вирусология . 384 (2): 274–284. дои : 10.1016/j.virol.2008.12.010 . ПМИД 19150725 .
- ^ Шеффнер М., Хуибрегце Дж.М., Виерстра Р.Д., Хоули П.М. (ноябрь 1993 г.). «Комплекс E6 и E6-AP HPV-16 действует как убиквитин-белковая лигаза при убиквитинировании p53». Клетка . 75 (3): 495–505. дои : 10.1016/0092-8674(93)90384-3 . ПМИД 8221889 . S2CID 27437768 .
- ^ Дайсон Н., Хоули П.М., Мюнгер К., Харлоу Э. (февраль 1989 г.). «Онкобелок E7 вируса папилломы человека-16 способен связываться с продуктом гена ретинобластомы». Наука . 243 (4893): 934–937. Бибкод : 1989Sci...243..934D . дои : 10.1126/science.2537532 . ПМИД 2537532 .
- ^ Перейти обратно: а б с д Фэн Х., Шуда М., Чанг Ю, Мур П.С. (февраль 2008 г.). «Клональная интеграция полиомавируса в клеточную карциному Меркеля человека» . Наука . 319 (5866): 1096–1100. Бибкод : 2008Sci...319.1096F . дои : 10.1126/science.1152586 . ПМК 2740911 . ПМИД 18202256 .
- ^ Шеффнер М., Вернесс Б.А., Хуибрегце Дж.М., Левин А.Дж., Хоули П.М. (декабрь 1990 г.). «Онкопротеин Е6, кодируемый вирусом папилломы человека типов 16 и 18, способствует деградации р53». Клетка . 63 (6): 1129–1136. дои : 10.1016/0092-8674(90)90409-8 . ПМИД 2175676 . S2CID 7268482 .
- ^ Перейти обратно: а б с Муньос Н., Бош Ф.К., де Санхосе С., Эрреро Р., Кастельсаге Х., Шах К.В. и др. (Многоцентровая группа по изучению рака шейки матки Международного агентства по исследованию рака) (февраль 2003 г.). «Эпидемиологическая классификация типов вируса папилломы человека, связанных с раком шейки матки». Медицинский журнал Новой Англии . 348 (6): 518–527. doi : 10.1056/NEJMoa021641 . hdl : 2445/122831 . ПМИД 12571259 . S2CID 1451343 .
- ^ Перейти обратно: а б Шиффман М., Касл П.Е., Джеронимо Дж., Родригес А.С., Вахолдер С. (сентябрь 2007 г.). «Вирус папилломы человека и рак шейки матки». Ланцет . 370 (9590): 890–907. дои : 10.1016/S0140-6736(07)61416-0 . ПМИД 17826171 . S2CID 20196938 .
- ^ Перейти обратно: а б с д и ж Креймер А.Р. (июнь 2014 г.). «Перспективы профилактики рака ротоглотки, вызванного ВПЧ» . Оральная онкология . 50 (6): 555–559. doi : 10.1016/j.oraloncology.2013.06.007 . ПМК 4058827 . ПМИД 23876626 . S2CID 13768854 .
- ^ Перейти обратно: а б с д и ж г Любоевич С, Скерлев М (2014). «Заболевания, связанные с ВПЧ». Клиники по дерматологии . 32 (2): 227–234. doi : 10.1016/j.clindermatol.2013.08.007 . ПМИД 24559558 . S2CID 24219797 .
- ^ Перейти обратно: а б «Вирус папилломы человека (ВПЧ) и рак шейки матки» . ВОЗ . Июнь 2016. Архивировано из оригинала 5 августа 2016 года.
- ^ Перейти обратно: а б Анджум Т., Зохаиб Дж. (4 декабря 2020 г.). «Плоскоклеточный рак ротоглотки» . Определения (Обновленная ред.). Остров сокровищ (Флорида): StatPearls Publishing. дои : 10.32388/G6TG1L . ПМИД 33085415 . S2CID 229252540 . Идентификатор книжной полки: NBK563268 . Проверено 7 февраля 2021 г. - через NCBI .
{{cite book}}:|work=игнорируется ( помогите ) - ^ Перейти обратно: а б Тан СМ, Яу ТО, Ю Дж (май 2014 г.). «Лечение хронического гепатита В: текущие рекомендации по лечению, проблемы и новые разработки» . Всемирный журнал гастроэнтерологии . 20 (20): 6262–6278. дои : 10.3748/wjg.v20.i20.6262 . ПМК 4033464 . ПМИД 24876747 .
- ^ Мельник М., Седгизаде П.П., Аллен С.М., Джасколл Т. (февраль 2012 г.). «Цитомегаловирус человека и мукоэпидермоидная карцинома слюнных желез: клеточно-специфическая локализация активных вирусных и онкогенных сигнальных белков является подтверждением причинно-следственной связи». Экспериментальная и молекулярная патология . 92 (1): 118–125. дои : 10.1016/j.yexmp.2011.10.011 . ПМИД 22101257 . S2CID 41446671 .
- ^ Чанг Ю, Цезарь Э., Пессин М.С., Ли Ф., Калпеппер Дж., Ноулз Д.М., Мур П.С. (декабрь 1994 г.). «Идентификация герпевирусоподобных последовательностей ДНК в саркоме Капоши, связанной со СПИДом» . Наука 266 (5192): 1865–1869. Бибкод : 1994Sci... 266.1865C дои : 10.1126/science.7997879 . ПМИД 7997879 . S2CID 29977325 .
- ^ НТП (Национальная токсикологическая программа) (2016). Отчет о канцерогенах (четырнадцатое изд.). Research Triangle Park, Северная Каролина: Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения . Проверено 8 января 2017 г.
- ^ Беллон М., Никот С. (2007). «Теломераза: решающий игрок в Т-клеточном лейкозе человека, вызванном HTLV-I» . Геномика и протеомика рака . 4 (1): 21–25. ПМИД 17726237 .
- ^ Сколько случаев рака связано с ВПЧ каждый год? CDC.gov
- ^ Кляйн Э., Кис Л.Л., Кляйн Г. (февраль 2007 г.). «Вирусная инфекция Эпштейна-Барра у человека: от безобидных до опасных для жизни взаимодействий вируса и лимфоцитов» . Онкоген . 26 (9): 1297–1305. дои : 10.1038/sj.onc.1210240 . ПМИД 17322915 .
- ^ Яу ТО, Тан СМ, Ю Дж (июнь 2014 г.). «Эпигенетическая дисрегуляция при раке желудка, связанном с вирусом Эпштейна-Барра: заболевание и лечение» . Всемирный журнал гастроэнтерологии . 20 (21): 6448–6456. дои : 10.3748/wjg.v20.i21.6448 . ПМК 4047330 . ПМИД 24914366 .
- ^ цур Хаузен Х (ноябрь 1991 г.). «Вирусы в раке человека». Наука . 254 (5035): 1167–1173. Бибкод : 1991Sci...254.1167Z . дои : 10.1126/science.1659743 . ПМИД 1659743 .
- ^ Перейти обратно: а б с д и Хавьер РТ, Butel JS (октябрь 2008 г.). «История опухолевой вирусологии» . Исследования рака . 68 (19): 7693–7706. дои : 10.1158/0008-5472.CAN-08-3301 . ПМК 3501656 . ПМИД 18829521 .
- ^ Эллерманн В.; Банг О (1908). «Экспериментальный лейкоз у кур». Центральный вид бактериол. Диск "Паразиты". Инфекция кр. Отдел гигиены 46 :595-609.
- ^ Эллерман С., Банг О (1908). «Экспериментальный лейкоз у кур». Центральный вид бактериол. Диск "Паразиты". Инфекция кр. Отдел гигиены 46 :595-609.
- ^ Роус П. (сентябрь 1910 г.). «Заразное птичье новообразование. (Саркома обыкновенной птицы)» . Журнал экспериментальной медицины . 12 (5): 696–705. дои : 10.1084/jem.12.5.696 . ПМК 2124810 . ПМИД 19867354 .
- ^ Перейти обратно: а б Роус П. (апрель 1911 г.). «Саркома птиц, передающаяся возбудителем, отделяемым от опухолевых клеток» . Журнал экспериментальной медицины . 13 (4): 397–411. дои : 10.1084/jem.13.4.397 . ПМК 2124874 . ПМИД 19867421 .
- ^ Ван Эппс, HL (февраль 2005 г.). «Пейтон Роус: отец опухолевого вируса» . Журнал экспериментальной медицины . 201 (3): 320. doi : 10.1084/jem.2013fta . ПМК 2213042 . ПМИД 15756727 .
- ^ Перейти обратно: а б Друг С (апрель 1957 г.). «Бесклеточная передача у взрослых швейцарских мышей заболевания, имеющего характер лейкемии» . Журнал экспериментальной медицины . 105 (4): 307–318. дои : 10.1084/jem.105.4.307 . ПМК 2136697 . ПМИД 13416470 .
- ^ Биттнер Дж. Дж. (май 1942 г.). «Влияние молока на опухоли молочной железы у мышей». Наука . 95 (2470): 462–463. Бибкод : 1942Sci....95..462B . дои : 10.1126/science.95.2470.462 . ПМИД 17736889 . S2CID 10527142 .
- ^ Бен Дэвид Ю., Придо В.Р., Чоу В., Бенчимол С., Бернштейн А. (август 1988 г.). «Инактивация онкогена p53 путем внутренней делеции или ретровирусной интеграции в линиях эритролейкозных клеток, индуцированных вирусом лейкемии Френда». Онкоген . 3 (2): 179–185. ПМИД 2842714 .
- ^ Гросс Л. (июнь 1953 г.). «Фильтрующийся агент, выделенный из экстрактов лейкемии Ak, вызывающий рак слюнных желез у мышей C3H». Труды Общества экспериментальной биологии и медицины . 83 (2): 414–421. дои : 10.3181/00379727-83-20376 . ПМИД 13064287 . S2CID 34223353 .
- ^ Стюарт С.Е., Эдди Б.Е., Боргезе Н. (июнь 1958 г.). «Новообразования у мышей, привитых опухолевым агентом, содержащимся в культуре тканей». Журнал Национального института рака . 20 (6): 1223–1243. дои : 10.1093/jnci/20.6.1223 . ПМИД 13549981 .
- ^ Эдди Б.Е., Стюарт С.Е. (ноябрь 1959 г.). «Характеристика вируса полиомы SE» . Американский журнал общественного здравоохранения и здоровья нации . 49 (11): 1486–1492. дои : 10.2105/AJPH.49.11.1486 . ПМК 1373056 . ПМИД 13819251 .
- ^ Перси Д.Х., Бартольд С.В. (2013). «Вирусная инфекция полиомы». Патология лабораторных грызунов и кроликов (3-е изд.). Джон Уайли и сыновья. ISBN 978-1118704639 .
- ^ Тонтоноз М (13 марта 2019 г.). «От противоречий к консенсусу: как Шарлотта Френд изменила биологию рака» . Мемориальный онкологический центр Слоана-Кеттеринга . Проверено 18 апреля 2019 г.
- ^ Кэрролл-Панхерст С., Энгельс Э.А., Стриклер Х.Д., Гедерт Дж.Дж., Вагнер Дж., Мортимер Э.А. (ноябрь 2001 г.). «Тридцатипятилетняя смертность после получения полиовакцины, зараженной SV40, в неонатальный период» . Британский журнал рака . 85 (9): 1295–1297. дои : 10.1054/bjoc.2001.2065 . ПМЦ 2375249 . ПМИД 11720463 .
- ^ Шах КВ (январь 2007 г.). «SV40 и рак человека: обзор последних данных» . Международный журнал рака . 120 (2): 215–223. дои : 10.1002/ijc.22425 . ПМИД 17131333 . S2CID 20679358 .
- ^ Эпштейн М.А., Ачонг Б.Г., Барр Ю.М. (март 1964 г.). «Вирусные частицы в культивируемых лимфобластах лимфомы Беркитта». Ланцет . 1 (7335): 702–703. дои : 10.1016/S0140-6736(64)91524-7 . ПМИД 14107961 .
- ^ «Барух С. Блумберг - Автобиография» . Нобелевская премия.org . Проверено 17 марта 2010 г.
- ^ Бизли Р.П., Хван Л.И., Линь К.С., Чиен К.С. (ноябрь 1981 г.). «Гепатоцеллюлярная карцинома и вирус гепатита В. Проспективное исследование с участием 22 707 мужчин на Тайване». Ланцет . 2 (8256): 1129–1133. дои : 10.1016/S0140-6736(81)90585-7 . ПМИД 6118576 . S2CID 32264986 .
- ^ Йошида М., Жанг К.Т. (2005). «Предисловие к 25-летию исследований HTLV-1 и ATL» . Онкоген . 24 (39): 5925. doi : 10.1038/sj.onc.1208967 .
- ^ Галло RC (сентябрь 2005 г.). «История открытия первых ретровирусов человека: HTLV-1 и HTLV-2» . Онкоген . 24 (39): 5926–5930. дои : 10.1038/sj.onc.1208980 . ПМИД 16155599 .
- ^ Сейки М., Хаттори С., Ёсида М. (ноябрь 1982 г.). «Вирус Т-клеточного лейкоза взрослых человека: молекулярное клонирование ДНК провируса и уникальная терминальная структура» . Труды Национальной академии наук Соединенных Штатов Америки . 79 (22): 6899–6902. Бибкод : 1982PNAS...79.6899S . дои : 10.1073/pnas.79.22.6899 . ПМК 347241 . ПМИД 6294664 .
- ^ «Харальд цур Хаузен – Автобиография» . Нобелевская премия.org . Проверено 17 марта 2010 г.
- ^ Чу К.Л., Куо Дж., Вайнер А.Дж., Оверби Л.Р., Брэдли Д.В., Хоутон М. (апрель 1989 г.). «Выделение клона кДНК, полученного из генома вирусного гепатита ни А, ни В, передающегося с кровью». Наука . 244 (4902): 359–362. Бибкод : 1989Sci...244..359C . дои : 10.1126/science.2523562 . ПМИД 2523562 .
- ^ Шмидт С. (апрель 2008 г.). «Юань Чанг и Патрик Мур: объединяемся для борьбы с вирусами, вызывающими рак» . Журнал Национального института рака . 100 (8): 524–5, 529. doi : 10.1093/jnci/djn122 . ПМИД 18398088 .
- ^ «Этель Сезарман, доктор медицинских наук, доктор философии | Медицинский колледж Вейла Корнелла» . Med.cornell.edu . Проверено 17 марта 2010 г.
- ^ Берал В., Петерман Т.А., Беркельман Р.Л., Джаффе Х.В. (январь 1990 г.). «Саркома Капоши у больных СПИДом: инфекция, передающаяся половым путем?» . Ланцет . 335 (8682): 123–128. дои : 10.1016/0140-6736(90)90001-L . ПМИД 1967430 . S2CID 35639169 .
- ^ Антман К., Чанг И (апрель 2000 г.). «Саркома Капоши». Медицинский журнал Новой Англии . 342 (14): 1027–1038. дои : 10.1056/NEJM200004063421407 . ПМИД 10749966 .
- ^ Фэн Х., Тейлор Дж.Л., Бенос П.В., Ньютон Р., Уодделл К., Лукас С.Б. и др. (октябрь 2007 г.). «Вычитание человеческого транскриптома с использованием меток коротких последовательностей для поиска опухолевых вирусов при карциноме конъюнктивы» . Журнал вирусологии . 81 (20): 11332–11340. дои : 10.1128/JVI.00875-07 . ПМК 2045575 . ПМИД 17686852 .
Внешние ссылки
[ редактировать ]- Онковирусы Национальной медицинской библиотеки США в медицинских предметных рубриках (MeSH)
