Плазмин
| Ср. | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | Plg , Plasminogen, Plasmin, Hae4 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Омим : 173350 ; MGI : 97620 ; Гомологен : 55452 ; GeneCards : PLG ; OMA : PLG - ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викидид | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Плазмин является важным ферментом ( EC 3.4.21.7 ), присутствующим в крови , который разрушает многие белки плазмы крови , включая фибриновые сгустки . Разложение фибрина называется фибринолизом . У людей белок плазмин (в зимогенном виде плазминогена ) кодируется PLG геном . [ 5 ]
Функция
[ редактировать ]
Плазмин - это сериновая протеаза , которая действует для растворения сгустков фибриновой крови. Помимо фибринолиза, белки протеолиза плазмин в различных других системах: он активирует коллагеназы , некоторые медиаторы системы комплемента и ослабляет стенку графского фолликула , что приводит к овуляции . Плазмин также неоднократно участвует в воспалении. [ 6 ] Он расщепляет фибрин , фибронектин , тромбоспондин , ламинин и фактор фон Виллебранда . Плазмин, как трипсин , принадлежит к семейству сериновых протеаз .
Плазмин высвобождается в виде зимогена, называемого плазминогеном (PLG) из печени в системное кровообращение. Две основные гликоформы плазминогена присутствуют у людей-плазминоген типа I содержит две гликозилиционные фрагменты (N-связанные с N289 и O-связанными с T346), тогда как плазминоген типа II содержит только один O-связанный сахар (O-связанный с T346), тогда как плазминоген типа содержит только один O-связанный сахар (O-связанный с T346), тогда как плазминоген типа содержит только один O-связанный сахар с T346), тогда как плазминоген типа содержит только один O-связанный сахарный Полем Плазминоген II типа преимущественно рекрутируется на клеточную поверхность над гликоформой I типа. И наоборот, плазминоген типа I кажется более легко набираемым в сгустки крови.
В циркуляции плазминоген принимает закрытую, устойчивую к активации конформацию. Upon binding to clots, or to the cell surface, plasminogen adopts an open form that can be converted into active plasmin by a variety of enzymes , including tissue plasminogen activator (tPA), urokinase plasminogen activator (uPA), kallikrein , and factor XII ( Фактор Hageman). Фибрин является кофактором для активации плазминогена активатором тканевого плазминогена. Рецептор активатора плазминогена урокиназы (UPAR) является кофактором активации плазминогена активатором урокиназы плазминогена. Превращение плазминогена в плазмин включает в себя расщепление пептидной связи между ARG-561 и VAL-562. [ 5 ] [ 7 ] [ 8 ] [ 9 ]
Плазминовое расщепление продуцирует ангиостатин .
Механизм активации плазминогена
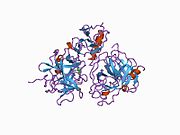
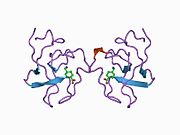
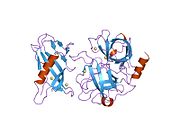
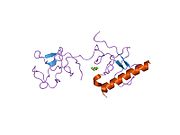
[ редактировать ]Полная длина плазминогена состоит из семи доменов. В дополнение к С-концевой химотрипсин-подобной сериновой протеазой, плазминоген содержит N-концевой домен Pan Apple (PAP) вместе с пятью доменами Kringle (KR1-5) . Домен пан-яблока содержит важные детерминанты для поддержания плазминогена в закрытой форме, а домены Kringle ответственны за связывание с остатками лизина, присутствующих в рецепторах и субстратах.
Рентгеновская кристаллическая структура закрытого плазминогена показывает, что домены PAP и SP поддерживают закрытую конформацию посредством взаимодействий, выполняемых во всем массиве Kringle. [ 9 ] Хлоридные ионы дополнительно соединяют интерфейсы PAP / KR4 и SP / KR2, объясняя физиологическую роль хлорида сыворотки в стабилизации закрытого конформера. Структурные исследования также показывают, что различия в гликозилировании изменяют положение KR3. Эти данные помогают объяснить функциональные различия между плазминогенными гликоформами типа I и типа II. [ Цитация необходима ]
В замкнутом плазминогене доступ к активационной связи (R561/V562), нацеленный на расщепление TPA, а UPA блокируется через положение последовательности линкера KR3/KR4 и сахарного сахара O на T346. Положение KR3 также может препятствовать доступу к циклу активации . Междоменные взаимодействия также блокируют все сайты связывания Kringle, помимо взаимосвязанного от KR-1, что позволяет предположить, что последний домен регулирует рекрутирование про-энзийона для целей. Анализ промежуточной структуры плазминогена позволяет предположить, что конформационные изменения плазминогена в открытой форме инициируются через KR-5, временно отслаиваясь от домена PAP. Эти движения подвергают сайт связывания лизина KR5 с потенциальными партнерами по связыванию и предполагают требование к пространственно различным остаткам лизина в выявлении рекрутирования плазминогена и конформационных изменений соответственно. [ 9 ]
Механизм инактивации плазмина
[ редактировать ]Плазмин инактивируется белками, такими как α2-макроглобулин и α2-антиплазмин . [ 10 ] Механизм инактивации плазмина включает в себя расщепление α2-макроглобулина в области приманки (сегмент AM, который особенно восприимчив к протеолитическому расщеплению) плазмином. Это инициирует конформационное изменение, так что α2-макроглобулин падает по плазминам. В полученном комплексе α2-макроглобулино-плазмин активный сайт плазмина стерически экранируется, что существенно уменьшает доступ плазмина к белковым субстратам. Два дополнительных события происходят в результате расщепления области приманки, а именно (i) h-цистеинил-G-глутамил тиол эфир α2-макроглобулина становится высоко реактивным, и (ii) основное конформационное изменение подвергает консервативного связывания COOH-концевого рецептора связы домен. Воздействие этого рецепторного связывающего домена позволяет α2-макроглобулиново-протеаз-комплекс связываться с рецепторами клиренса и удалять из кровообращения.
Патология
[ редактировать ]Дефицит плазмина может привести к тромбозу , так как сгустки не имеют адекватного ухудшения. Дефицит плазминогена у мышей приводит к дефектному восстановлению печени, [ 11 ] Дефектное заживление ран, репродуктивные аномалии. [ 12 ] [ 13 ]
У людей редкое расстройство, называемое дефицитом плазминогена типа I ( онлайн -наследство менделия у человека (OMIM): 217090 ), вызвано мутациями гена PLG и часто проявляется лигновым конъюнктивитом . [ 14 ]
Редкая миссенс-мутация в домене Kringle 3 плазминогена, приводящая к новому типу диспласплазмагеноемии, представляет молекулярную основу подтипа наследственного ангионеврена с нормальным ингибитором C1; [ 15 ] Мутация создает новый сайт связывания лизина в Kringle 3 и изменяет гликозилирование плазминогена. [ 15 ] Было показано, что мутантный плазминогенный белок является высокоэффективной кининогеназой, которая непосредственно высвобождает брадикинин из высоко- и низкого молекулярного кининогена. [ 16 ]
Взаимодействия
[ редактировать ]Было показано, что плазмин взаимодействует с тромбоспондином 1 , [ 17 ] [ 18 ] Альфа 2-антиплазмин [ 19 ] [ 20 ] и IGFBP3 . [ 21 ] Более того, плазмин индуцирует генерацию брадикинина у мышей и людей с помощью высокомолекулярного расщепления кининогена. [ 22 ]
Ссылки
[ редактировать ]- ^ Подпрыгнуть до: а беременный в GRCH38: Ensembl Release 89: ENSG00000122194 - ENSEMBL , май 2017 г.
- ^ Подпрыгнуть до: а беременный в GRCM38: Ensembl Release 89: Ensmusg00000059481 - Ensembl , май 2017 г.
- ^ «Человеческая PubMed ссылка:» . Национальный центр информации о биотехнологии, Национальная медицина США .
- ^ «Мышь Pubmed ссылка:» . Национальный центр информации о биотехнологии, Национальная медицина США .
- ^ Подпрыгнуть до: а беременный «Ген Entrez: плазминоген» .
- ^ Atsev S, Томов N (декабрь 2020 г.). «Использование антифибринолитики для борьбы с нейровоспалением» . Исследование нейронной регенерации . 15 (12): 2203–2206. doi : 10.4103/1673-5374.284979 . PMC 7749481 . PMID 32594031 .
- ^ Miyata T, Iwanaga S, Sakata Y, Aoki N (октябрь 1982). «Плазминоген Точиги: неактивный плазмин в результате замены аланина-600 треонином в активном участке» . Труды Национальной академии наук Соединенных Штатов Америки . 79 (20): 6132–6136. Bibcode : 1982pnas ... 79.6132M . doi : 10.1073/pnas.79.20.6132 . PMC 347073 . PMID 6216475 .
- ^ Forsgren M, Råden B, Israelsson M, Larsson K, Hedén Lo (март 1987 г.). «Молекулярное клонирование и характеристика полноразмерного клона кДНК для человеческого плазминогена» . Письма Febs . 213 (2): 254–260. doi : 10.1016/0014-5793 (87) 81501-6 . PMID 3030813 . S2CID 9075872 .
- ^ Подпрыгнуть до: а беременный в Law RH, Caradoc-Davies T, Cowieson N, Horvath AJ, Quek AJ, Encarnacao JA, et al. (Март 2012 г.). «Рентгеновская кристаллическая структура полноразмерного человеческого плазминогена» . Сотовые отчеты . 1 (3): 185–190. doi : 10.1016/j.celrep.2012.02.012 . PMID 22832192 .
- ^ Wu G, Quek AJ, Caradoc-Davies TT, Ekkel SM, Mazzitelli B, Whispock JC, Law RH (апрель 2019 г.). «Структурные исследования ингибирования плазмина». Биохимическое общество транзакций . 47 (2): 541–557. doi : 10.1042/bst20180211 . PMID 30837322 . S2CID 73463150 .
- ^ Bezerra JA, Bugge TH, Melin-Aldana H, Sabla G, Kombrinck KW, Witte DP, Degen JL (декабрь 1999 г.). «Дефицит плазминогена приводит к нарушению ремоделирования после токсического повреждения печени» . Труды Национальной академии наук Соединенных Штатов Америки . 96 (26): 15143–15148. Bibcode : 1999pnas ... 9615143b . doi : 10.1073/pnas.96.26.15143 . PMC 24787 . PMID 10611352 .
- ^ Romer J, Bugge TH, Pyke C, Lund LR, Flick MJ, Deden JL, Dano K (март 1996 г.). «Нарушение заживления ран у мышей с нарушенным геном плазминогена». Природная медицина . 2 (3): 287–292. doi : 10.1038/nm0396-287 . PMID 8612226 . S2CID 29981847 .
- ^ Ploplis VA, Carmeliet P, Vazirzadeh S, Van Vlaenderen I, Moons L, Plow EF, Collen D (ноябрь 1995). «Влияние нарушения гена плазминогена на тромбоз, рост и здоровье у мышей». Циркуляция . 92 (9): 2585–2593. doi : 10.1161/01.cir.92.9.2585 . PMID 7586361 .
- ^ Schuster V, Hügle B, Tefs K (декабрь 2007 г.). «Дефицит плазминогена» . Журнал тромбоза и гемостаза . 5 (12): 2315–2322. doi : 10.1111/j.1538-7836.2007.02776.x . PMID 17900274 .
- ^ Подпрыгнуть до: а беременный Dewald G (март 2018 г.). «Миссенс -мутация в гене плазминогена, в домене плазминогена Kringle 3, в наследственном ангиочедовом облегчении с нормальным ингибитором C1». Биохимическая и биофизическая исследовательская коммуникация . 498 (1): 193–198. doi : 10.1016/j.bbrc.2017.12.060 . PMID 29548426 .
- ^ Dickeson SK, Kumar S, Sun MF, Mohammed BM, Phillips DR, Whisstock JC, et al. (Май 2022). «Механизм наследственного ангионевротического образования, вызванный лизином 311-к-глутаминовой кислотой в плазминоген» . Кровь . 139 (18): 2816–2829. doi : 10.1182/blood.2021012945 . PMC 9074402 . PMID 35100351 .
- ^ Silverstein RL, Leung LL, Harpel PC, Nachman RL (ноябрь 1984 г.). «Сложное образование тромбоспондина тромбоцитов с плазминогеном. Модуляция активации активатором ткани» . Журнал клинических исследований . 74 (5): 1625–1633. doi : 10.1172/jci111578 . PMC 425339 . PMID 6438154 .
- ^ Depoli P, Bacon-Baguley T, Kendra-Franczak S, Cederholm MT, Walz Da (март 1989 г.). «Взаимодействие тромбоспондина с плазминогеном. Свидетельством связывания с определенной областью структуры Kringle плазминогена» . Кровь . 73 (4): 976–982. doi : 10.1182/blood.v73.4.976.976 . PMID 2522013 .
- ^ Wiman B, Collen D (сентябрь 1979 г.). «О механизме реакции между альфа-альфа-2-антиплазмином человека и плазмином» . Журнал биологической химии . 254 (18): 9291–9297. doi : 10.1016/s0021-9258 (19) 86843-6 . PMID 158022 .
- ^ Shieh BH, Travis J (май 1987). «Реактивный сайт человеческого альфа-2-антиплазмин» . Журнал биологической химии . 262 (13): 6055–6059. doi : 10.1016/s0021-9258 (18) 45536-6 . PMID 2437112 .
- ^ Кэмпбелл П.Г., Дарем С.К., Суваничкул А., Хейс Д.Д., Пауэлл Д.Р. (август 1998 г.). «Плазминоген связывает гепарин-связывающий домен инсулиноподобного фактора роста, связывающего белок-3». Американский журнал физиологии . 275 (2): E321 - E331. doi : 10.1152/ajpendo.1998.275.2.e321 . PMID 9688635 .
- ^ Marcos-Contreras OA, Martinez de Lizarrondo S, Bardou I, Orset C, Pruvost M, Anfray A, et al. (Ноябрь 2016). «Гиперфибринолиз увеличивает проницаемость гематоэнцефалического барьеры с помощью плазмин- и брадикикинина-зависимого механизма» . Кровь . 128 (20): 2423–2434. doi : 10.1182/blood-2016-03-705384 . PMID 27531677 .
Дальнейшее чтение
[ редактировать ]- Shanmukhappa K, Mourya R, Sabla GE, Degen JL, Bezerra Ja (июль 2005 г.). «Печеночный переключатель поджелудочной железы определяет роль гемостатических факторов в клеточной пластичности у мышей» . Труды Национальной академии наук Соединенных Штатов Америки . 102 (29): 10182–10187. Bibcode : 2005pnas..10210182S . doi : 10.1073/pnas.0501691102 . PMC 1177369 . PMID 16006527 .
- Anglés-Cano E, Rojas G (январь 2002 г.). «Аполипопротеин (а): структурная функция взаимосвязан в сайте связывания лизин и участком расщепления плазминогена». Биологическая химия . 383 (1): 93–99. doi : 10.1515/bc.2002.009 . PMID 11928826 . S2CID 29248198 .
- Ranson M, Andronicos NM (май 2003 г.). «Связывание плазминогена и рак: обещания и подводные камни». Границы в биологии . 8 (6): S294 - S304. doi : 10.2741/1044 . PMID 12700073 .
Внешние ссылки
[ редактировать ]- Онлайн-база данных Merops S01.233 для пептидаз и их ингибиторов: Archived 2019-09-13 на машине Wayback
- Плазмин в Национальной библиотеке медицинской библиотеки Медицинской библиотеки (Mesh)
Эта статья включает в себя текст из Национальной медицины Соединенных Штатов , которая находится в общественном достоянии .