Биомедицинская инженерия
Эта статья нуждается в дополнительных цитатах для проверки . ( июль 2017 г. ) |


Биомедицинская инженерия ( BME ) или медицинская инженерия — это применение инженерных принципов и концепций проектирования в медицине и биологии для медицинских целей (например, в диагностических или терапевтических целях). BME также традиционно является логической наукой, способствующей улучшению лечения, включая диагностику , мониторинг и терапию . [1] [2] В сферу деятельности биомедицинского инженера также входит управление имеющимся медицинским оборудованием в больницах с соблюдением соответствующих отраслевых стандартов. Это включает в себя закупки, плановые испытания, профилактическое обслуживание и рекомендации по оборудованию. Эта роль также известна как техник по биомедицинскому оборудованию (BMET) или клинический инженер .
Биомедицинская инженерия недавно стала отдельной областью исследований по сравнению со многими другими областями инженерии. [ нужна ссылка ] Такая эволюция является обычной, поскольку новая область переходит от междисциплинарной специализации среди уже существующих областей к тому, чтобы считаться областью сама по себе. Большая часть работы в области биомедицинской инженерии состоит из исследований и разработок , охватывающих широкий спектр областей (см. ниже). Выдающиеся применения биомедицинской инженерии включают разработку биосовместимых протезов , различных диагностических и терапевтических медицинских устройств, от клинического оборудования до микроимплантатов, технологий визуализации, таких как МРТ и ЭКГ / ЭКГ , регенеративный рост тканей и разработку фармацевтических препаратов , включая биофармацевтические препараты .
Подполя и связанные поля
[ редактировать ]Биоинформатика
[ редактировать ]
Биоинформатика — это междисциплинарная область, которая разрабатывает методы и программные инструменты для понимания биологических данных. Как междисциплинарная область науки, биоинформатика сочетает в себе информатику, статистику, математику и инженерию для анализа и интерпретации биологических данных.
Биоинформатика считается одновременно общим термином для совокупности биологических исследований, в которых компьютерное программирование является частью их методологии, а также ссылкой на конкретные «конвейеры» анализа, которые неоднократно используются, особенно в области геномики. Обычное использование биоинформатики включает идентификацию генов-кандидатов и нуклеотидов (SNP). Часто такая идентификация проводится с целью лучшего понимания генетической основы заболевания, уникальных адаптаций, желаемых свойств (особенно у сельскохозяйственных видов) или различий между популяциями. Менее формальным способом биоинформатика также пытается понять принципы организации последовательностей нуклеиновых кислот и белков.
Биомеханика
[ редактировать ]
Биомеханика — это изучение структуры и функций механических аспектов биологических систем на любом уровне, от целых организмов до органов , клеток и клеточных органелл . [3] используя методы механики . [4]
Биоматериалы
[ редактировать ]Биоматериал — это любая материя, поверхность или конструкция, которая взаимодействует с живыми системами. как науке Биоматериалам около пятидесяти лет. Изучение биоматериалов называется наукой о биоматериалах или инженерией биоматериалов . На протяжении всей своей истории он переживал устойчивый и сильный рост, при этом многие компании инвестировали большие суммы денег в разработку новых продуктов. Биоматериаловедение включает в себя элементы медицины, биологии, химии, тканевой инженерии и материаловедения.
Биомедицинская оптика
[ редактировать ]Биомедицинская оптика сочетает в себе принципы физики, инженерии и биологии для изучения взаимодействия биологических тканей и света и того, как это можно использовать для зондирования, визуализации и лечения. [5] Он имеет широкий спектр применений, включая оптическую визуализацию, микроскопию, офтальмоскопию, спектроскопию и терапию. Примеры методов и технологий биомедицинской оптики включают оптическую когерентную томографию (ОКТ), флуоресцентную микроскопию , конфокальную микроскопию и фотодинамическую терапию (ФДТ). ОКТ, например, использует свет для создания трехмерных изображений внутренних структур с высоким разрешением, таких как сетчатка глаза или коронарные артерии сердца. Флуоресцентная микроскопия включает в себя маркировку конкретных молекул флуоресцентными красителями и их визуализацию с помощью света, что дает представление о биологических процессах и механизмах заболеваний. В последнее время адаптивная оптика помогает в визуализации, исправляя аберрации в биологических тканях, позволяя получать изображения с более высоким разрешением и повышать точность таких процедур, как лазерная хирургия и визуализация сетчатки.
Тканевая инженерия
[ редактировать ]Тканевая инженерия, как и генная инженерия (см. ниже), является основным сегментом биотехнологии , который во многом пересекается с BME.
Одной из целей тканевой инженерии является создание искусственных органов (из биологического материала) для пациентов, нуждающихся в трансплантации органов. Биомедицинские инженеры в настоящее время исследуют методы создания таких органов. Исследователи вырастили твердые челюсти [6] и трахеи [7] с этой целью из стволовых клеток человека. Несколько искусственных мочевых пузырей были выращены в лабораториях и успешно трансплантированы пациентам-людям. [8] Биоискусственные органы, в которых используются как синтетические, так и биологические компоненты, также являются предметом исследований, например, вспомогательные устройства для печени, в которых используются клетки печени в конструкции искусственного биореактора. [9]

Генная инженерия
[ редактировать ]Генная инженерия, технология рекомбинантной ДНК, генетическая модификация/манипуляция (ГМ) и сплайсинг генов — это термины, которые применяются к прямому манипулированию генами организма. В отличие от традиционной селекции, косвенного метода генетических манипуляций, генная инженерия использует современные инструменты, такие как молекулярное клонирование и трансформация, для прямого изменения структуры и характеристик целевых генов. Методы генной инженерии нашли успех во многих приложениях. Некоторые примеры включают улучшение технологии выращивания сельскохозяйственных культур ( не медицинское применение , а см. инженерию биологических систем ), производство синтетического человеческого инсулина с использованием модифицированных бактерий, производство эритропоэтина в клетках яичников хомяка и производство новых типов экспериментальные мыши, такие как онкологическая мышь (раковая мышь), для исследований. [ нужна ссылка ]
Нейронная инженерия
[ редактировать ]Нейронная инженерия (также известная как нейроинженерия) — это дисциплина, которая использует инженерные методы для понимания, восстановления, замены или улучшения нейронных систем. Нейронные инженеры обладают уникальной квалификацией для решения проблем проектирования на стыке живой нервной ткани и неживых конструкций.
Фармацевтическая инженерия
[ редактировать ]Фармацевтическая инженерия — это междисциплинарная наука, которая включает в себя разработку лекарств, доставку и нацеливание новых лекарств, фармацевтические технологии, отдельные операции химической инженерии и фармацевтический анализ. Его можно рассматривать как часть аптеки, поскольку он ориентирован на использование технологий химических агентов для обеспечения лучшего медицинского лечения.
Больница и медицинское оборудование
[ редактировать ]
Это чрезвычайно широкая категория , по существу охватывающая все продукты здравоохранения, которые не достигают намеченных результатов преимущественно химическими (например, фармацевтические препараты) или биологическими (например, вакцины) средствами и не связаны с метаболизмом.
Медицинское изделие предназначено для использования:
- диагноз заболевания или других состояний
- в лечении, смягчении, лечении или профилактике заболеваний.
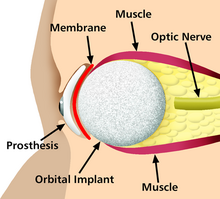
Некоторые примеры включают кардиостимуляторы , инфузионные насосы , аппараты искусственного кровообращения , аппараты для диализа , искусственные органы , имплантаты , протезы конечностей , корректирующие линзы , кохлеарные имплантаты , глазные протезы , лицевые протезы , соматические протезы и зубные имплантаты .
Стереолитография — практический пример медицинского моделирования, используемого для создания физических объектов. Помимо моделирования органов и человеческого тела, новые инженерные методы в настоящее время также используются в исследованиях и разработке новых устройств для инновационных методов лечения. [10] лечение, [11] наблюдение за пациентами, [12] сложных заболеваний.
Медицинские устройства регулируются и классифицируются (в США) следующим образом (см. также Регламент ):
- Устройства класса I представляют минимальный потенциал вреда для пользователя и часто имеют более простую конструкцию, чем устройства класса II или класса III. К устройствам этой категории относятся депрессоры языка, подкладные суда, эластичные бинты, смотровые перчатки, ручные хирургические инструменты и другие аналогичные типы общего оборудования.
- Устройства класса II подлежат специальному контролю в дополнение к общему контролю устройств класса I. Специальные меры контроля могут включать особые требования к маркировке, обязательные стандарты эффективности и послепродажный надзор . Устройства этого класса, как правило, неинвазивны и включают рентгеновские аппараты, PACS, инвалидные коляски с электроприводом, инфузионные насосы и хирургические простыни.
- Устройства класса III обычно требуют предварительного одобрения (PMA) или предпродажного уведомления (510k), научной экспертизы для обеспечения безопасности и эффективности устройства в дополнение к общим мерам контроля класса I. Примеры включают замену сердечных клапанов , имплантатов тазобедренного и коленного сустава, грудные имплантаты, наполненные силиконовым гелем, имплантированные стимуляторы мозжечка, имплантируемые генераторы импульсов кардиостимулятора и внутрикостные (внутрикостные) имплантаты.
Медицинская визуализация
[ редактировать ]Медицинская/биомедицинская визуализация является основным сегментом медицинского оборудования . Эта область посвящена предоставлению клиницистам возможности прямо или косвенно «видеть» вещи, которые не видны на виду (например, из-за их размера и/или местоположения). Это может включать использование ультразвука, магнетизма, ультрафиолета, радиологии и других средств.
Альтернативно, в оборудовании с навигационным управлением используется технология электромагнитного слежения, такая как установка катетера в мозг или системы размещения зонда для кормления . Например, ENvue от ENvizion Medical, электромагнитная навигационная система для размещения зонда для энтерального питания. Система использует внешний генератор поля и несколько пассивных ЭМ-датчиков, позволяющих масштабировать изображение в соответствии с контуром тела пациента, а также просматривать в реальном времени положение и направление кончика питательной трубки, что помогает медицинскому персоналу обеспечить правильное размещение в желудочно- кишечном тракте. тракт . [13]
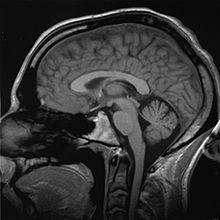
Технологии визуализации часто необходимы для медицинской диагностики и, как правило, представляют собой самое сложное оборудование, используемое в больнице, включая: рентгеноскопию , магнитно-резонансную томографию (МРТ), ядерную медицину , позитронно-эмиссионную томографию (ПЭТ), ПЭТ-КТ , проекционную рентгенографию, например Рентгеновские и компьютерные исследования , томография , УЗИ , оптическая микроскопия и электронная микроскопия .
Медицинские имплантаты
[ редактировать ]Имплантат – это своего рода медицинское устройство, предназначенное для замены и действия в качестве недостающей биологической структуры (по сравнению с трансплантатом, который означает пересаженную биомедицинскую ткань). Поверхность имплантатов, контактирующая с телом, может быть изготовлена из биомедицинского материала, такого как титан, силикон или апатит, в зависимости от того, что является наиболее функциональным. В некоторых случаях имплантаты содержат электронику, например, искусственные кардиостимуляторы и кохлеарные имплантаты. Некоторые имплантаты являются биоактивными, например устройства для подкожной доставки лекарств в форме имплантируемых таблеток или стентов с лекарственным покрытием .

Бионика
[ редактировать ]Замена частей тела искусственными — одно из многих применений бионики. Занимаясь сложным и тщательным изучением свойств и функций систем человеческого организма, бионика может применяться для решения некоторых инженерных задач. Тщательное изучение различных функций и процессов глаз, ушей и других органов проложило путь к созданию усовершенствованных фотоаппаратов, телевизоров, радиопередатчиков и приемников и многих других инструментов.
Биомедицинские датчики
[ редактировать ]В последние годы все больше внимания привлекают биомедицинские датчики, основанные на микроволновых технологиях. Различные датчики могут быть изготовлены для конкретных целей как при диагностике, так и при мониторинге заболеваний, например, микроволновые датчики могут использоваться в качестве дополнительного метода к рентгеновскому излучению для мониторинга травм нижних конечностей. [14] Датчик контролирует диэлектрические свойства и, таким образом, может заметить изменения в тканях (костях, мышцах, жире и т. д.) под кожей, поэтому при измерении в разное время в процессе заживления реакция датчика будет меняться по мере заживления травмы.
Клиническая инженерия
[ редактировать ]Клиническая инженерия — это отрасль биомедицинской инженерии, занимающаяся фактическим внедрением медицинского оборудования и технологий в больницах или других клинических учреждениях. Основные роли клинических инженеров включают обучение и контроль технических специалистов по биомедицинскому оборудованию (BMET) , выбор технологических продуктов/услуг и логистическое управление их внедрением, работу с государственными регулирующими органами при проведении инспекций/аудитов, а также работу в качестве технологических консультантов для другого персонала больницы (например, врачей, администраторов). , ИТ и др.). Клинические инженеры также консультируют и сотрудничают с производителями медицинского оборудования относительно перспективных усовершенствований конструкции на основе клинического опыта, а также отслеживают развитие современного уровня техники, чтобы соответствующим образом перенаправить схемы закупок.
Присущая им сосредоточенность на практическом внедрении технологий, как правило, заставляет их больше ориентироваться на постепенные изменения и реконфигурации на уровне, а не на революционные исследования и разработки или идеи, до клинического внедрения которых может пройти много лет; однако предпринимаются все большие усилия по расширению этого временного горизонта, в течение которого клинические инженеры могут влиять на траекторию биомедицинских инноваций. В своих различных ролях они образуют «мост» между основными проектировщиками и конечными пользователями, сочетая в себе возможность находиться рядом с точкой использования, а также обучаться разработке продуктов и процессов. Отделы клинической инженерии иногда нанимают не только биомедицинских инженеров, но и промышленных/системных инженеров для помощи в исследовании/оптимизации операций, человеческом факторе, анализе затрат и т. д. Также см. раздел « Инженерия безопасности» , где обсуждаются процедуры, используемые для проектирования безопасных систем. В состав отдела клинической инженерии входят менеджер, руководитель, инженер и техник. Таково соотношение: один инженер на восемьдесят коек в больнице. Клинические инженеры также уполномочены проводить аудит фармацевтических и связанных с ними магазинов, чтобы отслеживать отзыв FDA инвазивных товаров.
Реабилитационная инженерия
[ редактировать ]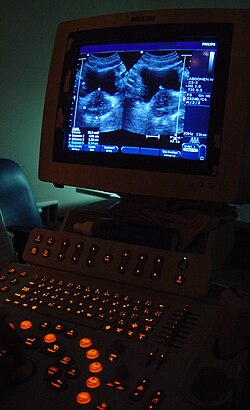
Реабилитационная инженерия — это систематическое применение технических наук для проектирования, разработки, адаптации, тестирования, оценки, применения и распространения технологических решений проблем, с которыми сталкиваются люди с ограниченными возможностями. Функциональные области, рассматриваемые с помощью реабилитационной техники, могут включать мобильность, общение, слух, зрение и познание, а также деятельность, связанную с трудоустройством, независимой жизнью, образованием и интеграцией в общество. [1]
Хотя некоторые инженеры по реабилитации имеют степени магистра в области реабилитационной инженерии, обычно являющейся узкой специализацией в области биомедицинской инженерии, большинство инженеров по реабилитации имеют степени бакалавра или магистра в области биомедицинской инженерии, машиностроения или электротехники. Португальский университет предоставляет степень бакалавра и магистра в области реабилитационной техники и доступности. [6] [8] Квалификацию инженера по реабилитации в Великобритании можно получить, пройдя университетский курс бакалавриата с отличием, например, в Институте дизайна и технологий здравоохранения Университета Ковентри. [9]
Процесс реабилитации людей с ограниченными возможностями часто влечет за собой разработку вспомогательных устройств, таких как приспособления для ходьбы, предназначенных для содействия включению их пользователей в основную жизнь общества, коммерцию и отдых.
Нормативные вопросы
[ редактировать ]Этот раздел нуждается в дополнительных цитатах для проверки . ( август 2017 г. ) |
В последние десятилетия нормативные вопросы постоянно увеличивались в связи с многочисленными инцидентами, вызванными использованием устройств для пациентов. Например, с 2008 по 2011 год в США было зарегистрировано 119 отзывов FDA медицинских устройств, отнесенных к классу I. По данным Управления по контролю за продуктами и лекарствами США (FDA), отзыв класса I связан с «ситуацией, в которой существует разумная вероятность того, что использование продукта или воздействие на него приведет к серьезным неблагоприятным последствиям для здоровья или смерти» [15]
Независимо от законодательства конкретной страны, основные цели регулирования совпадают во всем мире. [16] Например, в регламенте на медицинские изделия изделие должно быть: 1) безопасным и 2) эффективным и 3) для всех выпускаемых изделий (почему эта часть удалена?)
Продукт безопасен, если пациенты, пользователи и третьи лица не подвергаются неприемлемому риску физической опасности (смерть, травмы и т. д.) при его предполагаемом использовании. На устройствах должны быть внедрены защитные меры для снижения остаточных рисков на приемлемом уровне по сравнению с выгодой, получаемой от их использования.
Продукт эффективен, если при предполагаемом использовании он работает так, как указано производителем. Эффективность достигается за счет клинической оценки, соответствия стандартам эффективности или демонстрации существенной эквивалентности уже продаваемому устройству.
Прежние характеристики должны быть обеспечены для всех изготавливаемых изделий медицинского изделия. Это требует наличия системы качества для всех соответствующих объектов и процессов, которые могут влиять на безопасность и эффективность на протяжении всего жизненного цикла медицинского изделия.
Область разработки медицинского оборудования является одной из наиболее строго регулируемых областей техники, и практикующие биомедицинские инженеры должны регулярно консультироваться и сотрудничать с юристами по нормативному праву и другими экспертами. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) является основным регулирующим органом здравоохранения в Соединенных Штатах, обладающим юрисдикцией в отношении медицинских устройств, лекарств, биологических препаратов и комбинированных продуктов. Первостепенными целями, определяющими политические решения FDA, являются безопасность и эффективность медицинских продуктов, которые должны быть гарантированы посредством действующей системы качества, как указано в регламенте 21 CFR 829 . Кроме того, поскольку биомедицинские инженеры часто разрабатывают устройства и технологии для «потребительского» использования, такие как устройства физиотерапии (которые также являются «медицинскими» устройствами), они также могут в некоторых отношениях регулироваться Комиссией по безопасности потребительских товаров . Самыми большими препятствиями, как правило, являются «одобрение» 510 000 (обычно для устройств класса 2) или предпродажное «одобрение» (обычно для лекарств и устройств класса 3).
В европейском контексте безопасность, эффективность и качество обеспечиваются посредством «Оценки соответствия», которая определяется как «метод, с помощью которого производитель демонстрирует, что его устройство соответствует требованиям Европейской директивы по медицинскому оборудованию ». Директива определяет различные процедуры в зависимости от класса устройства, начиная от простой декларации соответствия (Приложение VII) для устройств класса I до проверки ЕС (Приложение IV), обеспечения качества производства (Приложение V), обеспечения качества продукции (Приложение VI). и Полная гарантия качества (Приложение II). Директива о медицинском оборудовании определяет подробные процедуры сертификации. В общих чертах, эти процедуры включают испытания и проверки, которые должны содержаться в конкретных поставках, таких как файл управления рисками, технический файл и поставки системы качества. Файл управления рисками — это первый результат, определяющий последующие этапы проектирования и производства. Этап управления рисками должен управлять продуктом таким образом, чтобы риски, связанные с продуктом, были снижены до приемлемого уровня с учетом преимуществ, ожидаемых для пациентов от использования устройства. технический файл содержит все данные документации и записи, подтверждающие сертификацию медицинского изделия. Технический файл FDA имеет аналогичное содержание, хотя и имеет другую структуру. Результаты системы качества обычно включают процедуры, обеспечивающие качество на протяжении всего жизненного цикла продукта. Один и тот же стандарт (ISO EN 13485) обычно применяется к системам менеджмента качества в США и во всем мире.

В Европейском Союзе существуют сертифицирующие организации, называемые « Уполномоченные органы », аккредитованные европейскими государствами-членами. Уполномоченные органы должны обеспечить эффективность процесса сертификации для всех медицинских изделий, за исключением изделий класса I, для которых декларации о соответствии, предоставленной производителем, достаточно для маркетинга. После того, как продукт прошел все этапы, требуемые Директивой о медицинском оборудовании, он имеет право иметь маркировку CE , указывающую, что устройство считается безопасным и эффективным при использовании по назначению, и, следовательно, его можно продавать в пределах территории Европейского Союза.
Различные механизмы регулирования иногда приводят к тому, что определенные технологии сначала разрабатываются либо в США, либо в Европе, в зависимости от более благоприятной формы регулирования. Хотя страны часто стремятся к существенной гармонии, чтобы облегчить межнациональное распределение, философские разногласия относительно оптимальной степени регулирования могут быть помехой; более строгие правила кажутся привлекательными на интуитивном уровне, но критики осуждают компромиссные издержки с точки зрения замедления доступа к жизненно важным разработкам.
РоХС II
[ редактировать ]Директива 2011/65/EU, более известная как RoHS 2, представляет собой переработку законодательства, первоначально введенного в 2002 году. Первоначальное законодательство ЕС «Ограничения использования некоторых опасных веществ в электрических и электронных устройствах» (Директива RoHS 2002/95/EC) было заменено и заменен документом 2011/65/EU, опубликованным в июле 2011 года и широко известным как RoHS 2. RoHS стремится ограничить количество опасных веществ, находящихся в обращении в электронных продуктах, в частности токсинов и тяжелых металлов, которые впоследствии выбрасываются в окружающую среду при переработке таких устройств.
Область применения RoHS 2 расширена за счет включения ранее исключенных продуктов, таких как медицинские приборы и промышленное оборудование. Кроме того, производители теперь обязаны предоставлять оценки рисков соответствия и отчеты об испытаниях – или объяснять, почему их нет. Впервые не только производители, но также импортеры и дистрибьюторы разделяют ответственность за то, чтобы электрическое и электронное оборудование, подпадающее под действие RoHS, соответствовало ограничениям по опасным веществам и имело маркировку CE на своей продукции.
МЭК 60601
[ редактировать ]Новый международный стандарт IEC 60601 для электромедицинских устройств для домашнего здравоохранения, определяющий требования к устройствам, используемым в домашних медицинских учреждениях. МЭК 60601-1-11 (2010 г.) теперь должен быть включен в проектирование и проверку широкого спектра медицинских устройств для домашнего использования и оказания медицинской помощи наряду с другими применимыми стандартами серии МЭК 60601, 3-е издание.
Обязательная дата внедрения европейской версии стандарта EN — 1 июня 2013 г. FDA США требует использования стандарта 30 июня 2013 г., а Министерство здравоохранения Канады недавно продлило обязательную дату с июня 2012 г. по апрель 2013 г. Североамериканские агентства будут требовать эти стандарты только для подачи новых устройств, в то время как ЕС будет применять более строгий подход, требуя, чтобы все применимые устройства, размещаемые на рынке, соответствовали стандарту домашнего здравоохранения.
АС/НЗС 3551:2012
[ редактировать ]AS/ANS 3551:2012 — это стандарты Австралии и Новой Зеландии по управлению медицинскими устройствами. Стандарт определяет процедуры, необходимые для обслуживания широкого спектра медицинских активов в клинических условиях (например, в больнице). [17] Стандарты основаны на стандартах IEC 606101.
Стандарт охватывает широкий спектр элементов управления медицинским оборудованием, включая закупку, приемочные испытания, техническое обслуживание (испытания на электробезопасность и профилактическое обслуживание) и вывод из эксплуатации.
Обучение и сертификация
[ редактировать ]Образование
[ редактировать ]Биомедицинским инженерам требуются значительные знания как в инженерии, так и в биологии, и они обычно имеют степень бакалавра (бакалавр наук, бакалавр наук, бакалавр технических наук или BSE) или магистра (MS, M.Sc., MSE или M.Eng.) или докторская степень (Ph.D. или MD-PhD) [18] [19] [20] ) степень в области BME (биомедицинская инженерия) или другой отрасли техники со значительным потенциалом совпадения BME. Поскольку интерес к BME растет, во многих инженерных колледжах теперь есть факультет или программа биомедицинской инженерии, предложения которых варьируются от уровня бакалавриата (бакалавр наук, бакалавр наук, бакалавр технических наук или BSE) до уровня докторантуры. Биомедицинская инженерия лишь недавно стала отдельной дисциплиной, а не междисциплинарной гибридной специализацией других дисциплин; и программы BME на всех уровнях становятся все более распространенными, включая степень бакалавра наук в области биомедицинской инженерии , которая включает в себя достаточно материалов по биологическим наукам, поэтому многие студенты используют ее в качестве « домедицинской » специальности при подготовке к медицинской школе . Ожидается, что число биомедицинских инженеров будет расти как причина, так и следствие усовершенствований в медицинских технологиях. [21]
В США все большее число программ бакалавриата также признается ABET как аккредитованные программы биоинженерии/биомедицинской инженерии. По состоянию на 2023 год ABET аккредитовано 155 программ. [22]
В Канаде и Австралии распространены аккредитованные программы магистратуры в области биомедицинской инженерии. [23] Например, Университет Макмастера предлагает степень магистра, доктора медицинских наук и доктора биомедицинской инженерии. [24] Первая канадская программа бакалавриата BME была предложена в Университете Гвельфа в качестве четырехлетней программы бакалавриата по инженерным специальностям. программа. [25] Политехнический институт в Монреале также предлагает степень бакалавра в области биомедицинской инженерии. [26] как и Университет Флиндерса. [27]
Как и в случае со многими степенями, репутация и рейтинг программы могут влиять на желательность обладателя степени для трудоустройства или поступления в аспирантуру. Репутация многих степеней бакалавра также связана с аспирантскими или исследовательскими программами учебного заведения, которые имеют некоторые ощутимые факторы для рейтинга, такие как финансирование и объем исследований, публикации и цитирование. В частности, что касается BME, рейтинг университетской больницы и медицинской школы также может быть важным фактором воспринимаемого престижа его отделения / программы BME.
Высшее образование является особенно важным аспектом в BME. Хотя многие инженерные области (например, машиностроение или электротехника) не требуют последипломной подготовки для получения работы начального уровня в своей области, большинство должностей BME предпочитают или даже требуют ее. [28] Поскольку большинство профессий, связанных с BME, связаны с научными исследованиями, например, в области разработки фармацевтических препаратов и медицинского оборудования , высшее образование является почти обязательным требованием (поскольку степень бакалавра обычно не предполагает достаточной исследовательской подготовки и опыта). Это может быть степень магистра или доктора; в то время как по некоторым специальностям доктор философии. встречается значительно чаще, чем в других странах, и почти никогда не составляет большинства (за исключением научных кругов). Фактически, осознаваемая потребность в каком-либо дипломе о высшем образовании настолько сильна, что некоторые программы бакалавриата BME активно отговаривают студентов от специализации BME без выраженного намерения также получить степень магистра или впоследствии подать заявление в медицинскую школу.
Программы магистратуры в BME, как и в других научных областях, очень разнообразны, и отдельные программы могут подчеркивать определенные аспекты в этой области. Они также могут включать в себя обширные совместные усилия с программами в других областях (например, с медицинской школой университета или другими инженерными подразделениями), опять же из-за междисциплинарного характера BME. Магистр и доктор философии. Программы обычно требуют от кандидатов наличия степени бакалавра в области BME или другой инженерной дисциплины (плюс определенные курсовые работы по наукам о жизни) или наукам о жизни (плюс определенные курсы по инженерным наукам).
Образование в BME также сильно различается по всему миру. Благодаря обширному биотехнологическому сектору, многочисленным крупным университетам и относительно небольшому количеству внутренних барьеров США добились значительного прогресса в развитии возможностей образования и обучения BME. Европа, которая также имеет крупный биотехнологический сектор и впечатляющую систему образования, столкнулась с трудностями при создании единых стандартов, поскольку европейское сообщество пытается заменить некоторые из национальных юрисдикционных барьеров, которые все еще существуют. Недавно появились такие инициативы, как BIOMEDEA, направленные на разработку образовательных и профессиональных стандартов, связанных с BME. [29] Другие страны, такие как Австралия, признают и стараются исправить недостатки в своем образовании BME. [30] Кроме того, поскольку развитие высоких технологий обычно является отличительной чертой развитых стран, в некоторых регионах мира наблюдается замедление развития образования, в том числе в BME.
Лицензия/сертификация
[ редактировать ]Как и в случае с другими изучаемыми профессиями, в каждом штате есть определенные (довольно схожие) требования для получения лицензии зарегистрированного профессионального инженера (PE), но в США в промышленности такая лицензия не требуется для работы в качестве инженера в большинстве случаев. ситуаций (из-за исключения, известного как промышленное освобождение, которое фактически применяется к подавляющему большинству американских инженеров). Американская модель, как правило, заключалась только в том, чтобы требовать лицензирования практикующих инженеров, предлагающих инженерные услуги, влияющие на общественное благосостояние, безопасность, защиту жизни, здоровья или собственности, в то время как инженеры, работающие в частной промышленности, не предлагают прямых инженерных услуг государству. общественный или другой бизнес, образование и правительство не нуждаются в лицензировании. В частности, дело обстоит иначе во многих других странах, где лицензия так же необходима по закону для инженерной деятельности, как и для юриспруденции или медицины.
Биомедицинская инженерия регулируется в некоторых странах, например в Австралии, но регистрация обычно только рекомендуется, но не требуется. [31]
В Великобритании инженеры-механики, работающие в области медицинской инженерии, биоинженерии или биомедицинской инженерии, могут получить статус дипломированного инженера через Институт инженеров-механиков . В учреждении также имеется отдел инженерии в области медицины и здравоохранения. [32] В Институте физики и техники в медицине (IPEM) есть комиссия по аккредитации курсов магистратуры в области биомедицинской инженерии, и статус дипломированного инженера также можно получить через IPEM.
Экзамен по основам инженерного дела – первый (и более общий) из двух экзаменов на получение лицензии для большинства юрисдикций США – теперь охватывает биологию (хотя технически это не BME). Для второго экзамена, называемого «Принципы и практика, часть 2», или экзамена по профессиональному инженерному делу, кандидаты могут выбрать содержание конкретной инженерной дисциплины для тестирования; в настоящее время нет возможности для BME, а это означает, что любые биомедицинские инженеры, претендующие на получение лицензии, должны подготовиться к сдаче этого экзамена по другой категории (что не влияет на фактическую лицензию, поскольку большинство юрисдикций все равно не признают специальности по дисциплинам). Однако с 2009 года Общество биомедицинской инженерии (BMES) изучает возможность внедрения версии этого экзамена, специфичной для BME, чтобы облегчить биомедицинским инженерам получение лицензии.
Помимо государственной регистрации, некоторые профессиональные/промышленные организации частного сектора также предлагают сертификаты различной степени значимости. Одним из таких примеров является сертификация сертифицированного клинического инженера (CCE) для клинических инженеров.
Карьерные перспективы
[ редактировать ]В 2012 году в США работало около 19 400 инженеров-биомедиков, и прогнозировалось, что эта область будет расти на 5% (быстрее среднего) с 2012 по 2022 год. [33] В биомедицинской инженерии самый высокий процент женщин-инженеров по сравнению с другими распространенными инженерными профессиями.
Известные цифры
[ редактировать ]Этот раздел нуждается в дополнительных цитатах для проверки . ( сентябрь 2016 г. ) |
- Юлия Тютельман Аптер (умерла) – один из первых специалистов в области нейрофизиологических исследований. [34] и член-основатель Общества биомедицинской инженерии. [35]
- Эрл Баккен (умер) – изобрел первый транзисторный кардиостимулятор, соучредитель Medtronic .
- Форрест Берд (умер) – летчик и пионер изобретения аппаратов искусственной вентиляции легких
- Ю. К. Фунг (умер) – почетный профессор , Калифорнийского университета в Сан-Диего которого многие считают основателем современной биомеханики. [36]
- Лесли Геддес (умерла) - почетный профессор Университета Пердью , инженер-электрик, изобретатель и педагог более 2000 биомедицинских инженеров, получил Национальную медаль технологий в 2006 году от президента Джорджа Буша. [37] за его более чем 50-летний вклад, который породил инновации, начиная от лечения ожогов и заканчивая миниатюрными дефибрилляторами, восстановлением связок и крошечными тонометрами для недоношенных детей, а также новым методом проведения сердечно-легочной реанимации (СЛР).
- Виллем Йохан Колфф (умер) – пионер гемодиализа , а также в области искусственных органов
- Роберт Лангер - профессор института Массачусетского технологического института , руководит крупнейшей лабораторией BME в мире, пионер в области доставки лекарств и тканевой инженерии. [38]
- Джон Маклауд (умер) — один из соавторов инсулина в Университете Кейс Вестерн Резерв .
- Альфред Э. Манн – физик, предприниматель и филантроп. Пионер в области биомедицинской инженерии. [39]
- Дж. Томас Мортимер – заслуженный профессор биомедицинской инженерии Университета Кейс Вестерн Резерв. Пионер в области функциональной электростимуляции (ФЭС) [40]
- Роберт М. Нерем – почетный профессор Технологического института Джорджии . Пионер в области регенерации тканей и биомеханики, автор более 300 опубликованных работ. Его работы в совокупности цитировались более 20 000 раз.
- П. Хантер Пекхэм – профессор биомедицинской инженерии и ортопедии Доннелла в Университете Кейс Вестерн Резерв. Пионер в области функциональной электростимуляции (ФЭС) [41]
- Николас А. Пеппас – профессор технических наук Техасского университета в Остине , пионер в области доставки лекарств , биоматериалов , гидрогелей и нанобиотехнологий .
- Роберт Плонси – почетный профессор Университета Дьюка , пионер электрофизиологии [42]
- Отто Шмитт (покойный) – биофизик, внесший значительный вклад в BME, работающий с биомиметикой.
- Ашер Шапиро (умер) - профессор института Массачусетского технологического института, внес вклад в развитие области BME и медицинских устройств (например, внутриаортальных баллонов)
- Гордана Вуньяк-Новакович – профессор Колумбийского университета , пионер в области тканевой инженерии и биореакторов. проектирования
- Джон Г. Вебстер – почетный профессор Университета Висконсин-Мэдисон , пионер в области инструментальных усилителей для записи электрофизиологических сигналов.
- Фред Вейбелл , соавтор книги «Биомедицинские приборы и измерения»
- У.А. Уитакер (покойный) – провайдер Фонда Уитакера , который поддерживал исследования и образование в области BME, предоставляя более 700 миллионов долларов различным университетам, помогая создать 30 программ BME и помогая финансировать строительство 13 зданий. [43]
См. также
[ редактировать ]- Биомедицина - отрасль медицинской науки, которая применяет биологические и физиологические принципы в клинической практике.
- Кардиофизика – междисциплинарная наука, стоящая на стыке кардиологии и медицинской физики.
- Вычислительная анатомия - междисциплинарная область биологии
- Медицинская физика - Применение физических концепций, теорий и методов в медицине или здравоохранении.
- Физиом
- Программа биомедицинской инженерии и приборостроения (BEIP)
Ссылки
[ редактировать ]- ^ Перейти обратно: а б Джон Денис Эндерле; Джозеф Д. Бронзино (2012). Введение в биомедицинскую инженерию . Академическая пресса. стр. 16–. ISBN 978-0-12-374979-6 . Архивировано из оригинала 26 июля 2024 г. Проверено 22 февраля 2016 г.
- ^ Фахруллин, Равиль; Львов, Юрий, ред. (2014). Инженерия клеточной поверхности . Серия «Умные материалы». Кембридж: Королевское химическое общество. дои : 10.1039/9781782628477 . ISBN 978-1-78262-847-7 . Архивировано из оригинала 25 января 2021 г. Проверено 28 марта 2019 г.
- ^ Александр Р. Макнил (2005). «Механика движения животных» . Современная биология . 15 (16): Р616–Р619. дои : 10.1016/j.cub.2005.08.016 . ПМИД 16111929 . S2CID 14032136 .
- ^ Хатце, Герберт (1974). «Значение термина биомеханика». Журнал биомеханики . 7 (12): 189–190. дои : 10.1016/0021-9290(74)90060-8 . ПМИД 4837555 .
- ^ «Введение в биомедицинскую оптику» (PDF) . Архивировано (PDF) из оригинала 26 июля 2024 г. Проверено 25 января 2018 г.
- ^ Перейти обратно: а б «Челюстная кость, созданная из стволовых клеток» . Новости Би-би-си . 10 октября 2009 года. Архивировано из оригинала 11 октября 2009 года . Проверено 11 октября 2009 г.
- ^ Уоллес Т. Трахеобронхиальная биоинженерия: биотехнология, удовлетворяющая неудовлетворенные медицинские потребности. Adv Drug Deliv, ред. 2011 г.; 63 (4–5): 367–74.
- ^ Перейти обратно: а б «Врачи выращивают органы из собственных клеток пациентов» . CNN . 3 апреля 2006 г. Архивировано из оригинала 25 мая 2017 г. Проверено 2 октября 2006 г.
- ^ Перейти обратно: а б Начинаются испытания первого устройства искусственной печени с использованием человеческих клеток. Архивировано 5 января 2011 г. в Wayback Machine , Чикагский университет , 25 февраля 1999 г.
- ^ « Нано»: новый враг рака Хеде С., Уильгол Н. – Дж. Кан Рес Тер» . www.cancerjournal.net . Архивировано из оригинала 22 декабря 2015 г. Проверено 2 февраля 2007 г.
- ^ Куврёр, Патрик; Вотье, Кристина (2006). «Нанотехнологии: интеллектуальный дизайн для лечения сложных заболеваний» . Фармацевтические исследования . 23 (7): 1417–1450 (34). дои : 10.1007/s11095-006-0284-8 . ПМИД 16779701 . S2CID 1520698 .
- ^ Кертис, Адам С.Г.; Далби, Мэтью; Гадегор, Николай (2006). «Клеточная сигнализация, возникающая в результате нанотопографии: последствия для наномедицинских устройств». Наномедицина . 1 (1): 67–72. дои : 10.2217/17435889.1.1.67 . ISSN 1743-5889 . ПМИД 17716210 .
- ^ Джейкобсон, Льюис Э.; Олаян, Мэй; Уильямс, Джейми М.; Шульц, Жаклин Ф.; Уайз, Ханна М.; Сингх, Амандип; Сакс, Джонатан М.; Бенджамин, Ричард; Эмери, Мари; Вилем, Хилари; Кирби, Дональд Ф. (1 ноября 2019 г.). «Возможность и безопасность нового электромагнитного устройства для установки питательной трубки малого диаметра» . Открытие отделения травматологической хирургии и неотложной помощи . 4 (1): e000330. дои : 10.1136/tsaco-2019-000330 . ISSN 2397-5776 . ПМК 6861064 . ПМИД 31799414 . Архивировано из оригинала 3 марта 2023 года . Проверено 3 марта 2023 г.
- ^ Шах, Сьяйфул; Веландер, Джейкоб; Матур, Парул; Перес, Маурисио; Асан, Нур; Куруп, Дханеш; Блокхейс, Тако; Августин, Робин (21 февраля 2018 г.). «Оценка глубины проникновения датчика с разрезным кольцевым резонатором с использованием in vivo отражательной способности микроволнового излучения и ультразвуковых измерений для реабилитации после травм нижних конечностей» . Датчики . 18 (2): 636. Бибкод : 2018Senso..18..636S . дои : 10.3390/s18020636 . ISSN 1424-8220 . ПМЦ 5855979 . ПМИД 29466312 .
- ^ Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, отзывы о медицинских устройствах и устройствах, излучающих радиацию http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfres/res.cfm. Архивировано 30 сентября 2013 г. на Wayback Machine.
- ^ «Правила в отношении медицинского оборудования: глобальный обзор и руководящие принципы» (PDF) . Всемирная организация здравоохранения (ВОЗ). 2003. Архивировано (PDF) из оригинала 25 октября 2013 г. Проверено 13 сентября 2013 г.
- ^ AS/NZS 3551:2012 Программы управления медицинским оборудованием . Стандарты Австралии. 18 октября 2016 г. ISBN 978-1-74342-277-9 . Архивировано из оригинала 11 марта 2014 г. Проверено 18 октября 2016 г.
- ^ «Программа докторантуры» . Биомедицинская инженерия Джонса Хопкинса . Архивировано из оригинала 29 ноября 2022 г. Проверено 29 ноября 2022 г.
- ^ «Доктор философии+доктор медицинских наук» . Дартмут Инжиниринг . Архивировано из оригинала 29 ноября 2022 г. Проверено 29 ноября 2022 г.
- ^ «Программа подготовки врачей-инженеров» . Школа биомедицинской инженерии Уэлдона – Университет Пердью . Архивировано из оригинала 29 ноября 2022 г. Проверено 29 ноября 2022 г.
- ^ Бюро статистики труда США - Профиль инженеров. Архивировано 19 февраля 2006 г., в Wayback Machine.
- ^ «Дисциплины. Страны. США» . Архивировано из оригинала 20 февраля 2023 г. Проверено 20 февраля 2023 г.
- ^ Гоял, Мег Р. (3 января 2018 г.). Научно-технические термины в биоинженерии и биологической инженерии . ЦРК Пресс. ISBN 978-1-351-36035-7 . Архивировано из оригинала 26 июля 2024 г. Проверено 5 мая 2023 г.
- ^ «Варианты дипломов» . Школа биомедицинской инженерии Макмастера . www.eng.mcmaster.ca. Архивировано из оригинала 24 октября 2019 года . Проверено 24 октября 2019 г.
- ^ «Календарь бакалавриата на 2010-2011 годы - биомедицинская инженерия» . Университет Гвельфа. 07.09.2010. Архивировано из оригинала 26 июля 2024 г. Проверено 7 апреля 2024 г.
- ^ «Степень бакалавра биомедицинской инженерии» . Политехнический институт Монреаля . 15 января 2018 года. Архивировано из оригинала 12 октября 2020 года . Проверено 11 октября 2020 г.
- ^ «Бакалавр технических наук (биомедицины) (с отличием)» . Университет Флиндерса . Архивировано из оригинала 26 июля 2024 года . Проверено 24 октября 2019 г.
- ^ «Перспективы работы инженеров» . Бюро статистики труда США . Архивировано из оригинала 19 декабря 2011 года.
- ^ «БИОМЕДЕЯ» . Сентябрь 2005 г. Архивировано из оригинала 6 мая 2008 г.
- ^ Литгоу, Би Джей (25 октября 2001 г.). «Учебная программа по биомедицинской инженерии: сравнение США, Европы и Австралии» . Архивировано из оригинала 1 мая 2008 года.
- ^ «Национальный инженерный регистр» . Инженеры Австралии. Архивировано из оригинала 5 января 2008 года . Проверено 11 марта 2023 г.
- ^ «Медицинская инженерия: Домашняя страница» . Институт инженеров-механиков . Архивировано из оригинала 2 мая 2007 года.
- ^ Бюро статистики труда, Министерство труда США. Справочник по профессиональным перспективам, издание 2014–2015 гг.: Инженеры-биомедики. Архивировано 17 апреля 2021 г. в Wayback Machine.
- ^ «Доктор Джулия Аптер, офтальмолог и исследователь, 61 год, из Чикаго» . Нью-Йорк Таймс . 18 апреля 1979 г. ISSN 0362-4331 . Архивировано из оригинала 01 марта 2023 г. Проверено 01 марта 2023 г.
- ^ Фагетт-младший, Пол Х.; Хорнер, Патрисия И., ред. (2004). Празднование 35-летия биомедицинской инженерии: историческая перспектива (PDF) . Ландовер, Мэриленд: Общество биомедицинской инженерии . п. 4. Архивировано (PDF) из оригинала 1 марта 2023 г. Проверено 01 марта 2023 г.
- ^ Кассаб, Гассан С. (2004). «ЮК «Берт» Фунг: отец современной биомеханики» (PDF) . Механика и химия биосистем . 1 (1). Tech Science Press: 5–22. дои : 10.3970/mcb.2004.001.005 . ПМИД 16783943 . Архивировано из оригинала (PDF) 2 декабря 2007 г.
- ^ «Лесли Геддес – Национальная медаль технологий 2006 г. » Ютуб. 31 июля 2007 г. Архивировано из оригинала 07.11.2021 . Проверено 24 сентября 2011 г.
- ^ О'Нил, Кэтрин М. (20 июля 2006 г.). «Коллеги чествуют Лангера за 30 лет инноваций» . Пресс-служба Массачусетского технологического института . Архивировано из оригинала 18 февраля 2014 года . Проверено 16 марта 2007 г.
- ^ Гальегос, Эмма (25 октября 2010 г.). «Фонд научных исследований Альфреда Манна (AMF)» . Aemf.org . Проверено 24 сентября 2011 г. [ постоянная мертвая ссылка ]
- ^ «Дж. Томас Мортимер» . Профили преподавателей/сотрудников CSE . Engineering.case.edu. Архивировано из оригинала 2 мая 2023 г. Проверено 14 июня 2018 г.
- ^ «П. Хантер Пекхэм, доктор философии | Заслуженный профессор университета | Университет Кейс Вестерн Резерв» . Заслуженный профессор университета | Университет Кейс Вестерн Резерв . 25 апреля 2018 г. Архивировано из оригинала 26 июля 2024 г. Проверено 14 июня 2018 г.
- ^ «Роберт Плонси, почетный профессор Pfizer-Pratt» . Факультет – Duke BME . Fds.duke.edu. Архивировано из оригинала 5 июня 2009 г. Проверено 11 октября 2009 г.
- ^ «Фонд Уитакера» . Уитакер.орг. Архивировано из оригинала 25 сентября 2011 г. Проверено 24 сентября 2011 г.
Дальнейшее чтение
[ редактировать ]- Бронзино, Джозеф Д. (апрель 2006 г.). Справочник по биомедицинской инженерии (Третье изд.). [ЦРК Пресс]. ISBN 978-0-8493-2124-5 . Архивировано из оригинала 24 февраля 2015 г. Проверено 22 июня 2009 г.
- Виллафане, Карлос (июнь 2009 г.). Биомед: с точки зрения студента (первое изд.). [Techniciansfriend.com]. ISBN 978-1-61539-663-4 .
Внешние ссылки
[ редактировать ] СМИ, связанные с биомедицинской инженерией , на Викискладе?
СМИ, связанные с биомедицинской инженерией , на Викискладе? - Биомедицинская инженерия в Керли

