Ядро клетки

| Клеточная биология | |
|---|---|
| Диаграмма клеток животных | |
 Компоненты типичной животной клетки:
|
Ядро клетки (от латинского kernel или nuculeus «ядро, семя»; мн .: ядра ) представляет собой мембраносвязанную органеллу, обнаруженную в эукариотических клетках . Эукариотические клетки обычно имеют одно ядро, но некоторые типы клеток, такие как эритроциты млекопитающих , не имеют ядер , а некоторые другие, включая остеокласты, имеют их много . Основными структурами, составляющими ядро, являются ядерная оболочка — двойная мембрана, окружающая всю органеллу и изолирующая ее содержимое от клеточной цитоплазмы ; и ядерная матрица , сеть внутри ядра, которая обеспечивает механическую поддержку.
клетки Ядро клетки содержит почти весь геном . Ядерная ДНК часто состоит из нескольких хромосом — длинных нитей ДНК, усеянных различными белками , такими как гистоны , которые защищают и организуют ДНК. Гены . в этих хромосомах структурированы таким образом, чтобы способствовать функционированию клеток Ядро поддерживает целостность генов и контролирует деятельность клетки, регулируя экспрессию генов .
Поскольку ядерная оболочка непроницаема для крупных молекул , ядерные поры необходимы для регулирования ядерного транспорта молекул через оболочку. Поры пересекают обе ядерные мембраны, обеспечивая канал , через который более крупные молекулы должны активно транспортироваться белками-переносчиками, обеспечивая при этом свободное перемещение малых молекул и ионов . Перемещение крупных молекул, таких как белки и РНК, через поры необходимо как для экспрессии генов, так и для поддержания хромосом. Хотя внутренняя часть ядра не содержит каких-либо мембраносвязанных субкомпартментов, существует ряд ядерных телец , состоящих из уникальных белков, молекул РНК и определенных частей хромосом. Самым известным из них является ядрышко , участвующее в сборке рибосом .
Структуры
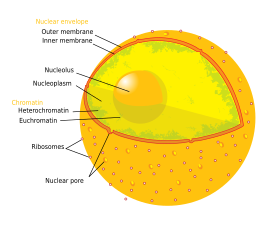
клетки Ядро содержит почти всю ДНК , окружено сетью волокнистых промежуточных нитей, называемых ядерным матриксом , и окружено двойной мембраной, называемой ядерной оболочкой . Ядерная оболочка отделяет жидкость внутри ядра, называемую нуклеоплазмой , от остальной части клетки. Размер ядра коррелирует с размером клетки, и это соотношение наблюдается для различных типов и видов клеток. [ 1 ] У эукариот ядро во многих клетках обычно занимает 10% объема клетки. [ 2 ] : 178 Ядро – самая крупная органелла в клетках животных. [ 3 ] : 12 В клетках человека диаметр ядра составляет примерно шесть микрометров (мкм). [ 2 ] : 179
Ядерная оболочка и поры

состоит Ядерная оболочка из двух мембран — внутренней и наружной ядерной мембраны , перфорированных ядерными порами . [ 2 ] : 649 Вместе эти мембраны служат для отделения генетического материала клетки от остального содержимого клетки и позволяют ядру поддерживать среду, отличную от остальной части клетки. Несмотря на близкое расположение вокруг большей части ядра, эти две мембраны существенно различаются по форме и содержимому. Внутренняя мембрана окружает ядерное содержимое, обеспечивая его определяющий край. [ 3 ] : 14 Различные белки, встроенные во внутреннюю мембрану, связывают промежуточные нити, которые придают ядру его структуру. [ 2 ] : 649 Наружная мембрана окружает внутреннюю мембрану и является продолжением прилегающей мембраны эндоплазматического ретикулума . [ 2 ] : 649 Внешняя ядерная мембрана, являющаяся частью мембраны эндоплазматического ретикулума, усеяна рибосомами , которые активно транслируют белки через мембрану. [ 2 ] : 649 Пространство между двумя мембранами называется перинуклеарным пространством и переходит в просвет эндоплазматической сети . [ 2 ] : 649
В ядерной оболочке млекопитающих имеется от 3000 до 4000 комплексов ядерных пор (NPC), перфорирующих оболочку. [ 2 ] : 650 Каждый NPC содержит восьмикратно симметричную кольцевую структуру в месте слияния внутренней и внешней мембран. [ 4 ] Количество NPC может значительно различаться в зависимости от типа клеток; мелких глиальных клеток насчитывается всего около нескольких сотен, а крупных клеток Пуркинье - около 20 000. [ 2 ] : 650 НПК обеспечивает избирательный транспорт молекул между нуклеоплазмой и цитозолем . [ 5 ] Комплекс ядерных пор состоит примерно из тридцати различных белков, известных как нуклеопорины . [ 2 ] : 649 пор составляет около 60–80 миллионов и дальтон Молекулярная масса состоит из от 50 (у дрожжей ) до нескольких сотен белков (у позвоночных ). [ 3 ] : 622–4 Общий диаметр пор составляет 100 нм; однако ширина щели, через которую молекулы свободно диффундируют, составляет всего около 9 нм из-за присутствия регуляторных систем в центре поры. Этот размер избирательно позволяет проходить небольшим водорастворимым молекулам, предотвращая при этом более крупных молекул, таких как нуклеиновые кислоты несанкционированный вход или выход из ядра и более крупные белки. Вместо этого эти большие молекулы должны активно транспортироваться в ядро. К кольцу прикреплена структура, называемая ядерной корзиной , которая простирается в нуклеоплазму, и ряд нитевидных отростков, доходящих до цитоплазмы. Обе структуры служат посредником связывания с ядерными транспортными белками. [ 6 ] : 509–10
Большинство белков, субъединиц рибосом и некоторые РНК транспортируются через комплексы пор в процессе, опосредованном семейством транспортных факторов, известных как кариоферины . Те кариоферины, которые опосредуют движение в ядро, также называются импортинами, тогда как те, которые опосредуют движение из ядра, называются экспортинами. Большинство кариоферинов взаимодействуют непосредственно со своим грузом, хотя некоторые используют адаптерные белки . [ 7 ] Стероидные гормоны, такие как кортизол и альдостерон , а также другие небольшие жирорастворимые молекулы, участвующие в межклеточной передаче сигналов , могут диффундировать через клеточную мембрану в цитоплазму, где они связывают белки ядерных рецепторов , которые доставляются в ядро. Там они служат факторами транскрипции , когда связаны со своим лигандом ; в отсутствие лиганда многие такие рецепторы функционируют как деацетилазы гистонов , которые подавляют экспрессию генов. [ 6 ] : 488
Ядерная пластинка
В животных клетках две сети промежуточных филаментов обеспечивают ядру механическую поддержку: ядерная пластинка образует организованную сеть на внутренней стороне оболочки, тогда как менее организованная поддержка обеспечивается на цитозольной стороне оболочки. Обе системы обеспечивают структурную поддержку ядерной оболочки и мест закрепления хромосом и ядерных пор. [ 8 ]
Ядерная пластинка состоит в основном из белков -ламинов . Как и все белки, ламины синтезируются в цитоплазме, а затем транспортируются внутрь ядра, где они собираются перед включением в существующую сеть ядерных пластинок. [ 9 ] [ 10 ] Ламины, обнаруженные на цитозольной поверхности мембраны, такие как эмерин и несприн , связываются с цитоскелетом, обеспечивая структурную поддержку. Ламины также обнаруживаются внутри нуклеоплазмы, где они образуют другую регулярную структуру, известную как нуклеоплазматическая завеса . [ 11 ] [ 12 ] это видно с помощью флуоресцентной микроскопии . Фактическая функция завесы не ясна, хотя она исключена из ядрышка и присутствует во время интерфазы . [ 13 ] Структуры ламина, составляющие завесу, такие как LEM3 , связывают хроматин, и нарушение их структуры ингибирует транскрипцию генов, кодирующих белок. [ 14 ]
Как и компоненты других промежуточных нитей, мономер ламина содержит альфа-спиральный домен, используемый двумя мономерами для свертывания друг вокруг друга, образуя димерную структуру, называемую спиральной спиралью . Две из этих димерных структур затем соединяются бок о бок в антипараллельном расположении, образуя тетрамер, называемый протофиламентом . Восемь из этих протофиламентов образуют боковое расположение, которое скручивается, образуя веревкообразную нить . Эти нити можно собирать или разбирать динамически, а это означает, что изменения длины нити зависят от конкурирующих скоростей добавления и удаления нитей. [ 8 ]
Мутации в генах ламинов, приводящие к дефектам сборки филаментов, вызывают группу редких генетических нарушений, известных как ламинопатии . Наиболее заметной ламинопатией является семейство заболеваний, известных как прогерия , которые вызывают преждевременное старение у людей с этим заболеванием. Точный механизм, посредством которого связанные биохимические изменения приводят к старению фенотипа , не совсем понятен. [ 15 ]
Хромосомы
Ядро клетки содержит большую часть генетического материала клетки в виде множества линейных молекул ДНК, организованных в структуры, называемые хромосомами . Каждая человеческая клетка содержит примерно два метра ДНК. [ 6 ] : 405 В течение большей части клеточного цикла они организованы в комплекс ДНК-белок, известный как хроматин , и во время клеточного деления хроматин образует четко определенные хромосомы, знакомые по кариотипу . Вместо этого небольшая часть клеточных генов расположена в митохондриях . [ 6 ] : 438
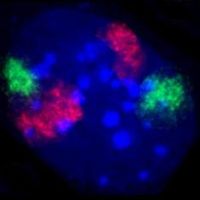
Существует два типа хроматина. Эухроматин является менее компактной формой ДНК и содержит гены, которые часто экспрессируются клеткой. [ 16 ] Другой тип, гетерохроматин , представляет собой более компактную форму и содержит ДНК, которая редко транскрибируется. Эта структура далее подразделяется на факультативный гетерохроматин , состоящий из генов, которые организованы в гетерохроматин только в определенных типах клеток или на определенных стадиях развития, и конститутивный гетерохроматин , который состоит из структурных компонентов хромосом, таких как теломеры и центромеры . [ 17 ] Во время интерфазы хроматин организуется в отдельные отдельные участки. [ 18 ] называемые хромосомными территориями . [ 19 ] Активные гены, которые обычно обнаруживаются в эухроматической области хромосомы, обычно располагаются ближе к границе территории хромосомы. [ 20 ]
Антитела к определенным типам организации хроматина, в частности, нуклеосомам , связаны с рядом аутоиммунных заболеваний , таких как системная красная волчанка . [ 21 ] Они известны как антиядерные антитела (АНА) и также наблюдаются при рассеянном склерозе как часть общей дисфункции иммунной системы. [ 22 ]
Ядрышко

Ядрышко ядерные — самая крупная из дискретных, плотно окрашенных, безмембранных структур, известных как тельца, обнаруженных в ядре. Он образуется вокруг тандемных повторов рДНК , ДНК , кодирующей рибосомальную РНК (рРНК). Эти регионы называются регионами ядрышкового организатора (ЯОР). Основные функции ядрышка — синтез рРНК и сборка рибосом . Структурная сплоченность ядрышка зависит от его активности, поскольку сборка рибосом в ядрышке приводит к временной ассоциации ядрышковых компонентов, облегчая дальнейшую сборку рибосом и, следовательно, дальнейшую ассоциацию. Эта модель подтверждается наблюдениями о том, что инактивация рДНК приводит к смешиванию ядрышковых структур. [ 23 ]
На первом этапе сборки рибосомы белок, называемый РНК-полимеразой I, транскрибирует рДНК, которая образует большой предшественник пре-рРНК. Он расщепляется на две большие субъединицы рРНК — 5,8S и 28S , а также небольшую субъединицу рРНК 18S . [ 2 ] : 328 [ 24 ] Транскрипция, посттранскрипционный процессинг и сборка рРНК происходят в ядрышке при помощи небольших молекул ядрышковой РНК (snoRNA), некоторые из которых происходят из сплайсированных интронов , информационных РНК кодирующих гены, связанные с функцией рибосом. Собранные рибосомальные субъединицы представляют собой самые крупные структуры, прошедшие через ядерные поры . [ 6 ] : 526
При наблюдении под электронным микроскопом можно увидеть, что ядрышко состоит из трех различимых областей: самых внутренних фибриллярных центров (FC), окруженных плотным фибриллярным компонентом (DFC) (который содержит фибрилларин и нуклеолин ), который, в свою очередь, граничит с гранулярный компонент (GC) (содержащий белок нуклеофосмин ). Транскрипция рДНК происходит либо в FC, либо на границе FC-DFC, поэтому при повышении транскрипции рДНК в клетке обнаруживается больше FC. Большая часть расщепления и модификации рРНК происходит в DFC, тогда как последние этапы, включающие сборку белка на субъединицы рибосом, происходят в GC. [ 24 ]
Другие ядерные организации
| Имя структуры | Диаметр конструкции | Ссылка. |
|---|---|---|
| Тела Кахаля | 0,2–2,0 мкм | [ 25 ] |
| Кластосомы | 0,2–0,5 мкм | [ 26 ] |
| ДЛИННЫЙ | 5 мкм | [ 27 ] |
| Органы ПМЛ | 0,2–1,0 мкм | [ 28 ] |
| Параспеклы | 0,5–1,0 мкм | [ 29 ] |
| Пятнышки | 20–25 нм | [ 27 ] |
Помимо ядрышка, ядро содержит ряд других ядерных телец. К ним относятся тельца Кахаля , близнецы тельца Кахаля, полиморфная интерфазная кариосомная ассоциация (PIKA), тельца промиелоцитарного лейкоза (ПМЛ), параспеклы и сплайсинговые крапинки. Хотя о некоторых из этих доменов мало что известно, они важны тем, что показывают, что нуклеоплазма не представляет собой однородную смесь, а скорее содержит организованные функциональные субдомены. [ 28 ]
Другие субъядерные структуры появляются как часть аномальных болезненных процессов. сообщалось о наличии небольших внутриядерных палочек Например, в некоторых случаях немалиновой миопатии . Это состояние обычно возникает в результате мутаций актина , а сами палочки состоят из мутантного актина, а также других белков цитоскелета. [ 30 ]
Тела и драгоценные камни Кахаля

Ядро обычно содержит от одной до десяти компактных структур, называемых тельцами Кахаля или спиральными тельцами (CB), диаметр которых составляет от 0,2 до 2,0 мкм в зависимости от типа и вида клеток. [ 25 ] Если рассматривать их под электронным микроскопом, они напоминают клубки запутанных ниток. [ 27 ] и являются плотными очагами распределения белка коилина . [ 31 ] CB участвуют в ряде различных ролей, связанных с процессингом РНК, в частности, в созревании малых ядрышковых РНК (мяРНК) и малых ядерных РНК (мяРНК), а также модификации мРНК гистонов. [ 25 ]
Подобными телам Кахаля являются тела Близнецов Кахаля, или драгоценные камни, название которых происходит от созвездия Близнецов в связи с их близкими «близнецовыми» отношениями с CB. Драгоценные камни по размеру и форме похожи на CB и практически неотличимы под микроскопом. [ 31 ] В отличие от CB, драгоценные камни не содержат малых ядерных рибонуклеопротеинов (мяРНП), но содержат белок, называемый выживанием двигательных нейронов (SMN), функция которого связана с биогенезом мяРНП. Считается, что драгоценные камни помогают CB в биогенезе мяРНП. [ 32 ] хотя на основе данных микроскопии также было высказано предположение, что ХБ и драгоценные камни представляют собой разные проявления одной и той же структуры. [ 31 ] Более поздние ультраструктурные исследования показали, что драгоценные камни являются близнецами тел Кахаля с разницей в койлиновом компоненте; Тельца Кахаля являются SMN-положительными и коилин-положительными, а драгоценные камни SMN-положительными и коилин-отрицательными. [ 33 ]
Домены PIKA и PTF
Домены PIKA, или полиморфные интерфазные кариосомные ассоциации, были впервые описаны в микроскопических исследованиях в 1991 году. Их функция остается неясной, хотя не считалось, что они связаны с активной репликацией ДНК, транскрипцией или процессингом РНК. [ 34 ] Было обнаружено, что они часто ассоциированы с дискретными доменами, определяемыми плотной локализацией транскрипционного фактора PTF, который способствует транскрипции малых ядерных РНК (мяРНК). [ 35 ]
ПМЛ-ядерные тела
Белок промиелоцитарного лейкоза (PML-ядерные тельца) представляет собой сферические тельца, разбросанные по нуклеоплазме, размером около 0,1–1,0 мкм. Они известны под рядом других названий, включая ядерный домен 10 (ND10), тельца Кремера и онкогенные домены PML. [ 36 ] ПМЛ-ядерные тельца названы в честь одного из их основных компонентов — белка промиелоцитарного лейкоза (ПМЛ). Их часто можно увидеть в ядре в сочетании с тельцами Кахаля и тельцами расщепления. [ 28 ] Мыши Pml-/-, которые не способны создавать PML-ядерные тельца, развиваются нормально без очевидных побочных эффектов, показывая, что PML-ядерные тельца не требуются для большинства важных биологических процессов. [ 37 ]
Сращивание спеклов
Спеклы представляют собой субъядерные структуры, обогащенные факторами сплайсинга премессенджерной РНК и расположенные в интерхроматиновых областях нуклеоплазмы клеток млекопитающих. [ 38 ] На уровне флуоресцентного микроскопа они выглядят как неправильные точечные структуры, которые различаются по размеру и форме, а при исследовании электронной микроскопией они видны как скопления интерхроматиновых гранул . Спеклы представляют собой динамические структуры, и их белковые и РНК-белковые компоненты могут непрерывно перемещаться между спеклами и другими местами ядра, включая активные сайты транскрипции. Спеклы могут работать с р53 как усилители активности генов, напрямую усиливая активность определенных генов. Более того, спекл-ассоциированные и неассоциирующие мишени гена р53 функционально различны. [ 39 ]
Исследования состава, структуры и поведения спеклов предоставили модель для понимания функциональной компартментализации ядра и организации механизма экспрессии генов. [ 40 ] сплайсинг snRNP [ 41 ] [ 42 ] и другие белки сплайсинга, необходимые для процессинга пре-мРНК. [ 40 ] Из-за меняющихся потребностей клетки состав и расположение этих телец изменяются в зависимости от транскрипции и регуляции мРНК посредством фосфорилирования специфических белков. [ 43 ] Сплайсинговые спеклы также известны как ядерные спеклы (ядерные спеклы), отсеки фактора сплайсинга (SF-отделения), кластеры интерхроматиновых гранул (IGC) и B-снурпосомы . [ 44 ] B-снурпосомы обнаружены в ядрах ооцитов амфибий и эмбрионах Drosophila melanogaster . На электронных микрофотографиях ядер амфибий B-снурпосомы появляются отдельно или прикреплены к тельцам Кахаля. [ 45 ] IGCs функционируют как места хранения факторов сплайсинга. [ 46 ]
Параспеклы
Обнаружено Фоксом и др. в 2002 г. параспеклы представляют собой отсеки неправильной формы в межхроматиновом пространстве ядра. [ 47 ] Впервые зарегистрировано в клетках HeLa, где обычно их насчитывается 10–30 на ядро. [ 48 ] Теперь известно, что параспеклы также существуют во всех первичных клетках человека, трансформированных клеточных линиях и срезах тканей. [ 49 ] Их название происходит от их распределения в ядре; «пара» — это сокращение от «параллель», а «пятнышки» относятся к точкам сращивания, с которыми они всегда находятся в непосредственной близости. [ 48 ]
Параспеклы изолируют ядерные белки и РНК и, таким образом, действуют как молекулярная губка. [ 50 ] который участвует в регуляции экспрессии генов. [ 51 ] Более того, параспеклы представляют собой динамические структуры, которые изменяются в ответ на изменения метаболической активности клеток. Они зависят от транскрипции [ 47 ] а в отсутствие транскрипции РНК Pol II параспекл исчезает, и все связанные с ним белковые компоненты (PSP1, p54nrb, PSP2, CFI(m)68 и PSF) образуют перинуклеолярный колпачок серповидной формы в ядрышке. Это явление проявляется во время клеточного цикла. В клеточном цикле параспеклы присутствуют во время интерфазы и на протяжении всего митоза, за исключением телофазы . отсутствует, РНК Pol II Во время телофазы, когда формируются два дочерних ядра, транскрипция поэтому вместо этого белковые компоненты образуют перинуклеолярный колпачок. [ 49 ]
Перихроматиновые фибриллы
Фибриллы перихроматина видны только под электронным микроскопом. Они расположены рядом с транскрипционно активным хроматином и предположительно являются сайтами активного процессинга пре-мРНК . [ 46 ]
Кластосомы
Кластосомы представляют собой небольшие ядерные тельца (0,2–0,5 мкм), имеющие форму толстого кольца из-за периферической капсулы вокруг этих телец. [ 26 ] Это имя происходит от греческих слов klastos — сломанный и soma — тело. [ 26 ] Кластосомы обычно не присутствуют в нормальных клетках, поэтому их трудно обнаружить. Они образуются в условиях высокого протеолитического уровня внутри ядра и разрушаются при снижении активности или при обработке клеток ингибиторами протеасом . [ 26 ] [ 52 ] Недостаток кластосом в клетках указывает на то, что они не необходимы для протеасом . функции [ 53 ] Также было показано, что осмотический стресс вызывает образование кластосом. [ 54 ] Эти ядерные тельца содержат каталитические и регуляторные субъединицы протеасомы и ее субстратов, что указывает на то, что кластосомы являются местами деградации белков. [ 53 ]
Функция
Ядро обеспечивает место для генетической транскрипции , отделенное от места трансляции в цитоплазме, обеспечивая уровни регуляции генов , недоступные прокариотам . Основная функция клеточного ядра — контроль экспрессии генов и опосредование репликации ДНК во время клеточного цикла. [ 6 ] : 171
Разделение клеток
Ядерная оболочка позволяет контролировать содержимое ядра и при необходимости отделяет его от остальной цитоплазмы. Это важно для контроля процессов по обе стороны ядерной мембраны: в большинстве случаев, когда цитоплазматический процесс необходимо ограничить, ключевой участник удаляется в ядро, где он взаимодействует с факторами транскрипции, подавляя выработку определенных ферментов в ядре. путь. Этот регуляторный механизм возникает в случае гликолиза — клеточного пути расщепления глюкозы для производства энергии. Гексокиназа — фермент, ответственный за первый этап гликолиза, образующий глюкозо-6-фосфат из глюкозы. При высоких концентрациях фруктозо-6-фосфата , молекулы, образующейся позже из глюкозо-6-фосфата, белок-регулятор удаляет гексокиназу в ядро, [ 55 ] где он образует комплекс репрессора транскрипции с ядерными белками для снижения экспрессии генов, участвующих в гликолизе. [ 56 ]
Чтобы контролировать, какие гены транскрибируются, клетка отделяет некоторые белки-факторы транскрипции, ответственные за регуляцию экспрессии генов, от физического доступа к ДНК до тех пор, пока они не будут активированы другими сигнальными путями. Это предотвращает даже низкие уровни нежелательной экспрессии генов. Например, в случае генов, контролируемых NF-κB , которые участвуют в большинстве воспалительных реакций, транскрипция индуцируется в ответ на сигнальный путь , например, инициируемый сигнальной молекулой TNF-α , связывающейся с рецептором клеточной мембраны, что приводит к рекрутированию сигнальных белков и, в конечном итоге, к активации транскрипционного фактора NF-κB. Сигнал ядерной локализации белка NF-κB позволяет ему транспортироваться через ядерную пору в ядро, где он стимулирует транскрипцию генов-мишеней. [ 8 ]
Компартментализация позволяет клетке предотвращать трансляцию несплайсированной мРНК. [ 57 ] Эукариотическая мРНК содержит интроны, которые необходимо удалить перед трансляцией для получения функциональных белков. Сплайсинг осуществляется внутри ядра до того, как рибосомы смогут получить доступ к мРНК для трансляции. Без ядра рибосомы будут транслировать вновь транскрибируемую (необработанную) мРНК, что приведет к образованию деформированных и нефункциональных белков. [ 6 ] : 108–15
Репликация
Основная функция клеточного ядра — контроль экспрессии генов и опосредование репликации ДНК во время клеточного цикла. [ 6 ] : 171 Было обнаружено, что репликация происходит локализованно в ядре клетки. В S-фазе интерфазы клеточного цикла; происходит репликация. Вопреки традиционному представлению о движении репликационных вилок вдоль застойной ДНК, возникла концепция репликационных фабрик , которая означает, что репликационные вилки концентрируются в некоторых иммобилизованных «фабричных» регионах, через которые нити матричной ДНК проходят, как конвейерные ленты. [ 58 ]
Экспрессия генов

Экспрессия генов сначала включает транскрипцию, при которой ДНК используется в качестве матрицы для производства РНК. В случае генов, кодирующих белки, РНК, образующаяся в результате этого процесса, представляет собой информационную РНК (мРНК), которую затем необходимо транслировать рибосомами для образования белка. Поскольку рибосомы расположены вне ядра, вырабатываемую мРНК необходимо экспортировать. [ 59 ]
Поскольку ядро является местом транскрипции, оно также содержит множество белков, которые либо непосредственно опосредуют транскрипцию, либо участвуют в регуляции этого процесса. К этим белкам относятся геликазы , которые раскручивают двухцепочечную молекулу ДНК, чтобы облегчить доступ к ней, РНК-полимеразы , которые связываются с промотором ДНК для синтеза растущей молекулы РНК, топоизомеразы , которые изменяют степень сверхспирализации ДНК, помогая ей скручиваться и раскручивать, а также большое разнообразие факторов транскрипции, которые регулируют экспрессию. [ 60 ]
Процессинг пре-мРНК
Вновь синтезированные молекулы мРНК известны как первичные транскрипты или пре-мРНК. Прежде чем экспортировать в цитоплазму, они должны подвергнуться посттранскрипционной модификации в ядре; мРНК, которая появляется в цитоплазме без этих модификаций, скорее деградирует, чем используется для трансляции белка. Тремя основными модификациями являются 5'-кэпирование , 3'- полиаденилирование и сплайсинг РНК . Находясь в ядре, пре-мРНК связана с различными белками в комплексах, известных как гетерогенные рибонуклеопротеиновые частицы (hnRNP). Добавление 5'-кэпа происходит котранскрипционно и является первым шагом посттранскрипционной модификации. 3'-полиадениновый хвост добавляется только после завершения транскрипции. [ 6 ] : 509–18
Сплайсинг РНК, осуществляемый комплексом, называемым сплайсосомой , представляет собой процесс, посредством которого интроны или участки ДНК, не кодирующие белок, удаляются из пре-мРНК, а оставшиеся экзоны соединяются, образуя одну непрерывную молекулу. . Этот процесс обычно происходит после 5'-кэпирования и 3'-полиаденилирования, но может начаться до завершения синтеза в транскриптах со многими экзонами. [ 6 ] : 494 Многие пре-мРНК можно сплайсировать разными способами с образованием разных зрелых мРНК, которые кодируют разные белковые последовательности . Этот процесс известен как альтернативный сплайсинг и позволяет производить большое количество белков из ограниченного количества ДНК. [ 61 ]
Динамика и регулирование
Ядерный транспорт

Вход и выход крупных молекул из ядра жестко контролируется комплексами ядерных пор. Хотя небольшие молекулы могут проникать в ядро без регулирования, [ 62 ] макромолекулам, таким как РНК и белки, требуется ассоциация кариоферинов, называемых импортинами, для входа в ядро и экспортинов для выхода. «Грузовые» белки, которые должны быть транслоцированы из цитоплазмы в ядро, содержат короткие аминокислотные последовательности, известные как сигналы ядерной локализации , которые связываются импортинами, в то время как те, которые транспортируются из ядра в цитоплазму, несут сигналы ядерного экспорта, связанные экспортинами. Способность импортинов и экспортинов транспортировать свой груз регулируется ГТФазами , ферментами, которые гидролизуют молекулу гуанозинтрифосфата (ГТФ) с высвобождением энергии. Ключевой ГТФазой ядерного транспорта является Ran , которая связана либо с ГТФ, либо с ВВП (гуанозиндифосфатом), в зависимости от того, находится ли она в ядре или цитоплазме. В то время как импортины зависят от RanGTP для отделения от своего груза, экспортинам требуется RanGTP для связывания со своим грузом. [ 7 ]
Ядерный импорт зависит от импортина, связывающего свой груз в цитоплазме и переносящего его через ядерную пору в ядро. Внутри ядра RanGTP отделяет груз от импортина, позволяя импортину покинуть ядро и повторно использовать. Ядерный экспорт аналогичен, поскольку экспортин связывает груз внутри ядра в процессе, которому способствует RanGTP, выходит через ядерную пору и отделяется от своего груза в цитоплазме. [ 63 ]
Существуют специализированные экспортные белки для транслокации зрелых мРНК и тРНК в цитоплазму после завершения посттранскрипционной модификации. Этот механизм контроля качества важен из-за центральной роли этих молекул в трансляции белков. Неправильная экспрессия белка из-за неполного удаления экзонов или неправильного включения аминокислот может иметь негативные последствия для клетки; таким образом, не полностью модифицированная РНК, достигающая цитоплазмы, скорее деградирует, чем используется в трансляции. [ 6 ]
Сборка и разборка

В течение своей жизни ядро может расщепляться или разрушаться либо в процессе деления клетки , либо вследствие апоптоза (процесса запрограммированной гибели клетки ). Во время этих событий структурные компоненты ядра — оболочка и пластинка — могут систематически разрушаться. В большинстве клеток разборка ядерной оболочки знаменует конец профазы митоза . Однако такая разборка ядра не является универсальной особенностью митоза и происходит не во всех клетках. Некоторые одноклеточные эукариоты (например, дрожжи) подвергаются так называемому закрытому митозу , при котором ядерная оболочка остается неповрежденной. При закрытом митозе дочерние хромосомы мигрируют к противоположным полюсам ядра, которое затем делится надвое. Однако клетки высших эукариот обычно подвергаются открытому митозу , который характеризуется разрушением ядерной оболочки. Затем дочерние хромосомы мигрируют к противоположным полюсам митотического веретена, и вокруг них снова собираются новые ядра. [ 6 ] : 854
В определенный момент клеточного цикла при открытом митозе клетка делится с образованием двух клеток. Чтобы этот процесс стал возможным, каждая из новых дочерних клеток должна иметь полный набор генов, а этот процесс требует репликации хромосом, а также разделения отдельных наборов. Это происходит посредством реплицированных хромосом, сестринских хроматид , прикрепляющихся к микротрубочкам , которые, в свою очередь, прикрепляются к различным центросомам . Затем сестринские хроматиды можно переместить в отдельные места клетки. Во многих клетках центросома расположена в цитоплазме, вне ядра; микротрубочки не смогут прикрепляться к хроматидам при наличии ядерной оболочки. [ 64 ] Следовательно, на ранних стадиях клеточного цикла, начиная с профазы и заканчивая прометафазой , ядерная мембрана демонтируется. [ 11 ] Аналогично, в тот же период ядерная пластинка также разбирается, и этот процесс регулируется фосфорилированием ламинов с помощью протеинкиназ, таких как протеинкиназа CDC2 . [ 65 ] К концу клеточного цикла ядерная мембрана реформируется, и примерно в то же время ядерная пластинка собирается заново за счет дефосфорилирования ламинов. [ 65 ]
Однако у динофлагеллят ядерная оболочка остается интактной, центросомы располагаются в цитоплазме, а микротрубочки контактируют с хромосомами, центромерные участки которых включены в ядерную оболочку (так называемый закрытый митоз с внеядерным веретеном). У многих других простейших (например, инфузорий , споровиков ) и грибов центросомы внутриядерные, и их ядерная оболочка также не разбирается при делении клеток. [ 66 ]
Апоптоз — это контролируемый процесс, при котором структурные компоненты клетки разрушаются, что приводит к гибели клетки. Изменения, связанные с апоптозом, непосредственно затрагивают ядро и его содержимое, например, при конденсации хроматина и распаде ядерной оболочки и пластинки. Разрушение сетей ламинов контролируется специализированными апоптотическими протеазами , называемыми каспазами , которые расщепляют белки ламинов и, таким образом, нарушают структурную целостность ядра. Расщепление ламина иногда используется в качестве лабораторного индикатора активности каспаз в анализах ранней апоптотической активности. [ 11 ] Клетки, которые экспрессируют мутантные каспазо-резистентные ламины, лишены ядерных изменений, связанных с апоптозом, что позволяет предположить, что ламины играют роль в инициировании событий, которые приводят к апоптотической деградации ядра. [ 11 ] Ингибирование сборки ламина само по себе является индуктором апоптоза. [ 67 ]
Ядерная оболочка действует как барьер, который предотвращает проникновение в ядро как ДНК, так и РНК-вирусов. Некоторым вирусам требуется доступ к белкам внутри ядра для репликации и/или сборки. ДНК-вирусы, такие как вирус герпеса, реплицируются и собираются в ядре клетки и выходят путем отпочкования через внутреннюю ядерную мембрану. Этот процесс сопровождается разборкой пластинки на ядерной стороне внутренней мембраны. [ 11 ]
Динамика заболеваемости
Первоначально предполагалось, что иммуноглобулины вообще и аутоантитела в частности не проникают в ядро. Сейчас имеется масса доказательств того, что при патологических состояниях (например, красной волчанке ) IgG могут проникать в ядро. [ 68 ]
Ядер на клетку
Большинство типов эукариотических клеток обычно имеют одно ядро, но у некоторых ядер нет, а у других их несколько. Это может быть результатом нормального развития, например, созревания эритроцитов млекопитающих , или неправильного деления клеток. [ 69 ]
Безъядерные клетки

Безъядерная клетка не содержит ядра и, следовательно, неспособна делиться с образованием дочерних клеток. Самая известная безъядерная клетка — это эритроцит или эритроцит млекопитающих , в котором также отсутствуют другие органеллы, такие как митохондрии, и который служит главным образом транспортным сосудом для транспортировки кислорода из легких в ткани организма. Эритроциты созревают посредством эритропоэза в костном мозге , где они теряют свои ядра, органеллы и рибосомы. Ядро выбрасывается в процессе дифференцировки эритробласта в ретикулоцит , который является непосредственным предшественником зрелого эритроцита. [ 70 ] Присутствие мутагенов может вызвать выброс некоторых незрелых «микроядерных» эритроцитов в кровоток. [ 71 ] [ 72 ] Безъядерные клетки также могут возникать в результате неправильного клеточного деления, при котором у одной дочерней клетки отсутствует ядро, а у другой — два ядра.
У цветковых растений это состояние возникает в элементах ситовидных трубок . [ 73 ]
Многоядерные клетки
Многоядерные клетки содержат несколько ядер. Большинство акантарейных видов простейших [ 74 ] и некоторые грибы в микоризе [ 75 ] имеют естественные многоядерные клетки. Другие примеры включают кишечных паразитов рода Giardia , которые имеют два ядра на клетку. [ 76 ] Инфузории имеют два типа ядер в одной клетке: соматический макронуклеус и зародышевый микронуклеус . [ 77 ] У человека клетки скелетных мышц , также называемые миоцитами и синцитиями , в процессе развития становятся многоядерными; В результате расположение ядер вблизи периферии клеток обеспечивает максимальное внутриклеточное пространство для миофибрилл . [ 6 ] Другие многоядерные клетки человека представляют собой остеокласты ( тип костных клеток) . Многоядерные и двуядерные клетки также могут быть аномальными у человека; например, клетки, возникающие в результате слияния моноцитов и макрофагов , известные как гигантские многоядерные клетки , иногда сопровождают воспаление [ 78 ] а также участвуют в образовании опухолей. [ 79 ]
ряда динофлагеллят Известно, что у имеется два ядра. В отличие от других многоядерных клеток, эти ядра содержат две различные линии ДНК: одну от динофлагеллят, а другую от симбиотических диатомовых водорослей . [ 80 ]
Эволюция
происхождение ядра, являющегося основной определяющей характеристикой эукариотической клетки, Эволюционное было предметом многочисленных спекуляций. Для объяснения существования ядра были предложены четыре основные гипотезы, хотя ни одна из них еще не получила широкой поддержки. [ 81 ] [ 82 ] [ 83 ]
Первая модель, известная как «синтрофная модель», предполагает, что симбиотические отношения между архей и бактериями привели к созданию эукариотической клетки, содержащей ядро. (Организмы домена Archaea и Bacteria не имеют клеточного ядра. [ 84 ] ) Предполагается, что симбиоз возник, когда древние археи, похожие на современные метаногенные археи, вторглись и жили внутри бактерий, подобных современным миксобактериям , в конечном итоге образуя раннее ядро. Эта теория аналогична принятой теории происхождения эукариотических митохондрий и хлоропластов , которые, как полагают, развились в результате аналогичных эндосимбиотических отношений между протоэукариотами и аэробными бактериями. [ 85 ] Одна из возможностей состоит в том, что ядерная мембрана возникла как новая мембранная система после возникновения митохондрий у архебактериального хозяина. [ 86 ] Ядерная мембрана, возможно, служила для защиты генома от повреждения активных форм кислорода, вырабатываемых протомитохондриями. [ 87 ] Архейное происхождение ядра подтверждается наблюдениями о том, что архей и эукариев имеют сходные гены для определенных белков, включая гистоны . Наблюдения за тем, что миксобактерии подвижны, могут образовывать многоклеточные комплексы и обладают киназами и G-белками, подобными эукариотическим, подтверждают бактериальное происхождение эукариотической клетки. [ 88 ]
Вторая модель предполагает, что протоэукариотические клетки произошли от бактерий без эндосимбиотической стадии. Эта модель основана на существовании современных бактерий Planctomycetota , которые обладают ядерной структурой с примитивными порами и другими разделенными мембранными структурами. [ 89 ] В аналогичном предположении говорится, что эукариоподобная клетка, хроноцит , развилась первой и фагоцитировала архей и бактерии, образуя ядро и эукариотическую клетку. [ 90 ]
Самая противоречивая модель, известная как вирусный эукариогенез , утверждает, что мембраносвязанное ядро, наряду с другими особенностями эукариот, возникло в результате заражения прокариот вирусом. Предположение основано на сходстве между эукариотами и вирусами, таком как линейные цепи ДНК, кэпирование мРНК и прочное связывание с белками (аналог гистонов вирусным оболочкам ). Одна из версий предположения предполагает, что ядро эволюционировало совместно с фагоцитозом, образуя раннего клеточного « хищника ». [ 91 ] Другой вариант предполагает, что эукариоты произошли от ранних архей, зараженных поксвирусами , на основании наблюдаемого сходства между ДНК-полимеразами современных поксвирусов и эукариот. [ 92 ] [ 93 ] Было высказано предположение, что нерешенный вопрос об эволюции пола может быть связан с гипотезой вирусного эукариогенеза. [ 94 ]
Более недавнее предложение, экзомембранная гипотеза , предполагает, что ядро возникло из единственной предковой клетки, у которой развилась вторая внешняя клеточная мембрана; внутренняя мембрана, окружающая исходную клетку, затем стала ядерной мембраной и развила все более сложные пористые структуры для прохождения внутренне синтезируемых клеточных компонентов, таких как рибосомальные субъединицы. [ 95 ]
История


Ядро было первой открытой органеллой. Самый старый из сохранившихся рисунков, скорее всего, принадлежит раннему микроскописту Антони ван Левенгуку (1632–1723). Он наблюдал «просвет», ядро, в эритроцитах лосося . [ 96 ] В отличие от эритроцитов млекопитающих, эритроциты других позвоночных все еще содержат ядра. [ 97 ]
Ядро было также описано Францем Бауэром в 1804 году. [ 98 ] и более подробно в 1831 году шотландским ботаником Робертом Брауном в докладе в Линнеевском обществе в Лондоне . Браун изучал орхидеи под микроскопом, когда заметил непрозрачную область, которую он назвал «ареолой» или «ядром», в клетках внешнего слоя цветка. [ 99 ] Он не предложил потенциальную функцию.
В 1838 году Маттиас Шлейден предположил, что ядро играет роль в образовании клеток, поэтому он ввел название « цитобласт » («строитель клеток»). Он считал, что наблюдал новые клетки, собирающиеся вокруг «цитобластов». Франц Мейен был ярым противником этой точки зрения, уже описав клетки, размножающиеся путем деления, и полагая, что многие клетки не будут иметь ядер. Идея о том, что клетки могут генерироваться de novo, с помощью «цитобластов» или иным образом, противоречила работам Роберта Ремака (1852) и Рудольфа Вирхова (1855), которые решительно пропагандировали новую парадигму, согласно которой клетки генерируются исключительно клетками (« Omnis cellula e целлюла »). Функция ядра оставалась неясной. [ 100 ]
Между 1877 и 1878 годами Оскар Гертвиг опубликовал несколько исследований об оплодотворении яиц морских ежей , показав, что ядро спермия проникает в яйцеклетку и сливается с ее ядром. Впервые было высказано предположение, что человек развивается из (одной) ядросодержащей клетки. Это противоречило теории Эрнста Геккеля о том, что полная филогения вида будет повторяться во время эмбрионального развития, включая образование первой ядросодержащей клетки из «монерулы», бесструктурной массы первичной протоплазмы (« Уршлейм »). Поэтому необходимость ядра спермия для оплодотворения обсуждалась довольно давно. Однако Гертвиг подтвердил свои наблюдения на других группах животных, включая земноводных и моллюсков . Эдуард Страсбургер получил те же результаты для растений в 1884 году. Это открыло возможность приписать ядру важную роль в наследственности. В 1873 году Август Вейсман постулировал эквивалентность материнских и отцовских половых клеток по наследственности. Функция ядра как носителя генетической информации стала ясна лишь позднее, после открытия митоза и открытия Менделевские правила были заново открыты в начале 20 века; поэтому была разработана хромосомная теория наследственности . [ 100 ]
См. также
Ссылки
- ^ Куме К., Кантвелл Х., Нойманн Ф.Р., Джонс А.В., Снейдерс А.П., Медсестра П. (май 2017 г.). «Систематический геномный скрининг предполагает ядерно-цитоплазматический транспорт и рост мембран в контроле размера ядра» . ПЛОС Генет . 13 (5): e1006767. дои : 10.1371/journal.pgen.1006767 . ПМЦ 5436639 . ПМИД 28545058 .
- ^ Jump up to: а б с д и ж г час я дж к Альбертс Б., Джонсон А., Льюис Дж., Морган Д., Рафф М., Робертс К., Уолтер П. (2015). Молекулярная биология клетки (6-е изд.). Нью-Йорк: Garland Science.
- ^ Jump up to: а б с Лодиш Х.Ф., Берк А., Кайзер С., Кригер М., Бретчер А., Плох Х. и др. (2016). Молекулярно-клеточная биология (Восьмое изд.). Нью-Йорк: WH Freeman. ISBN 978-1-4641-8339-3 .
- ^ Шульга Н., Мосаммапараст Н., Возняк Р., Гольдфарб Д.С. (май 2000 г.). «Дрожжевые нуклеопорины, участвующие в пассивной проницаемости ядерной оболочки» . Начальный. Журнал клеточной биологии . 149 (5): 1027–38. дои : 10.1083/jcb.149.5.1027 . ПМК 2174828 . ПМИД 10831607 .
- ^ Альбертс, Брюс (2019). Основная клеточная биология (Пятое изд.). Нью-Йорк. п. 242. ИСБН 9780393680393 .
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) - ^ Jump up to: а б с д и ж г час я дж к л м Лодиш Х., Берк А., Мацудайра П., Кайзер К.А., Кригер М., Скотт М.П., Зипурски С.Л., Дарнелл Дж. (2004). Молекулярно-клеточная биология (5-е изд.). Нью-Йорк: WH Freeman. ISBN 978-0-7167-2672-2 .
- ^ Jump up to: а б Пембертон Л.Ф., Паскаль Б.М. (март 2005 г.). «Механизмы рецептор-опосредованного ядерного импорта и ядерного экспорта» . Обзор. Трафик . 6 (3): 187–98. дои : 10.1111/j.1600-0854.2005.00270.x . ПМИД 15702987 . S2CID 172279 .
- ^ Jump up to: а б с Альбертс Б., Джонсон А., Льюис Дж., Рафф М., Робертс К., Уолтер П., ред. (2002). «Глава 4: ДНК и хромосомы». Молекулярная биология клетки (4-е изд.). Нью-Йорк: Garland Science. стр. 191–234. ISBN 978-0-8153-4072-0 .
- ^ Стурман Н., Хайнс С., Эби У. (1998). «Ядерные ламины: их структура, сборка и взаимодействие». Обзор. Журнал структурной биологии . 122 (1–2): 42–66. дои : 10.1006/jsbi.1998.3987 . ПМИД 9724605 .
- ^ Голдман А.Е., Мойр Р.Д., Монтаг-Лоуи М., Стюарт М., Голдман Р.Д. (ноябрь 1992 г.). «Путь включения микроинъецированного ламина А в ядерную оболочку» . Начальный. Журнал клеточной биологии . 119 (4): 725–35. дои : 10.1083/jcb.119.4.725 . ПМК 2289687 . ПМИД 1429833 .
- ^ Jump up to: а б с д и Гольдман Р.Д., Грюнбаум Ю., Мойр Р.Д., Шумейкер Д.К., Спанн Т.П. (март 2002 г.). «Ядерные ламины: строительные блоки ядерной архитектуры» . Обзор. Гены и развитие . 16 (5): 533–47. дои : 10.1101/gad.960502 . ПМИД 11877373 .
- ^ Броерс Дж.Л., Рамаекерс (2004). «Динамика сборки и разборки ядерной пластинки» . Обзор. Симпозиумы Общества экспериментальной биологии (56): 177–92. ISBN 9781134279838 . ПМИД 15565881 .
- ^ Мойр Р.Д., Юн М., Хуон С., Голдман Р.Д. (декабрь 2000 г.). «Ядерные ламины A и B1: разные пути сборки при формировании ядерной оболочки в живых клетках» . Начальный. Журнал клеточной биологии . 151 (6): 1155–68. дои : 10.1083/jcb.151.6.1155 . ПМК 2190592 . ПМИД 11121432 .
- ^ Спанн Т.П., Голдман А.Е., Ван С., Хуанг С., Голдман Р.Д. (февраль 2002 г.). «Изменение организации ядерного ламина ингибирует транскрипцию, зависимую от РНК-полимеразы II» . Начальный. Журнал клеточной биологии . 156 (4): 603–8. дои : 10.1083/jcb.200112047 . ПМК 2174089 . ПМИД 11854306 .
- ^ Мункес LC, Стюарт CL (июнь 2004 г.). «Старение и ядерная организация: ламины и прогерия» . Обзор. Современное мнение в области клеточной биологии . 16 (3): 322–7. дои : 10.1016/j.ceb.2004.03.009 . ПМИД 15145358 .
- ^ Эренхофер-Мюррей А.Е. (июнь 2004 г.). «Динамика хроматина при репликации, транскрипции и репарации ДНК» . Обзор. Европейский журнал биохимии . 271 (12): 2335–49. дои : 10.1111/j.1432-1033.2004.04162.x . ПМИД 15182349 .
- ^ Григорьев С.А., Булынко Ю.А., Попова Е.Ю. (2006). «Цель корректирует средства: ремоделирование гетерохроматина во время терминальной дифференцировки клеток». Обзор. Хромосомные исследования . 14 (1): 53–69. дои : 10.1007/s10577-005-1021-6 . ПМИД 16506096 . S2CID 6040822 .
- ^ Шардин М., Кремер Т., Хагер Х.Д., Ланг М. (декабрь 1985 г.). «Специфическое окрашивание хромосом человека в гибридных клеточных линиях китайского хомячка и человека демонстрирует территории интерфазных хромосом» (PDF) . Начальный. Генетика человека . 71 (4): 281–7. дои : 10.1007/BF00388452 . ПМИД 2416668 . S2CID 9261461 .
- ^ Ламонд А.И., Эрншоу WC (апрель 1998 г.). «Структура и функции ядра» (PDF) . Обзор. Наука . 280 (5363): 547–53. CiteSeerX 10.1.1.323.5543 . дои : 10.1126/science.280.5363.547 . ПМИД 9554838 .
- ^ Курц А., Лампель С., Николенко Дж.Е., Брэдл Дж., Беннер А., Зирбель Р.М. и др. (декабрь 1996 г.). «Активные и неактивные гены локализуются преимущественно на периферии хромосомных территорий» . Начальный. Журнал клеточной биологии . 135 (5): 1195–205. дои : 10.1083/jcb.135.5.1195 . ПМК 2121085 . ПМИД 8947544 . Архивировано из оригинала 29 сентября 2007 года.
- ^ Ротфилд Н.Ф., Столлар Б.Д. (ноябрь 1967 г.). «Связь класса иммуноглобулинов, структуры антиядерных антител и антител, связывающих комплемент, с ДНК в сыворотке крови пациентов с системной красной волчанкой» . Начальный. Журнал клинических исследований . 46 (11): 1785–94. дои : 10.1172/JCI105669 . ПМЦ 292929 . ПМИД 4168731 .
- ^ Барнед С., Гудман А.Д., Мэттсон Д.Х. (февраль 1995 г.). «Частота антиядерных антител при рассеянном склерозе». Начальный. Неврология . 45 (2): 384–5. дои : 10.1212/WNL.45.2.384 . ПМИД 7854544 . S2CID 30482028 .
- ^ Эрнандес-Верден Д. (январь 2006 г.). «Ядрышко: от структуры к динамике» . Обзор. Гистохимия и клеточная биология . 125 (1–2): 127–37. дои : 10.1007/s00418-005-0046-4 . ПМИД 16328431 . S2CID 20769260 .
- ^ Jump up to: а б Ламонд А.И., Слиман Дж.Э. (октябрь 2003 г.). «Ядерная субструктура и динамика» . Обзор. Современная биология . 13 (21): Р825-8. Бибкод : 2003CBio...13.R825L . дои : 10.1016/j.cub.2003.10.012 . ПМИД 14588256 . S2CID 16865665 .
- ^ Jump up to: а б с Чиосе М., Ламонд А.И. (2005). «Тела Кахаля: долгая история открытия». Обзор. Ежегодный обзор клеточной биологии и биологии развития . 21 : 105–31. doi : 10.1146/annurev.cellbio.20.010403.103738 . ПМИД 16212489 . S2CID 8807316 .
- ^ Jump up to: а б с д Лафарга М., Берчиано М.Т., Пенья Э., Майо И., Кастаньо Дж.Г., Боманн Д. и др. (август 2002 г.). «Кластосома: подтип ядерного тельца, обогащенный 19S и 20S протеасомами, убиквитином и белковыми субстратами протеасомы» . Начальный. Молекулярная биология клетки . 13 (8): 2771–82. CiteSeerX 10.1.1.321.6138 . дои : 10.1091/mbc.e02-03-0122 . ПМК 117941 . ПМИД 12181345 .
- ^ Jump up to: а б с Поллард Т.Д., Эрншоу У.К. (2004). Клеточная биология . Филадельфия: Сондерс. ISBN 978-0-7216-3360-2 .
- ^ Jump up to: а б с Дундр М., Мистели Т. (июнь 2001 г.). «Функциональная архитектура клеточного ядра» . Обзор. Биохимический журнал . 356 (Часть 2): 297–310. дои : 10.1042/0264-6021:3560297 . ПМЦ 1221839 . ПМИД 11368755 .
- ^ Bond CS, Fox AH (сентябрь 2009 г.). «Параспеклы: ядерные тельца, построенные на длинной некодирующей РНК» . Обзор. Журнал клеточной биологии . 186 (5): 637–44. дои : 10.1083/jcb.200906113 . ПМЦ 2742191 . ПМИД 19720872 .
- ^ Goebel HH, Варло I (январь 1997 г.). «Немалиновая миопатия с внутриядерными стержнями - внутриядерная стержневая миопатия». Обзор. Нервно-мышечные расстройства . 7 (1): 13–9. дои : 10.1016/S0960-8966(96)00404-X . ПМИД 9132135 . S2CID 29584217 .
- ^ Jump up to: а б с Матера А.Г., Фрей М.Р. (август 1998 г.). «Свернутые тела и драгоценные камни: Янус или Близнецы?» . Обзор. Американский журнал генетики человека . 63 (2): 317–21. дои : 10.1086/301992 . ПМЦ 1377332 . ПМИД 9683623 .
- ^ Матера АГ (август 1998 г.). «Из свернутых тел, драгоценных камней и лосося». Обзор. Журнал клеточной биохимии . 70 (2): 181–92. doi : 10.1002/(sici)1097-4644(19980801)70:2<181::aid-jcb4>3.0.co;2-k . ПМИД 9671224 . S2CID 44941483 .
- ^ Сондерс В.С., Кук Калифорния, Эрншоу В.К. (ноябрь 1991 г.). «Компартментализация внутри ядра: открытие новой субъядерной области» . Начальный. Журнал клеточной биологии . 115 (4): 919–31. дои : 10.1083/jcb.115.4.919 . ПМК 2289954 . ПМИД 1955462 .
- ^ Помбо А., Куэлло П., Шул В., Юн Дж.Б., Родер Р.Г., Кук П.Р., Мерфи С. (март 1998 г.). «Региональная и временная специализация ядра: транскрипционно-активный ядерный домен, богатый антигенами PTF, Oct1 и PIKA, ассоциируется со специфическими хромосомами на ранних стадиях клеточного цикла» . Начальный. Журнал ЭМБО . 17 (6): 1768–78. дои : 10.1093/emboj/17.6.1768 . ПМЦ 1170524 . ПМИД 9501098 .
- ^ Зимбер А., Нгуен КД, Геспач К. (октябрь 2004 г.). «Ядерные тела и компартменты: функциональные роли и клеточная передача сигналов в здоровье и болезни». Обзор. Сотовая сигнализация . 16 (10): 1085–104. doi : 10.1016/j.cellsig.2004.03.020 . ПМИД 15240004 .
- ^ Лаллеман-Брайтенбах В., де Те Х (май 2010 г.). «Ядерные тела ПМЛ» . Обзор. Перспективы Колд-Спринг-Харбор в биологии . 2 (5): а000661. doi : 10.1101/cshperspect.a000661 . ПМЦ 2857171 . ПМИД 20452955 .
- ^ Спектор Д.Л., Ламонд А.И. (февраль 2011 г.). «Ядерные спеклы» . Обзор. Перспективы Колд-Спринг-Харбор в биологии . 3 (2): а000646. doi : 10.1101/cshperspect.a000646 . ПМК 3039535 . ПМИД 20926517 .
- ^ Александр К.А., Коте А., Нгуен СК, Чжан Л., Бергер С.Л. (март 2021 г.). «p53 опосредует ассоциацию целевого гена с ядерными спеклами для усиленной экспрессии РНК» . Начальный. Молекулярная клетка . 81 (8): С1097-2765(21)00174-Х. doi : 10.1016/j.molcel.2021.03.006 . ПМЦ 8830378 . ПМИД 33823140 . S2CID 233172170 .
- ^ Jump up to: а б Ламонд А.И., Спектор Д.Л. (август 2003 г.). «Ядерные спеклы: модель ядерных органелл». Обзор. Обзоры природы. Молекулярно-клеточная биология . 4 (8): 605–12. дои : 10.1038/nrm1172 . ПМИД 12923522 . S2CID 6439413 .
- ^ Трипати К., Парнаик В.К. (сентябрь 2008 г.). «Дифференциальная динамика фактора сплайсинга SC35 во время клеточного цикла» (PDF) . Начальный. Журнал биологических наук . 33 (3): 345–54. дои : 10.1007/s12038-008-0054-3 . ПМИД 19005234 . S2CID 6332495 . Архивировано (PDF) из оригинала 15 ноября 2011 года.
- ^ Трипати К., Парнаик В.К. (сентябрь 2008 г.). «Дифференциальная динамика фактора сплайсинга SC35 во время клеточного цикла». Начальный. Журнал биологических наук . 33 (3): 345–54. дои : 10.1007/s12038-008-0054-3 . ПМИД 19005234 . S2CID 6332495 .
- ^ Хандвергер К.Е., Галл Дж.Г. (январь 2006 г.). «Субъядерные органеллы: новый взгляд на форму и функцию». Обзор. Тенденции в клеточной биологии . 16 (1): 19–26. дои : 10.1016/j.tcb.2005.11.005 . ПМИД 16325406 .
- ^ «Клеточный компонент Ядро спекл» . ЮниПрот: UniProtKB . Проверено 30 августа 2013 г.
- ^ Галл Дж.Г., Беллини М., Ву З., Мерфи С. (декабрь 1999 г.). «Сборка аппарата ядерной транскрипции и обработки: тельца Кахаля (спиральные тельца) и транскриптосомы» . Начальный. Молекулярная биология клетки . 10 (12): 4385–402. дои : 10.1091/mbc.10.12.4385 . ПМК 25765 . ПМИД 10588665 .
- ^ Jump up to: а б Матера А.Г., Тернс Р.М., Тернс MP (март 2007 г.). «Некодирующие РНК: уроки малых ядерных и малых ядрышковых РНК». Обзор. Обзоры природы. Молекулярно-клеточная биология . 8 (3): 209–20. дои : 10.1038/nrm2124 . ПМИД 17318225 . S2CID 30268055 .
- ^ Jump up to: а б Фокс А.Х., Ламонд А.И. (июль 2010 г.). «Параспеклы» . Обзор. Перспективы Колд-Спринг-Харбор в биологии . 2 (7): а000687. doi : 10.1101/cshperspect.a000687 . ПМК 2890200 . ПМИД 20573717 .
- ^ Jump up to: а б Фокс А., Бикмор В. (2004). «Ядерные отсеки: Параспеклы» . База данных ядерных белков. Архивировано из оригинала 10 сентября 2008 года . Проверено 6 марта 2007 г.
- ^ Jump up to: а б Fox AH, Bond CS, Lamond AI (ноябрь 2005 г.). «P54nrb образует гетеродимер с PSP1, который локализуется в параспеклах РНК-зависимым образом» . Начальный. Молекулярная биология клетки . 16 (11): 5304–15. doi : 10.1091/mbc.E05-06-0587 . ПМК 1266428 . ПМИД 16148043 .
- ^ Накагава С., Ямадзаки Т., Хиросе Т. (октябрь 2018 г.). «Молекулярное рассечение ядерных параспеклов: к пониманию развивающегося мира среды RNP» . Обзор. Открытая биология . 8 :180150.doi (10 ) : 10.1098/rsob.180150 . ПМК 6223218 . ПМИД 30355755 .
- ^ Пизани Г, барон Б (декабрь 2019 г.). «Ядерные параспеклы играют роль посредников в регуляторных и апоптотических путях генов» . Обзор. Исследование некодирующих РНК . 4 (4): 128–134. дои : 10.1016/j.ncrna.2019.11.002 . ПМК 7012776 . ПМИД 32072080 .
- ^ Kong XN, Yan HX, Chen L, Dong LW, Yang W, Liu Q и др. (октябрь 2007 г.). «Вызванное ЛПС снижение уровня сигнального регуляторного белка {альфа} способствует активации врожденного иммунитета в макрофагах» . Начальный. Журнал экспериментальной медицины . 204 (11): 2719–31. дои : 10.1084/jem.20062611 . ПМК 2118489 . ПМИД 17954568 .
- ^ Jump up to: а б Кармо-Фонсека М., Берчиано М.Т., Лафарга М. (сентябрь 2010 г.). «Сиротские ядерные тела» . Обзор. Перспективы Колд-Спринг-Харбор в биологии . 2 (9): а000703. doi : 10.1101/cshperspect.a000703 . ПМЦ 2926751 . ПМИД 20610547 .
- ^ Сампуда К.М., Райли М., Бойд Л. (апрель 2017 г.). «Вызванные стрессом ядерные гранулы образуются в ответ на накопление неправильно свернутых белков у Caenorhabditis elegans» . Начальный. Клеточная биология BMC . 18 (1): 18. дои : 10.1186/s12860-017-0136-x . ПМЦ 5395811 . ПМИД 28424053 .
- ^ Ленинджер А.Л., Нельсон Д.Л., Кокс М.М. (2000). Ленингерские принципы биохимии (3-е изд.). Нью-Йорк: Издательство Worth. ISBN 978-1-57259-931-4 .
- ^ Морено Ф., Ауаци Д., Риера А., Паломино К.А., Эрреро П. (февраль 2005 г.). «Ощущение глюкозы через Hxk2-зависимый сигнальный путь». Начальный. Труды Биохимического общества . 33 (Часть 1): 265–8. дои : 10.1042/BST0330265 . ПМИД 15667322 . S2CID 20647022 .
- ^ Герлих Д., Кутай У (1999). «Транспорт между ядром клетки и цитоплазмой». Обзор. Ежегодный обзор клеточной биологии и биологии развития . 15 (1): 607–60. дои : 10.1146/annurev.cellbio.15.1.607 . ПМИД 10611974 .
- ^ Хозак П., Кук PR (февраль 1994 г.). «Фабрики репликации». Обзор. Тенденции в клеточной биологии . 4 (2): 48–52. дои : 10.1016/0962-8924(94)90009-4 . ПМИД 14731866 .
- ^ Нирхаус К.Х., Уилсон Д.Н. (2004). Синтез белка и структура рибосом: трансляция генома . Вайли-ВЧ. ISBN 978-3-527-30638-1 .
- ^ Николини, Калифорния (1997). Структура и функция генома: от характеристики хромосом к технологии генов . Спрингер. ISBN 978-0-7923-4565-7 .
- ^ Черный ДЛ (2003). «Механизмы альтернативного сплайсинга премессенджерной РНК» (PDF) . Обзор. Ежегодный обзор биохимии . 72 (1): 291–336. doi : 10.1146/annurev.biochem.72.121801.161720 . ПМИД 12626338 . S2CID 23576288 .
- ^ Уотсон Дж.Д., Бейкер Т.А., Белл С.П., Ганн А., Левин М., Лосик Р. (2004). «Ч9–10». Молекулярная биология гена (5-е изд.). Писон Бенджамин Каммингс; ЦШЛ Пресс. ISBN 978-0-8053-9603-4 .
- ^ Кавацца Т, Вернос I (2015). «Путь RanGTP: от ядерно-цитоплазматического транспорта к сборке веретена и далее» . Обзор. Границы клеточной биологии и биологии развития . 3 : 82. дои : 10.3389/fcell.2015.00082 . ПМК 4707252 . ПМИД 26793706 .
- ^ Липпинкотт-Шварц Дж. (март 2002 г.). «Клеточная биология: разрыв ядерной оболочки» . Комментарий. Природа . 416 (6876): 31–2. Бибкод : 2002Natur.416...31L . дои : 10.1038/416031a . ПМИД 11882878 . S2CID 4431000 .
- ^ Jump up to: а б Буликас Т. (1995). «Фосфорилирование факторов транскрипции и контроль клеточного цикла». Обзор. Критические обзоры экспрессии генов эукариот . 5 (1): 1–77. ПМИД 7549180 .
- ^ Бетчер Б., Баррал Ю. (2013). «Клеточная биология открытого и закрытого митоза» . Обзор. Ядро . 4 (3). Остин, Техас: 160–5. дои : 10.4161/nucl.24676 . ПМЦ 3720745 . ПМИД 23644379 .
- ^ Стин Р.Л., Коллас П. (апрель 2001 г.). «Ошибочное направление ламинов B-типа в конце митоза: влияние на выживаемость клеток и регуляцию экспрессии ламинов A/C» . Начальный. Журнал клеточной биологии . 153 (3): 621–6. дои : 10.1083/jcb.153.3.621 . ПМК 2190567 . ПМИД 11331311 .
- ^ Бём I (ноябрь 2007 г.). «Отложения IgG можно обнаружить в ядрах клеток пациентов как с красной волчанкой, так и со злокачественными новообразованиями». Начальный. Клиническая ревматология . 26 (11): 1877–82. дои : 10.1007/s10067-007-0597-y . ПМИД 17364135 . S2CID 44879431 .
- ^ Рессел Л. (2017). «Ядерная морфология» . Морфология нормальных клеток в цитологии собак и кошек: руководство по идентификации . Хобокен, Нью-Джерси: John Wiley & Sons. п. 6. ISBN 978-1-119-27891-7 .
- ^ Скутельский Э., Данон Д. (июнь 1970 г.). «Сравнительное исследование изгнания ядра из позднего эритробласта и цитокинеза». Начальный. Экспериментальные исследования клеток . 60 (3): 427–36. дои : 10.1016/0014-4827(70)90536-7 . ПМИД 5422968 .
- ^ Торос Д.К., Дертингер С.Д., Холл Н.Е., Томецко Ч.Р. (февраль 2000 г.). «Подсчет микроядерных ретикулоцитов в периферической крови крыс: проточно-цитометрическое исследование». Начальный. Мутационные исследования . 465 (1–2): 91–9. дои : 10.1016/S1383-5718(99)00216-8 . ПМИД 10708974 .
- ^ Хаттер К.Дж., Стёр М. (1982). «Быстрое обнаружение микроядерных эритроцитов, индуцированных мутагеном, методом проточной цитометрии». Начальный. Гистохимия . 75 (3): 353–62. дои : 10.1007/bf00496738 . ПМИД 7141888 . S2CID 28973947 .
- ^ Хэм Б.К., Лукас У.Дж. (апрель 2014 г.). «Система ситовидных трубок флоэмы покрытосеменных: роль в передаче признаков, важных для современного сельского хозяйства» . Журнал экспериментальной ботаники . 65 (7): 1799–816. дои : 10.1093/jxb/ert417 . ПМИД 24368503 .
- ^ Зеттлер Л.А., Согин М.Л., Кэрон Д.А. (октябрь 1997 г.). «Филогенетические отношения между Acantharea и Polycystinea: молекулярный взгляд на радиолярии Геккеля» . Начальный. Труды Национальной академии наук Соединенных Штатов Америки . 94 (21): 11411–6. Бибкод : 1997PNAS...9411411A . дои : 10.1073/pnas.94.21.11411 . ПМК 23483 . ПМИД 9326623 .
- ^ Хортон Т.Р. (2006). «Число ядер в базидиоспорах 63 видов эктомикоризных гомобазидиомицетов». Начальный. Микология . 98 (2): 233–8. дои : 10.3852/микология.98.2.233 . ПМИД 16894968 .
- ^ Адам Р.Д. (декабрь 1991 г.). «Биология видов Giardia» . Обзор. Микробиологические обзоры . 55 (4): 706–32. дои : 10.1128/MMBR.55.4.706-732.1991 . ПМЦ 372844 . ПМИД 1779932 .
- ^ Фогт А., Гольдман А.Д., Мочизуки К., Ландвебер Л.Ф. (1 августа 2013 г.). «Одомашнивание транспозонов против мутуализма в перестройках генома инфузорий» . ПЛОС Генетика . 9 (8): e1003659. дои : 10.1371/journal.pgen.1003659 . ПМЦ 3731211 . ПМИД 23935529 .
- ^ Макиннес А., Ренник Д.М. (февраль 1988 г.). «Интерлейкин-4 побуждает культивируемые моноциты/макрофаги образовывать гигантские многоядерные клетки» . Начальный. Журнал экспериментальной медицины . 167 (2): 598–611. дои : 10.1084/jem.167.2.598 . ПМК 2188835 . ПМИД 3258008 .
- ^ Голдринг С.Р., Рулке М.С., Петрисон К.К., Бхан А.К. (февраль 1987 г.). «Гигантоклеточные опухоли человека, идентификация костей и характеристика типов клеток» . Начальный. Журнал клинических исследований . 79 (2): 483–91. дои : 10.1172/JCI112838 . ПМК 424109 . ПМИД 3027126 .
- ^ Иманян Б., Помберт Дж. Ф., Доррелл Р. Г., Бурки Ф., Килинг П. Дж. (2012). «Третичный эндосимбиоз у двух динотомов привел к небольшим изменениям в митохондриальных геномах их хозяев-динофлагеллят и эндосимбионтов диатомовых водорослей» . Начальный. ПЛОС ОДИН . 7 (8): е43763. Бибкод : 2012PLoSO...743763I . дои : 10.1371/journal.pone.0043763 . ПМЦ 3423374 . ПМИД 22916303 .
- ^ Пенниси Э. (август 2004 г.). «Эволюционная биология. Рождение ядра». Новости. Наука . 305 (5685): 766–8. дои : 10.1126/science.305.5685.766 . ПМИД 15297641 . S2CID 83769250 .
- ^ Девос Д.П., Греф Р., Field MC (июнь 2014 г.). «Эволюция ядра» . Обзор. Современное мнение в области клеточной биологии . 28 (100): 8–15. дои : 10.1016/j.ceb.2014.01.004 . ПМК 4071446 . ПМИД 24508984 .
- ^ Лопес-Гарсиа П., Морейра Д. (ноябрь 2015 г.). «Открытые вопросы происхождения эукариот» . Обзор. Тенденции в экологии и эволюции . 30 (11): 697–708. дои : 10.1016/j.tree.2015.09.005 . ПМК 4640172 . ПМИД 26455774 .
- ^ Хоган CM (2010). «Архея» . В Моноссон Э, Кливленд С (ред.). Энциклопедия Земли . Вашингтон, округ Колумбия: Национальный совет по науке и окружающей среде. Архивировано из оригинала 11 мая 2011 года.
- ^ Маргулис Л. (1981). Симбиоз в клеточной эволюции . Сан-Франциско: WH Freeman and Company. стр. 100-1 206–227 . ISBN 978-0-7167-1256-5 .
- ^ Мартин В. (декабрь 2005 г.). «Архебактерии (Archaea) и происхождение эукариотического ядра». Curr Opin Микробиол . 8 (6): 630–7. дои : 10.1016/j.mib.2005.10.004 . ПМИД 16242992 .
- ^ Бернштейн, Х., Бернштейн, К. (2017). Сексуальное общение у архей, предшественников эукариотического мейоза. В: Вицани, Г. (ред.) Биокоммуникация архей. Спрингер, Чам. https://doi.org/10.1007/978-3-319-65536-9_7
- ^ Лопес-Гарсиа П., Морейра Д. (май 2006 г.). «Силы отбора происхождения эукариотического ядра». Обзор. Биоэссе . 28 (5): 525–33. дои : 10.1002/bies.20413 . ПМИД 16615090 .
- ^ Фюрст Дж.А. (2005). «Внутриклеточная компартментация планктомицетов». Обзор. Ежегодный обзор микробиологии . 59 : 299–328. дои : 10.1146/annurev.micro.59.030804.121258 . ПМИД 15910279 .
- ^ Хартман Х, Федоров А (февраль 2002 г.). «Происхождение эукариотической клетки: геномное исследование» . Начальный. Труды Национальной академии наук Соединенных Штатов Америки . 99 (3): 1420–5. Бибкод : 2002PNAS...99.1420H . дои : 10.1073/pnas.032658599 . ПМК 122206 . ПМИД 11805300 .
- ^ Белл Пи Джей (сентябрь 2001 г.). «Вирусный эукариогенез: был ли предок ядра сложным ДНК-вирусом?» . Комментарий. Журнал молекулярной эволюции . 53 (3): 251–6. Бибкод : 2001JMolE..53..251L . дои : 10.1007/s002390010215 . ПМИД 11523012 . S2CID 20542871 .
- ^ Такемура М. (май 2001 г.). «Поксвирусы и происхождение эукариотического ядра». Начальный. Журнал молекулярной эволюции . 52 (5): 419–25. Бибкод : 2001JMolE..52..419T . дои : 10.1007/s002390010171 . ПМИД 11443345 . S2CID 21200827 .
- ^ Вильярреал LP, DeFilippis VR (август 2000 г.). «Гипотеза о том, что ДНК-вирусы являются источником репликационных белков эукариот» . Начальный. Журнал вирусологии . 74 (15): 7079–84. doi : 10.1128/JVI.74.15.7079-7084.2000 . ПМК 112226 . ПМИД 10888648 .
- ^ Белл Пи Джей (ноябрь 2006 г.). «Пол и цикл эукариотических клеток соответствуют вирусному происхождению эукариотического ядра». Начальный. Журнал теоретической биологии . 243 (1): 54–63. Бибкод : 2006JThBi.243...54B . дои : 10.1016/j.jtbi.2006.05.015 . ПМИД 16846615 .
- ^ де Роос А.Д. (2006). «Происхождение эукариотической клетки на основе сохранения существующих интерфейсов». Начальный. Искусственная жизнь . 12 (4): 513–23. дои : 10.1162/артл.2006.12.4.513 . ПМИД 16953783 . S2CID 5963228 .
- ^ Ван Левенгук А. самых точных микроскопов, подтвержденные различными экспериментами. Послания к различным выдающимся людям Дж. Арнольду и Дельфису, А. Беману, Lugdinum Batavorum Дела природы, или тайны природы с помощью были обнаружены и подтверждены множеством экспериментов, Послания к различным выдающимся доблестным людям Дж. Арнольду и Дельфи, А. Беману, Лугдине Йорк 1719-1730 ] (на латыни). Цитируется в Герлах Д. (2009). История микроскопии . Франкфурт-на-Майне, Германия: Verlag Harri Deutsch . ISBN 978-3-8171-1781-9 .
- ^ Коэн В.Д. (1982). «Цитоморфная система безъядерных эритроцитов немлекопитающих». Протоплазма . 113 : 23–32. дои : 10.1007/BF01283036 . S2CID 41287948 .
- ^ Харрис Х (1999). Рождение клетки . Нью-Хейвен: Издательство Йельского университета. ISBN 978-0-300-07384-3 .
- ^ Браун Р. (1866). «Об органах и способах оплодотворения Orchidex и Asclepiadea». Разные ботанические произведения I : 511–514.
- ^ Jump up to: а б Кремер Т. (1985). От клеточной теории к теории хромосом . Берлин, Гейдельберг, Нью-Йорк, Токио: Springer Verlag. ISBN 978-3-540-13987-4 . Онлайн-версия здесь
Дальнейшее чтение
- Гольдман Р.Д., Грюнбаум Ю., Мойр Р.Д., Шумейкер Д.К., Спанн Т.П. (март 2002 г.). «Ядерные ламины: строительные блоки ядерной архитектуры» . Гены и развитие . 16 (5): 533–47. дои : 10.1101/gad.960502 . ПМИД 11877373 .
- Обзорная статья о ядерных ламинах с объяснением их структуры и различных ролей.
- Герлих Д., Кутай У (1999). «Транспорт между ядром клетки и цитоплазмой». Ежегодный обзор клеточной биологии и биологии развития . 15 : 607–60. дои : 10.1146/annurev.cellbio.15.1.607 . ПМИД 10611974 .
- Обзорная статья о ядерном транспорте, объясняет принципы механизма и различные пути транспорта.
- Ламонд А.И., Эрншоу WC (апрель 1998 г.). «Структура и функции ядра» (PDF) . Наука . 280 (5363): 547–53. CiteSeerX 10.1.1.323.5543 . дои : 10.1126/science.280.5363.547 . ПМИД 9554838 .
- Обзорная статья о ядре, объясняющая структуру хромосом внутри органеллы и описывающая ядрышко и другие субъядерные тельца.
- Пенниси Э. (август 2004 г.). «Эволюционная биология. Рождение ядра». Наука . 305 (5685): 766–8. дои : 10.1126/science.305.5685.766 . ПМИД 15297641 . S2CID 83769250 .
- Обзорная статья об эволюции ядра, объясняющая ряд различных теорий.
- Поллард Т.Д., Эрншоу У.К. (2004). Клеточная биология . Филадельфия: Сондерс. ISBN 978-0-7216-3360-2 .
- Учебник университетского уровня по клеточной биологии. Содержит информацию о структуре и функциях ядра, включая ядерный транспорт и субъядерные домены.
Внешние ссылки
- «Ядро» . МБИнфо .
- «Узнайте о клеточном ядре» . cellnucleus.com . Веб-сайт кафедры онкологии Университета Альберты, посвященный структуре и функциям ядра.
- Бикмор В. «База данных ядерных белков» . Отдел генетики человека Совета медицинских исследований. Информация о ядерных компонентах.
- «Коллекция Ядро» . Библиотека изображений и видео . Американское общество клеточной биологии. Архивировано из оригинала 12 ноября 2006 г. Содержит рецензируемые неподвижные изображения и видеоклипы, иллюстрирующие ядро.
- Галл Дж.Г., Макинтош-младший (ред.). «Ядерный конверт и секция ядерного импорта» . Знаковые статьи по клеточной биологии . Архивировано из оригинала 17 ноября 2006 г. Содержит оцифрованные комментарии и ссылки на основополагающие исследовательские работы по ядру. Опубликовано онлайн в библиотеке изображений и видео. Архивировано 10 июня 2011 г. в Wayback Machine Американского общества клеточной биологии.
- «Цитоплазматические паттерны, генерируемые человеческими антителами» . AntibodyPatterns.com . Архивировано из оригинала 2 января 2007 года.