Фторборная кислота
 Тетрафторборат гидроксония
| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
Тетрафторборная кислота [ 1 ] | |||
Другие имена
| |||
| Идентификаторы | |||
| |||
3D model ( JSmol )
|
|||
| КЭБ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.037.165 | ||
| Номер ЕС |
| ||
| 21702 | |||
| МеШ | Фторборная+кислота | ||
ПабХим CID
|
|||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
| Число | 1775 | ||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| Ч[БФ 4 ] | |||
| Молярная масса | 87.81 g·mol −1 | ||
| Появление | Бесцветная жидкость | ||
| Температура плавления | -90 ° C (-130 ° F; 183 К) | ||
| Точка кипения | 130 ° С (266 ° F; 403 К) | ||
| Кислотность ( pKa ) | ~1,8 (раствор MeCN) [ 2 ] | ||
| Опасности | |||
| СГС Маркировка : | |||

| |||
| Опасность | |||
| H314 | |||
| P260 , P264 , P280 , P301+P330+P331 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P321 , P363 , P405 , P501 | |||
| NFPA 704 (огненный алмаз) | |||
| Паспорт безопасности (SDS) | Внешний паспорт безопасности материалов | ||
| Родственные соединения | |||
Родственные соединения
|
|||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Фторборная кислота или тетрафторборная кислота (архаично, фторборная кислота ) — неорганическое соединение с упрощенной химической формулой. ЧАС + [ Б Ж 4 ] − . Тетрафторборная кислота, не содержащая растворителей ( H[BF 4 ] ) не сообщалось. Термин «фторборная кислота» обычно относится к ряду соединений, включая тетрафторборат гидроксония ( [Н 3 О] + [БФ 4 ] − ), которые доступны в виде решений. Сольват этилового эфира также коммерчески доступен, где фторборная кислота может быть представлена формулой [H((CH 3 CH 2 ) 2 O) n ] + [БФ 4 ] − , где n равно 2.
В основном его производят как предшественник других фторборатных солей. [ 3 ] Это сильная кислота . Фторборная кислота вызывает коррозию и повреждает кожу. Он доступен коммерчески в виде раствора в воде и других растворителях, таких как диэтиловый эфир . Это сильная кислота со слабокоординирующим неокисляющим сопряженным основанием. [ 2 ] По своей структуре она похожа на хлорную кислоту , но лишена опасностей, связанных с окислителями .
Структура и производство
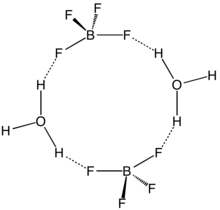
[ редактировать ]Чистый H[BF 4 ] не описан. То же самое справедливо и для суперкислот, известных по упрощенным формулам H[PF 6 ] и H[SbF 6 ] . [ 4 ] [ 5 ] Однако решение BF 3 в HF очень кислый, имеет приблизительный вид [Ч 2 Ф] + [БФ 4 ] − (тетрафторборат фторония) и функция кислотности Гаммета -16,6 при 7 мол. % BF 3 , легко квалифицируемый как суперкислота. [ 6 ] Несмотря на отсутствие растворителей H[BF 4 ] не выделен, его сольваты хорошо охарактеризованы. Эти соли состоят из протонированного растворителя в качестве катиона, например, Н 3 О + и H 5 O + 2 и тетраэдрический БФ - 4 анион. Анион и катионы имеют прочные водородные связи. [ 7 ]
Водные растворы H[BF 4 ] получают растворением борной кислоты в водном растворе плавиковой кислоты . [ 8 ] [ 9 ] Три эквивалента HF реагируют с образованием промежуточного трифторида бора, а четвертый - с образованием фторборной кислоты:
- B(OH) 3 + 4 HF → H 3 O + + БФ − 4 + 2 Ч 2 О
Раствор безводной фторборной кислоты можно приготовить добавлением водной фторборной кислоты к избытку уксусного ангидрида при 0°C, в результате чего образуется раствор фторборной кислоты, уксусной кислоты и остаточного уксусного ангидрида. [ 10 ]
Кислотность
[ редактировать ]Кислотность фторборной кислоты осложняется тем фактом, что ее название относится к ряду различных соединений, например [Н(СН 3 СН 2 ) 2 О] + [БФ 4 ] − (диметилоксоний тетрафторборат), [Н 3 О] + [БФ 4 ] − (тетрафторборат оксония) и HF·BF 3 ( аддукт фтороводород - трифторид бора 1:1) – каждый с разной кислотностью. Водное значение p K a указано как -0,44. [ 3 ] Титрование [Н((СН 2 ) 3 СН 3 ) 4 ] + [БФ 4 ] − (тетрабутиламмоний тетрафторборат) в ацетонитрила указывает на то, что растворе H[BF 4 ] , т.е. HF·BF 3 имеет ap K a 1,6 в этом растворителе. Таким образом, его кислотность сравнима с кислотностью фторсульфоновой кислоты . [ 2 ]
Приложения
[ редактировать ]Фторборная кислота является основным предшественником фторборатных солей, которые обычно получают путем обработки оксидов металлов фторборной кислотой. Неорганические соли являются промежуточными продуктами при производстве огнезащитных материалов и глазурных фритт , а также при электролитическом получении бора . H[BF 4 ] также используется при травлении алюминия и кислотном травлении.
Органическая химия
[ редактировать ][BF 4 ] используется в качестве катализатора алкилирования полимеризации и H . В реакциях защиты углеводов эфирная фторборная кислота является эффективным и экономичным катализатором реакций трансацетилирования и изопропилидирования. Растворы ацетонитрила расщепляют ацетали и некоторые простые эфиры . Многие реакционноспособные катионы были получены с использованием фторборной кислоты, например тетрафторборат тропилия ( С 7 Ч 7 + [БФ 4 ] − ), тетрафторборат трифенилкарбения ( Ф 3 С] + [БФ 4 ] − ), тетрафторборат триэтилоксония ( Et 3 О] + [БФ 4 ] − ) и тетрафторборат бензолдиазония ( [ФН 2 ] + [БФ 4 ] − ).
Гальваника
[ редактировать ]Решения H[BF 4 ] используются при гальванопокрытии олова и оловянных сплавов. В этом применении метансульфоновая кислота заменяет использование H[ BF4 ] . [ 11 ] Фторборатную кислоту применяют также для высокоскоростной гальваники меди во фторборатных ваннах. [ 12 ]
Безопасность
[ редактировать ]Фторборная кислота токсична и поражает кожу и глаза. Он атакует стекло. [ 3 ] Он гидролизуется, выделяя едкий летучий фторид водорода . [ 11 ]
Другие фторборные кислоты
[ редактировать ]Известен ряд фторборных кислот в водных растворах. Серию можно представить следующим образом: [ 13 ]
- ЧАС + [Б(ОН) 4 ] − (тетрагидроксиборат водорода) (не фторборная кислота)
- ЧАС + [БФ(ОН) 3 ] − (водород фтор(тригидрокси)борат)
- ЧАС + [БФ 2 (ОН) 2 ] − (дифтор(дигидрокси)борат водорода)
- ЧАС + [БФ 3 (ОН)] − (трифтор(гидрокси)борат водорода)
- ЧАС + [БФ 4 ] − (тетрафторборат водорода)
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ ИЮПАК . «Номенклатура неорганической химии» . Проверено 8 апреля 2021 г.
- ^ Jump up to: а б с Кютт А. и др., «Равновесная кислотность суперкислот», J. Org. хим. 2010, том 76, с. 391-395. два : 10.1021/jo101409p
- ^ Jump up to: а б с Грегори К. Фристад, Брюс П. Браншо «Тетрафторборная кислота» Электронная энциклопедия реагентов для органического синтеза E-Eros. дои : 10.1002/047084289X.rt035
- ^ Юхас, Марк; Хоффманн, Стефан; Стоянов Евгений; Ким, Ки-Чан; Рид, Кристофер А. (11 октября 2004 г.). «Самая сильная изолируемая кислота». Angewandte Chemie, международное издание . 43 (40): 5352–5355. дои : 10.1002/anie.200460005 . ISSN 1433-7851 . ПМИД 15468064 .
- ^ Рид, Кристофер А. (2005). «Карборановые кислоты. Новые «сильные, но мягкие» кислоты для органической и неорганической химии» (PDF) . хим. Коммун. (13): 1669–1677. дои : 10.1039/B415425H . ISSN 1359-7345 . ПМИД 15791295 .
- ^ Ола, Джордж А.; Сурья Пракаш, ГК; Соммер, Жан; Мольнар, Арпад (3 февраля 2009 г.). Суперкислотная химия . Ола, Джордж А. (Джордж Эндрю), 1927–2017 гг., Ола, Джордж А. (Джордж Эндрю), 1927–2017 гг. (2-е изд.). Хобокен, Нью-Джерси ISBN 9780471596684 . OCLC 191809598 .
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) - ^ Моотц, Д.; Стеффен, М. «Кристаллические структуры кислых гидратов и оксониевых солей. XX. Тетрафторбораты оксония H 3 OBF 4 , [H 5 O 2 ]BF 4 и [H(CH 3 OH) 2 ]BF 4 », Журнал неорганики и Общая химия 1981, вып. 482, стр. 193-200. два : 10.1002/zaac.19814821124
- ^ Браттон, Р.Дж.; Вебер, CJ; Гвиберт, ЧР; Литтл, Дж. Л. «Соединения бора». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a04_309 . ISBN 978-3527306732 .
- ^ Наводнение, DT (1933). «Фторбензол» (PDF) . Органические синтезы . 13:46 ; Сборник томов , т. 2, с. 295 .
- ^ Вудл, Ф.; Каплан, М.Л., «2,2'-би-1,3-дитиолиден (тетратиафульвален, TTF) и его катион-радикальные соли» Inorg. Синтез. 1979, вып. 19, 27. два : 10.1002/9780470132500.ch7
- ^ Jump up to: а б Баладжи, Р.; Пушпаванам, Малати (2003). «Метансульфоновая кислота в гальванических отраслях отделки металлов». Операции МВФ . 81 (5): 154–158. дои : 10.1080/00202967.2003.11871526 . S2CID 91584456 .
- ^ Бараускас, Ромуальдас «Рон» (1 января 2000 г.). «Меднение» . Металлическая отделка . 98 (1): 234–247. дои : 10.1016/S0026-0576(00)80330-X . ISSN 0026-0576 . Проверено 21 июля 2022 г.
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
Дальнейшее чтение
[ редактировать ]- Альберт, Р.; Дакс, К.; Плешко Р.; Штютц, А.Е. (1985). «Тетрафторборная кислота, эффективный катализатор реакций защиты и снятия защиты углеводов». Исследование углеводов . 137 : 282–290. дои : 10.1016/0008-6215(85)85171-5 .
- Бандгар, BP; Патил, А.В.; Чаван, ОС (2006). «Фторборная кислота на силикагеле как новый, эффективный и многоразовый катализатор для синтеза 1,5-бензодиазепинов в условиях без растворителей». Журнал молекулярного катализа A: Химический . 256 (1–2): 99–105. doi : 10.1016/j.molcata.2006.04.024 .
- Хайнц, РА; Смит, Дж.А.; Салай, PS; Вайсгербер, А.; Данбар, КР (2002). Гомолептические катионы ацетонитрила переходных металлов с анионами тетрафторбората или трифторметансульфоната . Неорганические синтезы. Том. 33. С. 75–83. дои : 10.1002/0471224502 . ISBN 9780471208259 .
- Хаускрофт, CE; Шарп, АГ (2004). Неорганическая химия (2-е изд.). Прентис Холл. п. 307. ИСБН 978-0-13-039913-7 .
- Меллер, А. (1988). «Бор». Гмелин Справочник по неорганической химии . Том. 3. Нью-Йорк: Спрингер-Верлаг. стр. 301–310.
- Перри, ДЛ; Филлипс, С.Л. (1995). Справочник неорганических соединений (1-е изд.). Бока-Ратон: CRC Press. п. 1203. ИСБН 9780849386718 .
- Вамсер, Калифорния (1948). «Гидролиз фторборной кислоты в водном растворе». Журнал Американского химического общества . 70 (3): 1209–1215. дои : 10.1021/ja01183a101 .
- Вильке-Дёрфурт, Э.; Бальц, Г. (1927). «О знании плавиковой кислоты и ее солей». Журнал неорганической и общей химии . 159 (1): 197–225. дои : 10.1002/zaac.19271590118 .
Внешние ссылки
[ редактировать ]- «Фторборная кислота ICSC: 1040» . ИНЧЕМ.


