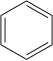
Нитросоединение

В органической химии нитросоединения — это органические соединения , содержащие одну или несколько нитрофункциональных групп ( −НЕТ 2 ). Нитрогруппа является одним из наиболее распространенных эксплозофоров (функциональной группы, образующей взрывчатое вещество), используемых во всем мире. Нитрогруппа также обладает сильным электроноакцепторным действием . Благодаря этому свойству Связи C-H альфа (соседние) с нитрогруппой могут быть кислыми. По тем же причинам присутствие нитрогрупп в ароматических соединениях замедляет электрофильное ароматическое замещение , но облегчает нуклеофильное ароматическое замещение . Нитрогруппы редко встречаются в природе. Они почти всегда образуются в результате реакций нитрования, начиная с азотной кислоты . [1]
Синтез
[ редактировать ]Получение ароматических нитросоединений
[ редактировать ]
Ароматические нитросоединения обычно синтезируют методом нитрования. Нитрование достигается с помощью смеси азотной и серной кислот , которые образуют ион нитрония ( NO + 2 ), который является электрофилом:
Продуктом нитрования, производимым в крупнейших масштабах, является нитробензол . Многие взрывчатые вещества производятся путем нитрования, включая тринитрофенол (пикриновая кислота), тринитротолуол (ТНТ) и тринитрорезорцин (стифиновая кислота). [3] Другой, но более специализированный метод получения арил-NO 2 -группы из галогенированных фенолов - это нитрование Цинке .
Получение алифатических нитросоединений
[ редактировать ]Алифатические нитросоединения могут быть синтезированы различными методами; примечательные примеры включают:
- Свободнорадикальное нитрование алканов . [4] В результате реакции образуются фрагменты исходного алкана, образуя разнообразную смесь продуктов; например, нитрометан , нитроэтан , 1-нитропропан и 2-нитропропан получают обработкой пропана в азотной кислотой газовой фазе (например, 350–450 ° C и 8–12 атм ).
- Реакции нуклеофильного замещения между галогенуглеродами. [5] или органосульфаты [6] с серебра или щелочи солями нитрита .
- Нитрометан можно получить в лаборатории обработкой хлорацетата натрия нитритом натрия . [7]
- Окисление оксимов [8] или первичные амины . [9]
- Восстановление β-нитроспиртов [10] или нитроалкены . [11]
- Путем декарбоксилирования нитрокарбоновых α - кислот образуются из нитрилов и этилнитрата . [12] [13]
Реакция Тер Меера
[ редактировать ]При нуклеофильном алифатическом замещении нитрит натрия (NaNO 2 ) замещает алкилгалогенид . В так называемой реакции Тер Меера (1876 г.), названной в честь Эдмунда тер Меера , [14] реагирующее вещество – 1,1-галонитроалкан:
протон отрывается Предлагается механизм реакции, при котором на первой медленной стадии от нитроалкана 1 до карбаниона 2 с последующим протонированием до ацинитро 3 и, наконец, нуклеофильным замещением хлора на основе экспериментально наблюдаемого кинетического изотопного эффекта водорода 3,3. [15] При взаимодействии того же реагента с гидроксидом калия продуктом реакции является 1,2-динитродимер. [16]
возникновение
[ редактировать ]На природе
[ редактировать ]Хлорамфеникол — редкий пример встречающегося в природе нитросоединения. По крайней мере, некоторые встречающиеся в природе нитрогруппы возникли в результате окисления аминогрупп. [17] 2-Нитрофенол агрегационный феромон клещей — .
Примеры нитросоединений редки в природе. 3-Нитропропионовая кислота содержится в грибах и растениях ( Indigofera ). Нитропентадецен — защитное соединение, обнаруженное у термитов . Аристолохиевые кислоты обнаружены в цветковых растениях семейства Aristolochiaceae . Нитрофенилэтан содержится в Aniba canelilla . [18] Нитрофенилэтан также встречается у представителей Annonaceae , Lauraceae и Papaveraceae . [19]
В фармацевтике
[ редактировать ]Несмотря на периодическое использование в фармацевтических препаратах, нитрогруппа связана с мутагенностью и генотоксичностью и поэтому часто рассматривается как помеха в процессе разработки лекарств . [20]
Реакции
[ редактировать ]Нитросоединения участвуют в ряде органических реакций , наиболее важной из которых является восстановление нитросоединений до соответствующих аминов:
- РНО 2 + 3 Н 2 → РНХ 2 + 2 Н 2 О
Практически все ароматические амины (например, анилин ) получают из нитроароматических соединений посредством такого каталитического гидрирования . Вариантом является образование диметиламиноарена с палладием на углероде и формальдегидом : [21]

α -углерод нитроалканов несколько кислый. pKa Значения нитрометана pKa растворе и 2-нитропропана составляют соответственно 17,2 и 16,9 в диметилсульфоксида (ДМСО), что предполагает водное значение около 11 . [22] Другими словами, эти углеродные кислоты можно депротонировать в водном растворе. Сопряженное основание называется нитронатом и ведет себя подобно еноляту . В нитроальдольной реакции он присоединяется непосредственно к альдегидам и вместе с енонами может служить донором Михаэля . И наоборот, нитроалкен реагирует с енолами как акцептор Михаэля. [23] [24]
Нитронаты также являются ключевыми промежуточными продуктами реакции Нефа : при воздействии кислот или окислителей нитронат гидролизуется до карбонила и азанона . [25]
Реагенты Гриньяра в сочетании с нитросоединениями дают нитрон ; но реактив Гриньяра с α-водородом затем снова добавляется к нитрону с образованием соли гидроксиламина . [26]
Синтез красителей
[ редактировать ]Синтез индола Леймгрубера -Батчо , Бартоли и Байера-Эммерлинга начинается с ароматических нитросоединений. Индиго можно синтезировать в реакции конденсации из орто -нитробензальдегида и ацетона в сильно основных условиях в реакции, известной как синтез индиго Байера-Дрюсона .
Биохимические реакции
[ редактировать ]Многие флавинзависимые . ферменты способны окислять алифатические нитросоединения до менее токсичных альдегидов и кетонов Нитроалканоксидаза и 3-нитропропионатоксидаза окисляют исключительно алифатические нитросоединения, тогда как другие ферменты, такие как глюкозооксидаза, имеют другие физиологические субстраты. [27]
Взрывы
[ редактировать ]Взрывное разложение нитроорганических соединений представляет собой окислительно-восстановительные реакции, в которых и окислитель (нитрогруппа), и горючее (углеводородный заместитель) связаны в одной молекуле. В процессе взрыва выделяется тепло за счет образования высокостабильных продуктов, включая молекулярный азот (N 2 ), углекислый газ и воду. Взрывная сила этой окислительно-восстановительной реакции усиливается, поскольку эти стабильные продукты при умеренных температурах представляют собой газы. Многие контактные взрывчатые вещества содержат нитрогруппу.
См. также
[ редактировать ]- Функциональная группа
- Восстановление нитросоединений
- Нитрование
- Нитрит (также группа NO 2 , но связывается по-другому)
- Нитроалкен
- Нитроглицерин
Ссылки
[ редактировать ]- ^ Генри Фойер, изд. (1970). Нитро и нитрозогруппы: Часть 2, Том 2 . Химия функциональных групп ПАТАИ. Том. 2. John Wiley & Sons Ltd., тел .: 10.1002/9780470771174 . ISBN 978-0-470-77117-4 . Сол Патай, изд. (1982). Нитро- и нитрозогруппы: Приложение F: Часть 2, Том 2 . Химия функциональных групп ПАТАИ. John Wiley & Sons Ltd. doi : 10.1002/9780470771679 . ISBN 978-0-470-77167-9 . Сол Патай, изд. (1982). Амино-, нитрозо- и нитросоединения и их производные: Приложение F: Часть 1, Том 1 . Химия функциональных групп ПАТАИ. John Wiley & Sons Ltd. doi : 10.1002/9780470771662 . ISBN 978-0-470-77166-2 .
- ^ Olga V. Dorofeeva; Yuriy V. Vishnevskiy; Natalja Vogt; Jürgen Vogt; Lyudmila V. Khristenko; Sergey V. Krasnoshchekov; Igor F. Shishkov; István Hargittai; Lev V. Vilkov (2007). "Molecular Structure and Conformation of Nitrobenzene Reinvestigated by Combined Analysis of Gas-Phase Electron Diffraction, Rotational Constants, and Theoretical Calculations". Structural Chemistry . 18 (6): 739–753. doi : 10.1007/s11224-007-9186-6 . S2CID 98746905 .
- ^ Джеральд, Бут. «Нитросоединения ароматические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a17_411 . ISBN 978-3527306732 .
- ^ Маркофски, Шелдон; Грейс, WG (2000). «Нитросоединения алифатические». Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a17_401 . ISBN 978-3-527-30673-2 .
- ^ Корнблюм, Н.; Уннаде, HE (1963). «1-Нитрооктан». Органические синтезы . 4 : 724. дои : 10.15227/orgsyn.038.0075 .
- ^ Уолден, П. (1907). «О представлении алифатических сульфоцианидов, цианидов и нитротел» . Отчеты Немецкого химического общества . 40 (3): 3214–3217. дои : 10.1002/cber.19070400383 .
- ^ Уитмор, ФК; Уитмор, Мэрион Г. (1923). «Нитрометан». Органические синтезы . 1 : 401. дои : 10.15227/orgsyn.003.0083 .
- ^ Ола, Джордж А.; Рамайя, Пичика; Чанг-Су, Ли; Пракаш, Сурья (1992). «Удобное окисление оксимов до нитросоединений перборатом натрия в ледяной уксусной кислоте». Синлетт . 1992 (4): 337–339. дои : 10.1055/s-1992-22006 .
- ^ Эхуд, Кейнан; Иегуда, Мазур (1977). «Сухое озонирование аминов. Превращение первичных аминов в нитросоединения». Журнал органической химии . 42 (5): 844–847. дои : 10.1021/jo00425a017 .
- ^ Чандрасекхар, С.; Шриниди, А. (2014). «Полезные расширения реакции Генри: быстрые пути к нитроалканам и нитроалкенам в водных средах» . Синтетические коммуникации . 44 (20): 3008–3018. дои : 10.1080/00397911.2014.926373 . S2CID 98439096 .
- ^ Шриниди, А. (2015). «Хемоселективное восстановление сопряженных нитроалкенов с помощью микроволновой печи до нитроалканов водным гидридом три-н-бутилолова» . Грамотная химия . 1 (1): 1061412. дои : 10.1080/23312009.2015.1061412 .
- ^ Вислицен, Вильгельм; Эндрес, Антон (1902). «О нитровании этилнитратом [Нитрификация этилнитратом]» . Отчеты Немецкого химического общества . 35 (2): 1755–1762. дои : 10.1002/cber.190203502106 .
- ^ Вейганд, Конрад (1972). Хильгетаг, Г.; Мартини, А. (ред.). Препаративная органическая химия Вейганда / Хильгетага (4-е изд.). Нью-Йорк: John Wiley & Sons, Inc. п. 1007. ИСБН 978-0-471-93749-4 .
- ^ Эдмунд тер Меер (1876 г.). «О динитросоединениях жирового ряда» . «Анналы химии» Юстуса Либиха . 181 (1): 1–22. дои : 10.1002/jlac.18761810102 .
- ^ Хоторн, М. Фредерик (1956). «Аци-нитроалканы. I. Механизм реакции тер Меера1». Журнал Американского химического общества . 78 (19): 4980–4984. дои : 10.1021/ja01600a048 .
- ^ 3-гексен, 3,4-динитро- Д.Е. Бисгроув, Дж. Ф. Браун-младший и Л. Б. Клэпп. Органические синтезы , Сб. Том. 4, с. 372 (1963); Том. 37, с. 23 (1957). ( Статья )
- ^ Зохер, Георг; Винклер, Роберт; Хертвек, Кристиан; Шульц, Георг Э (2007). «Структура и действие N-оксигеназы AurF Streptomyces thioluteus». Журнал молекулярной биологии . 373 (1): 65–74. дои : 10.1016/j.jmb.2007.06.014 . ПМИД 17765264 .
- ^ МАИА, Хосе Гильерме С.; АНДРАДЕ, Элоиза Хелена А. (2009). «База данных ароматических растений и их эфирных масел Amazon» (PDF) . Новая химия . 32 (3). FapUNIFESP (SciELO): 595–622. дои : 10.1590/s0100-40422009000300006 . ISSN 0100-4042 .
- ^ Крамер, КУ; Кубицкий, К.; Ровер, Дж.Г.; Биттрих, В. (1993). Цветковые растения, двудольные: семейства магнолид, гамамелид и кариофиллид . Семейства и роды сосудистых растений. Шпрингер-Верлаг, Берлин. ISBN 978-3-540-55509-4 .
- ^ Непали К., Ли Х.И., Лиу Дж.П. (март 2019 г.). «Нитрогруппсодержащие препараты». Дж. Мед. Хим . 62 (6): 2851–2893. doi : 10.1021/acs.jmedchem.8b00147 . ПМИД 30295477 . S2CID 52931949 .
- ^ «ЭТИЛ п-ДИМЕТИЛАМИНОФЕНИЛАЦЕТАТ» (PDF) . Органические синтезы . 47 : 69. 1967. doi : 10.15227/orgsyn.047.0069 .
- ^ Бордвелл, Фредерик Дж; Сатиш, А.В. (1994). «Важен ли резонанс для определения кислотности слабых кислот или энтальпии диссоциации гомолитических связей (БДЭ) их кислотных связей ГК?». Журнал Американского химического общества . 116 (20): 8885. doi : 10.1021/ja00099a004 .
- ^ Ранганатан, Даршан; Рао, Бхушан; Ранганатан, Субрамания; Мехротра, Ашок и Айенгар, Радха (1980). «Нитроэтилен: стабильный, чистый и реакционноспособный агент для органического синтеза». Журнал органической химии . 45 (7): 1185–1189. дои : 10.1021/jo01295a003 .
- ^ Жюберт, Кэрол и Кнохель, Пол (1992). «Получение полифункциональных нитроолефинов и нитроалканов с использованием медно-цинковых реагентов RCu(CN)ZnI». Журнал органической химии . 57 (20): 5431–5438. дои : 10.1021/jo00046a027 .
- ^ Смит (2020)), Органическая химия Марша , rxn. 16-3.
- ^ Бартоли, Джузеппе; Маркантони, Энрико; Петрини, Марино (1992) [14 апреля 1992 г.]. «Нитроны от присоединения бензильных и аллильных реактивов Гриньяра к алкилнитросоединениям: хемо-, регио- и стереоселективность реакции». Журнал органической химии . 57 (22). Американское химическое общество: 5834–5840. дои : 10.1021/jo00048a012 .
- ^ Нагпал, Аканкша; Вэлли, Майкл П.; Фитцпатрик, Пол Ф.; Орвилл, Аллен М. (2006). «Кристаллические структуры нитроалканоксидазы: понимание механизма реакции ковалентного комплекса флавофермента, захваченного во время оборота» . Биохимия . 45 (4): 1138–50. дои : 10.1021/bi051966w . ПМК 1855086 . ПМИД 16430210 .