История квантовой механики

История квантовой механики — фундаментальная часть истории современной физики . Основные главы этой истории начинаются с появления квантовых идей для объяснения отдельных явлений — излучения черного тела, фотоэлектрического эффекта, спектров солнечного излучения — эпохи, называемой Старыми или Старыми квантовыми теориями. [1] Основываясь на технологии, разработанной в классической механике , изобретение волновой механики Эрвином Шредингером и расширение многими другими запускают «современную» эпоху, начавшуюся примерно в 1925 году. Работы Поля Дирака по релятивистской квантовой теории привели его к исследованию квантовых теорий излучения, кульминацией которых стала квантовая теория. электродинамика , первая квантовая теория поля . История квантовой механики продолжается в истории квантовой теории поля . История квантовой химии , теоретические основы химической структуры , реакционной способности и связи переплетаются с событиями, обсуждаемыми в этой статье.
Фраза «квантовая механика» была придумана (по-немецки Quantenmechanik ) группой физиков, включая Макса Борна, Вернера Гейзенберга и Вольфганга Паули , в Геттингенском университете в начале 1920-х годов и впервые была использована в статье Борна 1925 года «Zur Квантенмеханик» . [2] [3]
Слово «квант» происходит от латинского слова «сколько» (как и количество ). То, что квантовано , например, энергия гармонических осцилляторов Планка, может принимать только определенные значения. Например, в большинстве стран деньги эффективно квантуются, при этом количество денег представляет собой монету с наименьшей стоимостью в обращении. Механика – раздел науки, изучающий действие сил на объекты. Итак, квантовая механика — это часть механики, которая имеет дело с объектами, для которых квантованы те или иные свойства.
в конце эпохи Триумф и неприятности классической
Открытия XIX века , как успехи, так и неудачи, подготовили почву для возникновения квантовой механики.
Волновая теория света [ править ]
Начиная с 1670 года и в течение трех десятилетий Исаак Ньютон развивал и отстаивал свою корпускулярную теорию , утверждая, что совершенно прямые линии отражения демонстрируют природу частиц света, поскольку в то время ни одна волновая теория не демонстрировала движение по прямым линиям. [1] : 19 Он объяснил преломление, постулируя, что частицы света ускоряются в поперечном направлении при входе в более плотную среду. Примерно в то же время современники Ньютона Роберт Гук и Христиан Гюйгенс , а позже Огюстен-Жан Френель математически уточнили волновую точку зрения, показав, что если бы свет распространялся с разными скоростями в разных средах, преломление можно было бы легко объяснить как зависящее от среды распространение света. легкие волны. Полученный в результате принцип Гюйгенса-Френеля чрезвычайно успешно воспроизводил поведение света и соответствовал Томасом Юнгом открытию волновой интерференции света в ходе его эксперимента с двумя щелями в 1801 году. [4] Волновая точка зрения не сразу вытеснила точку зрения лучей и частиц, но начала доминировать в научных размышлениях о свете в середине 19 века, поскольку она могла объяснить явления поляризации, которые альтернативы не могли объяснить. [5]
Джеймс Клерк Максвелл обнаружил, что он может применять свои ранее открытые уравнения Максвелла вместе с небольшой модификацией для описания самораспространяющихся волн колеблющихся электрических и магнитных полей. Быстро стало очевидно, что видимый свет, ультрафиолетовый свет и инфракрасный свет представляют собой электромагнитные волны разной частоты. [1] : 272 Эта теория стала решающим фактором в зарождении квантовой механики.
атомная теория Новая
В начале 19-го века химические исследования Джона Дальтона и Амедео Авогадро придали вес атомной теории материи, идее, которую Джеймс Клерк Максвелл , Людвиг Больцман и другие развили, чтобы создать кинетическую теорию газов . Успехи кинетической теории еще больше подтвердили идею о том, что материя состоит из атомов, однако у этой теории были и недостатки, которые могли быть устранены только с развитием квантовой механики. [6] Существование атомов не было общепринятым среди физиков и химиков; Эрнст Мах , например, был ярым антиатомистом. [7]

Первые намеки на проблемы классической механики возникли в связи с температурной зависимостью свойств газов. [8] Людвиг Больцман предположил в 1877 году, что энергетические уровни физической системы, такой как молекула , могут быть дискретными (а не непрерывными). Обоснование Больцманом наличия дискретных уровней энергии в молекулах, таких как молекулы газообразного йода, берет свое начало в его теориях статистической термодинамики и статистической механики и подкрепляется математическими аргументами, как и двадцать лет спустя с первой квантовой теорией. выдвинул Макс Планк.
Электроны [ править ]
В последние дни 1800-х годов Дж. Дж. Томсон установил, что электроны несут отрицательный заряд, противоположный, но того же размера, что и ион водорода, но при этом имеют массу более чем в тысячу раз меньшую. Известно, что с каждым атомом связано множество таких электронов. [1] : 365
Теория радиации [ править ]

На протяжении 1800-х годов во многих исследованиях изучались детали спектра интенсивности и частоты света, излучаемого пламенем, Солнцем или раскаленными объектами. [1] : 367 Формула Ридберга эффективно суммировала темные линии, видимые в спектре, но он не предоставил физической модели, объясняющей их. Спектр, излучаемый раскаленными объектами, можно объяснить как на высоких, так и на низких длинах волн, но эти две теории различались.
квантовая теория Старая
Квантовая механика развивалась в два отдельных этапа. Первый этап, известный как старая квантовая теория , начался примерно в 1900 году с радикально новых подходов к объяснению физических явлений, не понятных классической механикой 1800-х годов. [1]
излучения черного тела объяснения для Макс Планк вводит кванты


Тепловое излучение — это электромагнитное излучение, испускаемое поверхностью объекта за счет внутренней энергии объекта. Если объект достаточно нагрет, он начинает излучать свет в красной части видимого спектра , поскольку становится раскаленным докрасна .
Дальнейшее нагревание приводит к изменению цвета с красного на желтый, белый и синий, поскольку он излучает свет на все более коротких длинах волн (более высоких частотах). Идеальный излучатель является также идеальным поглотителем: когда холодно, такой объект выглядит совершенно черным, потому что он поглощает весь падающий на него свет и не излучает его. Следовательно, идеальный тепловой излучатель известен как черное тело , а излучаемое им излучение называется излучением черного тела .

К концу XIX века тепловое излучение было достаточно хорошо изучено экспериментально. Было создано несколько формул, которые могли бы описать некоторые экспериментальные измерения теплового излучения: то, как длина волны, при которой излучение является наиболее сильным, изменяется с температурой, определяется законом смещения Вина , общая мощность, излучаемая на единицу площади, определяется законом Стефана-Больцмана. закон . Лучшим теоретическим объяснением экспериментальных результатов был закон Рэлея-Джинса, который хорошо согласуется с экспериментальными результатами на больших длинах волн (или, что то же самое, на низких частотах), но сильно не согласуется на коротких длинах волн (или высоких частотах). Фактически, классическая физика предсказывала, что на коротких волнах энергия будет излучаться горячим телом с бесконечной скоростью. Этот результат, который явно неверен, известен как ультрафиолетовая катастрофа . Однако классическая физика привела к закону Рэлея-Джинса , который, как показано на рисунке, хорошо согласуется с экспериментальными результатами на низких частотах, но сильно не согласуется на высоких частотах. Физики искали единую теорию, объясняющую все экспериментальные результаты.
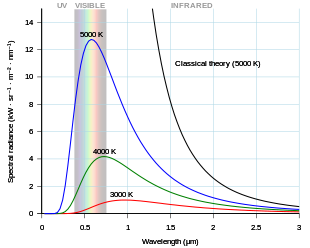
Первую модель, способную объяснить весь спектр теплового излучения, предложил Макс Планк в 1900 году. [9] Он предложил математическую модель, в которой тепловое излучение находилось в равновесии с набором гармонических осцилляторов . Чтобы воспроизвести результаты эксперимента, ему пришлось предположить, что каждый генератор излучает целое число единиц энергии на своей единственной характеристической частоте, а не способен излучать любое произвольное количество энергии. Другими словами, энергия, излучаемая генератором, была квантована . Квант энергии каждого осциллятора, согласно Планку, был пропорционален частоте осциллятора; константа пропорциональности теперь известна как постоянная Планка .
Закон Планка был первой квантовой теорией в физике, и Планк получил Нобелевскую премию в 1918 году «в знак признания заслуг, которые он оказал развитию физики, открыв энергетические кванты». [10] Однако в то время Планк считал, что квантование было чисто эвристической математической конструкцией, а не (как сейчас считается) фундаментальным изменением в нашем понимании мира. [11]
Альберт Эйнштейн применяет кванты для фотоэлектрического объяснения эффекта
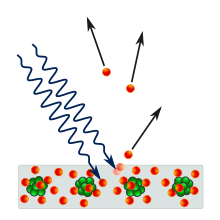
В 1887 году Генрих Герц заметил, что когда свет достаточной частоты падает на металлическую поверхность, эта поверхность испускает катодные лучи . [1] : Я:362 Десять лет спустя Дж. Дж. Томсон показал, что многочисленные сообщения о катодных лучах на самом деле были «тельцами», и их быстро стали называть электронами . В 1902 году Филипп Ленард обнаружил, что максимально возможная энергия выброшенного электрона не связана с его интенсивностью . [12] Это наблюдение противоречит классическому электромагнетизму, который предсказывает, что энергия электрона должна быть пропорциональна интенсивности падающего излучения. [13] : 24

В 1905 году Альберт Эйнштейн предположил, что, хотя непрерывные модели света чрезвычайно хорошо работают для оптических явлений, усредненных по времени, для мгновенных переходов энергия света может возникать с помощью конечного числа квантов энергии. [14] Во введении к своей квантовой статье «Об эвристической точке зрения на излучение и преобразование света», опубликованной в марте 1905 года, Эйнштейн утверждает:
Согласно рассматриваемому здесь предположению, при распространении светового луча из точки энергия не распределяется непрерывно по всевозрастающим пространствам, а состоит из конечного числа «квантов энергии», локализованных в точках пространства. движутся, не разделяясь, и могут быть поглощены или порождены только как единое целое.
Это заявление было названо самым революционным предложением, написанным физиком двадцатого века. [15] Энергия одного кванта света частоты определяется частотой, умноженной на постоянную Планка :
Эйнштейн предполагал, что квант света передает всю свою энергию одному электрону, сообщая не более энергии hf электрону . Следовательно, только частота света определяет максимальную энергию, которую можно сообщить электрону; интенсивность фотоэмиссии пропорциональна интенсивности светового луча. [14]
требуется определенное количество энергии, называемое работой выхода и обозначаемое φ . Эйнштейн утверждал, что для удаления электрона из металла [16] Это количество энергии различно для каждого металла. Если энергия квантов света меньше работы выхода, то они не несут достаточной энергии для отрыва электрона из металла. Пороговая частота f 0 — это частота квантов света, энергия которых равна работе выхода:
Если f больше f 0 , энергии hf достаточно, чтобы оторвать электрон. Выброшенный электрон имеет энергию кинетическую E k , которая в лучшем случае равна энергии света за вычетом энергии, необходимой для вытеснения электрона из металла:
Описание Эйнштейном света как состоящего из квантов энергии расширило идею Планка о квантованной энергии, которая заключается в том, что один квант заданной частоты f доставляет неизменное количество энергии hf .В природе одиночные кванты встречаются редко. Солнце и источники выбросов, доступные в 19 веке, каждую секунду излучают огромное количество энергии. Константа Планка h настолько мала , что количество энергии в каждом кванте hf очень и очень мало. Свет, который мы видим, включает в себя многие триллионы таких квантов.
Квантование материи: модель атома Бора [ править ]
К началу 20-го века для доказательства потребовалась модель атома с диффузным облаком отрицательно заряженных электронов, окружающим небольшое плотное положительно заряженное ядро . Эти свойства предложили модель, в которой электроны вращаются вокруг ядра, как планеты, вращающиеся вокруг звезды. Классическую модель атома называют планетарной моделью, а иногда и моделью Резерфорда — в честь Эрнеста Резерфорда , предложившего ее в 1911 году на основе эксперимента Гейгера-Марсдена с золотой фольгой , который впервые продемонстрировал существование ядра. Однако было также известно, что атом в этой модели будет нестабильным: согласно классической теории, вращающиеся по орбите электроны испытывают центростремительное ускорение и, следовательно, должны испускать электромагнитное излучение, потеря энергии также заставляет их двигаться по спирали к ядру, сталкиваясь. с ним за долю секунды.
Второй связанной с этим загадкой был спектр излучения атомов. Когда газ нагревается, он излучает свет только на дискретных частотах. Например, видимый свет, излучаемый водородом, состоит из четырех разных цветов, как показано на рисунке ниже. Интенсивность света на разных частотах также различна. Напротив, белый свет состоит из непрерывного излучения во всем диапазоне видимых частот. К концу девятнадцатого века простое правило, известное как формула Бальмера, показывало, как частоты различных линий связаны друг с другом, хотя и не объясняло, почему это так, и не делало каких-либо прогнозов относительно интенсивности. Формула также предсказала некоторые дополнительные спектральные линии в ультрафиолетовом и инфракрасном свете, которые в то время не наблюдались. Эти линии позже были обнаружены экспериментально, что повысило уверенность в ценности формулы.
В 1905 году Альберт Эйнштейн использовал кинетическую теорию для объяснения броуновского движения . Французский физик Жан Батист Перрен использовал модель из статьи Эйнштейна для экспериментального определения массы и размеров атомов, тем самым обеспечив прямую эмпирическую проверку атомной теории. [ нужна ссылка ]

В 1913 году Нильс Бор предложил новую модель атома , включающую квантованные орбиты электронов: электроны по-прежнему вращаются вокруг ядра так же, как планеты вращаются вокруг Солнца, но им разрешено обитать только на определенных орбитах, а не на любом произвольном расстоянии. [18] Когда атом излучал (или поглощал) энергию, электрон не двигался по непрерывной траектории от одной орбиты вокруг ядра к другой, как можно было бы ожидать классически. Вместо этого электрон мгновенно перепрыгивал бы с одной орбиты на другую, испуская излучаемый свет в виде фотона. [19] Возможные энергии фотонов, испускаемых каждым элементом, определялись разницей в энергии между орбитами, поэтому спектр излучения каждого элемента должен был содержать несколько линий. [20]

Начав всего лишь с одного простого предположения о правиле, которому должны подчиняться орбиты, модель Бора смогла связать наблюдаемые спектральные линии в спектре излучения водорода с ранее известными константами. В модели Бора электрону не разрешалось непрерывно излучать энергию и врезаться в ядро: как только он оказался на ближайшей разрешенной орбите, он стал стабильным навсегда. Модель Бора не объяснила, почему орбиты следует квантовать таким образом, не смогла сделать точные предсказания для атомов с более чем одним электроном или объяснить, почему некоторые спектральные линии ярче других.
Некоторые фундаментальные предположения модели Бора вскоре оказались ошибочными, но ключевой результат о том, что дискретные линии в спектрах излучения обусловлены некоторыми свойствами квантованных электронов в атомах, верен. То, как на самом деле ведут себя электроны, разительно отличается от поведения атома Бора и от того, что мы видим в мире нашего повседневного опыта; Эта современная квантово-механическая модель атома обсуждается ниже .
Важный шаг в развитии квантовой теории был сделан на первом Сольвеевском конгрессе в 1911 году. Там ведущие физики научного сообщества встретились, чтобы обсудить проблему «Излучение и кванты». К этому времени была опубликована модель атома Эрнеста Резерфорда. [21] [22] но большая часть дискуссий, касающихся атомной структуры, вращалась вокруг квантовой модели Артура Хааса в 1910 году. Кроме того, на Сольвеевском конгрессе в 1911 году Хендрик Лоренц предложил после выступления Эйнштейна о квантовой структуре положить энергию ротатора равной nhv. [23] [24] : 244 За этим последовали другие квантовые модели, такие как модель Джона Уильяма Николсона 1912 года, которая представляла собой ядерный и дискретизированный угловой момент. [25] [26] [27] Николсон ввел спектры в свою атомную модель, используя колебания электронов в атоме ядра, перпендикулярных плоскости орбиты, тем самым поддерживая стабильность. Атомные спектры Николсона идентифицировали множество неизвестных линий в солнечных и небулярных спектрах. [25] [28] [29] [24] : 278
В 1913 году Бор объяснил спектральные линии атома водорода , опять же с помощью квантования, в своей статье от июля 1913 года « О строении атомов и молекул», в которой он обсуждал и цитировал модель Николсона. [30] [31] [27] В модели Бора атом водорода изображается как тяжелое положительно заряженное ядро, вокруг которого вращается легкий отрицательно заряженный электрон. Электрон может существовать только на определенных, дискретно разделенных орбитах, помеченных их угловым моментом , который ограничен целым кратным приведенной постоянной Планка . Ключевой успех модели заключался в объяснении формулы Ридберга для спектральных линий излучения атомарного водорода с помощью переходов электронов между орбитами. [24] : 276 Хотя формула Ридберга была известна экспериментально, она не получила теоретического обоснования до тех пор, пока не была представлена модель Бора. Модель Бора не только объяснила причины структуры формулы Ридберга, но и дала обоснование фундаментальным физическим константам, которые составляют эмпирические результаты формулы.
Более того, применение квантовой теории Планка к электрону позволило Штефану Прокопиу затем Нильсу Бору в 1913 году вычислить магнитный момент электрона в 1911–1913 годах, а , который позже был назван « магнетоном »; аналогичные квантовые вычисления, но с совершенно другими численными значениями, впоследствии стали возможны как для магнитных моментов протона , так и для нейтрона , которые на три порядка меньше, чем у электрона.
Эти теории, хотя и были успешными, были строго феноменологическими : в то время не было строгого обоснования квантования , за исключением, возможно, обсуждения Анри Пуанкаре теории Планка в его статье 1912 года Sur la theorie des quanta . [32] [33] Все вместе они известны как старая квантовая теория .
Спиновое квантование
Квантование орбитального углового момента электрона в сочетании с магнитным моментом электрона предположило, что атомы с магнитным моментом должны проявлять квантованное поведение в магнитном поле. В 1922 году Отто Штерн и Вальтер Герлах решили проверить эту теорию. Они нагревали серебро в вакуумной трубке с рядом узких щелей, создавая молекулярный пучок атомов серебра. Они пропустили этот луч через неоднородное магнитное поле . Вместо непрерывного узора атомов серебра они обнаружили две группы. [34]
Относительно своего северного полюса, направленного вверх, вниз или куда-то посередине, в классической механике магнит, брошенный через магнитное поле, может отклоняться на небольшое или большое расстояние вверх или вниз. Атомы, которые Штерн и Герлах пропустили через магнитное поле, действовали аналогичным образом. Однако, хотя магниты можно было отклонять на разные расстояния, атомы всегда будут отклоняться на постоянное расстояние вверх или вниз. Это подразумевало, что свойство атома, соответствующее ориентации магнита, должно быть квантовано, принимая одно из двух значений (вверх или вниз), а не свободно выбираться под любым углом.
Выбор ориентации магнитного поля, используемого в эксперименте Штерна–Герлаха, произволен. В анимации, показанной здесь, поле вертикальное, поэтому атомы отклоняются либо вверх, либо вниз. Если магнит повернуть на четверть оборота, атомы отклонятся либо влево, либо вправо. Использование вертикального поля показывает, что вращение вдоль вертикальной оси квантуется, а использование горизонтального поля показывает, что вращение вдоль горизонтальной оси квантуется.
Результаты эксперимента Штерна-Герлаха вызвали сенсацию, особенно потому, что ведущие ученые, в том числе Эйнштейн и Пауль Эренфест, утверждали, что атомы серебра в условиях эксперимента должны иметь случайную ориентацию: квантование не должно было быть наблюдаемым. [34] Прошло не менее пяти лет, прежде чем эта загадка была раскрыта: квантование наблюдалось, но оно не было связано с орбитальным угловым моментом.
В 1925 году Ральф Крониг предположил, что электроны ведут себя так, как будто они самостоятельно вращаются или «вращаются» вокруг оси. [35] : 56 Спин будет генерировать крошечный магнитный момент, который разделит энергетические уровни, ответственные за спектральные линии, в соответствии с существующими измерениями. Два электрона на одной и той же орбитали заняли бы разные квантовые состояния, если бы они «вращались» в противоположных направлениях, что удовлетворяет принципу исключения . К сожалению, у теории было два существенных недостатка: два значения, вычисленные Кронигом, отличались в два раза. Старшие коллеги Кронига не одобряли его работу, и она так и не была опубликована.
Десять месяцев спустя голландские физики Джордж Уленбек и Сэмюэл Гаудсмит из Лейденского университета опубликовали свою теорию самовращения электронов. [36] Модель, как и модель Кронига, была по сути классической, но привела к квантовому предсказанию.
Бройля Гипотеза волны материи де

В 1924 году Луи де Бройль опубликовал революционную гипотезу: материя обладает волновыми свойствами. Основываясь на предложении Эйнштейна о том, что фотоэлектрический эффект можно описать с помощью квантованного переноса энергии, и на отдельном предложении Эйнштейна, исходя из специальной теории относительности, о том, что масса покоя эквивалентна энергии через де Бройль предположил, что движущаяся материя имеет связанную с ней волну с длиной волны где есть импульс материи от движения. [37] [38] Потребовав, чтобы его длина волны охватывала атом, он объяснил квантование орбит Бора. [1] : 217 Одновременно это показало, что волновое поведение света по существу является квантовым эффектом. [1] : 216
Де Бройль расширил модель атома Бора , показав, что электрон, обращающийся по орбите вокруг ядра, можно рассматривать как обладающий волновыми свойствами. В частности, электрон наблюдается только в ситуациях, допускающих наличие стоячей волны вокруг ядра . Примером стоячей волны является скрипичная струна, которая закреплена на обоих концах и ее можно заставить вибрировать. Волны, создаваемые струнным инструментом, кажутся колеблющимися на месте, перемещаясь от гребня к впадине вверх и вниз. Длина волны стоячей волны зависит от длины вибрирующего объекта и граничных условий. Например, поскольку струна скрипки закреплена на обоих концах, она может переносить стоячие волны с длинами волн , где l — длина, а n — целое положительное число. Де Бройль предположил, что разрешенными электронными орбитами являются те, для которых длина окружности орбиты будет равна целому числу длин волн. Таким образом, длина волны электрона определяет, что возможны только боровские орбиты на определенных расстояниях от ядра. В свою очередь, на любом расстоянии от ядра, меньшем определенной величины, установить орбиту было бы невозможно. Минимально возможное расстояние от ядра называется радиусом Бора. [39] Рассмотрение де Бройлем атома Бора в конечном итоге не увенчалось успехом, но его гипотеза послужила отправной точкой для волнового уравнения Шредингера.
Материя, ведущая себя как волна, была впервые экспериментально продемонстрирована для электронов: луч электронов может проявлять дифракцию , точно так же, как луч света или волна на воде. Через три года после того, как де Бройль опубликовал свою гипотезу, две разные группы продемонстрировали дифракцию электронов. В Абердинском университете Джордж Пейджет Томсон и Александр Рид пропускали луч электронов через тонкую целлулоидную пленку, а затем через металлические пленки и наблюдали предсказанные интерференционные картины. (Александр Рид, аспирант Томсона, провел первые эксперименты, но вскоре погиб в аварии на мотоцикле. [40] и редко упоминается.) В Bell Labs Клинтон Джозеф Дэвиссон и Лестер Халберт Гермер в своем эксперименте отразили электронный луч от образца никеля, наблюдая четко определенные лучи, предсказанные волновыми моделями, возвращающимися из кристалла. [1] : II:218 Де Бройль был удостоен Нобелевской премии по физике в 1929 году за свою гипотезу; Томсон и Дэвиссон получили Нобелевскую премию по физике в 1937 году за свои экспериментальные работы.
Основываясь на подходе де Бройля, современная квантовая механика родилась в 1925 году, когда немецкие физики Вернер Гейзенберг, Макс Борн и Паскуаль Йордан [41] [42] разработал матричную механику , а австрийский физик Эрвин Шредингер изобрел волновую механику и нерелятивистское уравнение Шредингера как приближение обобщенного случая теории де Бройля. [43] Впоследствии Шрёдингер показал, что эти два подхода эквивалентны. Первым применением квантовой механики к физическим системам было алгебраическое определение спектра водорода Вольфгангом Паули. [44] и трактовка двухатомных молекул Люси Менсинг . [45]
Развитие современной квантовой механики [ править ]
Конец первой эры квантовой механики был вызван публикацией де Бройлем своей гипотезы волн материи . [1] : 268 что привело к открытию Шрёдингером волновой механики материи. Точные предсказания спектра поглощения водорода обеспечили широкое признание новой квантовой теории. [1] : 275
Матричная механика [ править ]
В 1925 году Вернер Гейзенберг попытался решить одну из проблем, которые модель Бора оставила без ответа, объяснив интенсивность различных линий в спектре излучения водорода. С помощью серии математических аналогий он выписал квантовомеханический аналог классического вычисления интенсивностей. [46] Вскоре после этого коллега Гейзенберга Макс Борн понял, что метод Гейзенберга расчета вероятностей переходов между различными уровнями энергии лучше всего можно выразить с помощью математической концепции матриц .
Гейзенберг сформулировал раннюю версию принципа неопределенности в 1927 году, анализируя мысленный эксперимент , в котором пытались одновременно измерить положение и импульс электрона . Однако Гейзенберг не дал точных математических определений того, что означает «неопределенность» в этих измерениях, шаг, который вскоре предприняли Эрл Гессен Кеннард , Вольфганг Паули и Герман Вейль . [47] [48]
Волновая механика [ править ]
В первой половине 1926 года, опираясь на гипотезу де Бройля, Эрвин Шрёдингер разработал уравнение, описывающее поведение квантово-механической волны. [49] Математическая модель, названная в честь ее создателя уравнением Шредингера, занимает центральное место в квантовой механике, определяет разрешенные стационарные состояния квантовой системы и описывает, как квантовое состояние физической системы изменяется во времени. [50] Сама волна описывается математической функцией, известной как « волновая функция ». Шрёдингер сказал, что волновая функция предоставляет «средства прогнозирования вероятности результатов измерений». [51]
Шрёдингер смог рассчитать энергетические уровни водорода, рассматривая электрон атома водорода как классическую волну, движущуюся в яме электрического потенциала, созданного протоном. Этот расчет точно воспроизвел уровни энергии модели Бора.
Гейзенберга В мае 1926 года Шрёдингер доказал, что матричная механика и его собственная волновая механика делают одни и те же предсказания о свойствах и поведении электрона; математически эти две теории имели общую форму. Однако двое мужчин разошлись во мнениях по поводу интерпретации их общей теории. Например, Гейзенберг принял теоретическое предсказание о скачках электронов между орбиталями в атоме: [52] но Шрёдингер надеялся, что теория, основанная на свойствах непрерывных волн, сможет избежать того, что он назвал (в перефразировании Вильгельма Вина ) «этой чепухой о квантовых скачках». [53] В конце концов подход Гейзенберга победил, и квантовые скачки были подтверждены. [54]
Шрёдингер и волновая механика Института Нильса Бора [ править ]

Бор, Гейзенберг и другие пытались объяснить, что на самом деле означают эти экспериментальные результаты и математические модели. Термин «копенгагенская интерпретация» был применен к их взглядам в ретроспективе, замалчивая различия между ними. [55] [56] [57] [58] [59] [60] Хотя четкого утверждения «копенгагенской» интерпретации не существует, следующие идеи широко считаются ее характерными.
- Система полностью описывается квантовым состоянием (Гейзенберг).
- То, как квантовое состояние изменяется со временем, определяется волновым уравнением, уравнением Шредингера, придающим свету и материи волновые характеристики.
- Атомные взаимодействия прерывисты (Планк называл их « квантом действия »).
- Описание природы по существу вероятностно. Вероятность события — например, появления на экране частицы в двухщелевом эксперименте — связана с квадратом абсолютного значения амплитуды ее волновой функции. ( Правило Борна , принадлежащее Максу Борну , которое придает физический смысл волновой функции в копенгагенской интерпретации: амплитуда вероятности )
- Значения несовместимых пар свойств системы не могут быть известны одновременно. Гейзенберга ( принцип неопределенности )
- Материя, как и свет, демонстрирует корпускулярно-волновой дуализм. Эксперимент может продемонстрировать корпускулярные или волновые свойства материи; но не то и другое одновременно. ( Принцип дополнительности Бора [61] )
- Измерительные устройства по сути являются классическими устройствами и измеряют классические свойства, такие как положение и импульс.
- Квантово-механическое описание больших систем должно близко приближаться к классическому описанию. ( Принцип соответствия Бора и Гейзенберга)
Приложение к атому водорода [ править ]
Модель атома Бора была по существу планетарной, с электронами, вращающимися вокруг ядерного «Солнца». Однако принцип неопределенности гласит, что электрон не может одновременно иметь точное местоположение и скорость, как это имеет планета. Говорят, что вместо классических орбит электроны обитают на атомных орбиталях . Орбиталь — это «облако» возможных мест, в которых может быть найден электрон, скорее распределение вероятностей, чем точное местоположение. [62] Каждая орбиталь является трехмерной, а не двумерной орбитой, и часто изображается как трехмерная область, внутри которой существует 95-процентная вероятность найти электрон. [63]
Шрёдингер смог вычислить энергетические уровни водорода, рассматривая электрон атома водорода как волну, представленную « волновой функцией » Ψ в электрической потенциальной яме , V созданной протоном. Решения уравнения Шрёдингера [ нужны разъяснения ] представляют собой распределения вероятностей положений и местоположений электронов. Орбитали имеют различные формы в трех измерениях. Энергии различных орбиталей можно рассчитать, и они точно соответствуют уровням энергии модели Бора.
Согласно картине Шредингера, каждый электрон имеет четыре свойства:
- «Орбитальное» обозначение, указывающее, является ли частица-волна той, которая ближе к ядру с меньшей энергией, или той, которая находится дальше от ядра с большей энергией;
- «Форма» орбиты, сферическая или другая;
- «Наклон» орбитали, определяющий магнитный момент орбитали вокруг оси z .
- «Спин» электрона.
Коллективное название этих свойств — квантовое состояние электрона. Квантовое состояние можно описать, присвоив номер каждому из этих свойств; электрона они известны как квантовые числа . Квантовое состояние электрона описывается его волновой функцией. Принцип исключения Паули требует, чтобы никакие два электрона внутри атома не могли иметь одинаковые значения всех четырех чисел.

Первым свойством, описывающим орбиталь, является главное квантовое число , n которое такое же, как и в модели Бора. n обозначает энергетический уровень каждой орбитали. Возможные значения n — целые числа:
Следующее квантовое число, азимутальное квантовое число , обозначаемое l , описывает форму орбитали. Форма является следствием углового момента орбитали. Угловой момент представляет собой сопротивление вращающегося объекта ускорению или замедлению под действием внешней силы. Азимутальное квантовое число представляет собой орбитальный угловой момент электрона вокруг его ядра. Возможные значения l — целые числа от 0 до n − 1 (где n — главное квантовое число электрона):
Форма каждой орбитали обычно обозначается буквой, а не ее азимутальным квантовым числом. Первая форма ( l =0) обозначается буквой s ( мнемоническое обозначение « сфера »). Следующая фигура обозначается буквой р и имеет форму гантели. Остальные орбитали имеют более сложную форму (см. атомную орбиталь ) и обозначаются буквами d , f , g и т. д.
Третье квантовое число, магнитное квантовое число , описывает магнитный момент электрона и обозначается m l (или просто m ). Возможные значения m l — целые числа от − l до l (где l — азимутальное квантовое число электрона):
Магнитное квантовое число измеряет составляющую углового момента в определенном направлении. Выбор направления произволен; традиционно выбирается направление z.
Четвертое квантовое число, спиновое квантовое число (относящееся к «ориентации» спина электрона) обозначается m s , со значениями + 1 ⁄ 2 или - 1 ⁄ 2 .
Химик Лайнус Полинг писал, например:
В случае атома гелия с двумя электронами на 1 -секундной орбитали принцип исключения Паули требует, чтобы два электрона различались по значению одного квантового числа. Их значения n , l и m l одинаковы. Соответственно они должны отличаться значением m s , которое может иметь значение + 1 ⁄ 2 для одного электрона и — 1 ⁄ 2 для другого». [62]
Именно основная структура и симметрия атомных орбиталей, а также способ их заполнения электронами приводят к организации таблицы Менделеева . То, как атомные орбитали разных атомов объединяются в молекулярные орбитали, определяет структуру и прочность химических связей между атомами.
Пионерами области квантовой химии стали физики Уолтер Гейтлер и Фриц Лондон , опубликовавшие исследование ковалентной связи молекулы водорода в 1927 году. Квантовая химия впоследствии была разработана большим количеством исследователей, в том числе американским химиком-теоретиком Лайнусом Полингом в Калифорнийский технологический институт и Джон Слейтер в различных теориях, таких как теория молекулярных орбиталей или теория валентности.
Дирак, теория относительности и формальных развитие методов
Примерно с 1927 года Поль Дирак начал процесс объединения квантовой механики со специальной теорией относительности , предложив уравнение Дирака для электрона. Уравнение Дирака обеспечивает релятивистское описание волновой функции электрона, которое не удалось получить Шредингеру. Оно предсказывает спин электрона и привело Дирака к предсказанию существования позитрона . Он также был пионером в использовании теории операторов, включая влиятельную систему обозначений скобок , описанную в его знаменитом учебнике 1930 года. В тот же период венгерский эрудит Джон фон Нейман сформулировал строгую математическую основу квантовой механики как теорию линейных операторов в гильбертовых пространствах, как описано в его столь же знаменитом учебнике 1932 года . Они, как и многие другие произведения периода основания, все еще стоят и широко используются.
Квантовая теория поля [ править ]
Начиная с 1927 года исследователи пытались применить квантовую механику к полям, а не к отдельным частицам, что привело к созданию квантовых теорий поля. Среди первых исследователей в этой области — П. А. Дирак , В. Паули, В. Вайскопф и П. Джордан . Эта область исследований завершилась формулировкой квантовой электродинамики Р. П. Фейнманом , Ф. Дайсоном , Дж. Швингером и С. Томонагой в 1940-х годах. Квантовая электродинамика описывает квантовую теорию электронов, позитронов и электромагнитного поля и послужила моделью для последующих квантовых теорий поля . [41] [42] [64]

Теория квантовой хромодинамики была сформулирована в начале 1960-х годов. Теория, какой мы ее знаем сегодня, была сформулирована Политцером , Гроссом и Вильчеком в 1975 году.
Опираясь на новаторские работы Швингера , Хиггса и Голдстоуна , физики Глэшоу , Вайнберг и Салам независимо друг от друга показали, как слабое ядерное взаимодействие и квантовая электродинамика могут быть объединены в одно электрослабое взаимодействие , за что они получили Нобелевскую премию по физике 1979 года.
Квантовая информация [ править ]
Квантовая информатика развивалась в последние десятилетия 20-го века, начиная с таких теоретических результатов, как теорема Холево , концепция обобщенных измерений или POVM , предложение квантового распределения ключей Беннета и Брассара и алгоритм Шора .
эксперименты Основополагающие
- Томаса Янга, демонстрирующий Двухщелевой эксперимент волновую природу света. (ок. 1801 г.)
- Анри Беккерель открыл радиоактивность . (1896)
- Эксперименты Дж. Дж. Томсона с электронно-лучевой трубкой (открытие электрона и его отрицательного заряда). (1897)
- Исследование излучения черного тела между 1850 и 1900 годами, которое нельзя было объяснить без квантовых концепций.
- Фотоэлектрический эффект : Эйнштейн объяснил это в 1905 году (и позже получил за это Нобелевскую премию), используя концепцию фотонов, частиц света с квантованной энергией.
- Эксперимент Роберта Милликена с каплей масла , показавший, что электрический заряд возникает в виде квантов (целых единиц). (1909)
- Эрнеста Резерфорда с Эксперимент золотой фольгой опроверг модель атома сливового пудинга , согласно которой масса и положительный заряд атома распределены почти равномерно. Это привело к созданию планетарной модели атома (1911 г.).
- Джеймса Франка и Густава Герца Эксперимент по столкновению электронов показывает, что поглощение энергии атомами ртути квантовано. (1914)
- Отто Штерн и Вальтер Герлах проводят эксперимент Штерна-Герлаха частицы , который демонстрирует квантованную природу спина . (1920)
- Артур Комптон с экспериментом по комптоновскому рассеянию (1923)
- Клинтон Дэвиссон и Лестер Гермер демонстрируют волновую природу электрона [65] в электронографическом эксперименте. (1927)
- Карл Дэвид Андерсон, открывший позитрон (1932 г.), подтвердил теоретическое предсказание Поля Дирака об этой частице (1928 г.).
- Эксперимент Лэмба – Ретерфорда обнаружил лэмбовский сдвиг (1947 г.), что привело к развитию квантовой электродинамики.
- Клайд Л. Коуэн и Фредерик Райнс подтверждают существование нейтрино в нейтринном эксперименте . (1955)
- Клауса Йонссона Двухщелевой эксперимент с электронами. (1961)
- Квантовый эффект Холла , открытый в 1980 году Клаусом фон Клитцингом . Квантованная версия эффекта Холла позволила определить новый практический стандарт электрического сопротивления и чрезвычайно точное независимое определение постоянной тонкой структуры .
- Экспериментальная проверка квантовой запутанности Джоном Клаузером и Стюартом Фридманом . (1972)
- Эксперимент с интерферометром Маха -Цендера, проведенный Полом Квиатом , Гарольдом Винфуртером, Томасом Херцогом, Антоном Цайлингером и Марком Касевичем, обеспечил экспериментальную проверку бомбового тестера Элицура-Вайдмана и доказал измерения без взаимодействия возможность . (1994)
См. также [ править ]
Ссылки [ править ]
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л Уиттакер, Эдмунд Т. (1989). История теорий эфира и электричества. 2: Современные теории, 1900–1926 гг. (Ред.). Нью-Йорк: Dover Publ. ISBN 978-0-486-26126-3 .
- ^ Макс Борн, Моя жизнь: Воспоминания нобелевского лауреата , Тейлор и Фрэнсис, Лондон, 1978. («Мы все больше и больше убеждались, что необходимо радикальное изменение основ физики, т. е. новый вид механики, для которого мы использовали термин квантовая механика. Это слово впервые появляется в физической литературе в моей статье...")
- ^ Федак, Уильям А.; Прентис, Джеффри Дж. (1 февраля 2009 г.). «Доклад Борна и Джордана 1925 года «О квантовой механике» » (PDF) . Американский журнал физики . 77 (2): 128–139. Бибкод : 2009AmJPh..77..128F . дои : 10.1119/1.3009634 . ISSN 0002-9505 .
- ^ Янг, Томас (1804). «Бейкеровская лекция: Эксперименты и расчеты по физической оптике» . Философские труды Королевского общества . 94 : 1–16. Бибкод : 1804RSPT...94....1Y . дои : 10.1098/rstl.1804.0001 . S2CID 110408369 .
- ^ Бухвальд, Джед (1989). Возникновение волновой теории света: оптическая теория и эксперимент в начале девятнадцатого века . Чикаго: Издательство Чикагского университета. ISBN 978-0-226-07886-1 . OCLC 18069573 .
- ^ Фейнман, Ричард; Лейтон, Роберт; Сэндс, Мэтью (1964). Фейнмановские лекции по физике . Том. 1. Калифорнийский технологический институт. ISBN 978-0201500646 . Проверено 30 сентября 2021 г.
- ^ Пойман, Пол (2020), «Эрнст Мах» , в Залте, Эдвард Н. (редактор), Стэнфордская энциклопедия философии (изд. Зима 2020 г.), Лаборатория метафизических исследований, Стэнфордский университет , получено 30 сентября 2021 г.
- ^ «Фейнмановские лекции по физике, том I, глава 40: Принципы статистической механики» . www.feynmanlectures.caltech.edu . Проверено 10 марта 2024 г.
- ^ Этот результат был опубликован (на немецком языке) как Планк, Макс (1901). «О законе распределения энергии в нормальном спектре» . Энн. Физ. 309 (3): 553–63. Стартовый код : 1901АнП...309..553П . дои : 10.1002/andp.19013090310 . . Английский перевод: «О законе распределения энергии в нормальном спектре» . Архивировано из оригинала 18 апреля 2008 года.
- ^ «Нобелевская премия по физике 1918 года» . Нобелевский фонд . Проверено 1 августа 2009 г.
- ^ Краг, Хельге (1 декабря 2000 г.). «Макс Планк: сопротивляющийся революционер» . PhysicsWorld.com. Архивировано из оригинала 1 апреля 2012 года . Проверено 7 декабря 2009 г.
- ^ Уитон, Брюс Р. (1978). «Филипп Ленард и фотоэлектрический эффект, 1889–1911». Исторические исследования в физических науках . 9 : 299–322. дои : 10.2307/27757381 . JSTOR 27757381 .
- ^ Хокинг, Стивен (6 ноября 2001 г.) [5 ноября 2001 г.]. Коротко о Вселенной . Том. 55. Импи, CD Bantam Spectra (опубликовано в апреле 2002 г.). п. 80~. дои : 10.1063/1.1480788 . ISBN 978-0553802023 . S2CID 120382028 . Архивировано из оригинала 21 сентября 2020 года . Проверено 14 декабря 2020 г. - через аудиокниги Random House.
{{cite book}}:|journal=игнорируется ( помощь ) Альтернативный URL - ^ Jump up to: Перейти обратно: а б Эйнштейн, Альберт (1905). «Об эвристическом взгляде на образование и преобразование света» . Анналы физики . 17 (6): 132–48. Бибкод : 1905АнП...322..132Е . дои : 10.1002/andp.19053220607 . , переведено на английский язык как « С эвристической точки зрения на производство и преобразование света» . Архивировано 11 июня 2009 года в Wayback Machine . Термин «фотон» был введен в 1926 году.
- ^ Фолсинг, Альбрехт (1997), Альберт Эйнштейн: Биография , пер. Эвальд Озерс , Викинг
- ^ Тейлор, младший; Зафиратос, CD; Дубсон, Массачусетс (2004). Современная физика для ученых и инженеров . Прентис Холл. стр. 127–29. ISBN 0135897890 .
- ^ Jump up to: Перейти обратно: а б Тейлор, младший; Зафиратос, CD; Дубсон, Массачусетс (2004). Современная физика для ученых и инженеров . Прентис Холл. стр. 147–48. ISBN 0135897890 .
- ^ МакЭвой, JP; Сарате, О. (2004). Введение в квантовую теорию . Тотемные книги. стр. 70–89, [89]. ISBN 1840465778 .
- ^ World Book.Inc (2007). «22». Всемирная книжная энциклопедия (электронное воспроизведение). Энциклопедия Всемирной книги. Том. 22 (3-е изд.). Чикаго, Иллинойс: Всемирная книга. п. 6. ISBN 978-0716601074 . OCLC 894799866 . Архивировано из оригинала 30 января 2017 года . Проверено 14 декабря 2020 г. Альтернативный URL
- ^ Витке, JP; Дике, Р.Х. (1 июня 1961 г.) [1960]. «11». В Холладее, WG (ред.). Введение в квантовую механику (электронная книга). Том. 16. Нэшвилл, Теннесси: ADDISON WESLEY LONGMAN INC (опубликовано 1 января 1978 г.). п. 10. дои : 10.1063/1.3057610 . ISBN 978-0201015102 . OCLC 53473 . Получено 14 декабря 2020 г. - через Университет Вандербильта.
- ^ Лахтакиа, А (1996). Модели и моделисты водорода: Фалес, Томсон, Резерфорд, Бор, Зоммерфельд, Гаудсмит, Гейзенберг, Шредингер, Дирак, Зальгофер . Сингапур Ривер Эдж, Нью-Джерси: World Scientific. ISBN 981-02-2302-1 . OCLC 35643527 .
- ^ Резерфорд, Э. (1911). «LXXIX. Рассеяние α и β частиц веществом и строение атома». Лондонский, Эдинбургский и Дублинский философский журнал и научный журнал . 21 (125). Информа UK Limited: 669–688. дои : 10.1080/14786440508637080 . ISSN 1941-5982 .
- ^ Оригинальные материалы Сольвеевской конференции 1911 года, опубликованные в 1912 году. ТЕОРИЯ ИЗЛУЧЕНИЯ И КВАНТОВ. ОТЧЕТЫ И ДИСКУССИИ Совещания, проходившего в Брюсселе с 30 октября по 3 ноября 1911 г. под эгидой М. Е. Сольве. Опубликовано ММ. П. ЛАНЖЕВЕН и г-н де БРОЛЬИ. Перевод с французского, стр.447.
- ^ Jump up to: Перейти обратно: а б с Хейлброн, Джон Л.; Кун, Томас С. (1 января 1969 г.). «Происхождение атома Бора». Исторические исследования в физических науках . 1 . Издательство Калифорнийского университета: vi–290. дои : 10.2307/27757291 . ISSN 0073-2672 . JSTOR 27757291 .
- ^ Jump up to: Перейти обратно: а б Хейлброн, Джон Л. (2013). «Путь к квантовому атому». Природа . 498 (7452). ООО «Спрингер Сайенс и Бизнес Медиа»: 27–30. дои : 10.1038/498027a . ISSN 0028-0836 . ПМИД 23739408 . S2CID 4355108 .
- ^ Дж. В. Николсон, Месяц. Нет. Рой. Астр. Соц. lxxxii. стр. 49,130, 677, 693, 729 (1912).
- ^ Jump up to: Перейти обратно: а б МакКорммах, Рассел (1966). «Атомная теория Джона Уильяма Николсона». Архив истории точных наук . 3 (2). ООО «Спрингер Сайенс энд Бизнес Медиа»: 160–184. дои : 10.1007/bf00357268 . ISSN 0003-9519 . S2CID 120797894 .
- ^ Николсон, JW (14 июня 1912 г.). «Конституция солнечной короны. II» . Ежемесячные уведомления Королевского астрономического общества . 72 (8). Издательство Оксфордского университета (OUP): 677–693. дои : 10.1093/mnras/72.8.677 . ISSN 0035-8711 .
- ^ Николсон, JW (1912). «Конституция солнечной короны. III» . Ежемесячные уведомления Королевского астрономического общества . 72 (9). Издательство Оксфордского университета (OUP): 729–740. дои : 10.1093/mnras/72.9.729 . ISSN 0035-8711 .
- ^ Т. Хиросиге и С. Нисио, «Формирование теории атомного строения Бора», яп. Исследования ист. Sci, № 3 (1964), 6-28;
- ^ Дж. Л. Хейлброн, История атомных моделей от открытия электрона до истоков квантовой механики, дисс. (Калифорнийский университет, Беркли, 1964 г.).
- ^ МакКорммах, Рассел (весна 1967 г.), «Анри Пуанкаре и квантовая теория», Isis , 58 (1): 37–55, doi : 10.1086/350182 , S2CID 120934561
- ^ Айронс, Ф. Е. (август 2001 г.), «Доказательство квантовой неоднородности Пуанкаре 1911–12 годов, интерпретируемое как применимое к атомам», American Journal of Physics , 69 (8): 879–84, Bibcode : 2001AmJPh..69..879I , doi : 10.1119/1.1356056
- ^ Jump up to: Перейти обратно: а б Фридрих, Бретислав; Хершбах, Дадли (декабрь 2003 г.). «Штерн и Герлах: как плохая сигара помогла переориентировать атомную физику» . Физика сегодня . 56 (12): 53–59. Бибкод : 2003ФТ....56л..53Ф . дои : 10.1063/1.1650229 . ISSN 0031-9228 .
- ^ Бэгготт, Дж. Э. (2013). Квантовая история: история за 40 мгновений (Впечатление: 3-е изд.). Оксфорд: Оксфордский университет. Нажимать. ISBN 978-0-19-965597-7 .
- ^ Паис, Авраам. «Джордж Уленбек и открытие спина электрона». Физика сегодня 42.12 (1989): 34-40.
- ^ Аксель, Амир Д., Запутывание , стр. 51 и далее. (Пингвин, 2003) ISBN 978-1551926476
- ^ МакЭвой, JP; Сарате, О. (2004). Введение в квантовую теорию . Тотемные книги. п. 114. ИСБН 1840465778 .
- ^ МакЭвой, JP; Сарате, О. (2004). Введение в квантовую теорию . Тотемные книги. п. 87. ИСБН 1840465778 .
- ^ Наварро, Хауме (2010). «Дифракция электронов через Томсона: ранние ответы на квантовую физику в Великобритании» . Британский журнал истории науки . 43 (2): 245–275. дои : 10.1017/S0007087410000026 . ISSN 0007-0874 .
- ^ Jump up to: Перейти обратно: а б Эдвардс, Дэвид А. (1979). «Математические основы квантовой механики». Синтезируйте . 42 (1). ООО «Спрингер Сайенс энд Бизнес Медиа»: 1–70. дои : 10.1007/bf00413704 . ISSN 0039-7857 . S2CID 46969028 .
- ^ Jump up to: Перейти обратно: а б Эдвардс, Дэвид А. (1981). «Математические основы квантовой теории поля: фермионы, калибровочные поля и суперсимметрия, часть I: решетчатые теории поля». Международный журнал теоретической физики . 20 (7). ООО «Спрингер Сайенс энд Бизнес Медиа»: 503–517. Бибкод : 1981IJTP...20..503E . дои : 10.1007/bf00669437 . ISSN 0020-7748 . S2CID 120108219 .
- ^ Ханле, Пенсильвания (декабрь 1977 г.), «Реакция Эрвина Шредингера на диссертацию Луи де Бройля по квантовой теории», Isis , 68 (4): 606–609, doi : 10.1086/351880 , S2CID 121913205
- ^ Паули, Вольфганг (1 мая 1926 г.). «О спектре водорода с точки зрения новой квантовой механики». Журнал физики (на немецком языке). 36 (5): 336–363. Бибкод : 1926ZPhy...36..336P . дои : 10.1007/BF01450175 . ISSN 0044-3328 . S2CID 128132824 .
- ^ Менсинг, Люси (1 ноября 1926 г.). «Полосы вращательных колебаний согласно квантовой механике». Журнал физики (на немецком языке). 36 (11): 814–823. Бибкод : 1926ZPhy...36..814M . дои : 10.1007/BF01400216 . ISSN 0044-3328 . S2CID 123240532 .
- ^ Ван дер Варден, БЛ (1967). Источники квантовой механики . Минеола, Нью-Йорк: Dover Publications. стр. 261–76.
Поступило 29 июля 1925 г.
См. статью Вернера Гейзенберга «Квантово-теоретическая переинтерпретация кинематических и механических соотношений», стр. 261–76. - ^ Буш, Пол ; Лахти, Пекка; Вернер, Рейнхард Ф. (17 октября 2013 г.). «Доказательство соотношения ошибки и возмущения Гейзенберга». Письма о физических отзывах . 111 (16): 160405. arXiv : 1306.1565 . Бибкод : 2013PhRvL.111p0405B . doi : 10.1103/PhysRevLett.111.160405 . ISSN 0031-9007 . ПМИД 24182239 . S2CID 24507489 .
- ^ Эпплби, Дэвид Маркус (6 мая 2016 г.). «Квантовые ошибки и возмущения: ответ Бушу, Лахти и Вернеру» . Энтропия . 18 (5): 174. arXiv : 1602.09002 . Бибкод : 2016Entrp..18..174A . дои : 10.3390/e18050174 .
- ^ Организация Нобелевской премии. «Эрвин Шрёдингер – Биографический» . Проверено 28 марта 2014 г.
Его великое открытие — волновое уравнение Шредингера — было сделано в конце этой эпохи — в первой половине 1926 года.
- ^ «Уравнение Шрёдингера (физика)», Британская энциклопедия
- ^ Эрвин Шрёдингер, «Современная ситуация в квантовой механике», с. 9. «Этот перевод был первоначально опубликован в Proceedings of the American Philosophical Society, 124, 323–38, а затем появился как Раздел I.11 Части I книги «Квантовая теория и измерение» (Дж. А. Уилер и В. Х. Зурек, ред., Принстонский университет). Пресс, Нью-Джерси, 1983). Эту статью можно скачать здесь: Эрвин Шрёдингер. «Перевод «Кошачьего парадокса» Шрёдингера » . Перевод Джона Д. Триммера. Архивировано из оригинала 13 ноября 2010 г.
- ^ Гейзенберг, В. (1955). Развитие интерпретации квантовой теории, стр. 12–29 в книге « Нильс Бор и развитие физики: очерки, посвященные Нильсу Бору по случаю его семидесятилетия» , под редакцией Паули В. при содействии Розенфельда Л. и . Вайскопф В. , Пергамон, Лондон, с 13: «Одиночный квантовый скачок… «реален» по своей природе».
- ^ В. Мур, Шрёдингер: жизнь и мысль , издательство Кембриджского университета (1989), стр. 222. См. с. 227, собственные слова Шрёдингера.
- ^ Глейк, Джеймс (21 октября 1986 г.). «Физики наконец-то смогут увидеть квантовый скачок собственными глазами» . Нью-Йорк Таймс . Проверено 30 ноября 2019 г.
- ^ Фэй, Ян (2019). «Копенгагенская интерпретация квантовой механики» . В Залте, Эдвард Н. (ред.). Стэнфордская энциклопедия философии . Лаборатория метафизических исследований Стэнфордского университета.
- ^ Камиллери, К.; Шлоссхауэр, М. (2015). «Нильс Бор как философ эксперимента: бросает ли теория декогеренции вызов доктрине классических концепций Бора?». Исследования по истории и философии современной физики . 49 : 73–83. arXiv : 1502.06547 . Бибкод : 2015ШПМП..49...73С . дои : 10.1016/j.shpsb.2015.01.005 . S2CID 27697360 .
- ^ Омнес, Роланд (1999). «Копенгагенская интерпретация». Понимание квантовой механики . Издательство Принстонского университета. стр. 41–54. дои : 10.2307/j.ctv173f2pm.9 . S2CID 203390914 .
- ^ Шайбе, Эрхард (1973). Логический анализ квантовой механики . Пергамон Пресс. ISBN 9780080171586 . OCLC 799397091 .
[T]нет смысла искать копенгагенскую интерпретацию как единую и непротиворечивую логическую структуру. Такие термины, как «Копенгагенская интерпретация» или «Копенгагенская школа», основаны на истории развития квантовой механики; они представляют собой упрощенный и часто удобный способ ссылки на идеи ряда физиков, сыгравших важную роль в становлении квантовой механики и которые были сотрудниками Бора в его Институте или принимали участие в дискуссиях в решающие годы. При ближайшем рассмотрении довольно легко увидеть, что эти идеи расходятся в деталях и что, в частности, взгляды Бора, духовного лидера школы, образуют отдельную целостность, которую теперь можно понять только путем тщательного изучения как можно большего числа соответствующих публикаций самого Бора.
- ^ Перес, Ашер (2002). «Эксперимент Поппера и копенгагенская интерпретация». Исследования по истории и философии современной физики . 33 : 23. arXiv : quant-ph/9910078 . Бибкод : 1999quant.ph.10078P . дои : 10.1016/S1355-2198(01)00034-X .
Кажется, существует по крайней мере столько же различных интерпретаций Копенгагена, сколько людей, использующих этот термин; возможно, их больше.
- ^ Мермин, Н. Дэвид (01 января 2017 г.). «Почему кбизм не является копенгагенской интерпретацией и что мог об этом подумать Джон Белл». В Бертльманне, Рейнгольде; Цайлингер, Антон (ред.). Квантовые [Un]Speakables II . Коллекция «Границы». Международное издательство Спрингер. стр. 83–93. arXiv : 1409.2454 . дои : 10.1007/978-3-319-38987-5_4 . ISBN 9783319389851 . S2CID 118458259 .
- ^ Бор, Н. (1928). «Квантовый постулат и новейшее развитие атомной теории» . Природа . 121 (3050): 580–590. Бибкод : 1928Natur.121..580B . дои : 10.1038/121580a0 . Доступен в сборнике ранних сочинений Бора «Теория атома и описание природы» (1934).
- ^ Jump up to: Перейти обратно: а б Полинг, Лайнус (1960). Природа химической связи (3-е изд.). Итака, Нью-Йорк: Издательство Корнельского университета. п. 47 . ISBN 0801403332 . Проверено 1 марта 2016 г.
- ^ «Орбиталь (химия и физика)», Британская энциклопедия.
- ^ С. Ауян, Как возможна квантовая теория поля? , Издательство Оксфордского университета, 1995.
- ^ Эксперимент Дэвиссона-Гермера, демонстрирующий волновую природу электрона.
Дальнейшее чтение [ править ]
- Баччагалуппи, Гвидо; Валентини, Энтони (2009), Квантовая теория на распутье: пересмотр Сольвеевской конференции 1927 года , Кембридж, Великобритания: Cambridge University Press, стр. 9184, arXiv : quant-ph/0609184 , Bibcode : 2006quant.ph..9184B , ISBN 978-0-521-81421-8 , OCLC 227191829
- Бернштейн, Джереми (2009), Quantum Leaps , Кембридж, Массачусетс: Belknap Press of Harvard University Press, ISBN 978-0-674-03541-6
- Гринбергер, Дэниел, Хентшель, Клаус , Вайнерт, Фридель (ред.) Справочник по квантовой физике . Концепции, эксперименты, история и философия , Нью-Йорк: Springer, 2009. ISBN 978-3-540-70626-7 .
- Джаммер, Макс (1966), Концептуальное развитие квантовой механики , Нью-Йорк: McGraw-Hill, OCLC 534562.
- Джаммер, Макс (1974), Философия квантовой механики: интерпретации квантовой механики в исторической перспективе , Нью-Йорк: Wiley, ISBN 0-471-43958-4 , OCLC 969760
- А. Уитакер. Новый квантовый век: от теоремы Белла к квантовым вычислениям и телепортации , Oxford University Press, 2011, ISBN 978-0-19-958913-5
- Стивен Хокинг. Мечты, из которых сделаны вещи , Running Press, 2011, ISBN 978-0-76-243434-3
- А. Дуглас Стоун. Эйнштейн и квант, поиски доблестного шваба , Princeton University Press, 2006.






















