Тиол

В органической тиол θ ( / ˈ l aɪ ɒ / ; химии [ 1 ] от древнегреческого θεῖον (theion) ' сера ' [ 2 ] ), или производное тиола , является любого органосульфурного соединения формы R -sh , где R представляет собой алкил или другой органический заместитель . А –sh Сама функциональная группа называется либо тиольной группой , либо сульфгидрил -группой , либо сульфанильной группой . Тиолы являются аналогом спиртов серы (то есть сера занимает место кислорода в гидроксиле ( −oh ) группа алкоголя), и это слово представляет собой смесь « тио- » с «алкоголем».
Многие тиолы имеют сильные запахи, напоминающие чеснок или гнилые яйца. Тиолы используются в качестве одорантов, чтобы помочь в обнаружении природного газа (который в чистом виде не является запахом), а «запах природного газа» обусловлен запахом тиола, используемого в качестве одоранта. Тиолы иногда называют Меркаптанами ( / M ər ˈ K æ P T æ N / ) [ 3 ] или соединения Mercapto , [ 4 ] [ 5 ] [ 6 ] Термин, представленный в 1832 году Уильямом Кристофером Зейзом и получен из латинских каппонов Mercurio («захват Меркурия») [ 7 ] Потому что тиолатная группа ( Рупий − ) Очень сильно с помощью ртутных соединений. [ 8 ]
Структура и связь
[ редактировать ]Тиолы, имеющие структуру r - SH, в которой алкильная группа (R) прикреплена к сульфгидрил -группе (SH), называются алканетиолами или алкил -тиолами . [ 9 ] Тиолы и спирты имеют сходную связь. Поскольку атомы серы больше, чем атомы кислорода, длина связей C -S - обычно около 180 пикометрий - примерно на 40 пикометров длиннее типичных связей C -O. Углы C - S -H приближаются к 90 °, тогда как угол для группы C -O -H более тупой. У твердых веществ и жидкостей водородное соединение между отдельными тиольскими группами является слабым, основной сплоченной силой является взаимодействие ван-дер-ваальса между высоко поляризуемыми дивалентными центрами серы.
Связь S - H намного слабее, чем связь O -H, как отражена в их соответствующих энергиях диссоциации связи (BDE). Для CH 3 S - H BDE составляет 366 кДж/моль (87 ккал/моль), а для CH 3 O - H BDE - 440 кДж/моль (110 ккал/моль). [ 10 ]
Связь S -H является умеренно полярной из -за небольшой разницы в электроотрицательности серы и водорода. Напротив, связи O -H в гидроксильных группах более полярные. Тиолы имеют более низкий дипольный момент по сравнению с соответствующими спиртами.
Номенклатура
[ редактировать ]Есть несколько способов назвать алкилтиолы:
- Суффикс -Thiol добавляется к названию Алкане. Этот метод почти идентичен названию алкоголя и используется IUPAC , например, CH 3 SH будет метанетиолом .
- Слово Меркаптан заменяет алкоголь во имя эквивалентного спиртового соединения. Пример: CH 3 SH будет метилкаптан, так же, как CH 3 OH называется метиловым спиртом.
- Термин сульфгидрил- или меркапт- используется в качестве префикса, например, Mercaptopurine .
Физические свойства
[ редактировать ]Запах
[ редактировать ]Многие тиолы имеют сильные запахи, напоминающие запах чеснока . Запахи тиолов, особенно запахи с низкой молекулярной массой, часто являются сильными и отталкивающими. Брызги скунков состоит в основном из низкомолекулярных тиолов и производных. [ 11 ] [ 12 ] [ 13 ] [ 14 ] [ 15 ] Эти соединения обнаруживаются человеческим носом в концентрациях всего 10 частей на миллиард. [ 16 ] Человеческий пот содержит ( r )/( s ) -3-метил-3-меркапто-1-ол (MSH), обнаруживается по 2 частям на миллиард и имеет фруктовый, луковичный запах. (Метилтио) Метанатиол (Mesch 2 SH; MTMT) является сильным изменчивым летучести, также обнаруживаемым на уровнях частей на миллиард, обнаруженных в моче мыши . Лоуренс С. Кац и коллеги показали, что MTMT функционировал как полуохимические , активируя некоторые обонятельные сенсорные нейроны мыши и притягивающие самки мышей . [ 17 ] Было показано, что медь требуется специфическим обонятельным рецептором мыши, MOR244-3, который очень реагирует на MTMT, а также на различные другие тиолы и связанные с ними соединения. [ 18 ] Был идентифицирован обонятельный рецептор человека, OR2T11 , который, в присутствии меди, очень реагирует на газовые одоранты (см. Ниже) этанатиол и T -Бутил Меркаптан , а также другие тиолы с низкой молекулярной массой, в том числе аллил Меркаптан, обнаруженные у человека Чесновое дыхание и сильное циклическое сульфидное вожденое . [ 19 ]
Тиолы также ответственны за класс ошибок вина , вызванные непреднамеренной реакцией между серной и дрожжами , и «скунхим» запаха пива, который подвергался воздействию ультрафиолетового света.
Не все тиолы имеют неприятные запахи. Например, Furan-2-илметанетиол способствует аромату жареного кофе , тогда как грейпфрут Mercaptan , монотерпеноид тиола, отвечает за характерный аромат грейпфрута . Эффект последнего соединения присутствует только при низких концентрациях. Чистый Меркаптан имеет неприятный запах.
В Соединенных Штатах дистрибьюторы природного газа должны были добавить тиолов, первоначально этантиол , к природному газу (который естественно без запаха) после смертельного взрыва школы в Нью -Лондоне в Нью -Лондоне, штат Техас , в 1937 году. это событие. Большинство в настоящее время используемые газовые отдольты содержат смеси меркаптанов и сульфидов, с T -бутиловым серкаптаном в качестве основного запаха, составляющей природного газа и этана в сжиженном нефтяном газе (LPG, пропан). [ 20 ] В ситуациях, когда тиолы используются в коммерческой промышленности, таких как жидкие нефтяные газовые баки и объемные системы обработки, окислительный катализатор для уничтожения запаха используется . Катализатор окисления на основе меди нейтрализует летучие тиолы и превращает их в инертные продукты.
Точки кипения и растворимость
[ редактировать ]Тиолы показывают небольшую связь с помощью водородной связи , как с молекулами воды, так и между собой. Следовательно, они имеют более низкие точки кипения и менее растворимы в воде и других полярных растворителях, чем спирты сходной молекулярной массы. По этой причине также тиолы и их соответствующие изомеры функциональной группы сульфидной группы имеют сходные характеристики растворимости и точки кипения, тогда как то же самое не относится к спиртам и соответствующим их изомерным эфирам.
Связывание
[ редактировать ]Связь S - H в тиолах слаба по сравнению с связью O -H в спиртах. Для Ch 3 x - H энтальпии связи составляют 365,07 ± 2,1 ккал/моль для x = s и 440,2 ± 3,0 ккал/моль для x = o. [ 21 ] Абстракция с водородом от тиола дает титил радикал с формулой RS • , где r = алкил или арил.
Характеристика
[ редактировать ]Летучие тиолы легко и почти безошибочно обнаруживаются из -за их отличительного запаха. Специфичные для серы для газовых хроматографов полезны. Спектроскопические индикаторы являются D 2 O -обмена S H SIGNAL в 1 H ЯМР спектр ( 33 S -АКТВЕРЖДЕНИЕ ЯМР , но сигналы для двухвалентной серы очень широкие и мало полезности [ 22 ] ) Группа ν SH появляется около 2400 см −1 в ИК -спектре . [ 4 ] В реакции нитропрассида свободные тиоловые группы реагируют с нитропрассидом натрия и гидроксидом аммония с получением красного цвета.
Подготовка
[ редактировать ]В промышленности метанатиол готовится реакцией сероводорода с помощью метанола . Этот метод используется для промышленного синтеза метанатиола :
- CH 3 OH + H 2 S → CH 3 SH + H 2 O
Такие реакции проводятся в присутствии кислых катализаторов. Другой основной путь к тиолам включает добавление сероводорода в алкены . Такие реакции обычно проводятся в присутствии кислотного катализатора или ультрафиолетового света. галогенидов с использованием подходящего органического галогенида и серо водорода натрия. Также использовалось смещение [ 23 ]
Другой метод влечет за собой алкилирование гидросульфида натрия .
- RX + NaSH → RSH + NaX (X = Cl, Br, I)
Этот метод используется для выработки тиогликолевой кислоты из хлоруаксусной кислоты .
Лабораторные методы
[ редактировать ]В целом, в типичной лабораторной масштабе прямая реакция галоалкана с гидросульфидом натрия эффективна из -за конкурирующего образования сульфидов. Вместо этого алкилгалогениды преобразуются в тиолы посредством s -алкилирования тиомочевины . Этот многоэтапный процесс проходит через однопот через промежуточную соль изотиорониум , которая гидролизуется на отдельном этапе: [ 24 ] [ 25 ]
- CH 3 CH 2 BR + SC (NH 2 ) 2 → [CH 3 CH 2 SC (NH 2 ) 2 ] BR
- [Ch 3 ch 2 sc (nh 2 ) 2 ] br + naoh → ch 3 ch 2 sh + oc (nh 2 ) 2 + nabr
Маршрут ThioRea хорошо работает с первичными галогениками, особенно активированными. Вторичные и третичные тиолы менее легко подготовлены. Вторичные тиолы могут быть приготовлены из кетона через соответствующие дитиокеталы . [ 26 ] Связанный двухэтапный процесс включает в себя алкилирование тиосульфата с получением тиосульфоната (« соль Bunte ») с последующим гидролизом. Метод иллюстрируется одним синтезом тиогликолевой кислоты :
- CLCH 2 CO 2 H + NA 2 S 2 O 3 → NA [O 3 S 2 CH 2 CO 2 H] + NaCl
- Na[O 3 S 2 CH 2 CO 2 H] + H 2 O → HSCH 2 CO 2 H + NaHSO 4
Соединения органолита и реагенты Grignard реагируют с серной, давая тиолаты, которые легко гидролизуются: [ 27 ]
- Rli + s → rsli
- Rsli + hcl → rsh + licl
Фенолы могут быть преобразованы в тиофенолы посредством перегруппировки их o -maril диалкилтиокарбаматов. [ 28 ]
Тиолы готовится за счет восстановительного сделки сульфидов, особенно бензильных производных и тиоацеталов. [ 29 ]
Тиофенолы продуцируются с помощью S -арилирования или замены группы, выходящей из диазония на сульфгидрил (SH − ): [ 30 ] [ 31 ]
- Арн +
2 + sh − → ARSH + N 2
Реакция
[ редактировать ]Сродни химии спиртов, тиолов образуют сульфиды , тиоацеталы и тиоэфиры , которые аналогичны эфирам , ацеталам и эфирам соответственно. Тиолы и спирты также очень различаются по своей реактивности, тиолы легче окисляются, чем спирты. Тиолаты являются более мощными нуклеофилами, чем соответствующие алкоксиды .
S -alkylation
[ редактировать ]Тиолы, или, более специфичные их конъюгатные основания, легко алкилируются, чтобы дать сульфиды:
- Rsh + r'br + b → rsr ′ + [hb] br (b = base)
Кислотность
[ редактировать ]Тиолы легко депротонируются. [ 32 ] По сравнению с спиртами тиолы более кислые. Конъюгатное основание тиола называется тиолатом . Бутанетиол имеет P k a 10,5 против 15 для бутанола. Тиофенол имеет P k a 6, против 10 для фенола . Высококислый тиол - пентафторотиофенол (C 6 F 5 SH) с AP K A 2,68. Таким образом, тиолаты могут быть получены из тиолов путем обработки гидроксидами щелочных металлов.

Окислительно -восстановительный
[ редактировать ]Тиолы, особенно при наличии основания, легко окисляются реагентами, такими как бром и йод, чтобы получить органический дисульфид (r -s -s -r).
- 2 r -sh + br 2 → r -s -s -r + 2 hbr
Окисление более мощными реагентами, такими как гипохлорит натрия или перекись водорода, также может дать сульфоновые кислоты (RSO 3 H).
- R - sth + 3 H 2 O 2 → RSO 3 H + 3 H 2 O
Окисление также может осуществляться кислородом в присутствии катализаторов: [ 33 ]
- 2 r - -sho + 1 ⁄ 2 o 2 → RS -Sr + H 2 O
Тиолы участвуют в тиоло-дисульфидном обмене:
- Lol + 2 r'sh → 2 rsh + r's - sr ′
Эта реакция важна по своей природе.
Металлический ионный комплекс
[ редактировать ]С ионами металлов тиолаты ведут себя как лиганды, образуя тиолатные комплексы переходных металлов . Термин «Меркаптан» получен из латинского каппана Mercurium (захват Меркурия) [ 7 ] Потому что тиолатная группа так сильно связана с соединениями ртуть . Согласно теории твердой/мягкой кислоты/основания (HSAB) , сера является относительно мягким (поляризуемым) атом. Это объясняет тенденцию тиолов связываться с мягкими элементами и ионами, такими как ртуть, свинец или кадмий. Стабильность металлических тиолатов параллельны соответствующим сульфидным минералам.
Тиоксантаты
[ редактировать ]Тиолаты реагируют с дисульфидом углерода с получением тиоксантата ( RSCS −
2 ).
Тиил радикалы
[ редактировать ]Свободные радикалы, полученные из Меркаптанов, называемых тиельными радикалами , обычно вызываются для объяснения реакций в органической химии и биохимии . У них есть формула RS • где r является органическим заместителем, таким как алкил или арил . [ 6 ] Они возникают из или могут быть сгенерированы рядом маршрутов, но основным методом является абстракция H-атом от тиолов. Другой метод включает гомолиз органических дисульфидов. [ 34 ] В биологии THIYL радикалы отвечают за образование дезоксирибонуклеиновых кислот, строительных блоков для ДНК . Это преобразование катализируется рибонуклеотидной редуктазой (см. Рисунок). [ 35 ] Thiyl Intermediates также продуцируются окислением глутатиона , антиоксиданта в биологии. Thiyl-радикалы (сера, ориентированные) могут трансформироваться в углеродные радикалы через водорода обмена атома равновесия . Образование углеродных радикалов может привести к повреждению белка посредством образования связей C -C или фрагментации основной цепи. [ 36 ]
Из -за слабости связи S -H тиолы могут функционировать как мусорщики свободных радикалов . [ 37 ]
Биологическая важность
[ редактировать ]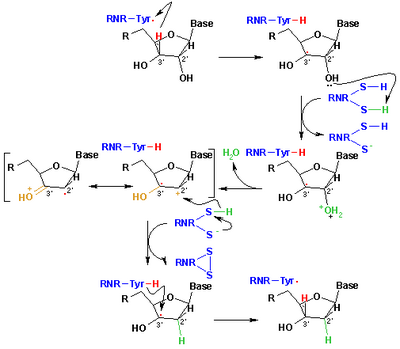
Цистеин и цистин
[ редактировать ]Как функциональная группа аминокислотного цистеина , Thiol Group играет очень важную роль в биологии. Когда тиольные группы двух остатков цистеина (как у мономеров или составляющих единиц) приближаются друг к другу в ходе складывания белка , реакция окисления может генерировать цистинную единицу с дисульфидной связью (-S-S-). белка, Дисульфидные связи могут способствовать третичной структуре если цистеины являются частью одной и той же пептидной цепи или способствуют четвертичной структуре многонациональных белков, образуя довольно сильные ковалентные связи между различными пептидными цепями. Физическое проявление цистеин-цистинового равновесия обеспечивается технологиями выпрямления волос . [ 38 ]
Сульфгидрильные группы в активном месте фермента , способствуя ковалентной каталитической могут образовывать нековалентные связи фермента с подложкой также активности в каталитических триадах . Остатки цистеина активного участка являются функциональной единицей в цистеиновых протеазовых каталитических триадах . Остатки цистеина также могут реагировать с ионами тяжелых металлов (Zn 2+ , CD 2+ , Pb 2+ , Hg 2+ , К + ) из -за высокой аффинности между мягким сульфидом и мягким металлом (см. твердые и мягкие кислоты и основания ). Это может деформировать и инактивировать белок и является одним из механизмов отравления тяжелыми металлами .
Препараты, содержащие тиоловую группу 6-меркаптопурин (противоопухолевые) Каптоприл (антигипертензивный) D-пеницилламина (антиартритный) Ауротиолат натрия (антиартритный) [ 39 ]
Кофакторы
[ редактировать ]Многие кофакторы (небетральные вспомогательные молекулы) оснащены тиолами. Биосинтез и деградация жирных кислот и связанных с ними длинноцепочечных углеводородов проводятся на каркасе, который закрепляет растущую цепь через тиоэфир, полученный из тиолового кофермента а . Биосинтез коферментом метана M , основного углеводорода на Земле, возникает из реакции, опосредованной , 2-меркаптоэтиловой сульфоновой кислотой. Тиолаты, конъюгатные основания, полученные из тиолов, образуют сильные комплексы со многими ионами металлов, особенно те, которые классифицируются как мягкие. Стабильность металлических тиолатов параллельны соответствующим сульфидным минералам.
В скунках
[ редактировать ]Оборонительная спрей Скунков состоит в основном из тиолов и производных низкомолекулярного веса и производных с грязным запахом, который защищает скунс от хищников. Совы могут охотиться на скунсов, так как им не хватает обоняния. [ 40 ]
Примеры тиолов
[ редактировать ]- Метанетиол - CH 3 SH [метилкаптан]
- Этантиол - C 2 H 5 SH [этилкаптан]
- 1 -пропанетиол -C 3 H 7 SH [ N -Propyl Mercaptan]
- 2-пропанетиол -Ch 3 CH (SH) Ch 3 [2C3 Mercaptan]
- Аллил Меркаптан -CH 2 = CHCH 2 SH [2-пропенетиол]
- Бутанетиол -C 4 H 9 SH [ n -Бутил -Меркаптан]
- ТЕРТ -Бутил Меркаптан -(Ch 3 ) 3 CSH [ T -Бутил -Меркаптан]
- Пентанетиолы - C 5 H 11 SH [Pentylyler Mercaptan]
- Тиофенол - C 6 H 5 SH
- Димеркаптосукциновая кислота
- Тиоаксусная кислота
- Коэнзим а
- Глутатион
- Metallothionein
- Цистеин
- 2-меркаптоэтанол
- Dithiothreitol / Dithiorythritol ( эпимерная пара)
- 2-меркаптоиндоль
- Грейпфрут Меркаптан
- Фуран-2-илметанетиол
- 3-меркаптопропановый-1,2-диол
- 3-меркапто-1-пропанесульфоновая кислота
- 1-гексадеканетиол
- Пентахлорбензентиол
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Ссылка на словарь : Тиол архивировал 2013-04-11 на машине Wayback
- ^ θεῖον архив 2017-05-10 в The Wayback Machine , Генри Джордж Лидделл, Роберт Скотт, грек-английский лексикон
- ^ Ссылка на словарь : Mercaptan Archived 2012-11-13 на машине Wayback
- ^ Подпрыгнуть до: а беременный Patai, Saul, ed. (1974). Химия тиоловой группы. Часть 1 . Лондон: Wiley. doi : 10.1002/9780470771310 . ISBN 9780470771310 .
- ^ Patai, Saul, ed. (1974). Химия тиоловой группы. Часть 2 . Лондон: Wiley. doi : 10.1002/9780470771327 . ISBN 9780470771327 .
- ^ Подпрыгнуть до: а беременный Р.Дж. Кремлин (1996). Введение в химию органосульфы . Чичестер: Джон Уайли и сыновья. ISBN 978-0-471-95512-2 .
- ^ Подпрыгнуть до: а беременный Оксфордские американские словаря ( Mac OS X Leopard ).
- ^ См.:
- Zeise, William Christopher (1834). "Mercaptanet, med bemaerkninger over nogle andre nye producter af svovelvinsyresaltene, som og af den tunge vinolie, ved sulfureter" [Mercaptan, with remarks on some other new products of salts of ethyl hydrogen sulfate as well as of heavy oil of wine, by means of hydrogen sulfide]. Kongelige Danske Videnskabers Selskabs Skrifter. 4th series (in Danish). 6: 1–70. On p. 13 the word "mercaptan" is coined.
- Немецкий перевод: Зейз, туалет (1834). «Меркаптан, в дополнение к некоторым новым продуктам от влияния серы на соли с кислотами для вина и на винное масло» [Mercaptan вместе с комментариями о некоторых новых продуктах от влияния сероводорода на соли этилсульфата ((C 2 H 5 ) HSO 4 ) и тяжелое масло вина (смесь диэтилсульфата, диэтилсульфита и полимеризованного этилена)]. Анналы физики и химии . 2 -я серия (на немецком языке). 31 (24): 369–431. От р. 378: «… Я называю торговую ткань Mercaptum (от: Corpus Mercurio Captum ) ...» (… Я называю вещество [которое] поглощено ртути по ртути) ...)
- Немецкий перевод перепечатан в: Zeise, W. C. (1834). "Das Mercaptan, nebst Bemerkungen über einige andere neue Erzeugnisse der Wirkung schwefelweinsaurer Salze, wie auch des schweren Weinöls auf Sulphurete". Journal für Praktische Chemie. 1 (1): 257–268, 345–356, 396–413, 457–475. doi:10.1002/prac.18340010154.
- Суммировано в: Zeise, WC (1834). "Ueber Das Mercaptan" [на Mercaptan]. Annalen der Pharmacie . 11 (1): 1–10. Doi : 10.1002/jlac.18340110102 . Архивировано с оригинала 2015-03-20.
- Зейз, Уильям Кристофер (1834). «Sur le Mercaptan; avec des наблюдения Sur d'Autres produits результируют de l'Action des sulfovinates ainsi que de l'huile de vin, sur des sulfures metalliques» [на Mercaptan; С наблюдениями на других продуктах, возникающих в результате действия сульфовинатов [обычно, этил -водорода, а также масла вина [смесь диэтилсульфата и этилен -полимеров] на сульфидах металла]. Annales de Chimie et dehique . 56 : 87–97. Архивировано с оригинала 2015-03-20. «Меркаптан» (этил тиол) был обнаружен в 1834 году датским профессором химии Уильям Кристофер Зейз (1789–1847). Он назвал это «Меркаптан», сокращением «Корпус Меркурио Каптанс» (вещество капитала ртути) [с. 88], потому что он насильственно реагировал с оксидом ртути («Deutoxide de Mercure») [с. 92].
- Статья в «Анналах» Чими и Физика (1834) была переведена из немецкой статьи: Зейз, туалет (1834). «Меркаптан, наряду с комментариями о некоторых новых продуктах от влияния серы на соли винной кислоты и на винном масле» . Анналы физики и химии . 107 (27): 369–431. Bibcode : 1834anp ... 107..369Z . Doi : 10.1002/andp.18341072402 . Архивировано с оригинала 2015-03-20.
- ^ «Алканетиолы» . Королевское общество химии . Получено 4 сентября 2019 года .
- ^ Lide, David R., ed. (2006). Справочник по химии и физике CRC (87 -е изд.). Boca Raton, FL: CRC Press . ISBN 0-8493-0487-3 .
- ^ Андерсен К.К.; Бернштейн Д.Т. (1978). «Некоторые химические компоненты аромата полосатого скунса ( мефит мефит )». Журнал химической экологии . 1 (4): 493–499. doi : 10.1007/bf00988589 . S2CID 9451251 .
- ^ Андерсен К.К., Бернштейн Д.Т.; Бернштейн (1978). «1-бутанетиол и полосатый скунс». Журнал химического образования . 55 (3): 159–160. Bibcode : 1978jched..55..159a . doi : 10.1021/ed055p159 .
- ^ Андерсен К.К.; Бернштейн DT; Каретка RL; Romanczyk LJ, Jr. (1982). «Химические компоненты защитной секреции полосатого скунса ( мефит мефит )». Тетраэдр . 38 (13): 1965–1970. doi : 10.1016/0040-4020 (82) 80046-x .
- ^ Дерево WF; Sollers BG; DragoO GA; Dragoo JW (2002). «Платильные компоненты в защитном распылении скунса с капюшоном, Mephitis macroura ». Журнал химической экологии . 28 (9): 1865–70. doi : 10.1023/a: 1020573404341 . PMID 12449512 . S2CID 19217201 .
- ^ Уильям Ф. Вуд. «Химия скунса спрея» . Департамент химии, Государственный университет Гумбольдта . Архивировано из оригинала 8 октября 2010 года . Получено 2 января 2008 года .
- ^ Олдрич, Т.Б. (1896). «Химическое исследование секреции анальных желез мефиита Мефитига (общий скунс) с замечаниями о физиологических свойствах этой секреции» . J. Exp. Медик 1 (2): 323–340. doi : 10.1084/jem.1.2.323 . PMC 2117909 . PMID 19866801 .
- ^ Лин, Дейу; Чжан, Шаочхон; Блок, Эрик; Кац, Лоуренс С. (2005). «Кодирование социальных сигналов в основной обонятельной лампочке мыши». Природа . 434 (7032): 470–477. Bibcode : 2005natur.434..470L . doi : 10.1038/nature03414 . PMID 15724148 . S2CID 162036 .
- ^ Дуан, Сюфанг; Блок, Эрик; Ли, Чжэнь; Коннелли, Тимоти; Чжан, Цзянь; Хуан, Жимин; Su, xubo; Пан, Yi; и др. (2012). «Важнейшая роль меди в обнаружении металлических координационных одорантов» . Прокурор Нат. Академический Наука США . 109 (9): 3492–3497. Bibcode : 2012pnas..109.3492d . doi : 10.1073/pnas.1111297109 . PMC 3295281 . PMID 22328155 .
- ^ «Медный ключ к нашей чувствительности к нечестному запаху яиц» . Chemistryworld.com . Архивировано из оригинала 10 мая 2017 года . Получено 3 мая 2018 года .
- ^ Робертс, JS, изд. (1997). Кирк-Отмер Энциклопедия химических технологий . Вейнхайм: Wiley-VCH. [ страница необходима ]
- ^ Luo, Y.-r.; Ченг, J.-P. (2017). «Энергии диссоциации связи». В Jr Rumble (ред.). Справочник по химии и физике . CRC Press.
- ^ Man, Pascal P. "Ссылки на ЯМР серы-33" . www.pascal-man.com . Архивировано из оригинала 23 августа 2017 года . Получено 3 мая 2018 года .
- ^ John S Roberts, «Тиолы», в кирк-отмерской энциклопедии химических технологий , 1997, Wiley-VCH, Вайнхайм. Два : 10.1002/0471238961.2008091518150205.a01
- ^ Speziale, AJ (1963). "Ethanedithiol" . Органические синтезы ; Собранные объемы , вып. 4, с. 401 ..
- ^ Urquhart, GG; Gates, JW Jr.; Коннор, Ральф (1941). « N -додецил Меркаптан». Орг Синтезатор 21 : 36. doi : 10.15227/orgsyn.021.0036 .
- ^ SR Wilson, GM Georgiadis (1990). «Мекаптаны из тиокеталов: циклододецил Меркаптан» . Органические синтезы ; Собранные объемы , вып. 7, с. 124 ..
- ^ Э. Джонс и Им Муди (1990). «2-тиофенетиол» . Органические синтезы ; Собранные объемы , вып. 6, с. 979 ..
- ^ Мелвин С. Ньюман и Фредерик В. Хетцель (1990). «Тиофенолы из фенолов: 2-нафталентиол» . Органические синтезы ; Собранные объемы , вып. 6, с. 824 ..
- ^ Элиэль, Эрнест Л.; Линч, Джозеф Э.; КУМ, ФУМИТАКА; Фрай, Стивен В. (1993). «Хирал 1,3-оксатиан из (+)-пулегоне: гексагидро-4,4,7-триметил-4 ч -1,3-бензоксатиин» . Органические синтезы ; Собранные объемы , вып. 8, с. 302
- ^ Казем-Ростами, Масуд; Khazaei, Ardeshir; Moosavi-Zare, Ахмад; Баят, Мохаммад; Saednia, Shahnaz (2012). «Новый синтез тиофенолов из одного POT из родственных триазен в мягких условиях». Синлетт 23 (13): 1893–1896. doi : 10.1055/s-0032-1316557 . S2CID 196805424 .
- ^ Leuckart, Rudolf (1890). «Новый метод для представления ароматических меркаптанов» [новый метод подготовки ароматического Меркаптана]. Журнал практической химии . 2 -я серия (на немецком языке). 41 : 179-224. Doi : 10.1002/prac.18900410114 .
- ^ Я Алонсо; Х. Арагона (1978). «Синтез сульфида при приготовлении несимметричных диалкил дисульфидов: сек-бутилзопропил дисульфид». Орг Синтезатор 58 : 147. doi : 10.15227/orgsyn.058.0147 .
- ^ Akhmadullina, Ag; Kizhaev, BV; Nurgalieva, GM; Хрушчева, IK; Шабава, как; и др. (1993). «Гетерогенное каталитическое декаптизация легкого углеводородного сырья» . Химия и технология топлива и масла . 29 (3): 108–109. doi : 10.1007/bf00728009 . S2CID 97292021 . Архивировано из оригинала 2011-08-15.
- ^ Рой, Катрин-Мария (2005). «Тиолы и органические сульфиды». Энциклопедия промышленной химии Уллмана . Вейнхайм: Wiley-VCH. doi : 10.1002/14356007.a26_767 . ISBN 978-3527306732 .
- ^ Стаббе, Джоан; Nocera, Daniel G.; Yee, Cyril S.; Чанг, Мишель Сай (2003). «Радикальная инициация в рибонуклеотидной редуктазе класса I: перенос электронов на большие расстояния?». Химический Преподобный 103 (6): 2167–2202. doi : 10.1021/cr020421u . PMID 12797828 .
- ^ Хофстеттер, Дастин; Тошнота, Томас; Koppenol, Willem H. (2010). «Уравновешивание обмена водорода в радикалах глутатиона: константы скорости» . Хим . 23 (10): 1596–1600. Doi : 10.1021/tx100185k . PMC 2956374 . PMID 20882988 .
- ^ Кох, Кэмерон Дж.; Парламент, Мэтью Б.; Браун, Дж. Мартин; Уртасун, Рауль С. (2010). «Химические модификаторы радиационного отклика». Лейбель и Филлипс Учебник из радиационной онкологии . Elsevier. С. 55–68. doi : 10.1016/b978-1-4160-5897-7.00004-4 . ISBN 978-1-4160-5897-7 Полем
Сульфгидрилы - это мусорщики свободных радикалов, защищая химическое повреждение, вызванное ионизирующим радиацией или алкилирующими агентами.
- ^ Рис, Урри; и др. (2011). Биология Кэмпбелла (девятое изд.). Нью -Йорк: Пирсон Бенджамин Каммингс. С. 65 , 83.
- ^ Malle, E (2007). "Миелопероксидаза: цель для разработки новых лекарств?" Полем Британский журнал фармакологии . 152 (6): 838–854. doi : 10.1038/sj.bjp.0707358 . PMC 2078229 . PMID 17592500 .
- ^ «Понимание сов - доверие Совы» . Theowlstrust.org . Архивировано из оригинала 5 февраля 2018 года . Получено 3 мая 2018 года .
Внешние ссылки
[ редактировать ]- Меркаптаны (или тиолы) за периодическим таблицей видео (Ноттингемский университет)
- Применения, свойства и синтез ω-функционализированных N-алканетиолов и дисульфидов-строительные блоки самосборных монослоев Д. Витт, Р. Клайн, П. Барски, Ба Гржибовски в Северо-Западном университете.
- Mercaptan , Columbia Electronic Encyclopedia
- Что такое Меркаптан? Колумбия газ Пенсильвании и Мэриленда.
- Что самое худшее химическое вещество? Архивированный 2011-06-06 в The Wayback Machine , по химии.