Тантал
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Тантал | |||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | / ˈ t æ n t al ə m / | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Появление | серо-синий | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стандартный атомный вес А р °(Та) | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Тантал в таблице Менделеева | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный номер ( Z ) | 73 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Группа | группа 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Период | период 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Блокировать | d-блок | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электронная конфигурация | [ Автомобиль ] 4f 14 5д 3 6 с 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электроны на оболочку | 2, 8, 18, 32, 11, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Физические свойства | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фаза в СТП | твердый | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Температура плавления | 3290 К (3017 °С, 5463 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка кипения | 5731 К (5458 °С, 9856 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Плотность (при 20°С) | 16,678 г/см 3 [3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| в жидком состоянии (при температуре плавления ) | 15 г/см 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота плавления | 36,57 кДж/моль | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота испарения | 753 кДж/моль | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярная теплоемкость | 25,36 Дж/(моль К) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
Давление пара
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомные свойства | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стадии окисления | , −1, 0, +1, +2, +3, +4, +5 (слабокислотный −3 оксид) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 1,5. | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Энергии ионизации |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный радиус | эмпирический: 146 вечера | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 170±20:00 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Другие объекты недвижимости | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Естественное явление | первобытный | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кристаллическая структура | объемно-центрированная кубическая (BCC) [3] ( сI2 ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Постоянная решетки | а = 15:330,29 (при 20 °С) [3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Тепловое расширение | 6,3 мкм/(м⋅К) (при 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплопроводность | 57,5 Вт/(м⋅К) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электрическое сопротивление | 131 нОм⋅м (при 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Магнитный заказ | парамагнитный [4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярная магнитная восприимчивость | +154.0 × 10 −6 см 3 /mol (293 K) [5] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модуль Юнга | 186 ГПа | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модуль сдвига | 69 ГПа | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Объемный модуль | 200 ГПа | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Скорость звука тонкого стержня | 3400 м/с (при 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| коэффициент Пуассона | 0.34 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по шкале Мооса | 6.5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по Виккерсу | 870–1200 МПа | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по Бринеллю | 440–3430 МПа | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Номер CAS | 7440-25-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| История | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Открытие | Андерс Густав Экеберг (1802) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| отдельным элементом Признан | Генрих Роуз (1844) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Изотопы тантала | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
Тантал — химический элемент ; он имеет символ Та и атомный номер 73. Ранее известный как тантал , он назван в честь Тантала , персонажа греческой мифологии. [7] Тантал — очень твердый, пластичный , блестящий , сине-серый переходный металл , обладающий высокой коррозионной стойкостью. Он входит в группу тугоплавких металлов , которые широко используются в качестве компонентов прочных тугоплавких сплавов . Это элемент 5-й группы , наряду с ванадием и ниобием , и он всегда встречается в геологических источниках вместе с химически близким ниобием, главным образом в минеральных группах танталита , колумбита и колтана .
Химическая инертность и очень высокая температура плавления тантала делают его ценным для лабораторного и промышленного оборудования, такого как реакционные сосуды и вакуумные печи . Он используется в танталовых конденсаторах для электронного оборудования, такого как компьютеры . Его исследуют на предмет использования в качестве материала для высококачественных сверхпроводящих резонаторов в квантовых процессорах. [8] [9] считает тантал технологически критически важным элементом . Европейская комиссия [10]
История
[ редактировать ]Тантал был открыт в Швеции в 1802 году Андерсом Экебергом в двух образцах минералов — одном из Швеции и другом из Финляндии. [11] [12] Годом ранее Чарльз Хэтчетт открыл колумбий (ныне ниобий). [13] В 1809 году английский химик Уильям Хайд Волластон сравнил оксиды колумбия и тантала, колумбит и танталит . Хотя два оксида имели разную измеренную плотность - 5,918 г/см. 3 и 7,935 г/см 3 , он пришел к выводу, что они идентичны, и сохранил название «тантал». [14] После того, как Фридрих Велер подтвердил эти результаты, считалось, что колумбий и тантал — один и тот же элемент. Этот вывод был оспорен в 1846 году немецким химиком Генрихом Розе , который утверждал, что в образце танталита были два дополнительных элемента, и назвал их в честь детей Тантала : ниобий (от Ниобы , богини слез) и пелопий ( от Пелопса ). [15] [16] Предполагаемый элемент «пелопий» позже был идентифицирован как смесь тантала и ниобия, и было обнаружено, что ниобий идентичен колумбию, уже открытому в 1801 году Хэтчеттом.
Различия между танталом и ниобием были недвусмысленно продемонстрированы в 1864 году Кристианом Вильгельмом Бломстрандом . [17] и Анри Этьена Сент-Клера Девиля , а также Луи Дж. Троста , определившего эмпирические формулы некоторых своих соединений в 1865 году. [17] [18] Дальнейшее подтверждение пришло от швейцарского химика Жана Шарля Галиссара де Мариньяка . [19] в 1866 году, который доказал, что элементов всего два. Эти открытия не помешали ученым публиковать статьи о так называемом ильмениуме вплоть до 1871 года. [20] Де Мариньяк был первым, кто получил металлическую форму тантала в 1864 году, когда он восстановил хлорид тантала, нагревая его в атмосфере водорода . [21] Первые исследователи могли производить только нечистый тантал, и первый относительно чистый пластичный металл был произведен Вернером фон Болтоном в Шарлоттенбурге в 1903 году. Провода, изготовленные из металлического тантала, использовались для нитей накаливания лампочек, пока вольфрам не заменил его в широком использовании. [22]
Название тантал произошло от имени мифологического Тантала, отца Ниобеи в греческой мифологии . По сюжету, после смерти он был наказан тем, что был приговорен стоять по колено в воде, а над его головой росли прекрасные плоды, и то и другое вечно мучило его. (Если он наклонялся, чтобы выпить воду, она стекала ниже уровня, которого он мог достичь, а если он тянулся за фруктом, ветки выпадали из его рук.) [23] Андерс Экеберг писал: «Этот металл я называю танталом … отчасти намекая на его неспособность при погружении в кислоту поглощать ее и насыщаться». [24]
На протяжении десятилетий коммерческая технология отделения тантала от ниобия включала фракционную кристаллизацию гептафторотанталата калия из моногидрата оксипентафторниобата калия - процесс, открытый Жаном Шарлем Галиссаром де Мариньяком в 1866 году. Этот метод был вытеснен экстракцией растворителем из фторидсодержащих веществ. растворы тантала. [18]
Характеристики
[ редактировать ]Физические свойства
[ редактировать ]Тантал темный (сине-серый), [25] плотный, пластичный, очень твердый, легко обрабатываемый и обладающий высокой проводимостью тепла и электричества. Металл обладает высокой устойчивостью к коррозии кислотами тантал : при температуре ниже 150° С почти полностью невосприимчив к воздействию обычно агрессивной царской водки . Его можно растворить плавиковой кислотой или кислыми растворами, содержащими фторид -ион и триоксид серы , а также расплавленным гидроксидом калия . Высокая температура плавления тантала 3017 ° C (точка кипения 5458 ° C) среди элементов превышает только вольфрам , рений и осмий для металлов, а также углерод .
Тантал существует в двух кристаллических фазах: альфа и бета. Альфа-фаза стабильна при всех температурах вплоть до температуры плавления и имеет объемноцентрированную кубическую структуру с постоянной решетки а = 0,33029 нм при 20 °С. [3] Он относительно пластичен , имеет твердость по Кнупу 200–400 HN и удельное сопротивление 15–60 мкОм⋅см. Бета-фаза твердая и хрупкая; его кристаллическая симметрия тетрагональная (пространственная группа P42/mnm , a = 1,0194 нм, c = 0,5313 нм), твердость по Кнупу составляет 1000–1300 HN, а удельное электросопротивление относительно высокое и составляет 170–210 мкОм⋅см. Бета-фаза метастабильна и переходит в альфа-фазу при нагревании до 750–775 °С. Объемный тантал почти полностью состоит из альфа-фазы, а бета-фаза обычно существует в виде тонких пленок. [26] полученный магнетроном распыление , химическое осаждение из паровой фазы или электрохимическое осаждение из эвтектического раствора расплавленной соли. [27]
изотопы
[ редактировать ]Природный тантал состоит из двух стабильных изотопов : 180 м Та (0,012%) и 181 По (99,988%). 180 м Прогнозируется, что Ta ( m обозначает метастабильное состояние) распадется тремя способами: изомерный переход в основное состояние 180 Та, бета-распад до 180 W , или захват электрона 180 Хф . Однако радиоактивность этого ядерного изомера никогда не наблюдалась, и лишь нижний предел его периода полураспада составляет 2,9 × 10. 17 лет установлено. [28] Основное состояние 180 Период полураспада Та составляет всего 8 часов. 180 м Та — единственный встречающийся в природе ядерный изомер (исключая радиогенные и космогенные короткоживущие нуклиды). Это также самый редкий первичный изотоп во Вселенной, если принять во внимание элементное содержание тантала и изотопное содержание тантала. 180 м Та в природной смеси изотопов (опять же исключая радиогенные и космогенные короткоживущие нуклиды). [29]
Тантал теоретически рассматривался как « солевой » материал для ядерного оружия ( кобальт более известным гипотетическим солевым материалом является ). Внешняя оболочка из 181 Та будет облучена интенсивным потоком нейтронов высокой энергии от гипотетического взрыва ядерного оружия. Это превратило бы тантал в радиоактивный изотоп. 182 Ta, период полураспада которого составляет 114,4 дня, и который производит гамма-лучи с энергией примерно 1,12 миллиона электрон-вольт (МэВ) каждое, что значительно увеличит радиоактивность ядерных осадков от взрыва на несколько месяцев. Насколько известно, такое «просоленное» оружие никогда не создавалось и не испытывалось, и уж точно никогда не использовалось в качестве оружия. [30]
Тантал может быть использован в качестве мишени для ускоренных протонных пучков для производства различных короткоживущих изотопов, в том числе 8 Что, 80 Рб и 160 Ыб. [31]
Химические соединения
[ редактировать ]Тантал образует соединения в степенях окисления от –III до +V. Чаще всего встречаются оксиды Та(V), в состав которого входят все минералы. Химические свойства Та и Nb очень схожи. В водной среде Та проявляет только степень окисления +V. Как и ниобий, тантал плохо растворяется в разбавленных растворах соляной , серной , азотной и фосфорной кислот из-за выпадения в осадок водного оксида Та(V). [32] В основных средах Та может растворяться за счет образования полиоксотанталатных форм. [33]
Оксиды, нитриды, карбиды, сульфиды
[ редактировать ]Пятиокись тантала (Ta 2 O 5 ) является наиболее важным соединением с точки зрения приложений. Оксиды тантала в низших степенях окисления многочисленны, в том числе имеют множество дефектных структур , малоизучены или плохо охарактеризованы. [34]
Танталаты, соединения, содержащие [TaO 4 ] 3− или [TaO 3 ] − многочисленны. Танталат лития (LiTaO 3 ) имеет структуру перовскита. Танталат лантана (LaTaO 4 ) содержит изолированный TaO. 3−
4 тетраэдра. [35]
Как и в случае с другими тугоплавкими металлами , наиболее твердыми известными соединениями тантала являются нитриды и карбиды. Карбид тантала TaC, как и более часто используемый карбид вольфрама , представляет собой твердую керамику , которая используется в режущих инструментах. Нитрид тантала (III) используется в качестве тонкопленочного изолятора в некоторых процессах производства микроэлектроники. [36]
Наиболее изученным халькогенидом является TaS 2 , слоистый полупроводник , как и другие дихалькогениды переходных металлов . Сплав тантала и теллура образует квазикристаллы . [35]
Галогениды
[ редактировать ]Галогениды тантала охватывают степени окисления +5, +4 и +3. Пентафторид тантала (TaF 5 ) представляет собой белое твердое вещество с температурой плавления 97,0 °С. Анион [TaF 7 ] 2- используется для его отделения от ниобия. [37] Хлорид TaCl
5 , существующий в виде димера, является основным реагентом в синтезе новых соединений Та. Он легко гидролизуется до оксихлорида . Низшие галогениды TaX
4 и налог
3 , содержат связи Ta-Ta. [35] [32]
Танталорганические соединения
[ редактировать ]Танталорганические соединения включают пентаметилтантал , смешанные хлориды алкилтантала, гидриды алкилтантала, алкилиденовые комплексы, а также их циклопентадиенильные производные. [38] [39] Известны разнообразные соли и замещенные производные гексакарбонила [Ta(CO) 6 ] − и родственные изоцианиды .

возникновение
[ редактировать ]
По оценкам, тантал составляет около 1 ppm. [40] или 2 ч/млн [32] земной коры по весу . Существует множество разновидностей минералов тантала, лишь некоторые из которых пока используются промышленностью в качестве сырья: танталит (ряд, состоящий из танталита-(Fe), танталита-(Mn) и танталита-(Mg)), микролита ( теперь название группы), воджинит , эвксенит (на самом деле эвксенит-(Y)) и поликраз (на самом деле поликраз-(Y)). [41] Танталит ( Fe , Mn )Ta 2 O 6 — важнейший минерал для добычи тантала. Танталит имеет ту же минеральную структуру, что и колумбит ( Fe , Mn ) (Ta, Nb ) 2 O 6 ; когда тантала больше, чем ниобия, его называют танталитом, а когда ниобия больше, чем тантала, его называют колумбитом (или ниобитом ). Высокая плотность танталита и других танталсодержащих минералов делает использование гравитационного разделения лучшим методом. Другие минералы включают самарскит и фергюсонит .
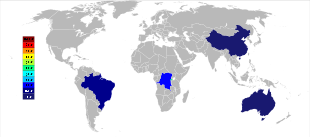
Австралия До 2010-х годов была основным производителем тантала, а Global Advanced Metals (ранее известная как Talison Minerals ) была крупнейшей компанией по добыче тантала в этой стране. Они управляют двумя рудниками в Западной Австралии: Гринбушес на юго-западе и Водгина в регионе Пилбара . Рудник Воджина был вновь открыт в январе 2011 года после того, как добыча на нем была приостановлена в конце 2008 года из-за мирового финансового кризиса . [42] Менее чем через год после возобновления работы компания Global Advanced Metals объявила, что из-за нового «... снижения спроса на тантал ...» и других факторов деятельность по добыче тантала должна быть прекращена в конце февраля 2012 года. [43] Wodgina производит первичный танталовый концентрат, который подвергается дальнейшей переработке на предприятии в Гринбушесе перед продажей покупателям. [44] Хотя крупные производители ниобия находятся в Бразилии и Канаде , руда там также содержит небольшой процент тантала. Некоторые другие страны, такие как Китай , Эфиопия и Мозамбик, добывают руды с более высоким содержанием тантала и производят значительную часть его мировой добычи. Тантал также производится в Таиланде и Малайзии как побочный продукт добычи олова . При гравитационном отделении руд россыпных месторождений обнаруживается не только касситерит (SnO 2 ), но и небольшой процент танталита. Шлак оловянных заводов содержит экономически полезные количества тантала, который выщелачивается из шлака. [18] [45]
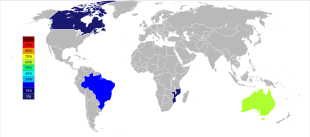
Мировое производство тантала претерпело важный географический сдвиг с начала 21 века, когда добыча осуществлялась преимущественно в Австралии и Бразилии. Начиная с 2007 года и по 2014 год основные источники добычи тантала из рудников резко переместились в Демократическую Республику Конго , Руанду и некоторые другие африканские страны. [46] Будущие источники поставок тантала (в порядке предполагаемого размера) изучаются в Саудовской Аравии , Египте , Гренландии , Китае, Мозамбике, Канаде, Австралии, США , Финляндии и Бразилии. [47] [48]
Статус как конфликтный ресурс
[ редактировать ]Тантал считается конфликтным ресурсом . Колтан — промышленное название колумбит - танталита, минерала, из которого добывают ниобий и тантал. [49] также можно найти в Центральной Африке , поэтому тантал связывают с войной в Демократической Республике Конго (бывший Заир ). Согласно отчету ООН от 23 октября 2003 г. , [50] Контрабанда и экспорт колтана способствовали разжиганию войны в Конго, кризиса, в результате которого с 1998 года погибло около 5,4 миллиона человек. [51] – что делает это самым смертоносным задокументированным конфликтом в мире со времен Второй мировой войны . Были подняты этические вопросы об ответственном корпоративном поведении, правах человека и угрозе дикой природе из-за эксплуатации таких ресурсов, как колтан, в регионах вооруженного конфликта в бассейне Конго . [52] [53] [54] [55] Геологическая служба США сообщает в своем ежегоднике, что в этом регионе производилось чуть менее 1% мирового производства тантала в 2002–2006 годах, достигнув пика в 10% в 2000 и 2008 годах. [45] Данные Геологической службы США, опубликованные в январе 2021 года, показали, что около 40% мировой добычи тантала приходится на Демократическую Республику Конго, а еще 18% — на соседние Руанду и Бурунди . [56]
Производство и изготовление
[ редактировать ]
Извлечение тантала из танталита включает несколько этапов. Сначала минерал измельчается и концентрируется гравитационным разделением . Обычно это делается недалеко от рудника .
Переработка
[ редактировать ]Очистка тантала из его руд является одним из наиболее сложных процессов разделения в промышленной металлургии. Основная проблема состоит в том, что танталовые руды содержат значительные количества ниобия , химические свойства которого практически идентичны свойствам Та. Для решения этой проблемы было разработано большое количество процедур.
В наше время разделение достигается с помощью гидрометаллургии . [58] Добычу начинают с выщелачивания руды плавиковой кислотой совместно с серной или соляной кислотой . Этот этап позволяет отделить тантал и ниобий от различных неметаллических примесей в породе. Хотя Та встречается в виде различных минералов, его удобно представлять в виде пентаоксида, поскольку большинство оксидов тантала (V) ведут себя в этих условиях аналогичным образом. Таким образом, упрощенное уравнение для его извлечения выглядит следующим образом:
- Ta 2 O 5 + 14 HF → 2 H 2 [TaF 7 ] + 5 H 2 O
Совершенно аналогичные реакции происходят с ниобиевым компонентом, но в условиях экстракции обычно преобладает гексафторид.
- Nb 2 O 5 + 12 HF → 2 H[NbF 6 ] + 5 H 2 O
Эти уравнения упрощены: предполагается, что бисульфат (HSO 4 − ) и хлорид конкурируют как лиганды за ионы Nb(V) и Ta(V) при использовании серной и соляной кислот соответственно. [58] Затем комплексы фторида тантала и ниобия удаляют из водного раствора жидкостно-жидкостной экстракцией в органические растворители , такие как циклогексанон , октанол и метилизобутилкетон . Эта простая процедура позволяет удалить большинство металлосодержащих примесей (например, железа, марганца, титана, циркония), которые остаются в водной фазе в виде их фторидов и других комплексов.
Отделение тантала от ниобия затем достигается за счет снижения ионной силы смеси кислот, что приводит к растворению ниобия в водной фазе. Предполагается, что оксифторид H 2 [NbOF 5 в этих условиях образуется ]. После удаления ниобия раствор очищенного H 2 [TaF 7 ] нейтрализуют водным раствором аммиака для осаждения гидратированного оксида тантала в виде твердого вещества, которое можно прокалить до пятиокиси тантала (Ta 2 O 5 ). [59]
Вместо гидролиза H 2 [TaF 7 ] можно обработать фторидом калия с получением гептафторотанталата калия :
- H 2 [TaF 7 ] + 2 KF → K 2 [TaF 7 ] + 2 HF
В отличие от H 2 [TaF 7 ], калиевая соль легко кристаллизуется и с ней обращаются как с твердым веществом.
K 2 [TaF 7 ] можно превратить в металлический тантал восстановлением натрием при температуре примерно 800° C в расплавленной соли . [60]
- К 2 [TaF 7 ] + 5 Na → Та + 5 NaF + 2 KF
В более старом методе, называемом процессом Мариньяка , смесь H 2 [TaF 7 ] и H 2 [NbOF 5 ] превращалась в смесь K 2 [TaF 7 ] и K 2 [NbOF 5 ], которую затем разделяли. путем фракционной кристаллизации , используя их различную растворимость в воде.
Электролиз
[ редактировать ]Тантал также можно очистить электролизом, используя модифицированную версию процесса Холла-Эру . Вместо того, чтобы требовать, чтобы входной оксид и выходной металл находились в жидкой форме, электролиз тантала работает с нежидкими порошкообразными оксидами. Первое открытие было сделано в 1997 году, когда исследователи из Кембриджского университета погрузили небольшие образцы некоторых оксидов в ванну с расплавленной солью и восстановили оксид электрическим током. В качестве катода используется порошкообразный оксид металла. Анод изготовлен из углерода. Расплавленная соль при температуре 1000 ° C (1830 ° F) является электролитом. Мощности первого нефтеперерабатывающего завода достаточны для удовлетворения 3–4% годового мирового спроса. [61]
Производство и металлообработка
[ редактировать ]Вся сварка тантала должна производиться в инертной атмосфере аргона или гелия , чтобы защитить его от загрязнения атмосферными газами. Тантал не паяется . Измельчить тантал сложно, особенно отожженный тантал. В отожженном состоянии тантал чрезвычайно пластичен и из него можно легко формовать металлические листы. [62]
Приложения
[ редактировать ]Электроника
[ редактировать ]
Тантал в качестве металлического порошка в основном используется в производстве электронных компонентов, в основном конденсаторов и некоторых мощных резисторов . Танталовые электролитические конденсаторы используют склонность тантала образовывать защитный оксидный поверхностный слой, используя танталовый порошок, спрессованный в форме гранул, в качестве одной «обкладки» конденсатора, оксид в качестве диэлектрика , а электролитический раствор или проводящее твердое вещество в качестве другая «тарелка». Поскольку диэлектрический слой может быть очень тонким (тоньше, чем аналогичный слой, например, в алюминиевом электролитическом конденсаторе), высокая емкость может быть достигнута в небольшом объеме. Благодаря преимуществам в размере и весе танталовые конденсаторы привлекательны для портативных телефонов , персональных компьютеров , автомобильной электроники и фотоаппаратов . [63]
Сплавы
[ редактировать ]Тантал также используется для производства различных сплавов , которые имеют высокие температуры плавления, прочность и пластичность. Сплавленный другими металлами, он также используется при изготовлении твердосплавных инструментов для металлообрабатывающего оборудования и в производстве суперсплавов для компонентов реактивных двигателей, химического технологического оборудования, ядерных реакторов , деталей ракет, теплообменников, резервуаров и сосудов. [64] [63] [65] Благодаря своей пластичности тантал можно вытягивать в тонкие проволоки или нити, которые используются для испарения таких металлов, как алюминий . Поскольку тантал устойчив к воздействию жидкостей организма и не вызывает раздражений, он широко используется при изготовлении хирургических инструментов и имплантатов. Например, пористые танталовые покрытия используются при изготовлении ортопедических имплантатов из-за способности тантала образовывать прямую связь с твердыми тканями. [66]
Тантал инертен по отношению к большинству кислот, за исключением плавиковой кислоты и горячей серной кислоты , а горячие щелочные растворы также вызывают коррозию тантала. Это свойство делает его полезным металлом для изготовления сосудов для химических реакций и труб для агрессивных жидкостей. Теплообменные змеевики для парового нагрева соляной кислоты изготовлены из тантала. [67] Тантал широко использовался в производстве сверхвысокой частоты электронных ламп для радиопередатчиков. Тантал способен захватывать кислород и азот путем образования нитридов и оксидов и, следовательно, помогает поддерживать высокий вакуум, необходимый для трубок, когда они используются для внутренних частей, таких как решетки и пластины. [37] [67]
Другое использование
[ редактировать ]
Тантал использовался НАСА для защиты компонентов космических кораблей, таких как «Вояджер-1» и «Вояджер-2» , от радиации. [68] Высокая температура плавления и стойкость к окислению привели к использованию металла в производстве деталей вакуумных печей . Тантал чрезвычайно инертен, поэтому из него изготавливают различные коррозионностойкие детали, такие как защитные гильзы , корпуса клапанов и танталовые крепежные детали. Из-за его высокой плотности кумулятивный заряд и вкладыши пенетратора, формируемые взрывным способом, были изготовлены из тантала. [69] Тантал значительно повышает бронепробиваемость кумулятивного заряда благодаря своей высокой плотности и высокой температуре плавления. [70] [71]
Он также иногда используется в драгоценных часах , например, от Audemars Piguet , FP Journe , Hublot , Montblanc , Omega и Panerai . Медицинский исследователь Джеральд Л. Берк впервые заметил в 1940 году, что тантал также обладает высокой биоинертностью и может безопасно использоваться в качестве материала для ортопедических имплантатов. [72] Высокая жесткость тантала делает необходимым использовать его в качестве высокопористой пены или каркаса с более низкой жесткостью для имплантатов замены тазобедренного сустава, чтобы избежать защиты от напряжений . [73] Поскольку тантал является цветным немагнитным металлом, эти имплантаты считаются приемлемыми для пациентов, проходящих процедуры МРТ. [74] Оксид используется для изготовления специального с высоким показателем преломления стекла для объективов фотоаппаратов . [75]
Экологические проблемы
[ редактировать ]Танталу уделяется гораздо меньше внимания в области окружающей среды, чем в других науках о Земле. Концентрация верхней коры (UCC) и соотношение Nb/Ta в верхней коре и минералах доступны, поскольку эти измерения полезны в качестве геохимического инструмента. [76] Последнее значение концентрации верхней коры составляет 0,92 ppm, а соотношение Nb/Ta(w/w) составляет 12,7. [77]
Имеется мало данных о концентрациях тантала в различных частях окружающей среды, особенно в природных водах, где даже не были получены надежные оценки концентрации «растворенного» тантала в морской и пресной воде. [78] Некоторые значения концентрации растворенных веществ в океанах были опубликованы, но они противоречивы. Значения в пресной воде немного лучше, но во всех случаях они, вероятно, ниже 1 нг/л. −1 , поскольку «растворенные» концентрации в природных водах значительно ниже большинства современных аналитических возможностей. [79] Анализ требует процедур предварительного концентрирования, которые на данный момент не дают последовательных результатов. И в любом случае, тантал, по-видимому, присутствует в природных водах в основном в виде твердых частиц, а не в растворенном виде. [78]
Легче определить значения концентраций в почвах, донных отложениях и атмосферных аэрозолях. [78] Значения в почвах близки к 1 ppm и, следовательно, к значениям UCC. Это указывает на детритное происхождение. Для атмосферных аэрозолей имеющиеся значения разрознены и ограничены. Когда наблюдается обогащение тантала, это, вероятно, связано с потерей большего количества водорастворимых элементов в аэрозолях в облаках. [80]
Загрязнения, связанного с использованием этого элемента человеком, не обнаружено. [81] Тантал, по-видимому, является очень консервативным элементом с биогеохимической точки зрения, но его круговорот и реакционная способность до сих пор полностью не изучены.
Меры предосторожности
[ редактировать ]Соединения, содержащие тантал, редко встречаются в лаборатории. Металл обладает высокой биосовместимостью. [72] и используется для имплантатов и покрытий тела , поэтому внимание может быть сосредоточено на других элементах или физической природе химического соединения . [82]
Люди могут подвергнуться воздействию тантала на рабочем месте при вдыхании, контакте с кожей или глазами. Управление по охране труда (OSHA) установило юридический предел ( допустимый предел воздействия ) для воздействия тантала на рабочем месте на уровне 5 мг/м. 3 более 8-часового рабочего дня. Национальный институт охраны труда (NIOSH) установил рекомендуемый предел воздействия (REL) 5 мг/м. 3 при 8-часовом рабочем дне и кратковременном пределе 10 мг/м 3 . На уровне 2500 мг/м 3 Танталовая пыль непосредственно опасна для жизни и здоровья . [83]
Ссылки
[ редактировать ]- ^ «Стандартные атомные массы: тантал» . ЦИАВ . 2005.
- ^ Прохаска, Томас; Ирргехер, Йоханна; Бенефилд, Жаклин; Бёлке, Джон К.; Чессон, Лесли А.; Коплен, Тайлер Б.; Дин, Типинг; Данн, Филип Дж. Х.; Грёнинг, Манфред; Холден, Норман Э.; Мейер, Харро Эй Джей (04 мая 2022 г.). «Стандартные атомные веса элементов 2021 (Технический отчет ИЮПАК)» . Чистая и прикладная химия . дои : 10.1515/pac-2019-0603 . ISSN 1365-3075 .
- ^ Перейти обратно: а б с д Арбластер, Джон В. (2018). Некоторые значения кристаллографических свойств элементов . Парк материалов, Огайо: ASM International. ISBN 978-1-62708-155-9 .
- ^ Лиде, Д.Р., изд. (2005). «Магнитная восприимчивость элементов и неорганических соединений». Справочник CRC по химии и физике (PDF) (86-е изд.). Бока-Ратон (Флорида): CRC Press. ISBN 0-8493-0486-5 .
- ^ Уэст, Роберт (1984). CRC, Справочник по химии и физике . Бока-Ратон, Флорида: Издательство компании Chemical Rubber Company. стр. E110. ISBN 0-8493-0464-4 .
- ^ Кондев, ФГ; Ван, М.; Хуанг, WJ; Наими, С.; Ауди, Г. (2021). «Оценка ядерных свойств NUBASE2020» (PDF) . Китайская физика C . 45 (3): 030001. doi : 10.1088/1674-1137/abddae .
- ^ Еврипид , Орест
- ^ Маклеллан, РА (2023). «Химические профили оксидов тантала в современных сверхпроводниковых схемах» . Передовая наука . 10 (21): e2300921. arXiv : 2301.04567 . дои : 10.1002/advs.202300921 . ПМЦ 10375100 . ПМИД 37166044 .
- ^ Кроули, Кевин Д.; Маклеллан, Рассел А.; Дутта, Авик; Шумия, Нана; Плейс, Александр ПМ; Ле, Сюань Хоанг; Банда, Юци; Мадхаван, Триша; Бланд, Мэтью П.; Чанг, Рэй; Хедкар, Нишаад; Фэн, Имин Кэди; Умбаркар, Эша А.; Гуй, Синь; Роджерс, Лила В.Х.; Цзя, Ичен; Фельдман, Майер М.; Лион, Стивен А.; Лю, Минчжао; Кава, Роберт Дж.; Хоук, Эндрю А .; де Леон, Натали П. (06 октября 2023 г.). «Распутывание потерь в танталовых сверхпроводящих цепях» . Физический обзор X . 13 (4): 041005. arXiv : 2301.07848 . Бибкод : 2023PhRvX..13d1005C . дои : 10.1103/PhysRevX.13.041005 .
- ^ «Европейская комиссия (2010). Критическое сырье для ЕС. Отчет специальной рабочей группы по определению критического сырья» . Европейская комиссия . 29 апреля 2015 г.
- ^ Экеберг, Андерс (1802). «О свойствах Земли Иттрии по сравнению со свойствами Глюцина; Окаменелостей, в которых содержалась первая из этих Земель; и Об Открытии металлической природы (танталия)» . Журнал естественной философии, химии и искусств . 3 : 251–255.
- ^ Экеберг, Андерс (1802). «Сведения о свойствах Внешней Земли, особенно в отношении Берилловой Земли: об Ископаемых, в которых содержится первая упомянутая земля, а также о вновь открытом теле металлической природы» . Труды Шведской королевской академии наук . 23 : 68–83 .
- ^ Гриффит, Уильям П.; Моррис, Питер Дж. Т. (2003). «Чарльз Хэтчетт FRS (1765–1847), химик и первооткрыватель ниобия». Заметки и отчеты Лондонского королевского общества . 57 (3): 299–316. дои : 10.1098/rsnr.2003.0216 . JSTOR 3557720 . S2CID 144857368 .
- ^ Волластон, Уильям Хайд (1809). «О тождестве колумбия и тантала». Философские труды Лондонского королевского общества . 99 : 246–252. дои : 10.1098/rstl.1809.0017 . JSTOR 107264 . S2CID 110567235 .
- ^ Роза, Генрих (1844). «О составе танталитов и новом металле, содержащемся в танталите из Баварии» . Анналы физики (на немецком языке). 139 (10): 317–341. Бибкод : 1844АнП...139..317Р . дои : 10.1002/andp.18441391006 .
- ^ Роза, Генрих (1847). «О кислоте в колумбите Северной Америки» . Анналы физики (на немецком языке). 146 (4): 572–577. Бибкод : 1847АнП...146..572Р . дои : 10.1002/andp.18471460410 .
- ^ Перейти обратно: а б Мариньяк, Бломстранд; Х. Девиль; Л. Трост и Р. Герман (1866). «Танталовая кислота, ниобиевая кислота (ильменовая кислота) и титановая кислота». Журнал аналитической химии Фрезениуса . 5 (1): 384–389. дои : 10.1007/BF01302537 . S2CID 97246260 .
- ^ Перейти обратно: а б с Гупта, СК; Сури, АК (1994). Добывающая металлургия ниобия . ЦРК Пресс. ISBN 978-0-8493-6071-8 .
- ^ Мариньяк, MC (1866 г.). «Исследование соединений ниобия» . Анналы химии и физики (на французском языке). 4 (8): 7–75.
- ^ Германн, Р. (1871). «Дальнейшие исследования соединений ильмения и ниобия, а также состава ниобиевых минералов)» . Журнал практической химии (на немецком языке). 3 (1): 373–427. дои : 10.1002/prac.18710030137 .
- ^ «Ниобий» . Университет Коимбры. Архивировано из оригинала 10 декабря 2007 г. Проверено 5 сентября 2008 г.
- ^ Бауэрс, Б. (2001). «Сканирование нашего прошлого из Лондона. Лампа накаливания и новые материалы». Труды IEEE . 89 (3): 413. дои : 10.1109/5.915382 . S2CID 28155048 .
- ^ Лемприер, Джон (1887). Классический словарь Лемприера . п. 659 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 1138. ИСБН 978-0-08-037941-8 .
- ^ Колакис, Марианте; Маселло, Мэри Джоан (30 июня 2007 г.). «Тантал» . Классическая мифология и многое другое: рабочая тетрадь для чтения . Издательство Больчази-Кардуччи. ISBN 978-0-86516-573-1 .
- ^ Магнусон, М.; Гречинский, Г.; Эрикссон, Ф.; Хультман, Л.; Хогберг, Х. (2019). «Электронная структура пленок β-Ta по данным рентгеновской фотоэлектронной спектроскопии и расчеты из первых принципов» . Прикладная наука о поверхности . 470 : 607–612. Бибкод : 2019АпсС..470..607М . дои : 10.1016/j.apsusc.2018.11.096 . S2CID 54079998 .
- ^ Ли, С.; Доксбек, М.; Мюллер, Дж.; Чиполло, М.; Кот, П. (2004). «Текстура, структура и фазовые превращения в напыленном покрытии бета-тантала» . Технология поверхностей и покрытий . 177–178: 44. doi : 10.1016/j.surfcoat.2003.06.008 .
- ^ Сотрудничество Майораны (11 октября 2023 г.). «Ограничения на распад 180 м Ta». Physical Review Letters . 131 (15): 152501. arXiv : 2306.01965 . doi : 10.1103/PhysRevLett.131.152501 . ISSN 0031-9007 .
- ^ Ауди, Жорж; Берсильон, Оливье; Блашо, Жан; Вапстра, Аалдерт Хендрик (2003), « Оценка NUBASE свойств ядра и распада» , Nuclear Physics A , 729 : 3–128, Бибкод : 2003NuPhA.729....3A , doi : 10.1016/j.nuclphysa.2003.11 .001
- ^ Вин, Дэвид Тин; Аль Масум, Мохаммед (2003). «Оружие массового поражения» (PDF) . Технологический журнал Успенского университета . 6 (4): 199–219.
- ^ «Целевые выходы тантала - База данных ISAC по урожайности - TRIUMF: Национальная лаборатория Канады по частицам и ядерной физике» . mis.triumf.ca .
- ^ Перейти обратно: а б с Агулянский, Анатолий (2004). Химия соединений фторидов тантала и ниобия . Эльзевир. ISBN 978-0-444-51604-6 . Проверено 2 сентября 2008 г.
- ^ Деблонд, Готье Ж.-П.; Шань, Александр; Белэр, Сара; Кот, Жерар (01 июля 2015 г.). «Растворимость ниобия (V) и тантала (V) в слабощелочных условиях». Гидрометаллургия . 156 : 99–106. Бибкод : 2015HydMe.156...99D . doi : 10.1016/j.гидромет.2015.05.015 . ISSN 0304-386X .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Перейти обратно: а б с Холлеман, AF; Виберг, Э.; Виберг, Н. (2007). Учебник неорганической химии (на немецком языке) (102-е изд.). де Грюйтер. ISBN 978-3-11-017770-1 .
- ^ Цукимото, С.; Морияма, М.; Мураками, Масанори (1961). «Микроструктура тонких пленок аморфного нитрида тантала». Тонкие твердые пленки . 460 (1–2): 222–226. Бибкод : 2004TSF...460..222T . дои : 10.1016/j.tsf.2004.01.073 .
- ^ Перейти обратно: а б Суассон, Дональд Дж.; Маклафферти, Джей-Джей; Пьере, Джеймс А. (1961). «Совместный отчет персонала и промышленности: тантал и ниобий». Индийский англ. Хим . 53 (11): 861–868. дои : 10.1021/ie50623a016 .
- ^ Шрок, Ричард Р. (1 марта 1979 г.). «Алкилиденовые комплексы ниобия и тантала». Отчеты о химических исследованиях . 12 (3): 98–104. дои : 10.1021/ar50135a004 . ISSN 0001-4842 .
- ^ Морс, премьер-министр; и др. (2008). «Этиленовые комплексы ранних переходных металлов: кристаллические структуры [HfEt
4 (С
22Ч
4 ) 2−
] и виды в отрицательном состоянии окисления [TaHEt(C
22Ч
4 ) 3−
3 ] и [WH(C
22Ч
4 ) 3−
4 ] ». Металлоорганики . 27 (5): 984. doi : 10.1021/om701189e . - ^ Эмсли, Джон (2001). «Тантал» . Строительные блоки природы: Путеводитель по элементам от А до Я. Оксфорд, Англия, Великобритания: Издательство Оксфордского университета. п. 420 . ISBN 978-0-19-850340-8 .
- ^ «Шахты, полезные ископаемые и многое другое» . Mindat.org.
- ^ «Талисон Танталум планирует перезапустить Уоджину в середине 2011 года 9 июня 2010 года» . Рейтер . 09.06.2010. Архивировано из оригинала 19 января 2011 г. Проверено 27 августа 2010 г.
- ^ Эмери, Кейт (24 января 2012 г.). «GAM закрывает танталовый рудник в Воджине» . Западная Австралия . Архивировано из оригинала 4 декабря 2012 года . Проверено 20 марта 2012 г.
Снижение спроса на тантал во всем мире и задержки в получении разрешения правительства на установку необходимого дробильного оборудования являются одними из факторов, способствующих принятию этого решения.
- ^ «Операции Воджины» . Глобальные перспективные металлы. 2008. Архивировано из оригинала 06 октября 2016 г. Проверено 28 марта 2011 г.
- ^ Перейти обратно: а б Папп, Джон Ф. (2006). «Ежегодник минералов Nb & Ta, 2006 г.» . Геологическая служба США . Проверено 3 июня 2008 г.
- ^ Блейвас, Дональд И.; Папп, Джон Ф.; Ягер, Томас Р. (2015). «Изменения в мировом производстве танталовых рудников, 2000–2014 гг.» (PDF) . Геологическая служба США.
- ^ MJ (ноябрь 2007 г.). «Танталовая добавка» (PDF) . Горный журнал . Архивировано из оригинала (PDF) 10 сентября 2008 г. Проверено 3 июня 2008 г.
- ^ «Международные ресурсы тантала – разведка и добыча» (PDF) . Бюллетень минеральных ресурсов GSWA . 22 (10). Архивировано из оригинала (PDF) 26 сентября 2007 г.
- ^ Международный исследовательский центр тантала-ниобия: Колтан. Архивировано 14 января 2016 г. на Wayback Machine. Получено 27 января 2008 г.
- ^ "S/2003/1027" . 26 октября 2003 г. Проверено 19 апреля 2008 г.
- ^ «Специальный репортаж: Конго» . Международный комитет спасения. Архивировано из оригинала 05 марта 2012 г. Проверено 19 апреля 2008 г.
- ^ Хейс, Карен; Бердж, Ричард (2003). Coltan Mining в Демократической Республике Конго: Как отрасли, использующие тантал, могут способствовать восстановлению ДРК . стр. 1–64. ISBN 978-1-903703-10-6 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Дизолеле, Мвемба Фезо (6 января 2011 г.). «Кровавый колтан Конго» . Пулитцеровский центр по освещению кризисов . Проверено 8 августа 2009 г.
- ^ «Война в Конго и роль Колтана» . Архивировано из оригинала 13 июля 2009 г. Проверено 8 августа 2009 г.
- ^ «Добыча колтана в бассейне реки Конго» . Архивировано из оригинала 30 марта 2009 г. Проверено 8 августа 2009 г.
- ^ Геологическая служба США (январь 2021 г.). «Краткая информация о минеральных сырьевых товарах USGS: тантал» (PDF) . Проверено 22 апреля 2021 г.
- ^ «Программа минеральных ресурсов» . Minerals.usgs.gov . Архивировано из оригинала 4 июня 2013 года.
- ^ Перейти обратно: а б Чжу, Чжаову; Ченг, Чу Юн (2011). «Технология экстракции растворителем для разделения и очистки ниобия и тантала: обзор». Гидрометаллургия . 107 (1–2): 1–12. Бибкод : 2011HydMe.107....1Z . doi : 10.1016/j.гидромет.2010.12.015 .
- ^ Агулянский, Анатолий (2004). Химия соединений фторидов тантала и ниобия (1-е изд.). Берлингтон: Эльзевир. ISBN 9780080529028 .
- ^ Окабе, Тору Х.; Садовей, Дональд Р. (1998). «Металлотермическое восстановление как электронно-опосредованная реакция». Журнал исследования материалов . 13 (12): 3372–3377. Бибкод : 1998JMatR..13.3372O . дои : 10.1557/JMR.1998.0459 . S2CID 98753880 .
- ^ «Производство металлов: заманчивая перспектива» . Экономист . 16 февраля 2013 г. Проверено 17 апреля 2013 г.
- ^ «NFPA 484 – Стандарт на горючие металлы, металлические порошки и металлическую пыль – издание 2002 г.» (PDF) . Национальная ассоциация пожарной безопасности . НФПА. 13 августа 2002 г. Архивировано из оригинала (PDF) 12 августа 2023 г. Проверено 12 февраля 2016 г.
- ^ Перейти обратно: а б «Отчет о сырьевых товарах за 2008 год: Тантал» (PDF) . Геологическая служба США . Проверено 24 октября 2008 г.
- ^ «Танталовые изделия: танталовые листы и пластины | Admat Inc» . Компания Адмат . Архивировано из оригинала 29 августа 2018 г. Проверено 28 августа 2018 г.
- ^ Бакман, Р.В. младший (2000). «Новые применения тантала и танталовых сплавов». JOM: Журнал Общества минералов, металлов и материалов . 52 (3): 40. Бибкод : 2000JOM....52c..40B . дои : 10.1007/s11837-000-0100-6 . S2CID 136550744 .
- ^ Коэн, Р.; Делла Валле, CJ; Джейкобс, Джей-Джей (2006). «Применение пористого тантала при тотальном эндопротезировании тазобедренного сустава». Журнал Американской академии хирургов-ортопедов . 14 (12): 646–55. дои : 10.5435/00124635-200611000-00008 . ПМИД 17077337 .
- ^ Перейти обратно: а б Балке, Кларенс В. (1935). «Колумбий и тантал». Промышленная и инженерная химия . 20 (10): 1166. doi : 10.1021/ie50310a022 .
- ^ Белл, Джим (2015). Межзвездная эпоха: история мужчин и женщин НАСА, которые летали на сорокалетней миссии «Вояджер» . Нью-Йорк: Даттон. п. 110. ИСБН 978-0-525-95432-3 .
- ^ Немат-Насер, Сиа; Айзекс, Джон Б.; Лю, Минци (1998). «Микроструктура высокодеформированного, высокоскоростно деформированного тантала». Акта Материалия 46 (4): 1307. Бибкод : 1998AcMat..46.1307N . дои : 10.1016/S1359-6454(97) 00746-5
- ^ Уолтерс, Уильям; Куч, Уильям; Беркинс, Мэтью; Буркинс, Мэтью (2001). «Пробивная стойкость титанового сплава к струям танталовых гильз кумулятивных зарядов» . Международный журнал ударной инженерии . 26 (1–10): 823. doi : 10.1016/S0734-743X(01)00135-X . S2CID 92307431 .
- ^ Рассел, Алан М.; Ли, Кок Лунг (2005). Соотношения структура-свойства в цветных металлах . Хобокен, Нью-Джерси: Wiley-Interscience. п. 218. ИСБН 978-0-471-64952-6 .
- ^ Перейти обратно: а б Берк, Джеральд Л. (август 1940 г.). «Коррозия металлов в тканях и введение в тантал» . Журнал Канадской медицинской ассоциации . 43 (2): 125–128. ПМК 538079 . ПМИД 20321780 .
- ^ Блэк, Дж. (1994). «Биологическая эффективность тантала». Клинические материалы . 16 (3): 167–173. дои : 10.1016/0267-6605(94)90113-9 . ПМИД 10172264 .
- ^ Паганиас, Христос Г.; Цакотос, Джордж А.; Кутсостатис, Стефанос Д.; Мачерас, Джордж А. (2012). «Костная интеграция в пористых танталовых имплантатах» . Индийский журнал ортопедии . 46 (5): 505–13. дои : 10.4103/0019-5413.101032 . ISSN 0019-5413 . ПМК 3491782 . ПМИД 23162141 .
- ^ Музыкант, Соломон (1985). «Композиция оптического стекла» . Оптические материалы: введение в выбор и применение . ЦРК Пресс. п. 28. ISBN 978-0-8247-7309-0 .
- ^ Грин, ТД. (1995). «Значение Nb/Ta как индикатора геохимических процессов в системе кора-мантия». Химическая геология . 120 (3–4): 347–359. Бибкод : 1995ЧГео.120..347Г . дои : 10.1016/0009-2541(94)00145-X .
- ^ Ху, З.; Гао, С. (2008). «Содержание микроэлементов в верхней коре: пересмотр и обновление». Химическая геология . 253 (3–4): 205. Бибкод : 2008ChGeo.253..205H . doi : 10.1016/j.chemgeo.2008.05.010 .
- ^ Перейти обратно: а б с Филелла, М. (2017). «Тантал в окружающей среде». Обзоры наук о Земле . 173 : 122–140. Бибкод : 2017ESRv..173..122F . doi : 10.1016/j.earscirev.2017.07.002 .
- ^ Филелла, М.; Родушкин И. (2018). «Краткое руководство по определению менее изученных технологически важных элементов (Nb, Ta, Ga, In, Ge, Te) методом масс-спектрометрии с индуктивно связанной плазмой в пробах окружающей среды». Spectrochimica Acta Часть B. 141 : 80–84. Бибкод : 2018AcSpe.141...80F . дои : 10.1016/j.sab.2018.01.004 .
- ^ Властелич, И.; Сухорский, К.; Селлегри, К.; Коломб, А.; Науре, Ф.; Бувье, Л.; Пиро, Дж.Л. (2015). «Бюджет элементов атмосферного аэрозоля с высокой напряженностью поля (Пюи-де-Дом, Франция)». Geochimica et Cosmochimica Acta . 167 : 253–268. Бибкод : 2015GeCoA.167..253В . дои : 10.1016/j.gca.2015.07.006 .
- ^ Филелла, М.; Родригес-Мурильо, Х.К. (2017). «Менее изученные ТВК: увеличивается ли их концентрация в окружающей среде из-за их использования в новых технологиях?». Хемосфера . 182 : 605–616. Бибкод : 2017Chmsp.182..605F . doi : 10.1016/j.chemSphere.2017.05.024 . ПМИД 28525874 .
- ^ Мацуно, Х.; Ёкояма, А.; Ватари, Ф.; Уо, М.; Кавасаки, Т. (2001). «Биосовместимость и остеогенез имплантатов из тугоплавких металлов, титана, гафния, ниобия, тантала и рения. Биосовместимость тантала». Биоматериалы . 22 (11): 1253–1262. дои : 10.1016/S0142-9612(00)00275-1 . ПМИД 11336297 .
- ^ «CDC - Карманный справочник NIOSH по химическим опасностям - Тантал (металлическая и оксидная пыль, как Та)» . www.cdc.gov . Проверено 24 ноября 2015 г.

