Дифосген
| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Трихлорметилкарбохлоридат | |
| Другие имена
Трихлорметилхлорформиат, сурпалит
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.007.242 |
| Номер ЕС |
|
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 2 Cl 4 О 2 | |
| Молярная масса | 197.82 g/mol |
| Появление | жидкость комнатной температуры |
| Плотность | 1,65 г/см 3 |
| Температура плавления | -57 ° C (-71 ° F; 216 К) |
| Точка кипения | 128 ° С (262 ° F; 401 К) |
| нерастворим, реагирует | |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности
|
высокотоксичный, возможно коррозионный; удушающий |
| СГС Маркировка : | |
 
| |
| Опасность | |
| Х300 , Х301 , Х314 , Х330 | |
| P260 , P264 , P270 , P271 , P280 , P284 , P301+P310 , P301+P330+P331 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P320 , P321 , П330 , П363 , П403+ П233 , П405 , П501 | |
| точка возгорания | 32 ° С (90 ° F; 305 К) |
| Родственные соединения | |
Родственные соединения
|
COCl 2 , Cl 2 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
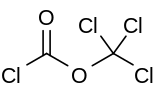
Дифосген представляет собой органическое химическое соединение с формулой ClCO 2 CCl 3 . Эта бесцветная жидкость — ценный реагент при синтезе органических соединений . Дифосген родственен фосгену и имеет сопоставимую токсичность , но с ним удобнее обращаться, поскольку он представляет собой жидкость, тогда как фосген представляет собой газ.
Производство и использование
[ редактировать ]Дифосген получают радикальным хлорированием метилхлорформиата в УФ-свете : [ 1 ]
- Cl-CO-OCH 3 + 3 Cl 2 —(hv)→ Cl-CO-OCCl 3 + 3 HCl
Другой метод — радикальное хлорирование метилформиата: [ 2 ]
- H-CO-OCH 3 + 4 Cl 2 —(hv)→ Cl-CO-OCCl 3 + 4 HCl
Дифосген превращается в фосген при нагревании или при катализе углем древесным . Таким образом, он полезен для реакций, традиционно основанных на фосгене. Например, он превращает амины в изоцианаты , вторичные амины в карбамоилхлориды , карбоновые кислоты в хлорангидриды , а формамиды в изоцианиды . Дифосген служит источником двух эквивалентов фосгена:
- 2 RNH 2 + ClCO 2 CCl 3 → 2 RNCO + 4 HCl
С α- аминокислотами дифосген дает в зависимости от условий хлорангидриды-изоцианаты, OCNCHRCOCl или ангидриды N -карбоксиаминокислот. [ 3 ]
Он гидролизуется с выделением HCl во влажном воздухе.
Дифосген используется в некоторых лабораторных препаратах, поскольку с ним легче обращаться, чем с фосгеном.
Роль в войне
[ редактировать ]Дифосген изначально был разработан как легочное вещество для химического оружия , через несколько месяцев после первого применения фосгена. Он использовался в качестве отравляющего газа в артиллерийских снарядах Германией во время Первой мировой войны . Первое зарегистрированное использование на поле боя произошло в мае 1916 года. [ 4 ] Дифосген был разработан потому, что его пары могли разрушить фильтры противогазов, использовавшихся в то время.
Безопасность
[ редактировать ]Дифосген имеет относительно высокое давление паров - 10 мм рт. ст. (1,3 кПа) при 20 ° C и разлагается на фосген при температуре около 300 ° C. Воздействие дифосгена по своей опасности аналогично фосгену.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Кейсуке Курита и Ёсио Ивакура (1979). «Трихлорметилхлорформиат как эквивалент фосгена: 3-изоцианатопропаноилхлорид» . Органические синтезы . 59 :195 ; Сборник томов , т. 6, с. 715 .
- ^ Лос, К.Х.: Синтетические яды ; Берлин (восток), 1974 год (немецкий).
- ^ Курита, К. «Трихлорметилхлорформиат» в Энциклопедии реагентов для органического синтеза (под редакцией: Л. Пакетт), 2004, J. Wiley & Sons, Нью-Йорк. дои : 10.1002/047084289X .
- ^ Джонс, Саймон; Крюк, Ричард (2007). Тактика и оборудование газовой войны Первой мировой войны . Издательство Оспри. ISBN 978-1-84603-151-9 .
Внешние ссылки
[ редактировать ]- руководство по медицинскому обслуживанию .
- Руководство НАТО , включает рекомендации по лечению
- паспорт безопасности материала (PDF, для фосгена и дифосгена, рассматриваемых как одно целое).
- Паспорт безопасности для дифосгена, в частности