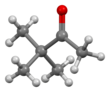
Пинаколоне
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
3,3-Диметилбутан-2-он | |||
| Другие имена
т -Бутилметилкетон
1,1,1-Триметилацетон | |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| 1209331 | |||
| КЭБ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.000.838 | ||
| Номер ЕС |
| ||
| МеШ | Пинаколоне | ||
ПабХим CID
|
|||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
| Число | 1224 | ||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| С 6 Н 12 О | |||
| Молярная масса | 100.161 g·mol −1 | ||
| Появление | Бесцветная жидкость | ||
| Плотность | 0,801 г см −3 | ||
| Температура плавления | −52 [ 1 ] ° C (-62 ° F; 221 К) | ||
| Точка кипения | От 103 до 106 ° C (от 217 до 223 ° F; от 376 до 379 К) | ||
| -69.86·10 −6 см 3 /моль | |||
| Опасности | |||
| СГС Маркировка : | |||
 
| |||
| Опасность | |||
| Х225 , Х302 , Х315 , Х319 , Х332 , Х335 , Х412 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P261 , P264 , P270 , P271 , P273 , P280 , P301+P312 , P302+P352 , P303+P361+P353 , P304+P312 , 04+P340 , P305+P351+ P338 , P312 , P321 , P330 , P332+P313 , P337+P313 , P362 , P370+P378 , P403+P233 , P403+P235 , P405 , P501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 5 ° C (41 ° F; 278 К) | ||
| Паспорт безопасности (SDS) | Внешний паспорт безопасности материалов | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Пинаколон (3,3-диметил-2-бутанон) является важным кетоном в органической химии . Это бесцветная жидкость со слабым запахом мяты или камфоры. Он является предшественником триазолилпинаколона в синтезе фунгицида триадимефона и гербицида метрибузина . Молекула представляет собой несимметричный кетон . α-метильная группа может участвовать в реакциях конденсации. Карбонильная группа может вступать в обычные реакции (гидрирование, восстановительное аминирование и др.). Это соединение включено в Список 3 Конвенции о химическом оружии 1993 года, поскольку оно связано с пинаколиловым спиртом , который используется при производстве зомана . [ 2 ] Это также контролируемый экспорт в государствах-членах Австралийской группы . [ 3 ]
Подготовка
[ редактировать ]Наиболее известно, по крайней мере, в классе, что пинаколон возникает в результате перегруппировки пинакола , которая происходит путем протонирования пинакола (2,3-диметилбутан-2,3-диола). [ 4 ]
В промышленности пинаколон получают гидролизом 4,4,5-триметил-1,3- диоксана , который является продуктом образования изопрена и формальдегида по реакции Принса . Он также образуется в результате кетонизации пивалиновой кислоты и уксусной кислоты или ацетона на катализаторах на основе оксидов металлов. 3-Метилбутаналь является исходным материалом для 2,3-диметил-2-бутена, который, в свою очередь, превращается в пинаколон. Пинаколон также можно получить из 2-метил-2-бутанола при взаимодействии со спиртами C5. [ 5 ]
Использование
[ редактировать ]Пинаколон производится в больших количествах для использования в фунгицидах, гербицидах и пестицидах. Некоторые производные включают в себя:
- ретросинтетический анализ вибуназола показал , что он получен из пинаколона.
- Из него также готовят пинацидил и наминидил .
- Стирипентол
- Трибузон
- Пивалойлацетонитрил используется в синтезе дорамапимода .
- Триадимефон
- Диклобутразол
- Паклобутразол
- Валконазол
- Диэтилстильбэстрол пинаколон [18922-13-9]. [ 6 ]
- Какая-то бисфенола А производная , также патент США 4 599 463.
- Тиофанокс
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ «Пинаколон | C6H12O | ChemSpider» .
- ^ Справочник по боевым химическим и биологическим агентам (2-е изд.). ЦРК Пресс. 24 августа 2007 г. ISBN. 9780849314346 .
- ^ «Список экспортного контроля: прекурсоры химического оружия» . Группа Австралии . australiagroup.net . Проверено 7 апреля 2017 г.
- ^ Г. А. Хилл и Э. В. Флосдорф (1941). «Пинаколоне» . Органические синтезы ; Сборник томов , т. 1, с. 462 .
- ^ Сигел, Х; Эггерсдорфер (2012). Кетоны . 5. Том. 20. дои : 10.1002/14356007.a15_077 . ISBN 9783527306732 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Ода, Т; Сато, Ю; Кодама, М; Канеко, М. (июль 1993 г.). «Ингибирование активности ДНК-топоизомеразы I диэтилстильбестролом и его аналогами» . Биологический и фармацевтический вестник . 16 (7): 708–10. дои : 10.1248/bpb.16.708 . ПМИД 8401407 .