Кроветворение
Кровотворение ( / h ɪ ˌ m æ t ə p ɔɪ ˈ iː s ɪ s , ˌ h iː m ə to oʊ -, ˌ h ɛ m ə -/ , [1] [2] от греческого αἷμα «кровь» и ποιεῖν «делать»; также гемопоэз в американском английском ; иногда также ч(а)эмопоэз ) — образование клеточных компонентов крови . Все клеточные компоненты крови происходят из гемопоэтических стволовых клеток . [3] У здорового взрослого человека примерно десять миллиардов (10 10 ) до ста миллиардов (10 11 ) новые клетки крови производятся каждый день для поддержания стабильного уровня в периферическом кровообращении. [4] [5] [ нужна страница ]
Процесс
[ редактировать ]Гемопоэтические стволовые клетки (ГСК)
[ редактировать ]Гемопоэтические стволовые клетки (ГСК) находятся в мозговом веществе кости ( костном мозге ) и обладают уникальной способностью давать начало всем различным типам зрелых клеток крови и тканям. [3] ЗКП являются самообновляющимися клетками: когда они дифференцируются, по крайней мере, некоторые из их дочерних клеток остаются в виде ЗКП, поэтому пул стволовых клеток не истощается. [6] Это явление называется асимметричным делением. [7] Другие дочерние клетки ЗКП ( миелоидные и лимфоидные клетки-предшественники) могут следовать любому из других путей дифференцировки, которые приводят к производству одного или нескольких специфических типов клеток крови, но не могут обновляться. Пул предшественников неоднороден и может быть разделен на две группы; долгосрочные самообновляющиеся HSC и только временно самообновляющиеся HSC, также называемые краткосрочными. [8] Это один из основных жизненно важных процессов в организме.
Типы ячеек
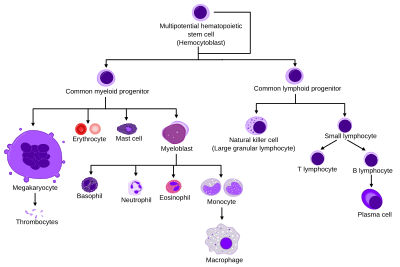
[ редактировать ]Все клетки крови делятся на три линии. [9]
- Красные кровяные тельца , которые также называются эритроцитами, представляют собой клетки, переносящие кислород . Эритроциты функционируют и попадают в кровь. Количество ретикулоцитов, представляющих собой незрелые эритроциты, дает оценку скорости эритропоэза .
- Лимфоциты являются краеугольным камнем адаптивной иммунной системы. Они происходят от общих лимфоидных предшественников. Лимфоидная линия состоит из Т-клеток , В-клеток и естественных клеток-киллеров . Это лимфопоэз .
- Клетки миелоидного ряда, включающие гранулоциты , мегакариоциты , моноциты и макрофаги , происходят от общих миелоидных предшественников и участвуют в таких разнообразных функциях, как врожденный иммунитет и свертывание крови . Это миелопоэз .
Гранулопоэз (или гранулоцитопоэз) — это кроветворение гранулоцитов, за исключением тучных клеток , которые представляют собой гранулоциты, но с экстрамедуллярным созреванием. [10]
Тромбопоэз – это кроветворение тромбоцитов (тромбоцитов) .
Терминология
[ редактировать ]В 1948—50 Комитет по уточнению номенклатуры клеток и болезней крови и кроветворных органов выпустил доклады по номенклатуре клеток крови. [11] [12] Ниже представлен обзор терминологии, от самой ранней до финальной стадии разработки:
- [корень]взрыв
- про[корневой]цит
- [корень]цит
- мета[коренной]цит
- имя зрелой клетки
Корень для эритроцитарных колониеобразующих единиц (КОЕ-Э) - «рубри», для гранулоцитарно-моноцитарных колониеобразующих единиц (КОЕ-ГМ) - «грануло» или «миело» и «моно», для колониеобразующих единиц лимфоцитов. (КОЕ-Л) — «лимфо», а для колониеобразующих единиц мегакариоцитов (КОЕ-Мег) — «мегакарио». Согласно этой терминологии, стадии образования эритроцитов будут следующими: рубробласт, прорубрицит, рубрицит, метарубрицит и эритроцит. Однако в настоящее время наиболее распространенной представляется следующая номенклатура:
| комитет | "лимфо" | "красный" | «грануло» или «миело» | "мононуклеоз" | "мегакарио" |
|---|---|---|---|---|---|
| Родословная | лимфоидный | миелоидный | миелоидный | миелоидный | миелоидный |
| КОЕ | КОЕ-Л | КОЕ-ГЕММ → КОЕ-Э | КОЕ-ГЕММ→ КОЕ-ГМ → КОЕ-Г | КОЕ-ГЕММ→ КОЕ-ГМ → КОЕ-М | КОЕ-GEMM→ КОЕ-Мг |
| Процесс | лимфоцитопоэз | эритропоэз | гранулоцитопоэз | моноцитопоэз | тромбоцитопоэз |
| [корень]взрыв | лимфобласт | Проэритробласт | Миелобласт | Монобласт | Мегакариобласт |
| про[корневой]цит | Пролимфоцит | Полихроматофильный эритроцит | Промиелоцит | Промоноцит | Промегакариоцит |
| [корень]цит | – | Нормобласт | Эозино / нейтро / базофильный миелоцит | Мегакариоцит | |
| мета[коренной]цит | Большой лимфоцит | Ретикулоцит | Эозинофильный/нейтрофильный/базофильный метамиелоцит , эозинофильная/нейтрофильная/базофильная полосчатая клетка | Ранний моноцит | - |
| имя зрелой клетки | Малый лимфоцит | Эритроцит | гранулоциты ( эозино / нейтро / базофилы ) | моноцит | тромбоциты ( тромбоциты ) |
Остеокласты также возникают из гемопоэтических клеток линии моноцитов/нейтрофилов, в частности CFU-GM.
Расположение
[ редактировать ]
У развивающихся эмбрионов кроветворение происходит в скоплениях клеток крови в желточном мешке, называемых кровяными островками . По мере развития кроветворение происходит в селезенке , печени и лимфатических узлах . [13] Когда костный мозг развивается, он со временем берет на себя задачу формирования большей части клеток крови для всего организма. [3] Однако созревание, активация и некоторая пролиферация лимфоидных клеток происходит в селезенке, тимусе и лимфатических узлах. У детей кроветворение происходит в костном мозге длинных костей, таких как бедренная и большеберцовая кость. У взрослых это происходит главным образом в области таза, черепа, позвонков и грудины. [14]
Экстрамедуллярный
[ редактировать ]В некоторых случаях печень, тимус и селезенка при необходимости могут возобновить свою кроветворную функцию. Это называется экстрамедуллярным кроветворением . Это может привести к существенному увеличению размеров этих органов. В период внутриутробного развития, поскольку кости и, следовательно, костный мозг развиваются позже, печень функционирует как главный кроветворный орган. Поэтому печень во время развития увеличивается. [15] Экстрамедуллярный гемопоэз и миелопоэз могут поставлять лейкоциты при сердечно-сосудистых заболеваниях и воспалениях в зрелом возрасте. [16] [17] селезенки Макрофаги и молекулы адгезии могут участвовать в регуляции образования экстрамедуллярных миелоидных клеток при сердечно-сосудистых заболеваниях . [18] [19]
Созревание
[ редактировать ]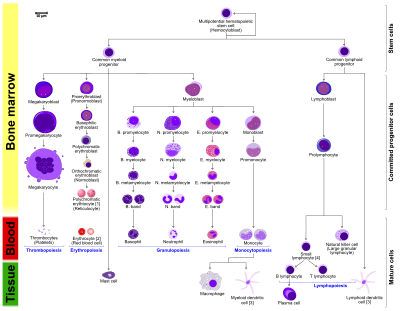
- Морфологические характеристики гемопоэтических клеток показаны при окраске Райта, окраске Мэй-Гимзы или окраске Мэй-Грюнвальда-Гимзы. В круглых скобках указаны альтернативные названия отдельных ячеек.
- Некоторые клетки могут иметь более одного характерного внешнего вида. В этих случаях было включено более одного представления одной и той же ячейки.
- Вместе моноциты и лимфоциты составляют агранулоциты, в отличие от гранулоцитов (базофилов, нейтрофилов и эозинофилов), которые образуются во время гранулопоэза.
- Б., Н. и Е. обозначают базофильный, нейтрофильный и эозинофильный соответственно – как в базофильном промиелоците. Для лимфоцитов фактическими обозначениями являются Т и В.
- Полихроматический эритроцит (ретикулоцит) справа демонстрирует свой характерный вид при окрашивании метиленовым синим или лазурью B.
- Эритроцит справа представляет собой более точное представление о его реальном виде, если смотреть через микроскоп.
- Другие клетки, возникающие из моноцита: остеокласты, микроглия (центральная нервная система), клетка Лангерганса (эпидермис), клетка Купфера (печень).
- Для ясности Т- и В-лимфоциты разделены, чтобы лучше показать, что плазматическая клетка возникает из В-клетки. Обратите внимание, что нет никакой разницы во внешнем виде В- и Т-клеток, если не применяется специфическое окрашивание.
По мере созревания стволовой клетки в ней происходят изменения в экспрессии генов , которые ограничивают типы клеток, которыми она может стать, и приближают ее к определенному типу клеток ( клеточная дифференциация ). Эти изменения часто можно отследить, наблюдая за наличием белков на поверхности клетки. Каждое последующее изменение приближает клетку к конечному типу клеток и еще больше ограничивает ее потенциал перехода в другой тип клеток. [ нужна ссылка ]
Определение судьбы клеток
[ редактировать ]Были предложены две модели кроветворения: детерминизм и стохастическая теория. [20] Для стволовых клеток и других недифференцированных клеток крови в костном мозге такая детерминация обычно объясняется теорией детерминизма кроветворения, утверждающей, что колониестимулирующие факторы и другие факторы кроветворного микроокружения заставляют клетки следовать определенному пути клеточной дифференцировки. [3] Это классический способ описания кроветворения. Согласно стохастической теории, недифференцированные клетки крови дифференцируются в определенные типы клеток случайным образом. Эта теория была подтверждена экспериментами, показывающими, что внутри популяции гемопоэтических клеток-предшественников мышей, лежащая в основе стохастической изменчивости в распределении Sca-1 , фактора стволовых клеток , подразделяется популяция на группы, демонстрирующие переменные скорости клеточной дифференцировки . Например, под влиянием эритропоэтина (фактора дифференцировки эритроцитов) субпопуляция клеток (определяемая уровнем Sca-1) дифференцируется в эритроциты с семикратной скоростью, чем остальная часть популяции. [21] Более того, было показано, что если позволить этой субпопуляции расти, она восстановит исходную субпопуляцию клеток, что подтверждает теорию о том, что это стохастический обратимый процесс. Другой уровень, на котором стохастичность может быть важна, — это процесс апоптоза и самообновления. В этом случае кроветворное микроокружение преобладает над тем, чтобы часть клеток выжила, а часть, наоборот, осуществила апоптоз и погибла. [3] Регулируя этот баланс между различными типами клеток, костный мозг может изменять количество различных клеток, которые в конечном итоге будут вырабатываться. [22]
Факторы роста
[ редактировать ]
Производство красных и лейкоцитов регулируется с большой точностью у здоровых людей, а производство лейкоцитов быстро увеличивается во время инфекции. Пролиферация и самообновление этих клеток зависят от факторов роста. Одним из ключевых игроков в самообновлении и развитии гемопоэтических клеток является фактор стволовых клеток (SCF). [25] который связывается с рецептором c-kit на HSC. Отсутствие SCF смертельно. Существуют и другие важные факторы роста гликопротеинов , которые регулируют пролиферацию и созревание, такие как интерлейкины IL-2 , IL-3 , IL-6 , IL-7 . Другие факторы, называемые колониестимулирующими факторами (CSF), специфически стимулируют выработку коммитированных клеток. Три CSF представляют собой гранулоцитарно-макрофагальный CSF (GM-CSF), гранулоцитарный CSF (G-CSF) и макрофагальный CSF (M-CSF). [26] Они стимулируют образование гранулоцитов и активны либо в отношении клеток-предшественников , либо в отношении клеток-конечных продуктов.
Эритропоэтин необходим для превращения миелоидной клетки-предшественника в эритроцит. [23] С другой стороны, тромбопоэтин заставляет миелоидные клетки-предшественники дифференцироваться в мегакариоциты ( тромбоцитообразующие клетки). [23] На диаграмме справа приведены примеры цитокинов и дифференцированных клеток крови, которые они дают. [27]
Транскрипционные факторы
[ редактировать ]Факторы роста инициируют пути передачи сигнала , которые приводят к активации факторов транскрипции . Факторы роста вызывают разные результаты в зависимости от комбинации факторов и стадии дифференцировки клетки. Например, долговременная экспрессия PU.1 приводит к коммитированию миелоида, а кратковременная индукция активности PU.1 приводит к образованию незрелых эозинофилов. [28] Недавно сообщалось, что факторы транскрипции, такие как NF-κB, могут регулироваться микроРНК (например, miR-125b) в гемопоэзе. [29]
Первым ключевым игроком в дифференцировке HSC в мультипотентный предшественник (MPP) является белок α, связывающий энхансер транскрипционного фактора CCAAT ( C/EBP α). Мутации C/EBPα связаны с острым миелолейкозом . [30] С этого момента клетки могут дифференцироваться либо по линии эритроид-мегакариоцитов, либо по лимфоидной и миелоидной линии, которые имеют общего предшественника, называемого мультипотентным предшественником с лимфоидной праймацией. Существует два основных фактора транскрипции. PU.1 для линии эритроид-мегакариоцитов и GATA-1 , что приводит к образованию мультипотентного предшественника с лимфоидной праймацией. [31]
Другие факторы транскрипции включают Ikaros. [32] ( развитие B-клеток ) и Gfi1 [33] (способствует развитию Th2 и ингибирует Th1) или IRF8 [34] ( базофилы и тучные клетки ). Примечательно, что определенные факторы вызывают разные реакции на разных стадиях кроветворения. Например, CEBPα в развитии нейтрофилов или PU.1 в развитии моноцитов и дендритных клеток. Важно отметить, что процессы не являются однонаправленными: дифференцированные клетки могут восстановить атрибуты клеток-предшественников. [1]
Примером является фактор PAX5 , который важен для развития B-клеток и связан с лимфомами. [35] Удивительно, но мыши с условным нокаутом pax5 позволили периферическим зрелым B-клеткам дедифференцироваться в ранние предшественники костного мозга. Эти данные показывают, что факторы транскрипции действуют как хранители уровня дифференцировки, а не только как инициаторы. [36]
Мутации в факторах транскрипции тесно связаны с раком крови, таким как острый миелоидный лейкоз (ОМЛ) или острый лимфобластный лейкоз (ОЛЛ). Например, известно, что Икарос является регулятором многих биологических событий. У мышей без Ikaros отсутствуют B-клетки , естественные киллеры и T-клетки . [37] Ikaros имеет шесть «цинковых пальцев» доменов , четыре из которых являются консервативными ДНК-связывающими доменами и два предназначены для димеризации . [38] Очень важным открытием является то, что разные цинковые пальцы участвуют в связывании с разными местами ДНК, и это является причиной плейотропного эффекта Икароса и различного участия в развитии рака, но в основном это мутации, связанные с пациентами с BCR-Abl , и это плохой прогностический маркер. . [39]
Другие животные
[ редактировать ]У некоторых позвоночных кроветворение может возникать везде, где есть рыхлая строма соединительной ткани и медленное кровоснабжение, например, в кишечнике , селезенке или почках . [40]
В отличие от плацентарных млекопитающих, печень новорожденных сумчатых активно кроветворна. [41] [42] [43] [44]
См. также
[ редактировать ]- Клональный кроветворение
- Стимуляторы эритропоэза
- Стимуляторы кроветворения:
- Экстравазация лейкоцитов
Ссылки
[ редактировать ]- ^ Jump up to: а б «кроветворение» . Словарь Merriam-Webster.com . Проверено 16 мая 2022 г.
- ^ «кроветворение» . Dictionary.com Полный (онлайн). нд . Проверено 16 октября 2019 г.
- ^ Jump up to: а б с д и Бирбрайр, Александр; Френетт, Пол С. (1 марта 2016 г.). «Неоднородность ниш в костном мозге» . Анналы Нью-Йоркской академии наук . 1370 (1): 82–96. Бибкод : 2016NYASA1370...82B . дои : 10.1111/nyas.13016 . ISSN 1749-6632 . ПМЦ 4938003 . ПМИД 27015419 .
- ^ Медицинские лекции 4 семестра в Уппсальском университете, 2008 г., Лейф Янссон
- ^ Парслоу Т.Г., Стайтс Д.П., Терр А.И., Имбоден Дж.Б. (1997). Медицинская иммунология (1-е изд.). Эпплтон и Ланге. ISBN 978-0-8385-6278-9 .
- ^ Монга I, Каур К., Дханда С. (март 2022 г.). «Возвращаясь к гемопоэзу: применение объемной и одноклеточной транскриптомики, анализирующей транскрипционную гетерогенность в гемопоэтических стволовых клетках». Брифинги по функциональной геномике . 21 (3): 159–176. дои : 10.1093/bfgp/elac002 . ПМИД 35265979 .
- ^ Моррисон, Дж.; Джудит Кимбл (2006). «Асимметричное и симметричное деление стволовых клеток в развитии и раке» (PDF) . Природа . 441 (7097): 1068–74. Бибкод : 2006Natur.441.1068M . дои : 10.1038/nature04956 . hdl : 2027.42/62868 . ПМИД 16810241 . S2CID 715049 .
- ^ Моррисон С.Дж., Вайсман И.Л. (ноябрь 1994 г.). «Длительная репопуляция гемопоэтических стволовых клеток является детерминированной и поддается выделению по фенотипу». Иммунитет . 1 (8): 661–73. дои : 10.1016/1074-7613(94)90037-х . ПМИД 7541305 .
- ^ «Гематопоэз из плюрипотентных стволовых клеток» . Библиотека ресурсов по антителам . ТермоФишер Сайентифик . Проверено 25 апреля 2020 г.
- ^ Малер (2013). Хашек, Ванда; Руссо, Колин Г.; Уоллиг, Мэтью А. (ред.). Справочник Гашека и Руссо по токсикологической патологии . помощники редактора Брэд Болон и Рикардо Очоа; редактор иллюстраций Бет В. (Третье изд.). [Sl]: Академическая пресса. п. 1863. ISBN 978-0-12-415759-0 .
- ^ «ПЕРВЫЙ доклад комиссии по уточнению номенклатуры клеток и болезней крови и кроветворных органов» . Американский журнал клинической патологии . 18 (5): 443–50. Май 1948 г. doi : 10.1093/ajcp/18.5_ts.443 . ПМИД 18913573 .
- ^ «ТРЕТИЙ, четвертый и пятый отчеты комиссии по уточнению номенклатуры клеток и болезней крови и кроветворных органов» . Американский журнал клинической патологии . 20 (6): 562–79. Июнь 1950 г. doi : 10.1093/ajcp/20.6.562 . ПМИД 15432355 .
- ^ Сингх, Ранбир; Зоман-Фолкнер, Кристина; Сугумар, Кавин (2022). «Эмбриология, кроветворение» . НКБИ . СтатПерлз. ПМИД 31334965 . Проверено 4 сентября 2022 г.
- ^ Фернандес К.С., де Аларкон, Пенсильвания (декабрь 2013 г.). «Развитие системы кроветворения и нарушения кроветворения, возникающие в младенчестве и раннем детстве» . Детские клиники Северной Америки . 60 (6): 1273–89. дои : 10.1016/j.pcl.2013.08.002 . ПМИД 24237971 .
- ^ Георгиадес К.С., Нейман Э.Г., Фрэнсис И.Р., Снайдер М.Б., Фишман Е.К. (ноябрь 2002 г.). «Типичные и атипичные проявления экстрамедуллярного кроветворения» . АЖР. Американский журнал рентгенологии . 179 (5): 1239–43. дои : 10.2214/ajr.179.5.1791239 . ПМИД 12388506 .
- ^ Свирски, Филип К.; Либби, Питер; Айкава, Елена; Алькаид, Пилар; Лусцинскас, Ф. Уильям; Вайсследер, Ральф; Питтет, Микаэль Дж. (2 января 2007 г.). «Моноциты Ly-6Chi доминируют в моноцитозе, связанном с гиперхолестеринемией, и дают начало макрофагам в атеромах» . Журнал клинических исследований . 117 (1): 195–205. дои : 10.1172/JCI29950 . ПМК 1716211 . ПМИД 17200719 .
- ^ Свирски Ф.К., Нарендорф М., Эцродт М., Вильдгрубер М., Кортес-Ретамозо В., Паницци П., Фигейредо Х.Л., Колер Р.Х., Чудновский А., Уотерман П., Айкава Э., Мемпель Т.Р., Либби П., Вайсследер Р., Питте М.Дж. (30 июля 2009 г.) ). «Идентификация моноцитов селезеночного резервуара и их размещение в очагах воспаления» . Наука . 325 (5940): 612–616. Бибкод : 2009Sci...325..612S . дои : 10.1126/science.1175202 . ПМК 2803111 . ПМИД 19644120 .
- ^ Дутта, П; Хойер, ФФ; Григорьева Л.С.; Сагер, HB; Лейшнер, Ф; Куртис, Дж; Бородовский А; Новобранцева Т; Руда, В.М.; Фицджеральд, К; Ивамото, Ю; Войткевич, Г; Солнце, Ю; Да Силва, Н.; Либби, П; Андерсон, генеральный директор; Свирски, ФК; Вайсследер, Р; Нарендорф, М. (6 апреля 2015 г.). «Макрофаги сохраняют гемопоэтические стволовые клетки в селезенке посредством VCAM-1» . Журнал экспериментальной медицины . 212 (4): 497–512. дои : 10.1084/jem.20141642 . ПМЦ 4387283 . ПМИД 25800955 .
- ^ Дутта, П; Хойер, ФФ; Солнце, Ю; Ивамото, Ю; Трико, Б; Вайсследер, Р; Маньяни, JL; Свирски, ФК; Нарендорф, М. (сентябрь 2016 г.). «Ингибирование E-селектина снижает активацию ЗКП селезенки и миелопоэз у мышей с гиперхолестеринемией и инфарктом миокарда» . Атеросклероз, тромбоз и сосудистая биология . 36 (9): 1802–8. дои : 10.1161/ATVBAHA.116.307519 . ПМК 5001901 . ПМИД 27470513 .
- ^ Киммель, Марек (1 января 2014 г.). «Стохастичность и детерминизм в моделях кроветворения». Системный биологический подход к крови . Достижения экспериментальной медицины и биологии. Том. 844. стр. 119–152. дои : 10.1007/978-1-4939-2095-2_7 . ISBN 978-1-4939-2094-5 . ISSN 0065-2598 . ПМИД 25480640 .
- ^ Чанг, Ханна Х.; Хемберг, Мартин; Бараона, Маурисио; Ингбер, Дональд Э.; Хуан, Суй (2008). «Шум во всем транскриптоме контролирует выбор линии в клетках-предшественниках млекопитающих» . Природа . 453 (7194): 544–547. Бибкод : 2008Natur.453..544C . дои : 10.1038/nature06965 . ПМК 5546414 . ПМИД 18497826 .
- ^ Аленци, FQ; Аленази, БК; Ахмад, С.Ю.; Салем, ML; Аль-Джабри, А.А.; Вайс, РК (март 2009 г.). «Гемопоэтические стволовые клетки: между апоптозом и самообновлением» . Йельский журнал биологии и медицины . 82 (1): 7–18. ПМЦ 2660591 . ПМИД 19325941 .
- ^ Jump up to: а б с д Молекулярно-клеточная биология. Лодиш, Харви Ф. 5. изд. : – Нью-Йорк: WH Freeman and Co., 2003, 973 с. счет. ISBN 0-7167-4366-3
Лодиш Х., Берк А., Зипурски С.Л., Мацудайра П., Балтимор Д., Дарнелл Дж. (2000). «Рак возникает в пролиферирующих клетках». Молекулярно-клеточная биология (4-е изд.). Нью-Йорк: WH Freeman. Рисунок 24-8: Образование дифференцированных клеток крови из гемопоэтических стволовых клеток в костном мозге. ISBN 0-7167-3136-3 – через книжную полку NCBI. - ^ Род Цветок; Хамфри П. Ранг; Морин М. Дейл; Риттер, Джеймс М. (2007). Фармакология Ранг и Дейл . Эдинбург: Черчилль Ливингстон. ISBN 978-0-443-06911-6 .
- ^ Броуди, ВК (15 августа 1997 г.). «Фактор стволовых клеток и кроветворение» . Кровь . 90 (4): 1345–64. дои : 10.1182/blood.V90.4.1345 . ПМИД 9269751 .
- ^ Кетли, Нью-Джерси; AC Ньюленд (1997). «Гемопоэтические факторы роста» . Аспирант Мед Дж . 73 (858): 215–221. дои : 10.1136/pgmj.73.858.215 . ПМЦ 2431295 . ПМИД 9156123 .
- ^ Хауке, Ральф; Стефано Р. Тарантоло (ноябрь 2000 г.). «Гематопоэтические факторы роста» . Лабораторная медицина . 31 (11): 613–5. doi : 10.1309/HNTM-ELUV-AV9G-MA1P .
- ^ Энгель, я; Мурре, К. (октябрь 1999 г.). «Транскрипционные факторы в кроветворении» . Текущее мнение в области генетики и развития . 9 (5): 575–9. дои : 10.1016/s0959-437x(99)00008-8 . ПМИД 10508690 .
- ^ О'Коннелл, Р.; Рао, Д.; Балтимор, Д. (2012). «Регуляция микроРНК воспалительных реакций» . Ежегодный обзор иммунологии . 30 : 295–312. doi : 10.1146/annurev-immunol-020711-075013 . ПМИД 22224773 .
- ^ Хо, Пенсильвания; Алонзо, штат Калифорния; Гербинг, РБ; Поллард, Дж; Стайруолт, Д.Л.; Гурвиц, К; Хирема, Северная Каролина; Хирш, Б; Раймонди, Южная Каролина; Ланге, Б; Франклин, Дж.Л.; Радич, JP; Мешинчи, С (25 июня 2009 г.). «Распространенность и прогностические последствия мутаций CEBPA при остром миелоидном лейкозе у детей (ОМЛ): отчет Детской онкологической группы» . Кровь . 113 (26): 6558–66. дои : 10.1182/кровь-2008-10-184747 . ПМЦ 2943755 . ПМИД 19304957 .
- ^ Вултуис, Кэролин М.; Парк, Кристофер Ю. (10 марта 2016 г.). «Приверженность гематопоэтических стволовых клеток/клеток-предшественников линии мегакариоцитов» . Кровь . 127 (10): 1242–1248. doi : 10.1182/blood-2015-07-607945 . ISSN 0006-4971 . ПМК 5003506 . ПМИД 26787736 . S2CID 206939258 .
- ^ Томпсон, Элизабет К.; Кобб, Брэдли С.; Саббаттини, Пьерангела; Мейксльспергер, Соня; Парельо, Ваня; Либерг, Дэвид; Тейлор, Бенджамин; Диллон, Найл; Георгопулос, Катя (1 марта 2007 г.). «ДНК-связывающие белки Ikaros как неотъемлемые компоненты регуляторных цепей, специфичных для стадии развития B-клеток» . Иммунитет . 26 (3): 335–344. doi : 10.1016/j.immuni.2007.02.010 . ISSN 1074-7613 . ПМИД 17363301 .
- ^ Сузуки, Дзюмпей; Маруяма, Сахо; Тамаучи, Хидекадзу; Кувахара, Макото; Хориучи, Мика; Мизуки, Масуми; Очи, Мизуки; Савасаки, Тацуя; Чжу, Цзиньфан (1 апреля 2016 г.). «Gfi1, репрессор транскрипции, ингибирует индукцию программы Т-хелперов типа 1 в активированных Т-клетках CD4» . Иммунология . 147 (4): 476–487. дои : 10.1111/imm.12580 . ISSN 1365-2567 . ПМЦ 4799889 . ПМИД 26749286 .
- ^ Сасаки, Харука; Куротаки, Дайсуке; Тамура, Томохико (1 апреля 2016 г.). «Регуляция развития базофилов и тучных клеток факторами транскрипции» . Международная аллергология . 65 (2): 127–134. дои : 10.1016/j.alit.2016.01.006 . ISSN 1440-1592 . ПМИД 26972050 .
- ^ О'Брайен, П; Морен, П. младший; Уэллетт, Р.Дж.; Робишо, Джорджия (15 декабря 2011 г.). «Ген Pax-5: плюрипотентный регулятор дифференцировки B-клеток и раковых заболеваний» . Исследования рака . 71 (24): 7345–50. дои : 10.1158/0008-5472.CAN-11-1874 . ПМИД 22127921 .
- ^ Кобаледа, К; Йохум, В; Бусслингер, М. (27 сентября 2007 г.). «Превращение зрелых В-клеток в Т-клетки путем дедифференцировки в незафиксированные предшественники» . Природа . 449 (7161): 473–7. Бибкод : 2007Natur.449..473C . дои : 10.1038/nature06159 . ПМИД 17851532 . S2CID 4414856 .
- ^ Ван, Дж. Х.; Ничогианнопулу, А; Ву, Л; Солнце, Л; Шарп, АХ; Бигби, М; Георгопулос, К. (декабрь 1996 г.). «Селективные дефекты развития лимфоидной системы плода и взрослого человека у мышей с нулевой мутацией Ikaros» . Иммунитет . 5 (6): 537–49. дои : 10.1016/s1074-7613(00)80269-1 . ПМИД 8986714 .
- ^ Солнце, Л; Лю, А; Георгопулос, К. (1 октября 1996 г.). «Взаимодействия белков, опосредованные цинковыми пальцами, модулируют активность Икароса, молекулярный контроль развития лимфоцитов» . Журнал ЭМБО . 15 (19): 5358–69. дои : 10.1002/j.1460-2075.1996.tb00920.x . ПМК 452279 . ПМИД 8895580 .
- ^ Шервен, Х; Маклафлин, Дж; Арензана, TL; Фритце, С; Ченг, Д; Уодсворт, SE; Лоусон, GW; Бенсингер, С.Дж.; Фарнхэм, ПиДжей; Витте, ОН; Смейл, ST (октябрь 2013 г.). «Избирательная регуляция лимфопоэза и лейкемогенеза отдельными цинковыми пальцами Икароса» . Природная иммунология . 14 (10): 1073–83. дои : 10.1038/ni.2707 . ПМК 3800053 . ПМИД 24013668 .
- ^ Зон, Л.И. (15 октября 1995 г.). «Эволюционная биология кроветворения» . Кровь (Обзор). 86 (8): 2876–91. дои : 10.1182/blood.V86.8.2876.2876 . ПМИД 7579378 .
- ^ Старый JM (2016). Кроветворение у сумчатых. Развивающая и сравнительная иммунология. 58, 40-46. DOI: 10.1016/j.dci.2015.11.009
- ^ Старый JM, Дин EM (2000). Развитие иммунной системы и иммунологической защиты у молодняка сумчатой сумки. Развивающая и сравнительная иммунология. 24(5), 445-454. DOI: 10.1016/S0145-305X(00)00008-2
- ^ Старый JM, Дин EM (2003). Лимфоидная и иммуногемопоэтическая ткани эмбрионального опоссума ( Trichosurus vulpecula ). Анатомия и эмбриология (теперь называемая «Структура и функции мозга»). 206(3), 193-197. DOI: 10.1007/s00429-002-0285-2
- ^ Старый Дж. М., Селвуд Л. , Дин Э. М. (2003). Гистологическое исследование лимфоидной и иммуногемопоэтической тканей взрослой особи полосатого даннарта ( Sminthopsis macroura ). Клетки Ткани Органы. 173(2), 115-121. DOI: 10.1159/000068946
Дальнейшее чтение
[ редактировать ]- Годен, Изабель; Кумано, Ана, ред. (2006). Развитие гемопоэтических стволовых клеток . Спрингер. ISBN 978-0-306-47872-7 .