Фенилкетонурия
| Фенилкетонурия | |
|---|---|
| Другие имена | Дефицит фенилаланингидроксилазы, дефицит ФАГ, болезнь Фёллинга [1] |
 | |
| Фенилаланин | |
| Специальность | Медицинская генетика , педиатрия , диетология |
| Симптомы | Без лечения умственная отсталость , судороги , поведенческие проблемы, психические расстройства , затхлый запах. [1] |
| Обычное начало | При рождении [2] |
| Типы | Классический, вариант [1] |
| Причины | Генетический ( аутосомно-рецессивный ) [1] |
| Метод диагностики | Программы скрининга новорожденных во многих странах [3] |
| Уход | Диета с низким содержанием продуктов, содержащих фенилаланин; специальные добавки [2] |
| Медикамент | сапроптерина дигидрохлорид , [2] пегвалиаза [4] |
| Прогноз | Нормальное здоровье при лечении [5] |
| Частота | ~1 из 12 000 новорожденных [6] |
Фенилкетонурия ( ФКУ ) – врожденное нарушение метаболизма которое приводит к снижению метаболизма аминокислоты , фенилаланина . [3] Невылеченная ФКУ может привести к умственной отсталости , судорогам , поведенческим проблемам и психическим расстройствам . [1] [7] Это также может привести к появлению затхлого запаха и осветлению кожи. [1] У ребенка, рожденного от матери, которая плохо лечилась ФКУ, могут быть проблемы с сердцем, маленькая голова и низкий вес при рождении . [1]
Фенилкетонурия — наследственное генетическое заболевание. [1] Это вызвано мутациями в гене PAH , которые могут привести к неэффективной или нефункциональной фенилаланингидроксилазе , ферменту, ответственному за метаболизм избытка фенилаланина. [1] Это приводит к накоплению пищевого фенилаланина до потенциально токсичного уровня. [1] Это аутосомно-рецессивный тип заболевания , что означает, что для развития заболевания должны быть мутированы обе копии гена. [1] Существует два основных типа: классическая ФКУ и вариантная ФКУ, в зависимости от того, сохраняется ли какая-либо функция фермента. [1] Те, у кого есть одна копия мутировавшего гена, обычно не имеют симптомов. [1] Во многих странах существуют программы скрининга новорожденных на это заболевание. [3]
Лечение заключается в соблюдении диеты, которая (1) содержит мало продуктов, содержащих фенилаланин, и которая (2) включает специальные добавки. [2] Детям следует использовать специальную смесь с небольшим количеством грудного молока . [2] Диету следует начинать как можно скорее после рождения и продолжать всю жизнь. [2] Люди, которым поставлен диагноз на ранней стадии и соблюдают строгую диету, могут иметь нормальное здоровье и нормальную продолжительность жизни . [5] Эффективность контролируется посредством периодических анализов крови. [5] препарат сапроптерина дигидрохлорид . В некоторых случаях может быть полезен [2]
Фенилкетонурия поражает примерно 1 из 12 000 младенцев. [6] Мужчины и женщины страдают одинаково. [8] Заболевание было обнаружено в 1934 году Иваром Асбьёрном Фёллингом , а важность диеты была определена в 1935 году. [9] По состоянию на 2023 год генетическая терапия , направленная на прямое восстановление активности ФАГ печени, станет многообещающим и активным направлением исследований. [10]
Признаки и симптомы
[ редактировать ]
Невылеченная ФКУ может привести к умственной отсталости , судорогам , поведенческим проблемам и психическим расстройствам . [1] Это также может привести к появлению затхлого запаха и осветлению кожи. [1] У ребенка, рожденного от матери, которая плохо лечилась ФКУ, могут быть проблемы с сердцем, маленькая голова и низкий вес при рождении . [1]
Поскольку организм матери способен расщеплять фенилаланин во время беременности, дети с ФКУ при рождении нормальны. В то время болезнь не может быть обнаружена при физическом осмотре, поскольку никаких повреждений еще не было нанесено. Скрининг новорожденных проводится для выявления заболевания и начала лечения до того, как будет нанесен какой-либо ущерб. Образец крови обычно берут с помощью прокола пятки , который обычно проводится через 2–7 дней после рождения. Этот тест может выявить повышенный уровень фенилаланина после одного или двух дней нормального кормления ребенка. [11] [12]
Если ребенку не поставлен диагноз во время обычного скринингового обследования новорожденных и не введена диета с ограничением фенилаланина, то уровень фенилаланина в крови со временем увеличится. Токсичные уровни фенилаланина (и недостаточные уровни тирозина ) могут влиять на развитие ребенка, оказывая необратимое воздействие. Клинически заболевание может проявляться судорогами , гипопигментацией (чрезмерно светлые волосы и кожа) и «затхлым запахом» пота и мочи ребенка (из-за фенилацетата , карбоновой кислоты, образующейся в результате окисления фенилацетона). В большинстве случаев повторный тест следует провести примерно в возрасте двух недель, чтобы подтвердить первоначальный тест и выявить любую фенилкетонурию, которая изначально была пропущена. [13]
Не получающие лечения дети часто не достигают ранних этапов развития, у них развивается микроцефалия и наблюдаются прогрессивные нарушения функций головного мозга. Гиперактивность , нарушения ЭЭГ , судороги и тяжелая неспособность к обучению являются основными клиническими проблемами в более позднем возрасте. Характерный «затхлый или мышиный» запах на коже, а также предрасположенность к экземе сохраняются на протяжении всей жизни при отсутствии лечения. [14]
Повреждения головного мозга, если ФКУ не лечить в первые месяцы жизни, необратимы. Крайне важно очень тщательно контролировать питание детей с ФКУ, чтобы мозг имел возможность нормально развиваться. У больных детей, выявленных при рождении и получивших лечение, гораздо реже развиваются неврологические проблемы, судороги и умственная отсталость (хотя такие клинические расстройства все еще возможны, включая астму, экзему, анемию, увеличение веса, почечную недостаточность, остеопороз, гастрит, поражение пищевода, и почечная недостаточность, камни в почках и гипертония). Кроме того, серьезные депрессивные расстройства встречаются на 230% чаще, чем в контрольной группе; головокружение и головокружение возникают на 180% чаще; хроническая ишемическая болезнь сердца, астма, диабет и гастроэнтерит встречаются на 170% чаще; а стресс и расстройства адаптации встречаются на 160% чаще. [15] [16] Однако в целом результаты лечения пациентов с ФКУ хорошие. У проходящих лечение людей может вообще не быть заметных физических, неврологических проблем или проблем с развитием.
Генетика
[ редактировать ]
ФКУ — аутосомно-рецессивное метаболическое генетическое заболевание . Поскольку это аутосомно-рецессивное заболевание, два аллеля для того, чтобы у человека возникли симптомы заболевания, необходимы ФКУ. Чтобы ребенок унаследовал ФКУ, оба родителя должны иметь и передать дефектный ген. [17] Если оба родителя являются носителями ФКУ, существует 25%-ная вероятность, что любой их ребенок родится с этим расстройством, 50%-ная вероятность, что ребенок будет носителем, и 25%-ная вероятность, что ребенок не разовьется и не станет носителем ФКУ. болезнь. [5]
ФКУ характеризуется гомозиготными или сложными гетерозиготными мутациями в гене печеночного фермента фенилаланингидроксилазы (ФАГ), что делает его нефункциональным. [18] : 541 Этот фермент необходим для метаболизма аминокислоты фенилаланина (Phe) в аминокислоту тирозин (Tyr). Когда активность ПАУ снижается, фенилаланин накапливается и превращается в фенилпируват (также известный как фенилкетон), который можно обнаружить в моче . [19]
Носители одного аллеля ФКУ не проявляют симптомов заболевания, но, по-видимому, в некоторой степени защищены от грибкового токсина охратоксина А. [20] Луи Вульф предположил, что это объясняет сохранение аллеля в определенных популяциях. [20] в том смысле, что это дает селективное преимущество — иными словами, быть гетерозиготой выгодно . [21]
Ген PAH расположен на хромосоме 12 в полосах 12q22-q24.2. [22] По состоянию на 2000 год в гене PAH было обнаружено около 400 мутаций, вызывающих заболевания. Это пример аллельной генетической гетерогенности . [5]
Патофизиология
[ редактировать ]Когда фенилаланин (Phe) не может метаболизироваться в организме, типичная диета, которая была бы здорова для людей без ФКУ, приводит к накоплению в крови аномально высоких уровней Phe, что токсично для мозга. Если не лечить (а часто даже лечить), осложнения ФКУ включают тяжелую умственную отсталость, нарушения функции мозга, микроцефалию, расстройства настроения, нерегулярное двигательное функционирование и поведенческие проблемы, такие как синдром дефицита внимания с гиперактивностью , а также физические симптомы, такие как «затхлый» запах, экзема и необычно светлый цвет кожи и волос. [23]
Классическая ФКУ
[ редактировать ]Классическая ФКУ и ее менее тяжелые формы «легкая ФКУ» и «легкая гиперфенилаланинемия» вызваны мутированным геном фермента фенилаланингидроксилазы ( PAH), который превращает аминокислоту фенилаланин («Phe») в другие незаменимые соединения в организме. , в частности тирозин. Тирозин является условно незаменимой аминокислотой для пациентов с ФКУ, поскольку без ФАГ он не может вырабатываться в организме путем распада фенилаланина.
Дефицит ФАГ вызывает целый ряд нарушений, включая классическую фенилкетонурию (ФКУ) и легкую гиперфенилаланинемию (также известную как «гиперфе» или «легкая ГГН»). [24] менее сильное накопление фенилаланина. По сравнению с пациентами с классической ФКУ, пациенты с «гиперфеей» имеют более высокую активность фермента ФАГ и способны переносить большее количество фенилаланина в своем рационе. Без диетического вмешательства у пациентов с легкой формой HPA уровень Phe в крови выше, чем у пациентов с нормальной активностью ЛАГ. В настоящее время не существует международного консенсуса по определению легкой степени HPA, однако ее чаще всего диагностируют при уровне Phe в крови 2–6 мг/дл. [25]
Фенилаланин — это большая нейтральная аминокислота (LNAA). LNAA конкурируют за транспорт через гематоэнцефалический барьер (ГЭБ) через большой переносчик нейтральных аминокислот (LNAAT). Если фенилаланин в крови в избытке, он насытит транспортер. Чрезмерные уровни фенилаланина имеют тенденцию снижать уровни других LNAA в мозге. Поскольку эти аминокислоты необходимы для синтеза белков и нейромедиаторов, накопление Phe препятствует развитию мозга , вызывая умственную отсталость . [26]
Недавние исследования показывают, что нейрокогнитивные, психосоциальные показатели, качество жизни, рост, питание, патология костей слегка неоптимальны даже для пациентов, которые проходят лечение и поддерживают уровень Phe в целевом диапазоне, если их диета не дополнена другими аминокислотами. [27]
Классическая ФКУ поражает миелинизацию и участки белого вещества у нелеченных младенцев; это может быть одной из основных причин неврологических проблем, связанных с фенилкетонурией. Различия в развитии белого вещества наблюдаются при магнитно-резонансной томографии . Также могут быть обнаружены аномалии серого вещества. [28] особенно в моторной и премоторной коре, таламусе и гиппокампе. [29]
Недавно было высказано предположение, что ФКУ может напоминать амилоидные заболевания, такие как болезнь Альцгеймера и болезнь Паркинсона, из-за образования токсичных амилоидных комплексов фенилаланина. [30]
Гиперфенилаланинемия с дефицитом тетрагидробиоптерина
[ редактировать ]Более редкой формой гиперфенилаланинемии является дефицит тетрагидробиоптерина , который возникает, когда фермент ФАГ в норме, и обнаруживается дефект биосинтеза или рециркуляции кофактора тетрагидробиоптерина ( ВН 4 ). [31] BH 4 необходим для правильной активности фермента PAH, и этот кофермент можно дополнять в качестве лечения. У людей с этой формой гиперфенилаланинемии может быть дефицит тирозина (который образуется из фенилаланина под действием ПАУ), и в этом случае лечение заключается в добавлении тирозина для компенсации этого дефицита. [ нужна ссылка ]
Уровни дофамина можно использовать, чтобы отличить эти два типа. Тетрагидробиоптерин необходим для превращения Phe в Tyr и необходим для превращения Tyr в L-ДОФА с помощью фермента тирозингидроксилазы . L-ДОФА, в свою очередь, превращается в дофамин . Низкий уровень дофамина приводит к высокому уровню пролактина . Напротив, при классической ФКУ (без участия дигидробиоптерина) уровень пролактина будет относительно нормальным. [32] [ нужна ссылка ]
По состоянию на 2020 год было известно, что дефицит тетрагидробиоптерина возникает в результате дефектов пяти генов. [33]
Метаболические пути
[ редактировать ]
Фермент фенилаланингидроксилаза обычно превращает аминокислоту фенилаланин в аминокислоту тирозин . Если этой реакции не происходит, происходит накопление фенилаланина и дефицит тирозина. Избыток фенилаланина может метаболизироваться в фенилкетоны второстепенным путем - трансаминазным путем с глутаматом . Метаболиты включают фенилацетат , фенилпируват и фенэтиламин . [34] Повышенный уровень фенилаланина в крови и обнаружение фенилкетонов в моче являются диагностическими показателями, однако у большинства пациентов диагноз диагностируется при скрининге новорожденных. [ нужна ссылка ] [35]
Скрининг
[ редактировать ]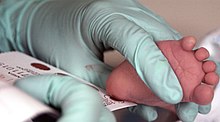
ФКУ обычно включается в программу скрининга новорожденных во многих странах с использованием различных методов выявления. Большинство детей, рожденных в Европе, Северной Америке и Австралии, проходят обследование на ФКУ вскоре после рождения. [36] [37] Скрининг ФКУ проводится с помощью анализа ингибирования бактерий ( тест Гатри ), иммуноанализа с использованием флуорометрического или фотометрического обнаружения или измерения аминокислот с использованием тандемной масс-спектрометрии (МС/МС). Измерения, выполненные с помощью МС/МС, определяют концентрацию Phe и соотношение Phe и тирозина , при ФКУ это соотношение будет повышено. [38]
Уход
[ редактировать ]ФКУ неизлечима. Однако, если ФКУ диагностируется достаточно рано, больной новорожденный может вырасти с нормальным развитием мозга, управляя и контролируя уровень фенилаланина («Фе») с помощью диеты или комбинации диеты и лекарств. [39] Если диетическое лечение не начать в течение 2 недель после рождения, у ребенка, скорее всего, разовьется необратимая умственная отсталость, даже если вскоре после этого начнутся диетические вмешательства. [37]
Диета
[ редактировать ]Люди, соблюдающие предписанное диетическое лечение с рождения, могут (но не всегда) не иметь симптомов. Их ФКУ можно будет обнаружить только с помощью анализа крови. Для оптимального развития мозга люди должны придерживаться специальной диеты с низким содержанием Phe. Поскольку Phe необходим для синтеза многих белков, он необходим для соответствующего роста, но его уровни необходимо строго контролировать. [37]

Оптимальные диапазоны для здоровья (или «целевые диапазоны») составляют от 120 до 360 мкмоль/л или, что эквивалентно, от 2 до 6 мг/дл. Оптимально достичь этого в течение как минимум первых 10 лет. [40] чтобы мозг мог нормально развиваться.
Диета требует ограничения или исключения продуктов с высоким содержанием Phe, таких как соевые бобы , яичные белки , креветки , куриная грудка , спирулина , кресс-салат , рыба , орехи , раки , омары , тунец , индейка , бобовые и обезжиренный творог . [41] Крахмалистые продукты, такие как картофель и кукуруза , обычно допустимы в контролируемых количествах, но необходимо контролировать количество потребляемого из этих продуктов Phe. В некоторых случаях может быть назначена беззерновая диета. Обычно ведется дневник питания, в котором фиксируется количество фена, потребляемого с каждым приемом пищи, закуской или напитком. «Обменную» систему можно использовать для расчета количества Phe в порции пищи на основе содержания белка, указанного на этикетке с информацией о пищевой ценности. Заменители «лечебной пищи» с низким содержанием белка часто используются вместо обычного хлеба , макарон и других зерновых продуктов, которые содержат значительное количество Phe. Многие фрукты и овощи содержат меньше Phe, и их можно есть в больших количествах. Младенцев по-прежнему можно кормить грудью, чтобы обеспечить все преимущества грудного молока, но необходимо также контролировать количество и добавлять недостающие питательные вещества. Также следует избегать подсластителя аспартама , присутствующего во многих диетических продуктах и безалкогольных напитках, поскольку аспартам содержит фенилаланин. [42]
Аминокислота тирозин становится незаменимой у людей с дефицитом фенилаланингидроксилазы. Таким образом, в дополнение к осторожному снижению содержания Phe в рационе, Tyr необходимо добавлять в пищу , чтобы обеспечить удовлетворение потребностей в питании. [37]
Разные люди могут переносить разное количество фена в своем рационе. Регулярные анализы крови используются для определения влияния потребления Phe с пищей на уровень Phe в крови. [ нужна ссылка ]
Пищевые добавки
[ редактировать ]Дополнительные смеси «заменителей белка» обычно назначают людям с фенилкетонурией (начиная с младенчества), чтобы обеспечить их аминокислотами и другими необходимыми питательными веществами, которых в противном случае не хватало бы при диете с низким содержанием фенилаланина. Обычно добавляют тирозин, который обычно получается из фенилаланина и необходим для нормальной работы мозга. Потребление белковых заменителей может фактически снизить уровень фенилаланина, вероятно, потому, что это останавливает процесс катаболизма белка и высвобождение Phe, хранящегося в мышцах и других тканях, в кровь. У многих пациентов с ФКУ самые высокие уровни Phe наблюдаются после периода голодания (например, в течение ночи), поскольку голодание запускает катаболизм. [43] Диета с низким содержанием фенилаланина, но не включающая заменители белка, также может не снизить уровень Phe в крови, поскольку недостаточное питание может также вызвать катаболизм. По всем этим причинам рецептурная формула является важной частью лечения пациентов с классической ФКУ. [ нужна ссылка ]
Имеющиеся данные подтверждают наличие в рационе пищевых добавок с большими нейтральными аминокислотами (LNAA). [44] LNAA (например, leu , tyr , trp , met , his , ile , val , thr ) могут конкурировать с phe за специфические белки-переносчики, которые транспортируют LNAA через слизистую оболочку кишечника в кровь и через гематоэнцефалический барьер в мозг. Его использование ограничено в США из-за стоимости, но доступно в большинстве стран как часть диеты с низким содержанием белка / PHE для замены недостающих питательных веществ.
Еще одна интересная стратегия лечения — казеиновый гликомакропептид (CGMP), который представляет собой молочный пептид, естественно не содержащий фена в чистой форме. [45] CGMP может заменить основную часть свободных аминокислот в диете при фенилкетонурии и обеспечивает несколько полезных питательных эффектов по сравнению со свободными аминокислотами. Тот факт, что CGMP является пептидом, гарантирует, что скорость всасывания его аминокислот увеличивается по сравнению со свободными аминокислотами, что приводит к улучшению удержания белка. [46] и повышенное чувство сытости [47] по сравнению со свободными аминокислотами. Еще одним важным преимуществом CGMP является то, что вкус значительно улучшается. [46] когда CGMP заменяет часть свободных аминокислот, и это может помочь улучшить соблюдение диеты при ФКУ.
Кроме того, CGMP содержит большое количество LNAA, снижающих уровень Phe, что составляет около 41 г на 100 г белка. [45] и, следовательно, поможет поддерживать уровни фена в плазме в целевом диапазоне.
Заменители ферментов
[ редактировать ]В 2018 году FDA одобрило заменитель фермента под названием пегвалиаза , который метаболизирует фенилаланин. [4] Это для взрослых, которые плохо справляются с другими методами лечения. [4]
Тетрагидробиоптерин (BH4) (кофактор окисления фенилаланина ) при приеме внутрь может снизить в крови у некоторых людей. уровень этой аминокислоты [48] [49]
Матери
[ редактировать ]Для женщин с ФКУ для здоровья их детей важно поддерживать низкий уровень Phe до и во время беременности. [50] Хотя развивающийся плод может быть только носителем гена ФКУ, внутриутробная среда может содержать очень высокий уровень фенилаланина, который может проникать через плаценту. В результате у ребенка могут развиться врожденные пороки сердца, задержка роста, микроцефалия и умственная отсталость. [51] Сами женщины, страдающие ФКУ, не подвергаются риску дополнительных осложнений во время беременности. [ нужна ссылка ]
В большинстве стран женщинам с ФКУ, желающим иметь детей, рекомендуется снизить уровень фенола в крови (обычно от 2 до 6 мг/дл) до того, как они забеременеют, и тщательно контролировать его уровень на протяжении всей беременности. Это достигается путем проведения регулярных анализов крови и строгого соблюдения диеты, обычно контролируемой на ежедневной основе специалистом-диетологом по метаболическим заболеваниям. Во многих случаях, когда печень плода начинает нормально развиваться и вырабатывать ПАУ, уровень Phe в крови матери падает, что требует увеличения потребления, чтобы оставаться в безопасном диапазоне 2–6 мг/дл. В результате к концу беременности суточное потребление фена матерью может удвоиться или даже утроиться. По неофициальным данным, когда уровень Phe в крови матери падает ниже 2 мг/дл, у матери могут возникнуть побочные эффекты, включая головные боли, тошноту, выпадение волос и общее недомогание. Когда низкие уровни фенилаланина поддерживаются на протяжении всей беременности, нет повышенного уровня риска врожденных дефектов по сравнению с ребенком, рожденным от матери, не болеющей ФКУ. [52]
Эпидемиология
[ редактировать ]| Страна | Заболеваемость |
|---|---|
| Австралия | 1 из 10 000 [53] |
| Бразилия | 1 из 8690 |
| Канада | 1 из 22 000 [53] |
| Китай | 1 из 17 000 [53] |
| Чехословакия | 1 из 7000 [53] |
| Дания | 1 из 12 000 [53] |
| Финляндия | 1 из 200 000 [53] |
| Франция | 1 из 13 500 [53] |
| Индия | 1 из 18 300 |
| Ирландия | 1 из 4500 [54] |
| Италия | 1 из 17 000 [53] |
| Япония | 1 из 125 000 [53] |
| Корея | 1 из 41 000 [55] |
| Нидерланды | 1 из 18 000 [56] |
| Норвегия | 1 из 14 500 [53] |
| Филиппины | 1 из 102 000 [57] |
| Польша | 1 из 8000 [56] |
| Шотландия | 1 из 5300 [53] |
| Испания | 1 из 20 000 [56] |
| Швеция | 1 из 20 000 [56] |
| Турция | 1 из 2600 [53] |
| Великобритания | 1 из 10 000 [56] |
| Соединенные Штаты | 1 из 25 000 [58] |
Среднее количество новых случаев ФКУ варьируется в разных популяциях людей. Представители европеоидной расы в США заболевают в среднем у 1 из 10 000. [59] В Турции самый высокий зарегистрированный показатель в мире: 1 на 2600 рождений, в то время как в таких странах, как Финляндия и Япония, показатели крайне низкие: менее одного случая ФКУ на 100 000 рождений. Исследование, проведенное в Словакии в 1987 году, сообщает цыган (один случай на 40 рождений) из-за обширного инбридинга. о чрезвычайно высокой частоте случаев ФКУ среди [60] Это наиболее распространенная проблема метаболизма аминокислот в Соединенном Королевстве. [ нужна ссылка ]
История
[ редактировать ]До того, как были поняты причины ФКУ, ФКУ вызывала тяжелую инвалидность у большинства людей, унаследовавших соответствующие мутации. лауреата Нобелевской и Пулитцеровской премий, У писательницы Перл С. Бак, была дочь по имени Кэрол, которая жила с фенилкетонурией до того, как стало доступно лечение, и написала отчет о его эффектах в книге под названием « Ребенок, который никогда не рос». [61] Многие нелеченные пациенты с ФКУ, родившиеся до широкомасштабного скрининга новорожденных, все еще живы, в основном в домах/учреждениях для иждивенцев. [62]
Фенилкетонурию открыл норвежский врач Ивар Асбьёрн Фёллинг в 1934 году. [63] когда он заметил, что гиперфенилаланинемия (ГФА) связана с умственной отсталостью. В Норвегии это заболевание известно как болезнь Фёллинга, по имени его первооткрывателя. [64] Фёллинг был одним из первых врачей, применивших подробный химический анализ для изучения болезней.
В 1934 году в Rikshospitalet Фёллинг увидел молодую женщину по имени Боргни Эгеланд. У нее было двое детей, Лив и Даг, которые при рождении были нормальными, но впоследствии у них развилась умственная отсталость. Когда Дагу было около года, мать заметила сильный запах его мочи. Фёллинг получил образцы мочи детей и после многих тестов обнаружил, что веществом, вызывающим запах мочи, была фенилпировиноградная кислота. Он пришел к выводу, что у детей наблюдался избыток фенилпировиноградной кислоты в моче, состояние, которое получило название фенилкетонурия (ФКУ). [19]
Его тщательный анализ мочи двух больных братьев и сестер побудил его попросить многих врачей недалеко от Осло проверить мочу других больных пациентов. Это привело к открытию того же вещества, которое он обнаружил у восьми других пациентов. Он провел тесты и обнаружил реакции, которые привели к образованию бензальдегида и бензойной кислоты , что привело его к выводу, что это соединение содержит бензольное кольцо. Дальнейшие испытания показали, что температура плавления такая же, как у фенилпировиноградной кислоты , что указывало на то, что вещество находилось в моче. [65]
В 1954 году Хорст Бикель , Эвелин Хикманс и Джон Джеррард опубликовали статью, в которой описывалось, как они создали диету с низким содержанием фенилаланина и пациент выздоровел. [66] Бикель, Джеррард и Хикманс были награждены медалью Джона Скотта в 1962 году за свое открытие. [66]
ФКУ была первым заболеванием, которое рутинно диагностировали посредством широкомасштабного скрининга новорожденных . Роберт Гатри представил скрининговый тест новорожденных на ФКУ в начале 1960-х годов. [67] Поскольку было известно, что ФКУ можно обнаружить до того, как симптомы станут очевидными и начнется лечение, скрининг был быстро принят во всем мире. Ирландия была первой страной, которая ввела национальную программу скрининга в феврале 1966 года. [68] Австрия также начала показ в 1966 году. [69] и Англия в 1968 году. [70]
В 2017 году были опубликованы Европейские рекомендации. [71] Их призвали организации пациентов, такие как Европейское общество фенилкетонурии и родственных заболеваний, трактуемых как фенилкетонурия . [72] [73] Они получили некоторую критику. [74]
Этимология и произношение
[ редактировать ]Слово фенилкетонурия использует сочетание фенил + + кетон ; -урия форм произносится / ˌ f iː n aɪ l ˌ k iː t ə ˈ nj ʊər i ə , ˌ f ɛ n -, - n ɪ l -, - n əl -, - t oʊ -/ [75] [76] .
Исследовать
[ редактировать ]Другие методы лечения находятся в стадии изучения, включая генную терапию .
BioMarin проводит клинические испытания по изучению PEG-PAL (ПЭГилированная рекомбинантная фенилаланин-аммиаклиаза или PAL) — фермент-заместительной терапии, при которой недостающий фермент PAH заменяется аналогичным ферментом, который также расщепляет Phe. По состоянию на 2015 год PEG-PAL находился на второй фазе клинической разработки. [77] но его клиническое лечение было приостановлено в сентябре 2021 года. В феврале 2022 года FDA опубликовало заявление, требующее дополнительных данных доклинических исследований для оценки онкогенного риска в результате лечения PEG-PAL. [78]
См. также
[ редактировать ]- Гиперфенилаланемия
- Лофеналак
- Дефицит тетрагидробиоптерина
- «Цветы для Алджернона» — персонаж, страдающий умственной отсталостью.
- 1968 — Фильм «Чарли» , киноверсия «Цветы для Алджернона».
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п «фенилкетонурия» . Домашний справочник по генетике . 8 сентября 2016 г. Архивировано из оригинала 27 июля 2016 г. Проверено 12 сентября 2016 г.
- ^ Перейти обратно: а б с д и ж г «Каковы общие методы лечения фенилкетонурии (ФКУ)?» . НИЧД . 23 августа 2013 г. Архивировано из оригинала 5 октября 2016 года . Проверено 12 сентября 2016 г.
- ^ Перейти обратно: а б с Аль Хафид Н., Христодулу Дж. (октябрь 2015 г.). «Фенилкетонурия: обзор текущих и будущих методов лечения» . Трансляционная педиатрия . 4 (4): 304–17. doi : 10.3978/j.issn.2224-4336.2015.10.07 . ПМЦ 4728993 . ПМИД 26835392 .
- ^ Перейти обратно: а б с «Сообщения в прессе – FDA одобряет новый метод лечения ФКУ, редкого и серьезного генетического заболевания» . www.fda.gov . Проверено 9 декабря 2018 г.
- ^ Перейти обратно: а б с д и «Заявление конференции по выработке консенсуса Национальных институтов здравоохранения Фенилкетонурия: скрининг и лечение» . НИЧД . 16–18 октября 2000 г. Архивировано из оригинала 5 октября 2016 г. Проверено 12 сентября 2016 г.
- ^ Перейти обратно: а б Бернштейн Л.Е., Рор Ф., Хелм-младший (2015). Управление питанием при наследственных метаболических заболеваниях: уроки Метаболического университета . Спрингер. п. 91. ИСБН 9783319146218 . Архивировано из оригинала 11 сентября 2017 г.
- ^ Кэннон Хомаи С., Бароне Х., Клеппе Р., Бетари Н., Рейф А., Хаавик Дж. (ноябрь 2021 г.). «Симптомы СДВГ при нейрометаболических заболеваниях: основные механизмы и клинические последствия» . Неврологические и биоповеденческие обзоры . 132 : 838–856. doi : 10.1016/j.neubiorev.2021.11.012 . ПМИД 34774900 . S2CID 243983688 .
- ^ Маркданте К., Клигман Р.М. (2014). Нельсон Основы педиатрии (7-е изд.). Elsevier Науки о здоровье. п. 150. ИСБН 9780323226981 . Архивировано из оригинала 11 сентября 2017 г.
- ^ Кальтер Х (2010). Тератология в двадцатом веке плюс десять . Springer Science & Business Media. стр. 89–92. ISBN 9789048188208 . Архивировано из оригинала 11 сентября 2017 г.
- ^ Мартинес М., Хардинг К.О., Шванк Г., Тони Б. (январь 2024 г.). «Состояние генной терапии фенилкетонурии на 2023 год». Журнал наследственных метаболических заболеваний . 47 (1): 80–92. дои : 10.1002/jimd.12651 . ISSN 0141-8955 . ПМК 10764640. ПМИД 37401651 .
- ^ «Тест на фенилкетонурию (ФКУ)» . ХелсЛинк БК . Архивировано из оригинала 17 мая 2018 года . Проверено 28 августа 2020 г.
- ^ Берри С.А., Браун С., Грант М., Грин К.Л., Юрецки Е., Кох Дж., Мозли К., Сатер Р., ван Калкар С.С., Уайлс Дж., Седербаум С. (август 2013 г.). «Скрининг новорожденных 50 лет спустя: проблемы доступа, с которыми сталкиваются взрослые с ФКУ» . Генетика в медицине . 15 (8): 591–9. дои : 10.1038/gim.2013.10 . ПМЦ 3938172 . ПМИД 23470838 .
- ^ «Фенилкетонурия (ФКУ)» . Сеть Мадриэлла Доула . Сеть Мадриэлла. 14 октября 2016 г. Проверено 11 апреля 2021 г.
- ^ «Фенилкетонурия» . МаркерБД . Исследовательская группа Уишарта . Проверено 11 апреля 2021 г.
- ^ Бертон Б.К., Джонс К.Б., Седербаум С., Рор Ф., Вайсбрен С., Ирвин Д.Е. и др. (2018). «Распространенность коморбидных состояний среди взрослых пациентов с диагнозом фенилкетонурия» . Мол Генет Метаб . 125 (3): 228–234. дои : 10.1016/j.ymgme.2018.09.006 . ПМИД 30266197 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Трефц К.Ф., Мунтау А.С., Кольшин К.М., Альтеверс Дж., Джейкоб С., Браун С. и др. (2019). «Клиническое бремя болезней у пациентов с фенилкетонурией (ФКУ) и сопутствующими заболеваниями - ретроспективное исследование данных о выплатах по страхованию здоровья в Германии» . Orphanet J Редкий дис . 14 (1): 181. doi : 10.1186/s13023-019-1153-y . ПМК 6647060 . ПМИД 31331350 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ «Фенилкетонурия (ФКУ) – Симптомы и причины» . Клиника Мэйо . Проверено 10 марта 2020 г.
- ^ Джеймс В.Д., Бергер Т.Г. (2006). Болезни кожи Эндрюса: клиническая дерматология . Сондерс Эльзевир. ISBN 978-0-7216-2921-6 .
- ^ Перейти обратно: а б Гонсалес Дж., Уиллис М.С. (февраль 2010 г.). «Ивар Асбьёрн Фёллинг» . Лабораторная медицина . 41 (2): 118–119. doi : 10.1309/LM62LVV5OSLUJOQF .
- ^ Перейти обратно: а б Вульф Л.И. (май 1986 г.). «Преимущество гетерозигот при фенилкетонурии» . Американский журнал генетики человека . 38 (5): 773–5. ПМК 1684820 . ПМИД 3717163 .
- ^ Льюис Р. (1997). Генетика человека . Чикаго, Иллинойс: Wm. К. Браун. стр. 247–248. ISBN 978-0-697-24030-9 .
- ^ Розенберг Р.Н., Барчи Р.Л. , ДиМауро С. , Прусинер С.Б. , Нестлер Э.Дж. (2003). Молекулярные и генетические основы неврологических и психиатрических заболеваний . Баттерворт-Хайнеманн. п. 820. ИСБН 9780750673600 .
- ^ Эш К., Келсо В., Фарранд С., Панетта Дж., Фацио Т., Де Йонг Дж., Уолтерфанг М. (2019). «Психиатрические и когнитивные аспекты фенилкетонурии: ограничения диеты и перспективы новых методов лечения» . Передний. Психиатрия . 10 (561): 561. doi : 10.3389/fpsyt.2019.00561 . ПМК 6748028 . ПМИД 31551819 .
- ^ Реджер Д.С., Грин К.Л. (25 июля 1993 г.). «Дефицит фенилаланингидроксилазы». Адам М.П., Мирзаа Г.М., Пагон Р.А., Уоллес С.Е., Бин Л.Дж., Грипп К.В., Амемия А. (ред.). GeneReviews® . Вашингтонский университет, Сиэтл. PMID 20301677 – через PubMed.
- ^ де ла Парра А., Гарсиа М.И., Вайсбрен С.Е., Корнехо В., Райманн Э. (декабрь 2015 г.). «Когнитивные функции при легкой гиперфенилаланинемии» . Отчеты о молекулярной генетике и метаболизме . 5 : 72–75. дои : 10.1016/j.ymgmr.2015.10.009 . ПМЦ 5471391 . ПМИД 28649547 .
- ^ Пиц Дж., Крейс Р., Рупп А., Маятепек Э., Рейтинг D, Боеш С., Бремер Х.Дж. (1999). «Большие нейтральные аминокислоты блокируют транспорт фенилаланина в ткани головного мозга у пациентов с фенилкетонурией» . Журнал клинических исследований . 103 (8): 1169–1178. дои : 10.1172/JCI5017 . ПМК 408272 . ПМИД 10207169 .
- ^ Эннс Г.М., Кох Р., Брамм В., Блейкли Э., Сутер Р., Юрецки Э. (1 октября 2010 г.). «Субоптимальные результаты у пациентов с ФКУ, которых лечили на ранней стадии только диетой: пересмотр доказательств». Молекулярная генетика и обмен веществ . 101 (2–3): 99–109. дои : 10.1016/j.ymgme.2010.05.017 . ПМИД 20678948 .
- ^ Террибилли Д., Шауфельбергер М.С. (10 мая 2020 г.). «Возрастные изменения объема серого вещества в мозге в пожилом возрасте» . Нейробиология старения . 32 (2–6): 354–368. doi : 10.1016/j.neurobiolaging.2009.02.008 . ПМК 3004040 . ПМИД 19282066 .
- ^ Хоукс З., Худ А.М., Лерман-Синькофф Д.Б., Шимони Дж.С., Ратлин Дж., Лагони Д., Грейндж Д.К., Уайт Д.А. (01.01.2019). «Развитие белого и серого вещества мозга у детей и молодых людей с фенилкетонурией» . НейроИмидж: Клинический . 23 : 101916. doi : 10.1016/j.nicl.2019.101916 . ISSN 2213-1582 . ПМК 6627563 . ПМИД 31491833 .
- ^ Адлер-Абрамович Л., Вакс Л., Карни О., Трудлер Д., Магно А., Кафлиш А., Френкель Д., Газит Е. (август 2012 г.). «Сборка фенилаланина в токсичные фибриллы предполагает амилоидную этиологию фенилкетонурии». Химическая биология природы . 8 (8): 701–6. дои : 10.1038/nchembio.1002 . ПМИД 22706200 .
- ^ Сёртиз Р., Блау Н. (2000). «Нейрохимия фенилкетонурии». Европейский журнал педиатрии . 169 : С109–С113. дои : 10.1007/PL00014370 . ПМИД 11043156 . S2CID 26196359 .
- ^ Опладен Т., Лопес-Ласо Э (26 мая 2020 г.). «Консенсусное руководство по диагностике и лечению дефицита тетрагидробиоптерина (BH4)» . Сиротский журнал редких заболеваний . 15 (1): 126. дои : 10.1186/s13023-020-01379-8 . ПМЦ 7251883 . ПМИД 32456656 .
- ^ Опладен Т., Лопес-Ласо Е., Кортес-Саладелафонт Е., Пирсон Т.С., Сиври Х.С., Йилдиз И., Ассманн Б., Куриан М.А., Леуцци В., Хилс С., Поуп С., Порта Ф., Гарсиа-Касорла А., Хонзик Т., Понс Р. , Регал Л, Гоэз Х, Артуч Р, Хоффманн Г.Ф., Хорват Г., Тони Б., Шолль-Бюрги С., Бурлина А., Вербеек М.М., Мастранджело М., Фридман Дж., Вассенберг Т., Елч К., Кулханек Дж., Кусейри Хюбшманн О (май). 2020). «Консенсусное руководство по диагностике и лечению дефицита тетрагидробиоптерина (BH4)» . Сиротский журнал редких заболеваний . 15 (1): 126. дои : 10.1186/s13023-020-01379-8 . ПМЦ 7251883 . ПМИД 32456656 .
- ^ Михалс К., Маталон Р. (1985). «Метаболиты фенилаланина, концентрация внимания и гиперактивность». Американский журнал клинического питания . 42 (2): 361–5. дои : 10.1093/ajcn/42.2.361 . ПМИД 4025205 .
- ^ «Фенилкетонурия (ФКУ) – Диагностика» . Клиника Мэйо . Проверено 18 июля 2024 г.
- ^ Сотрудники клиники Мэйо (20 декабря 2007 г.). «Фенилкетонурия (ФКУ)» . Клиника Мэйо . Архивировано из оригинала 17 марта 2008 г. Проверено 13 марта 2008 г.
- ^ Перейти обратно: а б с д Лонго Н. (2022). «Глава 420: Наследственные нарушения метаболизма аминокислот у взрослых». Принципы внутренней медицины Харрисона (21-е изд.). Нью-Йорк: МакГроу Хилл.
- ^ Сарафоглу К., Хоффманн Г.Ф., Рот К.С. (ред.). Детская эндокринология и врожденные нарушения обмена веществ . Нью-Йорк: McGraw Hill Medical. п. 26.
- ^ Видаман К.Ф. (1 февраля 2009 г.). «Фенилкетонурия у детей и матерей: гены, окружающая среда, поведение» . Современные направления психологической науки . 18 (1): 48–52. дои : 10.1111/j.1467-8721.2009.01604.x . ISSN 0963-7214 . ПМК 2705125 . ПМИД 20126294 .
- ^ Глава 55, страница 255. Архивировано 11 мая 2016 г. в Wayback Machine в: Берман, Ричард Э., Клигман, Роберт, Нельсон, Уолдо Э., Карен Маркданте, Дженсон, Хэл Б. (2006). Нельсон Основы педиатрии . Эльзевир/Сондерс. ISBN 978-1-4160-0159-1 .
- ^ «Продукты с высоким содержанием фенилаланина» . self.com . Архивировано из оригинала 5 мая 2015 г.
- ^ «CFR – Свод федеральных правил, Раздел 21, Часть 172: Пищевые добавки, разрешенные для прямого добавления в пищу для потребления человеком. Подчасть I – Многоцелевые добавки; Раздел 172.804 Аспартам» . Управление по контролю за продуктами и лекарствами США. 1 апреля 2018 года . Проверено 22 августа 2019 г.
- ^ Макдональд А., Райланс Г.В., Асплин Д., Холл С.К., Бут И.В. (1998). «Предсказывает ли одиночный фенилаланин в плазме качество контроля фенилкетонурии?» . Архив болезней в детстве . 78 (2): 122–6. дои : 10.1136/adc.78.2.122 . ПМЦ 1717471 . ПМИД 9579152 .
- ^ ван Спронсен Ф.Дж., де Гроот М.Дж., Хоксма М., Рейнгуд Дж., ван Рейн М. (декабрь 2010 г.). «Большие нейтральные аминокислоты в лечении ФКУ: от теории к практике» . Журнал наследственных метаболических заболеваний . 33 (6): 671–6. дои : 10.1007/s10545-010-9216-1 . ПМЦ 2992655 . ПМИД 20976625 .
- ^ Перейти обратно: а б Этцель М.Р. (апрель 2004 г.). «Производство и применение молочных белковых фракций» . Журнал питания . 134 (4): 996С–1002С. дои : 10.1093/jn/134.4.996S . ПМИД 15051860 .
- ^ Перейти обратно: а б ван Калкар СК, Маклеод Э.Л., Глисон С.Т., Этцель М.Р., Клейтон М.К., Вольф Дж.А., Ней Д.М. (апрель 2009 г.). «Улучшение диетического контроля фенилкетонурии за счет использования диеты, содержащей гликомакропептид по сравнению с аминокислотами» . Американский журнал клинического питания . 89 (4): 1068–77. дои : 10.3945/ajcn.2008.27280 . ПМЦ 2667457 . ПМИД 19244369 .
- ^ Маклеод Э.Л., Клейтон М.К., ван Калкар СК, Ней Д.М. (август 2010 г.). «Завтрак с гликомакропептидом по сравнению с аминокислотами подавляет уровень грелина в плазме у людей с фенилкетонурией» . Молекулярная генетика и обмен веществ . 100 (4): 303–8. дои : 10.1016/j.ymgme.2010.04.003 . ПМК 2906609 . ПМИД 20466571 .
- ^ Бертон Б.К., Кар С., Киркпатрик П. (2008). «Сапроптерин». Nature Reviews Открытие лекарств . 7 (3): 199–200. дои : 10.1038/nrd2540 . S2CID 263991793 .
- ^ Михалс-Маталон К. (февраль 2008 г.). «Сапроптерина дигидрохлорид, 6-RL-эритро-5,6,7,8-тетрагидробиоптерин в лечении фенилкетонурии». Экспертное заключение об исследуемых препаратах . 17 (2): 245–51. дои : 10.1517/13543784.17.2.245 . ПМИД 18230057 . S2CID 207475494 .
- ^ Ли П.Дж., Ридаут Д., Уолтер Дж.Х., Кокберн Ф. (2005). «Материнская фенилкетонурия: отчет из реестра Соединенного Королевства за 1978–97 годы» . Архив болезней в детстве . 90 (2): 143–146. дои : 10.1136/adc.2003.037762 . ПМК 1720245 . ПМИД 15665165 .
- ^ Роуз Б., Азен С., Кох Р., Маталон Р., Хэнли В., де ла Крус Ф., Трефз Ф., Фридман Э., Шифрин Х. (1997). «Совместное исследование материнской фенилкетонурии (MPKUCS) у потомства: аномалии лица, пороки развития и ранние неврологические последствия». Американский журнал медицинской генетики . 69 (1): 89–95. doi : 10.1002/(SICI)1096-8628(19970303)69:1<89::AID-AJMG17>3.0.CO;2-K . PMID 9066890 .
- ^ lsuhsc.edu. Архивировано 8 апреля 2008 г. в Wayback Machine Genetics and Louisiana Families.
- ^ Перейти обратно: а б с д и ж г час я дж к л Уильямс Р.А., Мамотт К.Д., Бернетт-младший (февраль 2008 г.). «Фенилкетонурия: врожденная ошибка метаболизма фенилаланина» . Клинический биохимик. Отзывы . 29 (1): 31–41. ПМЦ 2423317 . ПМИД 18566668 .
- ^ ДиЛелла АГ, Квок СК, Ледли Ф.Д., Марвит Дж., Ву С.Л. (1986). «Молекулярная структура и полиморфная карта гена фенилаланингидроксилазы человека». Биохимия . 25 (4): 743–749. дои : 10.1021/bi00352a001 . ПМИД 3008810 .
- ^ Ли Д.Х., Ку СК, Ли КС, Ён Ю.Дж., О Х.Дж., Ким С.В., Ли С.Дж., Ким СС, Ли Дж.Э., Джо И, Юнг СК (2004). «Молекулярная основа фенилкетонурии у корейцев» . Журнал генетики человека . 49 (1): 617–621. дои : 10.1007/s10038-004-0197-5 . ПМИД 15503242 . S2CID 21446773 .
- ^ Перейти обратно: а б с д и «ФКУ: устранение пробелов в медицинской помощи» (PDF) . Проверено 28 августа 2020 г.
- ^ «Филиппинское общество орфанных заболеваний – текущий реестр» . psod.org.ph. Архивировано из оригинала 4 января 2015 г.
- ^ Фенилкетонурия в eMedicine
- ^ Бикель Х., Бахманн К., Беккерс Р., Брандт, Нью-Джерси, Клейтон, Б.Е., Коррадо, Г. и др. (1981). «Массовый неонатальный скрининг метаболических нарушений» . Европейский журнал педиатрии . 137 (137): 133–139. дои : 10.1007/BF00441305 . S2CID 44705699 .
- ^ Ферак В, Сивакова Д, Сеглова З (1987). «Словацкие цыгане (цыгане) – популяция с самым высоким коэффициентом инбридинга в Европе». Братиславские медицинские письма . 87 (2): 168–175.
- ^ Борг К., Мондо С., Местре М., Каверо I (ноябрь 1991 г.). «Никорандил: дифференциальный вклад открытия K +-каналов и стимуляции гуанилатциклазы в его вазорелаксантное действие на различные артериальные препараты, сокращающие эндотелин-1. Сравнение с априкалимом (RP 52891) и нитроглицерином». Журнал фармакологии и экспериментальной терапии . 259 (2): 526–34. ПМИД 1682478 .
- ^ «НПКУА > Образование > О ФКУ» . npkua.org . Архивировано из оригинала 1 января 2015 г.
- ^ Фёллинг А. (1 января 1934 г.). «О выделении фенилпировиноградной кислоты с мочой как метаболическом нарушении, связанном с имбецильностью». Журнал физиологической химии Хоппе-Зейлера . 227 (1–4): 169–181. дои : 10.1515/bchm2.1934.227.1-4.169 .
- ^ Centerwall SA, Centerwall WR (2000). «Открытие фенилкетонурии: история молодой пары, двух больных детей и ученого». Педиатрия . 105 (1 Пт 1): 89–103. дои : 10.1542/педс.105.1.89 . ПМИД 10617710 . S2CID 35922780 .
- ^ Уильямс Р.А., Мамотт КД, Бернетт-младший (2008). «Фенилкетонурия: врожденная ошибка метаболизма фенилаланина» . Обзоры клинического биохимика . 29 (1): 31–41. ПМЦ 2423317 . ПМИД 18566668 .
В результате легкого окисления очищенного вещества образовалось соединение, пахнущее бензойной кислотой, что привело Фёллинга к предположению, что это соединение представляет собой фенилпировиноградную кислоту. действительно фенилпировиноградная кислота.
- ^ Перейти обратно: а б Марелин Рейнер-Кэнхэм, Джефф Рейнер-Кэнхэм (2008), «Эвелин Хикманс», «Химия была их жизнью: британские женщины-химики-пионеры, 1880–1949» , World Scientific, стр. 198, ISBN 9781908978998
- ^ Митчелл Дж.Дж., Тракадис Ю.Дж., Скривер Ч.Р. (2011). «Дефицит фенилаланингидроксилазы» . Генетика в медицине . 13 (8): 697–707. дои : 10.1097/GIM.0b013e3182141b48 . ПМИД 21555948 . S2CID 25921607 .
- ^ Кох Дж (1997). Роберт Гатри — история ФКУ: крестовый поход против умственной отсталости . Пасадена, Калифорния: Паб Hope. Дом. стр. 65–66. ISBN 0932727913 . OCLC 36352725 .
- ^ Каспер Д.К., Ратшманн Р., Мец Т.Ф., Мехтлер Т.П., Мёслингер Д., Константопулу В., Итем CB, Поллак А., Херкнер К.Р. (2010). «Национальная австрийская программа скрининга новорожденных - восьмилетний опыт масс-спектрометрии. Прошлые, настоящие и будущие цели». Венская клиническая больница . 122 (21–22): 607–613. дои : 10.1007/s00508-010-1457-3 . ПМИД 20938748 . S2CID 27643449 .
- ^ Комроуэр Г.М., Сардхарвалла И.Б., Фаулер Б., Бридж С (1979). «Региональная программа скрининга в Манчестере: 10-летний опыт ухода за пациентами и их семьями» . Британский медицинский журнал . 2 (6191): 635–638. дои : 10.1136/bmj.2.6191.635 . ПМК 1596331 . ПМИД 497752 .
- ^ ван Вегберг А.М., Макдональд А., Аринг К., Беланжер-Кинтана А., Блау Н., Бош А.М., Бурлина А., Кампистол Дж., Фейе Ф., Гижевска М., Уйбрегтс СК, Кирни С., Леуцци В., Майо Ф., Мунтау А.С., ван Рейн М., Трефц Ф., Уолтер Дж. Х., ван Спронсен Ф. Дж. (октябрь 2017 г.). «Полные европейские рекомендации по фенилкетонурии: диагностика и лечение» . Сиротский журнал редких заболеваний . 12 (1): 162. дои : 10.1186/s13023-017-0685-2 . ПМЦ 5639803 . ПМИД 29025426 .
- ^ «Консенсусный документ – ЕСПКУ» . ЭСПКУ . Проверено 23 ноября 2018 г.
- ^ Хагедорн Т.С., ван Беркель П., Хаммершмидт Г., Лготакова М., Салудес Р.П. (декабрь 2013 г.). «Требования к минимальному стандарту медицинской помощи при фенилкетонурии: взгляд пациентов» . Сиротский журнал редких заболеваний . 8 (1): 191. дои : 10.1186/1750-1172-8-191 . ПМЦ 3878574 . ПМИД 24341788 .
- ^ Бургард П., Ульрих К., Бальхаузен Д., Хеннерманн Дж.Б., Холлак С.Э., Лангевельд М., Каралл Д., Константопулу В., Майер Э.М., Ланг Ф., Лахманн Р., Мерфи Е., Гарбаде С., Хоффманн Г.Ф., Кёлькер С., Линднер М., Зшоке Дж. (сентябрь 2017 г.). «Проблемы европейских рекомендаций по фенилкетонурии» . «Ланцет». Диабет и эндокринология . 5 (9): 681–683. дои : 10.1016/S2213-8587(17)30201-2 . ПМИД 28842158 .
- ^ «Фенилкетонурия» . Словарь Merriam-Webster.com .
- ^ «Фенилкетонурия» . Lexico Британский словарь английского языка . Издательство Оксфордского университета . Архивировано из оригинала 5 августа 2020 г.
- ^ «BioMarin: Трубопровод: Обзор трубопровода: BMN 165 для ФКУ» . bmrn.com . Архивировано из оригинала 1 января 2015 г.
- ^ «BioMarin предоставляет обновленную информацию о прогрессе в программах генной терапии» . БиоМарин Инвесторы . Проверено 4 сентября 2023 г.